Слайд 2

Цель: Исследовать сущность химической термодинамики в биологических процессах на основе решения
задач.
Задачи:
1. Рассмотреть историю развития термодинамики
2. Раскрыть сущность химической термодинамики
3. Исследовать роль химической термодинамики в биологических проессах
4. Решить практические задания.
Слайд 3
1.Теоритическая часть
1.1 История развития термодинамики
Термодинамика как наука сформировалась в первой
половине XIX в. Как видно из ее названия, она изучает тепловое движение и связанные с ним процессы и явления.
Слайд 4

Слайд 5

Первое начало термодинамики
Сущность первого начала термодинамики заключается в следующем:
При сообщении термодинамической
системе некоторого количества теплоты Q в общем случае происходит изменение внутренней энергиисистемы DU и система совершает работу А:
Q = DU + A (1)
Слайд 6
Второе начало термодинамики
Второе начало термодинамики является законом, в соответствии с которым
макроскопические процессы, протекающие с конечной скоростью, необратимы.
Слайд 7

Третье начало термодинамики
Третье начало термодинамики - закон термодинамики, сформулированный В. Нерстом
в 1906 году (тепловой закон Нернста), согласно которому энтропия S любой системы стремится к конечному для неё пределу, не зависящему от давления, плотности или фазы, при стремлении температуры (Т) к абсолютному нулю.
Слайд 8

1.2 Химическая термодинамика
Химическая термoдинамика, рассматривает взаимосвязи между работой и энергией
применительнo к химическим превращениям.
Слайд 9

Термохимические уравнения
Теплота, высвобождаемая или поглощаемая конкретной химической реакцией, пропорциональна степени превращения
реагентов, определяемой по количеству любого из расходуемых либо образующихся продуктов.
Например, сгорание смеси газообразных метана и кислорода описывается термохимическим уравнением:
СН4(г) + 2О2 (г) = СО2(г) + 2 Н2О (ж)
Слайд 10

1.3 Термодинамика в биологических процессах
Термодинамика биологических процессов послужила основой для разработки
представлений об источниках энергии процессов жизнедеятельности, оказалась плодотворной для понимания и количественного анализа таких биологических процессов, как генерация биопотенциалов, осмотические явления, мышечные сокращения.
Слайд 11

Термодинамика рассматривает три типа систем, они отличаются по характеру взаимодействия с
внешней средой:
1) изолированные системы не обмениваются с окружающей средой ни веществом, ни энергией, т. е. границы такой системы непроницаемы;
2) системы, обменивающиеся через свои границы энергией с окружающей средой, но непроницаемые для веществ, относятся к замкнутым системам;
3) реальные системы в природе никогда не бывают абсолютно изолированными и закрытыми.
Слайд 12

Биофизические процессы, происходящие в живых организмах, с точки зрения термодинамики, являются
необратимыми. При совершении работы в организме осуществляется превращение химической энергии, заключенной в макроэргичсских связях АТФ, в другие виды энергии: механическую (при мышечном сокращении), электрическую (при нервном возбуждении); часть энергии рассеивается в окружающей среде в виде теплоты.
Слайд 13

Таким образом, работоспособность биологических систем, обусловленная наличием свободной энергии, определяется градиентами,
которые являются результатом неравновесного распределения вещества в биологической системе и непрерывного переноса из одной части системы в другую. При отмирании клеток их градиенты уменьшаются, выравнивание градиентов означает смерть организма.
Слайд 14

2. Практическая часть
Решение задач
Слайд 15

Слайд 16

Слайд 17

Слайд 18

Слайд 19

Слайд 20

Слайд 21

Слайд 22

Заключение
Термодинамический аспект необходимо учитывать при изучении физико-химических процессов. Термодинамика биологических процессов
послужила основой для разработки представлений об источниках энергии процессов жизнедеятельности, оказалась плодотворной для понимания и количественного анализа таких биологических процессов, как генерация биопотенциалов, осмотические явления, мышечные сокращения.
Слайд 23
![СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ 1.Химическая термодинамика. [Интернет-ресурс]. – [М.,2018].– Режим доступа:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/267648/slide-22.jpg)
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1.Химическая термодинамика. [Интернет-ресурс]. – [М.,2018].– Режим доступа: http://files.school-collection.edu.ru
2.Киреев В.А. Методы практических расчетов в термодинамике химических реакций. М., 1975 ; с.296.
3.Еремин Е.Н. Основы химической термодинамики. М., 1978 ; с.263.
4.Термодинамика и кинетика химических процессов. Л., 1981 ; с.302.
5.Глазов В.М., Павлова Л.М. Химическая термодинамика и фазовые равновесия. М., 1988; с. 297.
6.Химическая термодинамика. Энциклопедия Кругосвет . [Интернет-ресурс]. – [М.,2018].– Режим доступа: http://www.krugosvet.ru
7.Химический факультет МГУ. Элементы химической термодинамики и кинетики. [Интернет-ресурс]. – [М.,2018]. – Режим доступа: http://www.chem.msu.ru





















![СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ 1.Химическая термодинамика. [Интернет-ресурс]. – [М.,2018].– Режим доступа:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/267648/slide-22.jpg)
 Иван Петрович Павлов (1849-1936)
Иван Петрович Павлов (1849-1936) Мәмлерің түрлері
Мәмлерің түрлері разработка урока для 7 класса на тему: Тип плоские черви. Белая планария
разработка урока для 7 класса на тему: Тип плоские черви. Белая планария Сердечно-сосудистая система
Сердечно-сосудистая система Саморазвитие экосистемы
Саморазвитие экосистемы Раціональне харчування
Раціональне харчування Вегетативное размножение растений
Вегетативное размножение растений Классификацая органического мира
Классификацая органического мира Презентация Грибы
Презентация Грибы Альтернативные способы обеззараживания семенного материала
Альтернативные способы обеззараживания семенного материала энергетический обмен
энергетический обмен Ямчатость стебля
Ямчатость стебля Цитология. Клетка как биологическая система
Цитология. Клетка как биологическая система Влияние условий хранения хлеба на образование плесени на нём
Влияние условий хранения хлеба на образование плесени на нём Микробиология мяса
Микробиология мяса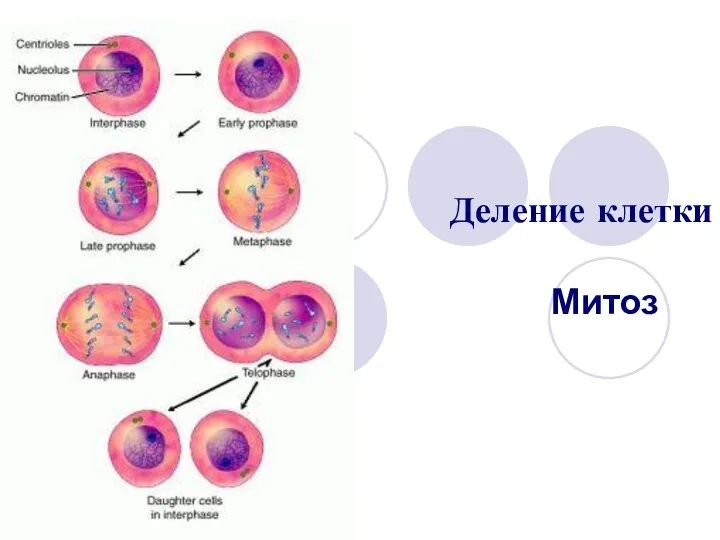 Деление клетки
Деление клетки Рослини – символи України
Рослини – символи України Тип Членистоногие (Arthropoda)
Тип Членистоногие (Arthropoda)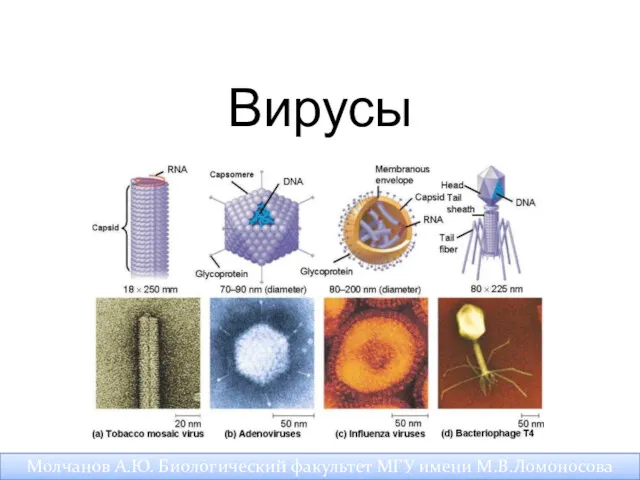 Вирусы. Живые ли вирусы или нет?
Вирусы. Живые ли вирусы или нет? Химиотерапевтические препараты. Антибиотики. Бактериофаги
Химиотерапевтические препараты. Антибиотики. Бактериофаги Строение и функции клетки
Строение и функции клетки Тотығу стрестің өсімдіктерге әсері
Тотығу стрестің өсімдіктерге әсері Экологическая ниша
Экологическая ниша Желудочная секреция
Желудочная секреция Формы размножения организмов
Формы размножения организмов Рекомбинантные антитела для диагностики и терапии
Рекомбинантные антитела для диагностики и терапии Урок на тему: ВОДА – ИСТОЧНИК ЖИЗНИ
Урок на тему: ВОДА – ИСТОЧНИК ЖИЗНИ Порядок Capparales - каперсоцветные
Порядок Capparales - каперсоцветные