Содержание
- 2. План: 1. Химический состав бактериальной клетки: вода, белки, липиды, углеводы, нуклеиновые кислоты, ферменты.
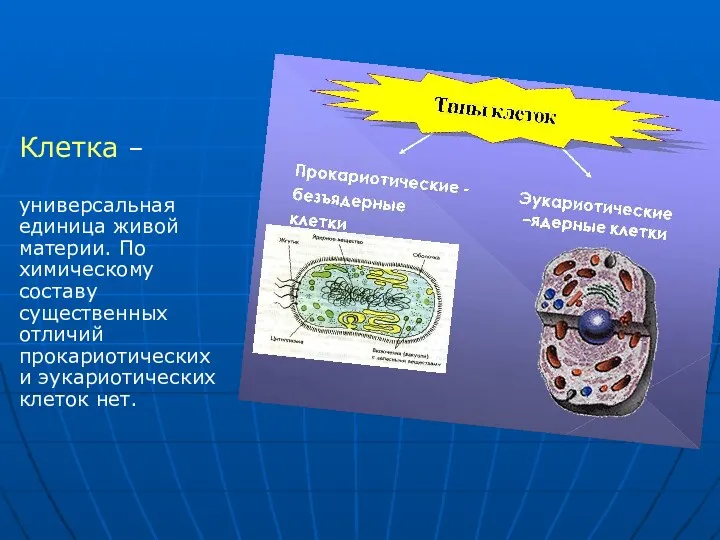
- 3. Клетка – универсальная единица живой материи. По химическому составу существенных отличий прокариотических и эукариотических клеток нет.
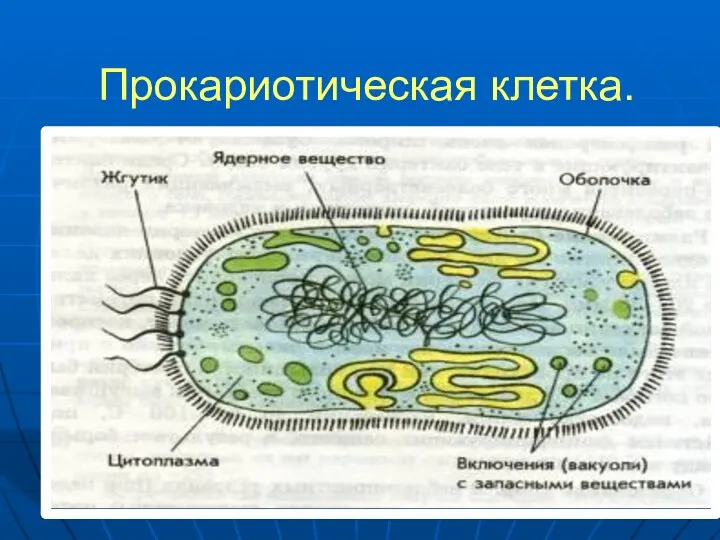
- 4. Прокариотическая клетка.
- 5. Химические элементы, входящие в состав живой материи, можно разделить на три основные группы: Биогенные химические элементы
- 6. Макроэлементы. Это химические элементы или их соединения, используемые организмами в сравнительно больших количествах: кислород, водород, углерод,
- 7. Фосфор. Физиологическое значение фосфора определяется тем, что он входит в состав ряда органических соединений, таких, как
- 8. СЕРА. Сера входит в состав органических соединений, играющих важную роль в обмене веществ организма. Так, сера
- 9. Кальций. Роль кальция разнообразна. Кальций, соединяясь с пектиновыми веществами, дает пектаты кальция, которые являются важнейшей составной
- 10. Магний. Магний поддерживает структуру рибосом, связывая РНК и белок. Магний является активатором многих фермент. Магний активирует
- 11. КАЛИЙ. Физиологическую роль калия нельзя считать полностью выясненной. Калий не входит ни в одно органическое соединение.
- 12. Микроэлементы. Это химические элементы или их соединения, используемые организмами в сравнительно больших количествах: кислород, водород, углерод,
- 13. Железо. Роль железа в большинстве случаев связана с его способностью переходить из окисленной формы (Fe3+) в
- 14. Цинк. Цинк не участвует в окислительно-восстановительных реакциях, поскольку не меняет степень окисления. Он входит в состав
- 15. Медь. Медь входит непосредственно в состав ряда ферментных систем, относящихся к группе оксидаз, таких, как полифенолоксидаза,
- 16. Молибден. Молибден входит в состав более 20 ферментов, выполняя при этом не только каталитическую, но и
- 17. Химические элементы входят в состав различных "веществ- воды, белков, липидов, нейтральных жиров, углеводов, нуклеиновых кислот. Синтез
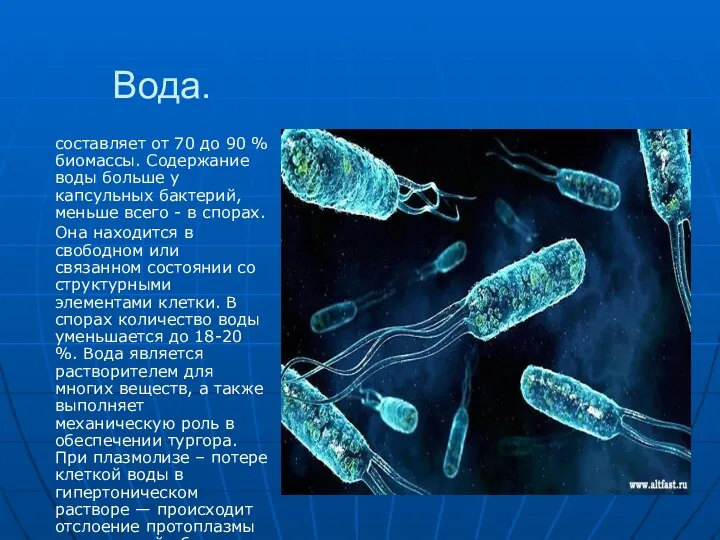
- 18. Вода. составляет от 70 до 90 % биомассы. Содержание воды больше у капсульных бактерий, меньше всего
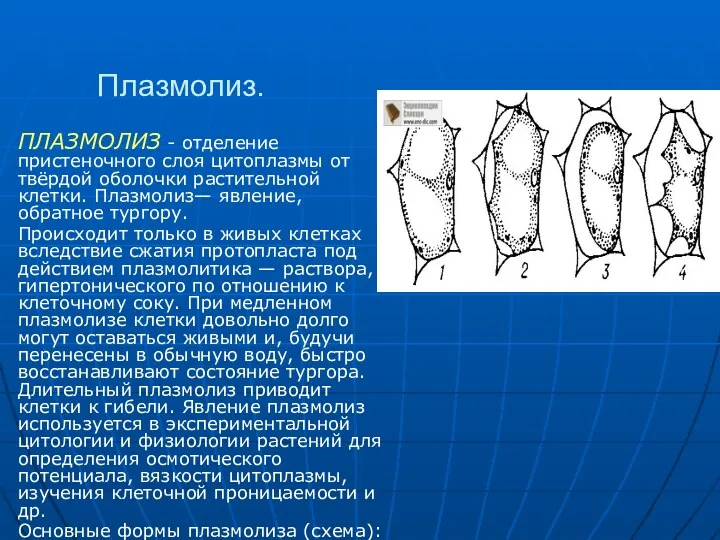
- 19. Плазмолиз. ПЛАЗМОЛИЗ - отделение пристеночного слоя цитоплазмы от твёрдой оболочки растительной клетки. Плазмолиз— явление, обратное тургору.
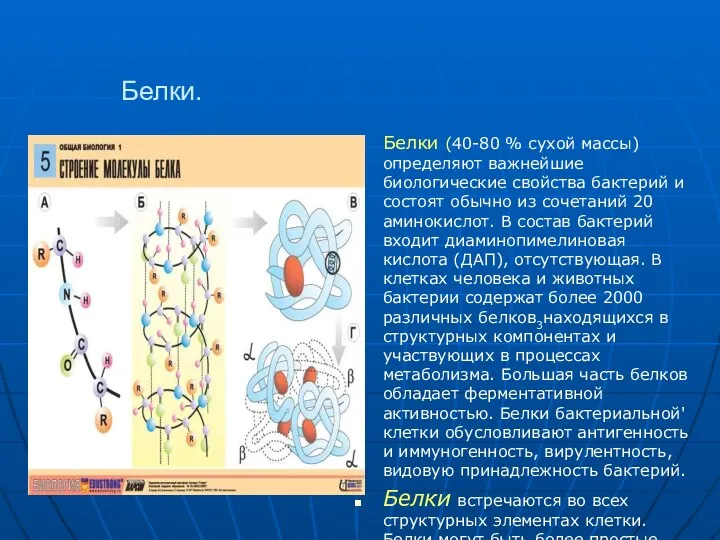
- 20. Белки. Белки (40-80 % сухой массы) определяют важнейшие биологические свойства бактерий и состоят обычно из сочетаний
- 21. В состав белков входят как обычные для эукариотов аминокислоты, так и оригинальные – диаминопимелиновая, (ДАП) D-аланин,
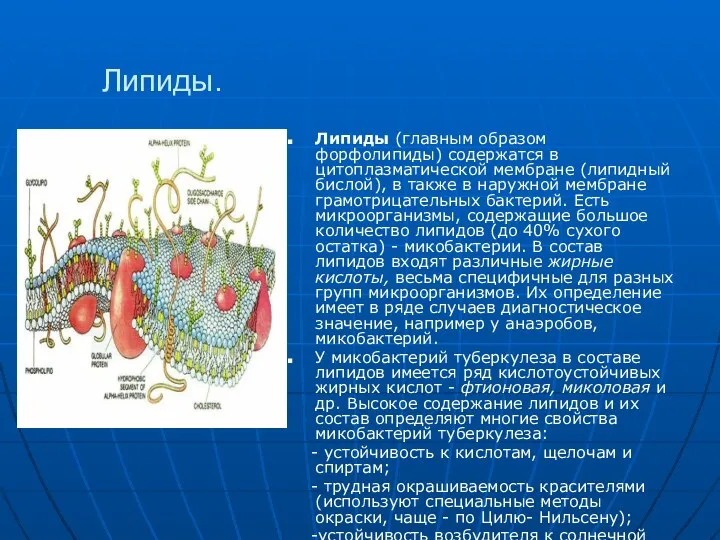
- 22. Липиды. Липиды (главным образом форфолипиды) содержатся в цитоплазматической мембране (липидный бислой), в также в наружной мембране
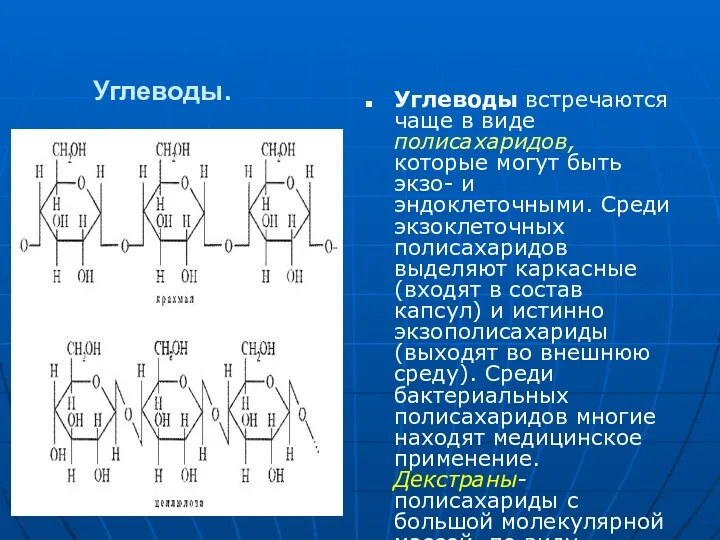
- 23. Углеводы. Углеводы встречаются чаще в виде полисахаридов, которые могут быть экзо- и эндоклеточными. Среди экзоклеточных полисахаридов
- 24. Липополисахарид (ЛПС). Липополисахарид (ЛПС) - один из основных компонентов клеточной стенки грамот-рицательных бактерий, это соединение липида
- 25. Нуклеиновые кислоты. Нуклеиновые кислоты- ДНК и РНК. Рибонуклеиновые кислоты (РНК) находятся главным образом в рибосомах (р-РНК-
- 26. Микроорганизмы синтезируют различные ферменты - специфические белковые катализаторы. У бактерий обнаружены ферменты 6 основных классов: 1.Оксидоредуктазы
- 27. Ферменты. В бактериологии для дифференциации микроорганизмов по биохимическим свойствам основное значение часто имеют конечные продукты и
- 28. Ферменты микроорганизмов. Экзоферменты. Выделяются наружу в среду. Подготавливают пищу к ее поступлению в клетку, расщепляют сложные
- 30. Скачать презентацию




















 Оси и плоскости в анатомии
Оси и плоскости в анатомии Отряд млекопитающие
Отряд млекопитающие Родина Пасльонові
Родина Пасльонові Гербициды. (Лекция 8)
Гербициды. (Лекция 8) Методы исследования биологии
Методы исследования биологии Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Удаление продуктов обмена. Обмен веществ
Удаление продуктов обмена. Обмен веществ Необычный живой мир континента
Необычный живой мир континента Жиры (липиды)
Жиры (липиды) Поле чудес
Поле чудес Предмет и задачи зоопсихологии и сравнительной психологии
Предмет и задачи зоопсихологии и сравнительной психологии В тесном сотрудничестве: лингвистика - нейропсихология - нейролингвистика
В тесном сотрудничестве: лингвистика - нейропсихология - нейролингвистика Многообразие микробного мира
Многообразие микробного мира Методологическая роль лабораторных и практических работ по биологии в рамках ФГОС.
Методологическая роль лабораторных и практических работ по биологии в рамках ФГОС. Осенние явления в жизни растений
Осенние явления в жизни растений Митохондрии, пластиды, клеточный центр, органоиды движения, клеточные включения
Митохондрии, пластиды, клеточный центр, органоиды движения, клеточные включения Семейство крестоцветные растения
Семейство крестоцветные растения Биотехнологии. Значение биотехнологий
Биотехнологии. Значение биотехнологий Многоствольные формы
Многоствольные формы Рысь
Рысь Классификация и характеристика промысловых рыб
Классификация и характеристика промысловых рыб Состав и свойства помидоров
Состав и свойства помидоров Мониезиоз жвачных животных. Разработка мер борьбы и профилактики
Мониезиоз жвачных животных. Разработка мер борьбы и профилактики Ағзалардың көбею формалары
Ағзалардың көбею формалары Передвижение воды и минеральных веществ в растениях
Передвижение воды и минеральных веществ в растениях Общее строение клетки
Общее строение клетки Среды обитания живых организмов
Среды обитания живых организмов Зелёная аптека
Зелёная аптека