Содержание
- 2. Вопросы устного экзамена по метаболизму липидов Транспорт липидов в организме. Липопротеины сыворотки крови. Химия высших жирных
- 3. Структура темы Классификация липидов ВЖК Ацилглицеролы (МАГ, ДАГ, ТАГ) Глицерофосфолипиды (фосфатидилхолин, фосфатидилсерин, фосфатидилэтаноламин, фосфатидилинозитол) Сфинголипиды (сфингомиелин,
- 4. БЕТА-ОКИСЛЕНИЕ ВЖК
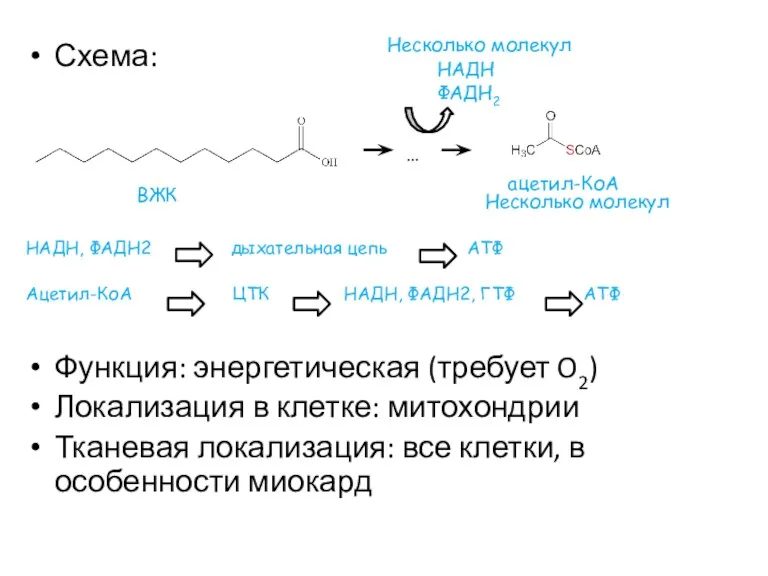
- 5. Схема: НАДН, ФАДН2 дыхательная цепь АТФ Ацетил-КоА ЦТК НАДН, ФАДН2, ГТФ АТФ Функция: энергетическая (требует O2)
- 6. Этапы Попадание ВЖК внутрь клетки из крови, и активация ВЖК в цитозоле клетки Транспорт ВЖК в
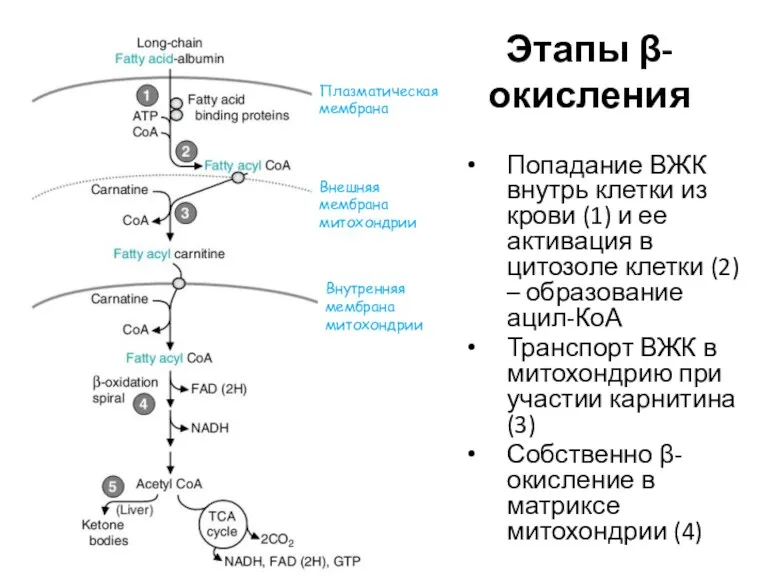
- 7. Этапы β-окисления Попадание ВЖК внутрь клетки из крови (1) и ее активация в цитозоле клетки (2)
- 8. Попадание ВЖК внутрь клетки из крови, и активация ВЖК в цитозоле клетки ВЖК в крови транспортируются
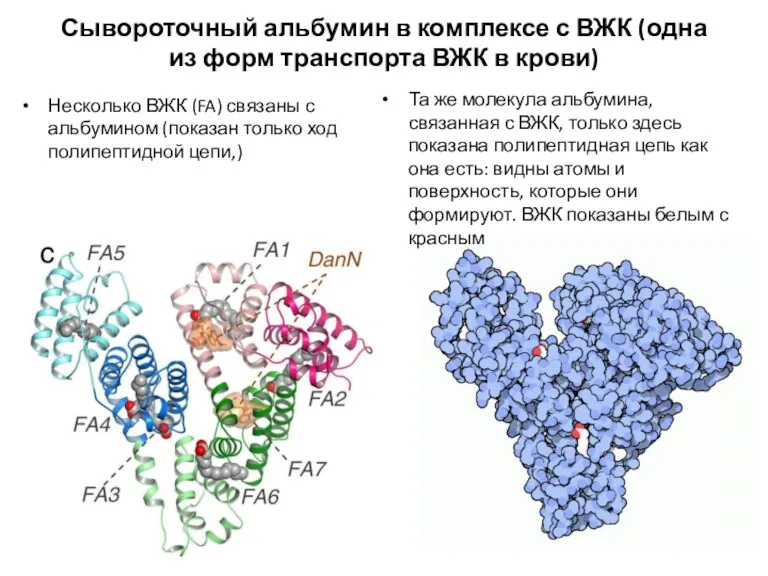
- 9. Сывороточный альбумин в комплексе с ВЖК (одна из форм транспорта ВЖК в крови) Несколько ВЖК (FA)
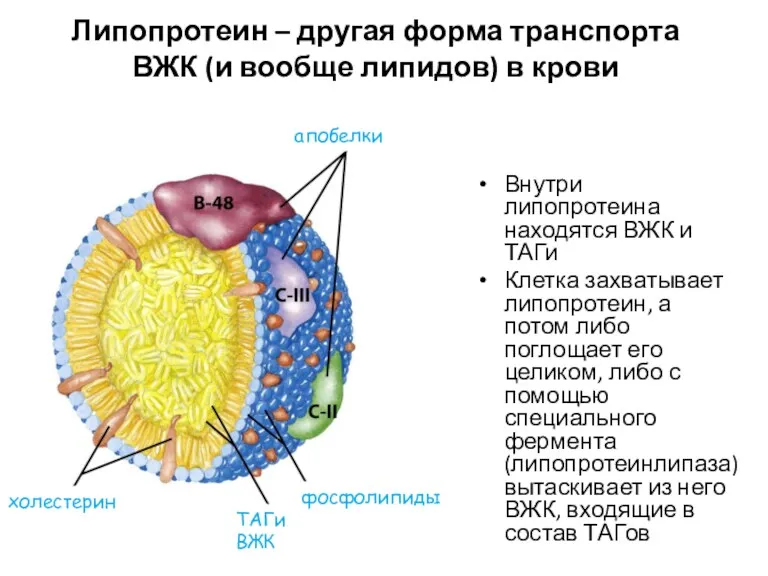
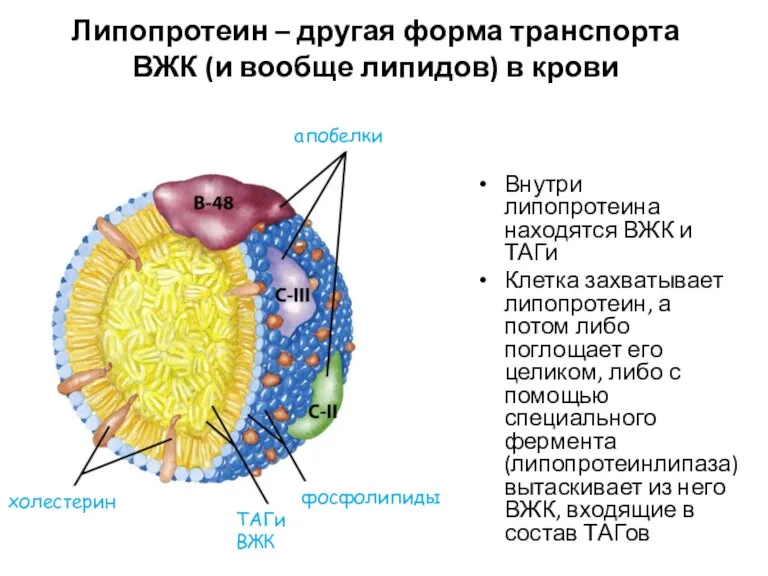
- 10. Липопротеин – другая форма транспорта ВЖК (и вообще липидов) в крови Внутри липопротеина находятся ВЖК и
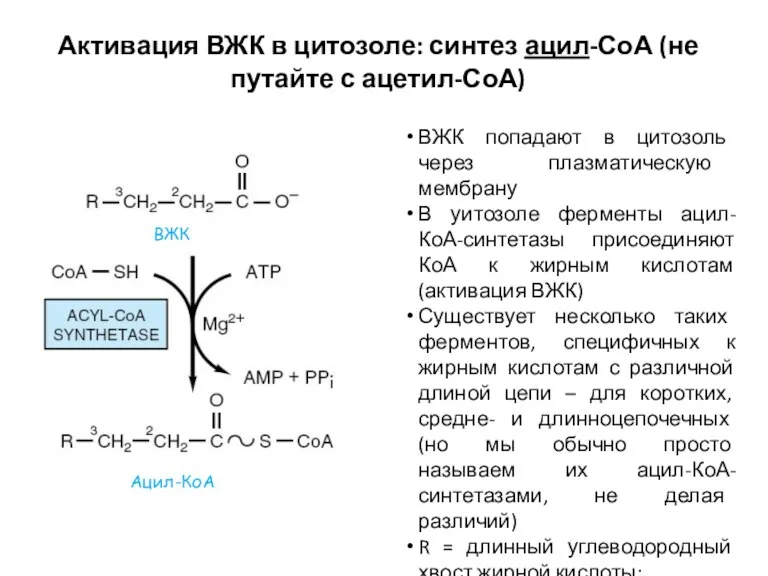
- 11. Активация ВЖК в цитозоле: синтез ацил-СоА (не путайте с ацетил-СоА) ВЖК попадают в цитозоль через плазматическую
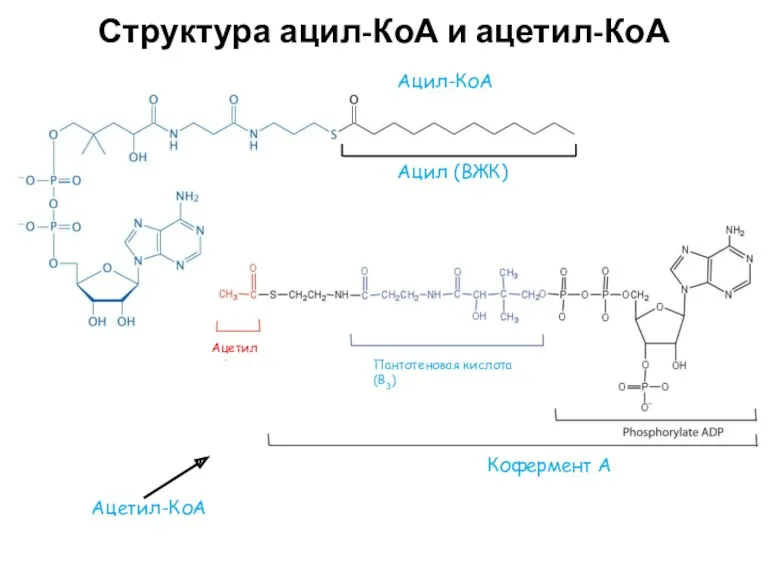
- 12. Структура ацил-КоА и ацетил-КоА Ацил-КоА Ацил (ВЖК) Кофермент А Пантотеновая кислота (В3) Ацетил Ацетил-КоА
- 13. Транспорт ВЖК в митохондрию при участии карнитина Ферменты: карнитин-ацилтрансфераза 1 и 2. 1-я находится в цитозоле
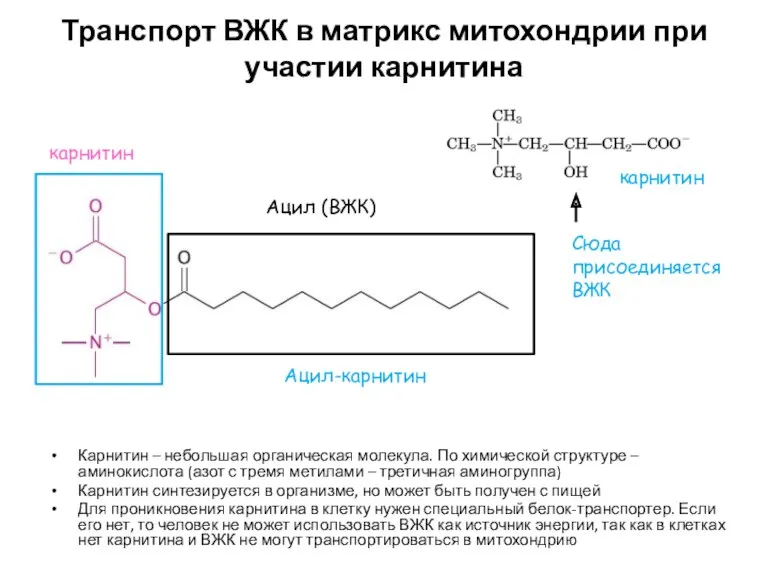
- 14. Транспорт ВЖК в матрикс митохондрии при участии карнитина Карнитин – небольшая органическая молекула. По химической структуре
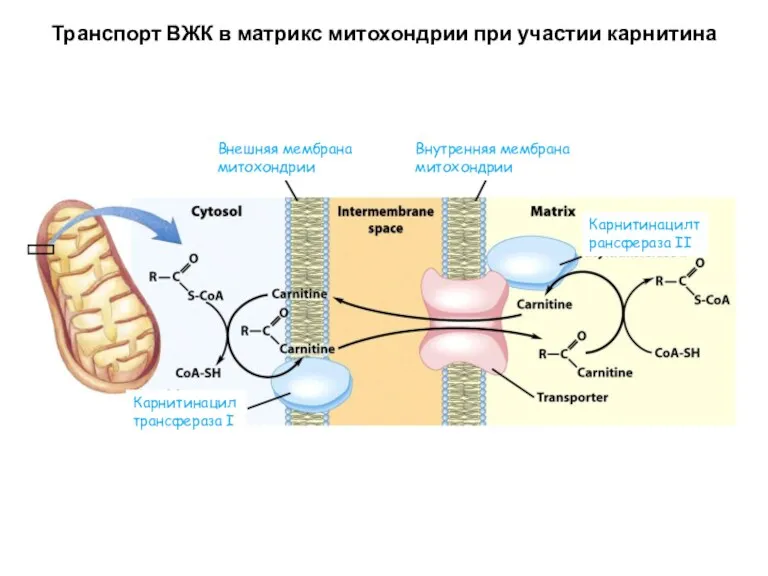
- 15. Транспорт ВЖК в матрикс митохондрии при участии карнитина Внешняя мембрана митохондрии Внутренняя мембрана митохондрии Карнитинацилтрансфераза I
- 16. Собственно β-окисление в матриксе митохондрии Последовательное отщепление 2С-фрагмента (ацетил-КоА) от ацил-КоА (ВЖК), начиная от карбоксильной группы
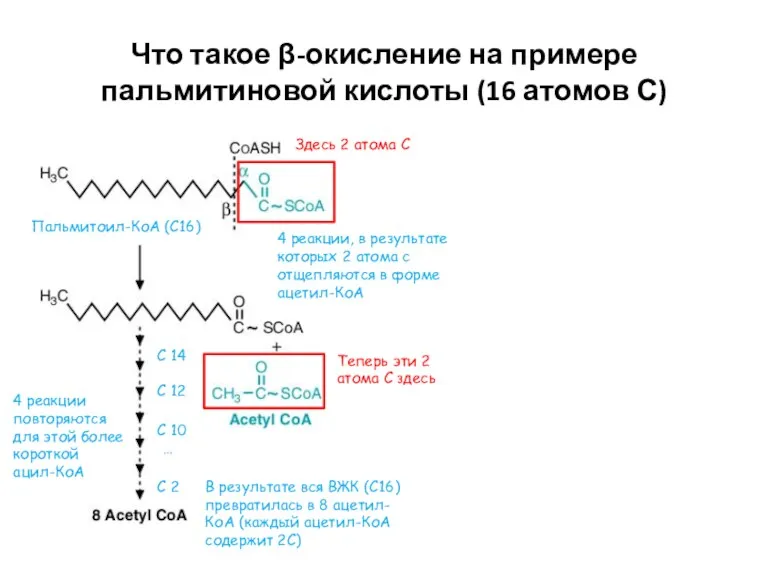
- 17. Что такое β-окисление на примере пальмитиновой кислоты (16 атомов С) Пальмитоил-КоА (С16) 4 реакции, в результате
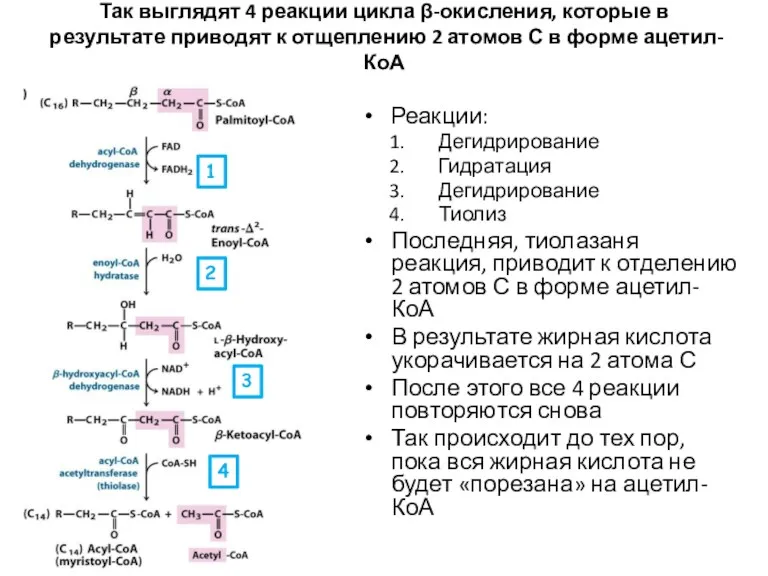
- 18. Так выглядят 4 реакции цикла β-окисления, которые в результате приводят к отщеплению 2 атомов С в
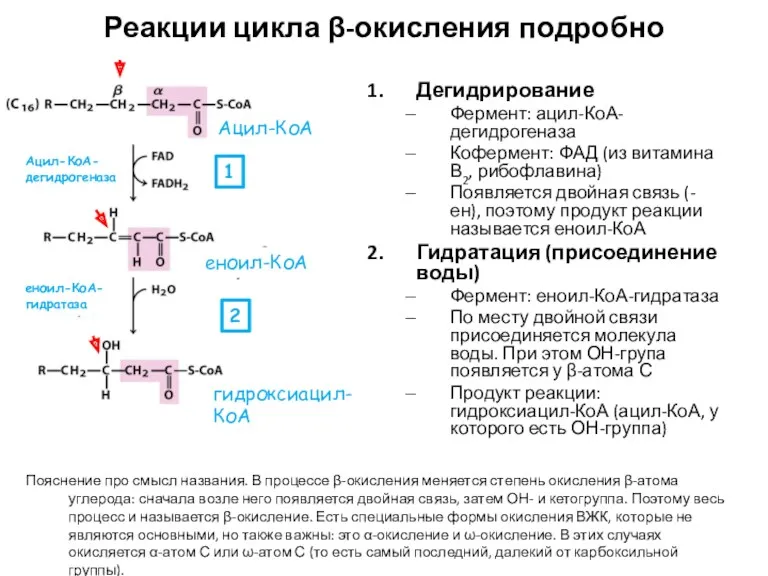
- 19. Реакции цикла β-окисления подробно Дегидрирование Фермент: ацил-КоА-дегидрогеназа Кофермент: ФАД (из витамина В2, рибофлавина) Появляется двойная связь
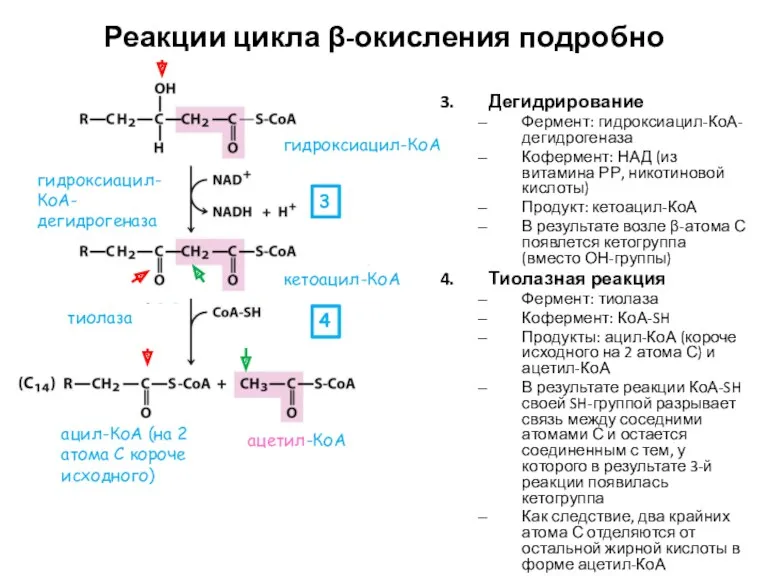
- 20. Реакции цикла β-окисления подробно Дегидрирование Фермент: гидроксиацил-КоА-дегидрогеназа Кофермент: НАД (из витамина РР, никотиновой кислоты) Продукт: кетоацил-КоА
- 21. Особенности β-окисления ненасыщенных ВЖК β-окисление происходит как обычно до тех пор, пока очередь не дойдет до
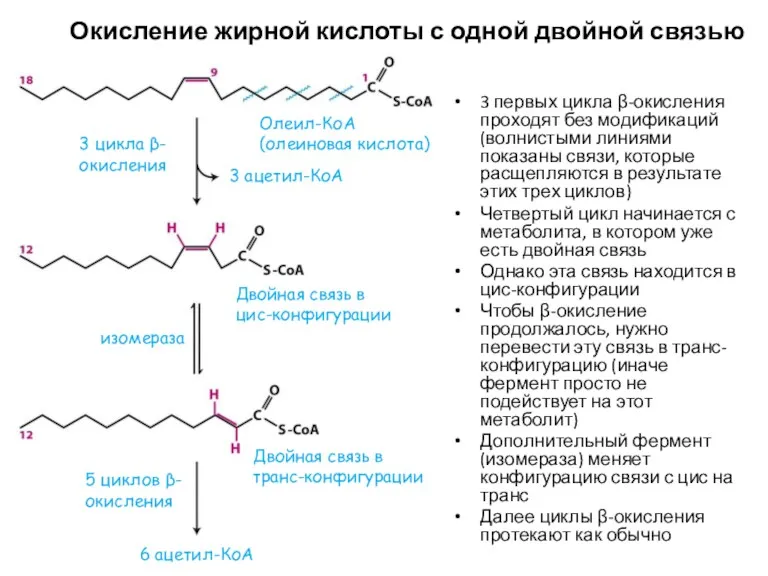
- 22. Окисление жирной кислоты с одной двойной связью 3 первых цикла β-окисления проходят без модификаций (волнистыми линиями
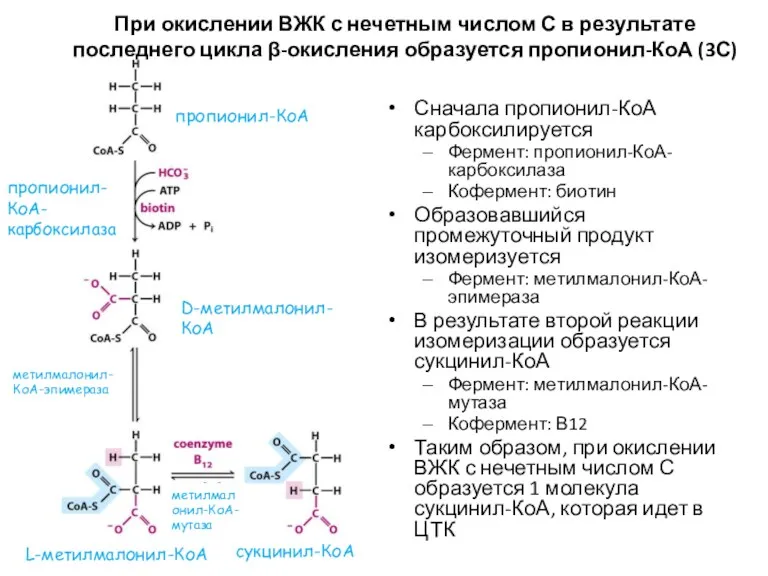
- 23. Особенности β-окисления ВЖК с нечетным числом С При β-окислении ВЖК с четным числом С в результате
- 24. Сначала пропионил-КоА карбоксилируется Фермент: пропионил-КоА-карбоксилаза Кофермент: биотин Образовавшийся промежуточный продукт изомеризуется Фермент: метилмалонил-КоА-эпимераза В результате второй
- 25. СИНТЕЗ ВЖК
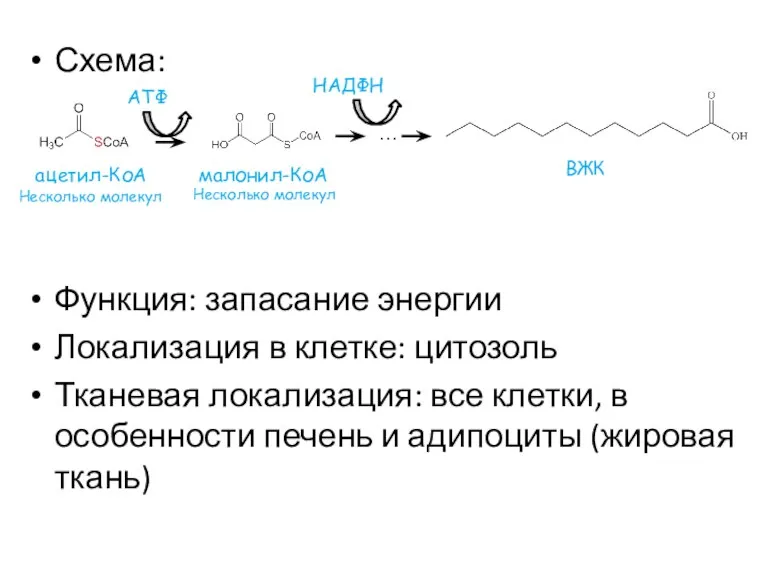
- 26. Схема: Функция: запасание энергии Локализация в клетке: цитозоль Тканевая локализация: все клетки, в особенности печень и
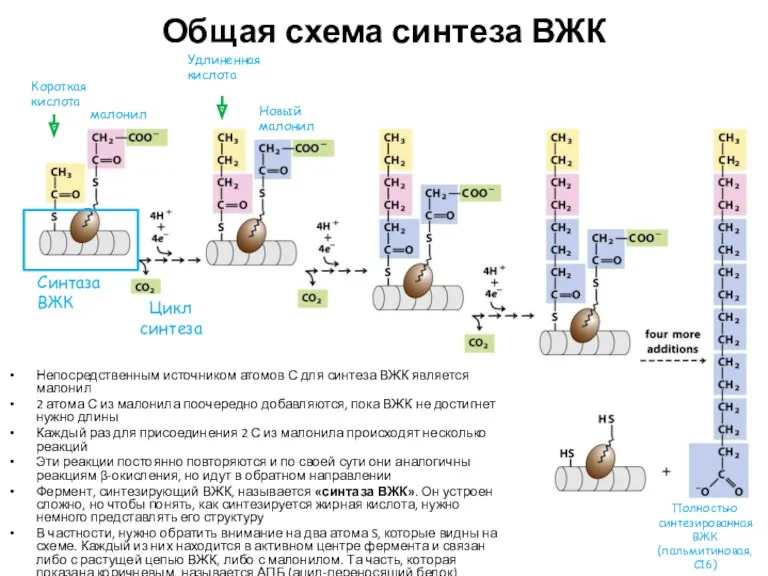
- 27. Общая схема синтеза ВЖК Синтаза ВЖК Короткая кислота малонил Цикл синтеза Удлиненная кислота Новый малонил Непосредственным
- 28. Этапы Превращение ацетил-КоА в малонил-КоА (карбоксилирование = присоединение карбоксильной группы): Фермент: ацетил-КоА-карбоксилаза (регуляторный фермент синтеза ВЖК)
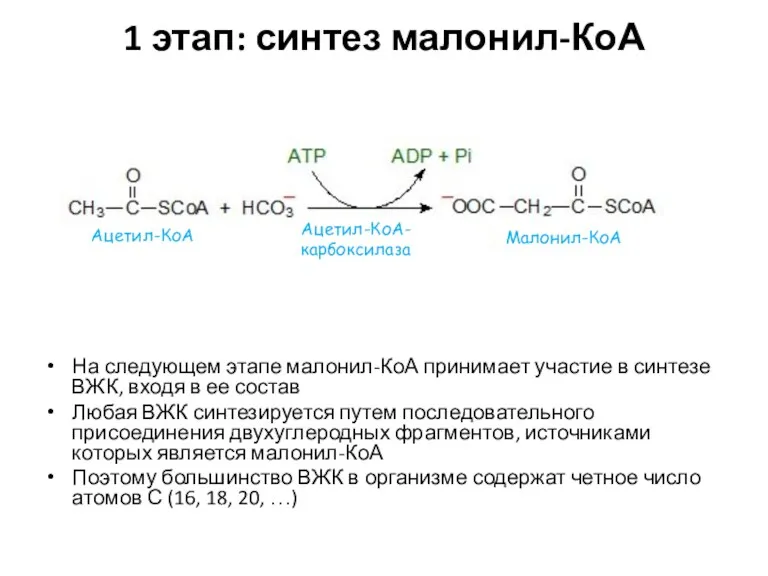
- 29. 1 этап: синтез малонил-КоА На следующем этапе малонил-КоА принимает участие в синтезе ВЖК, входя в ее
- 30. Присоединение малонил-КоА к растущей цепи жирной кислоты и дальнейшие реакции Фермент: синтаза ВЖК. Состоит из нескольких
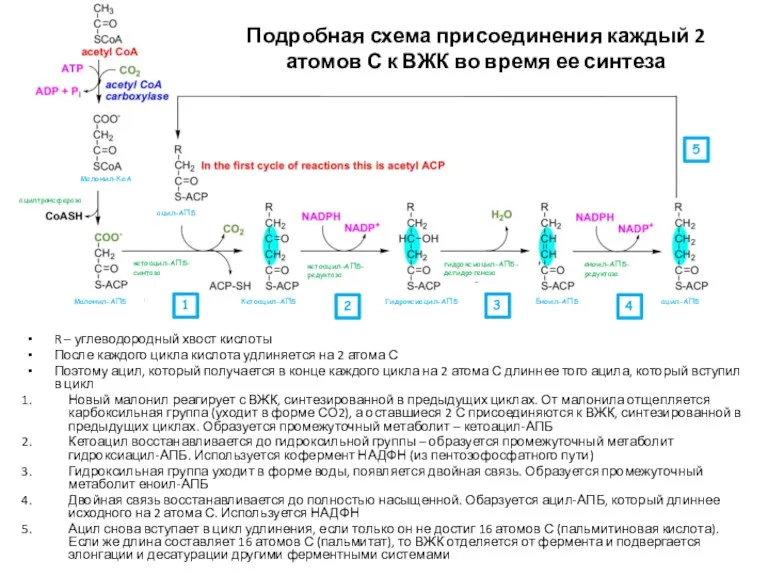
- 31. R – углеводородный хвост кислоты После каждого цикла кислота удлиняется на 2 атома С Поэтому ацил,
- 32. Элонгация и десатурация (синтез более длинных и ненасыщенных ВЖК) Элонгация (удлинение) происходит в митохондриях и гладком
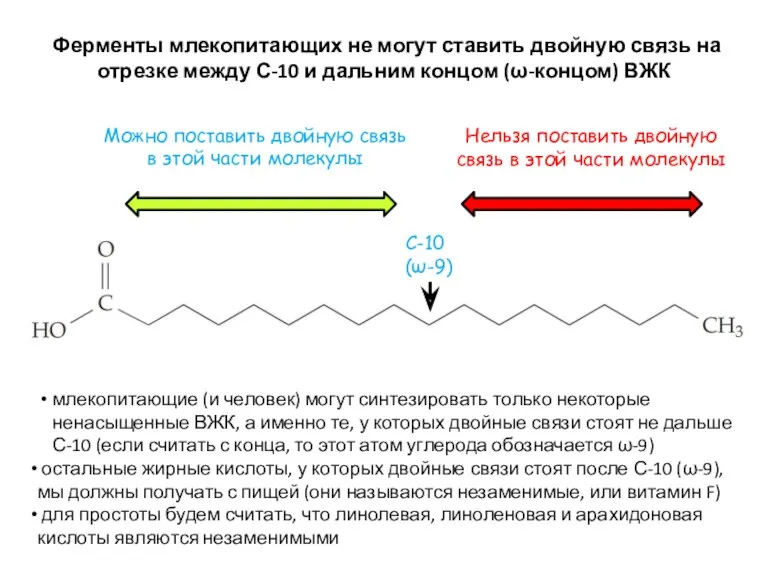
- 33. Ферменты млекопитающих не могут ставить двойную связь на отрезке между С-10 и дальним концом (ω-концом) ВЖК
- 34. Дополнение Источники ацетил-КоА для синтеза ВЖК Источники НАДФ (и сравнение НАДФН и НАДН)
- 35. Источники ацетил-КоА для синтеза ВЖК Откуда такой вопрос? Дело в том, что синтез ВЖК происходит в
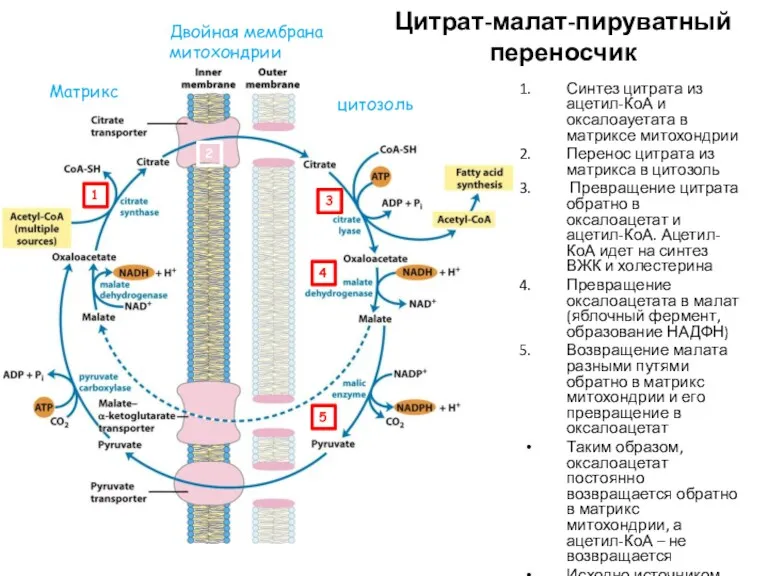
- 36. Синтез цитрата из ацетил-КоА и оксалоауетата в матриксе митохондрии Перенос цитрата из матрикса в цитозоль Превращение
- 37. Источники НАДФ (и сравнение НАДФН и НАДН) Что такое: НАДФН = никотинамидадениндинуклеотидфосфат, из витамина РР (никотиновая
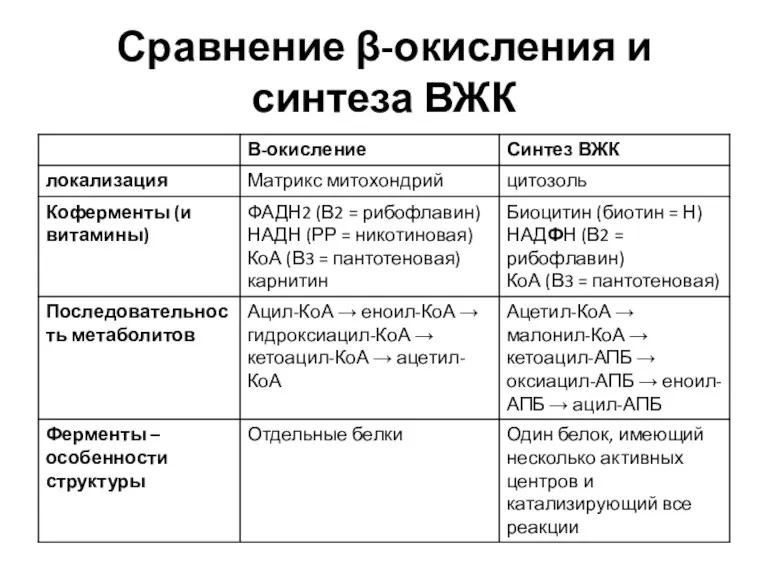
- 38. Сравнение β-окисления и синтеза ВЖК
- 39. СИНТЕЗ ХОЛЕСТЕРИНА
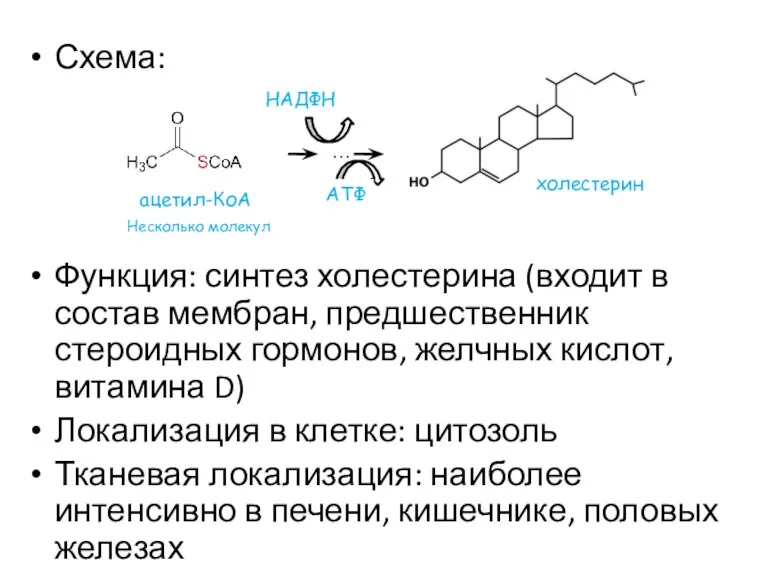
- 40. Схема: Функция: синтез холестерина (входит в состав мембран, предшественник стероидных гормонов, желчных кислот, витамина D) Локализация
- 41. Основной принцип Последовательное соединение молекул, содержащих небольшое количество атомов С На каждом этапе количество атомов С
- 42. 4 этапа синтеза холестерина Синтез мевалоновой кислоты Исходное вещество – ацетил-КоА Используется НАДФН Регуляторный фермент –
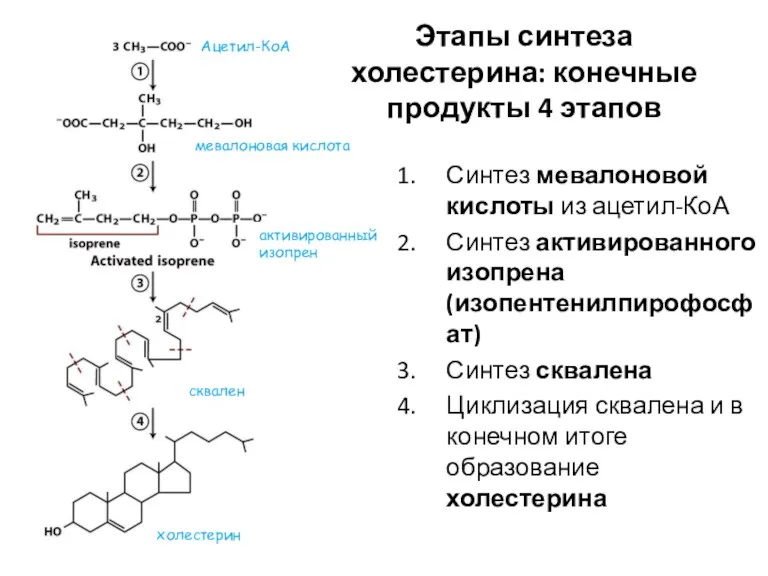
- 43. Этапы синтеза холестерина: конечные продукты 4 этапов Синтез мевалоновой кислоты из ацетил-КоА Синтез активированного изопрена (изопентенилпирофосфат)
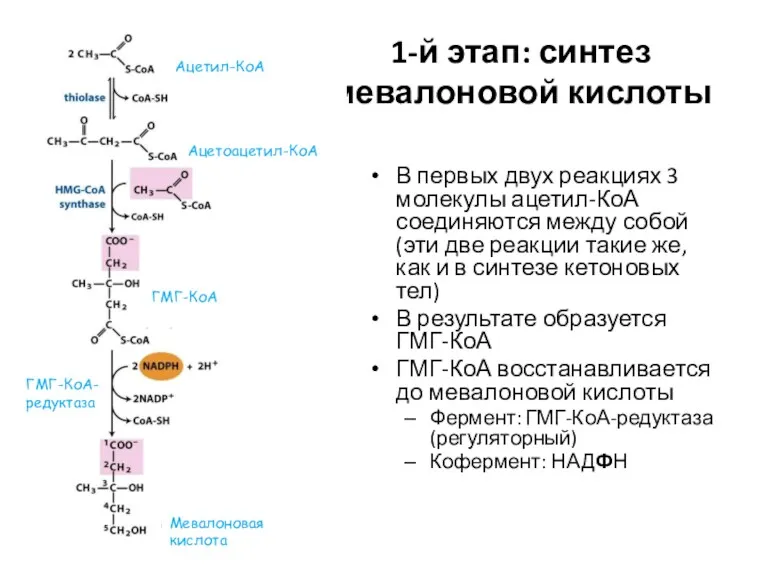
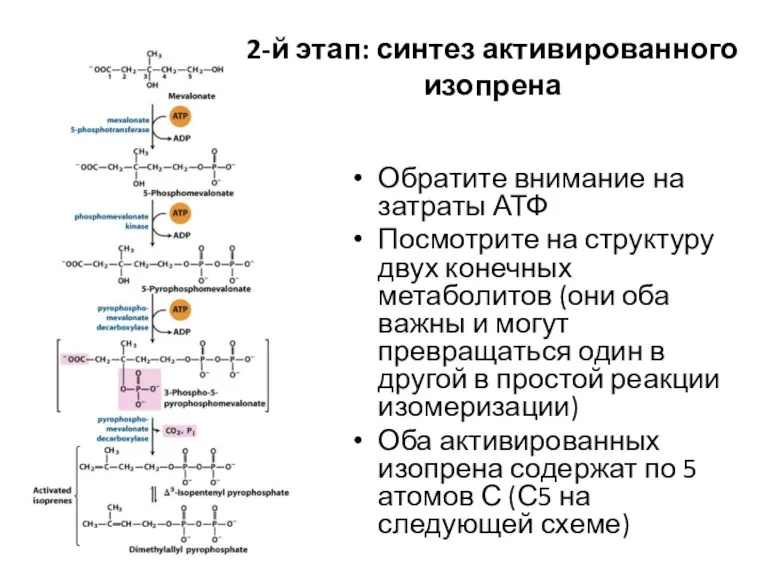
- 44. 1-й этап: синтез мевалоновой кислоты В первых двух реакциях 3 молекулы ацетил-КоА соединяются между собой (эти
- 45. Обратите внимание на затраты АТФ Посмотрите на структуру двух конечных метаболитов (они оба важны и могут
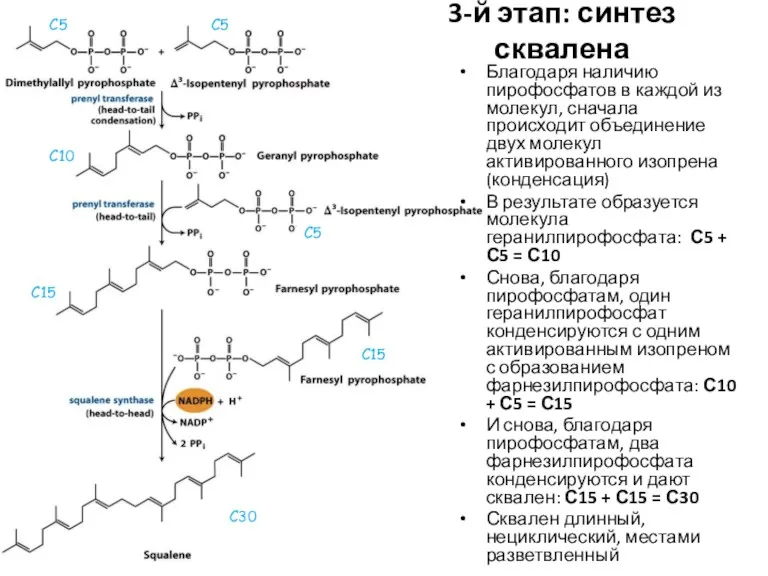
- 46. 3-й этап: синтез сквалена Благодаря наличию пирофосфатов в каждой из молекул, сначала происходит объединение двух молекул
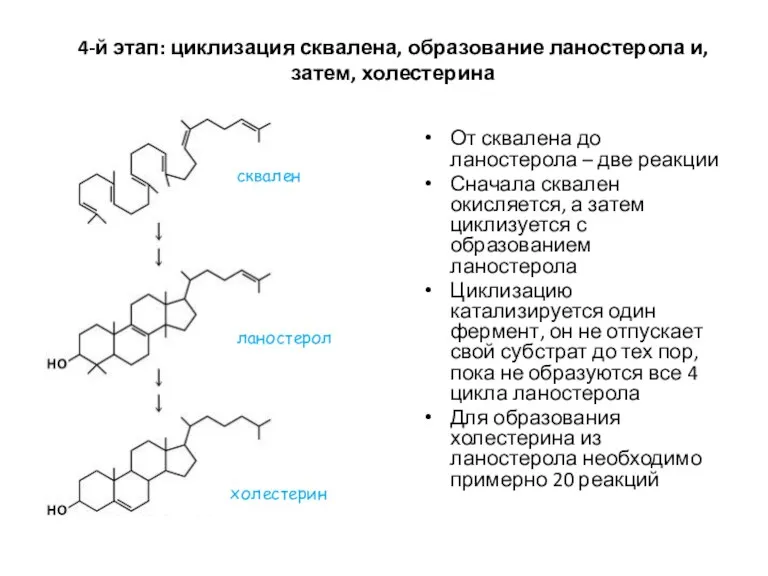
- 47. От сквалена до ланостерола – две реакции Сначала сквален окисляется, а затем циклизуется с образованием ланостерола
- 48. КЕТОНОВЫЕ (АЦЕТОНОВЫЕ) ТЕЛА
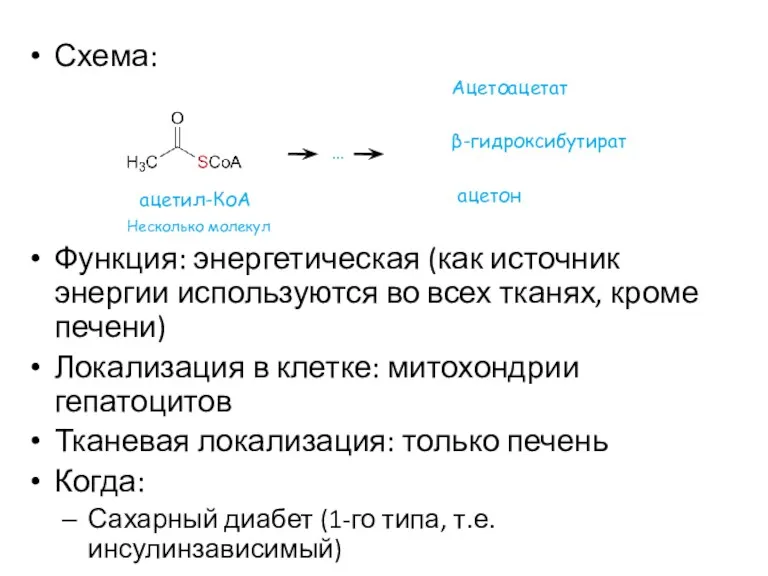
- 49. Схема: Функция: энергетическая (как источник энергии используются во всех тканях, кроме печени) Локализация в клетке: митохондрии
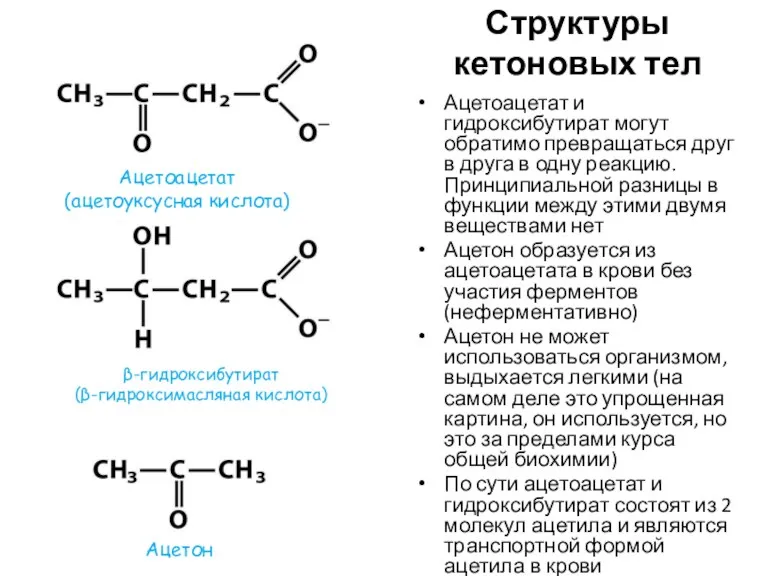
- 50. Структуры кетоновых тел Ацетоацетат и гидроксибутират могут обратимо превращаться друг в друга в одну реакцию. Принципиальной
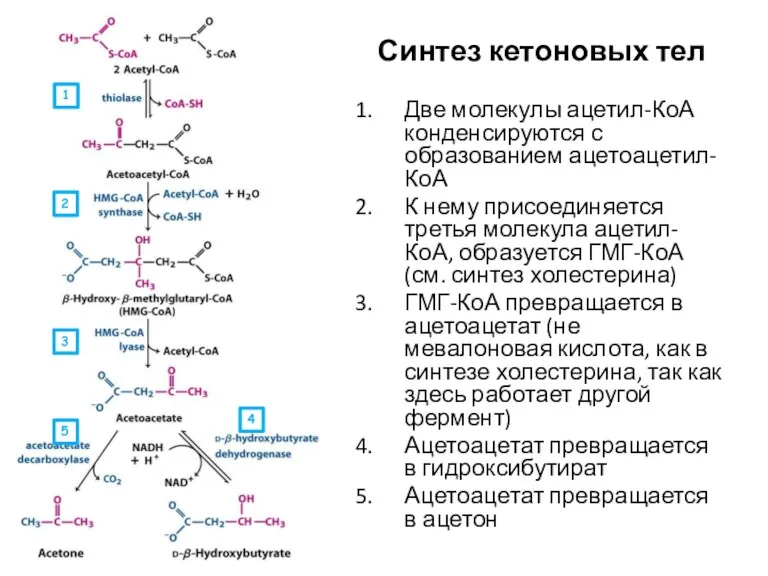
- 51. Синтез кетоновых тел Две молекулы ацетил-КоА конденсируются с образованием ацетоацетил-КоА К нему присоединяется третья молекула ацетил-КоА,
- 52. Условия образования кетоновых тел в печени Усиление β-окисления приводит к образованию большого количества ацетил-КоА Так как
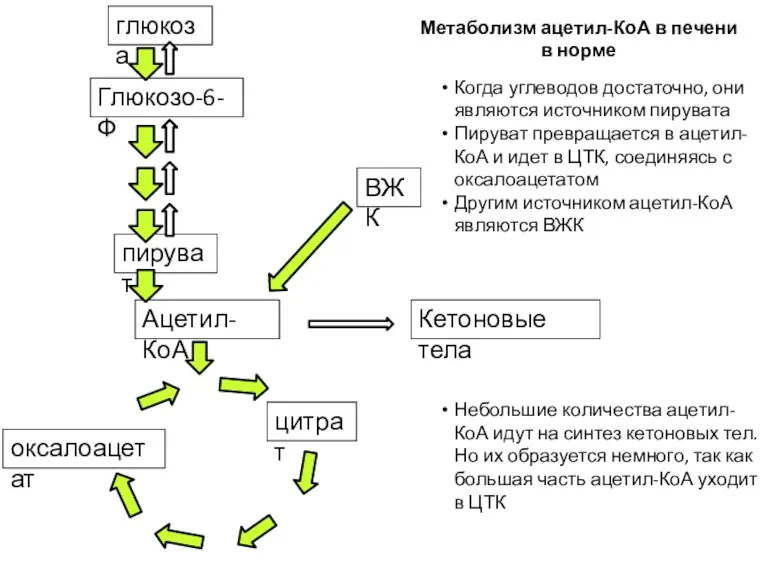
- 53. Ацетил-КоА пируват глюкоза Глюкозо-6-Ф Кетоновые тела ВЖК цитрат оксалоацетат Метаболизм ацетил-КоА в печени в норме Когда
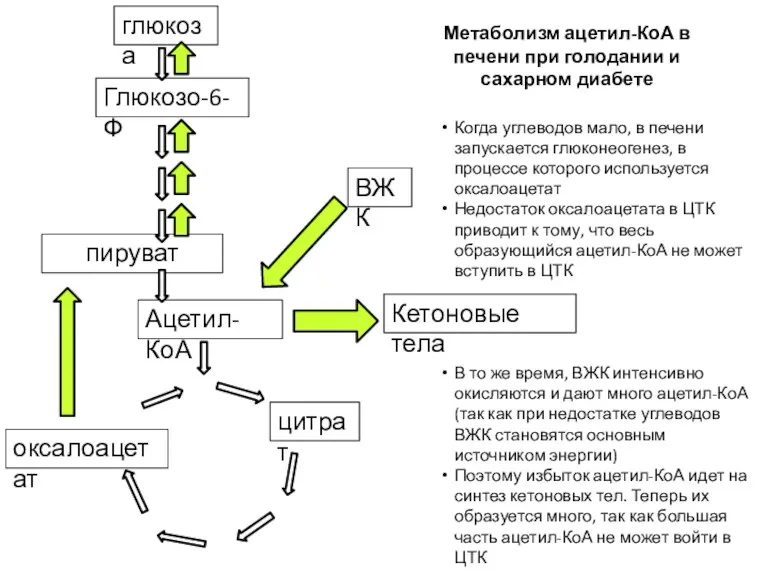
- 54. Ацетил-КоА пируват глюкоза Глюкозо-6-Ф Кетоновые тела ВЖК цитрат оксалоацетат Метаболизм ацетил-КоА в печени при голодании и
- 55. Использование кетоновых тел Из печени кетоновые тела (ацетоацетат и β-гидроксибутират) выделяются в кровь В крови ацетоацетат
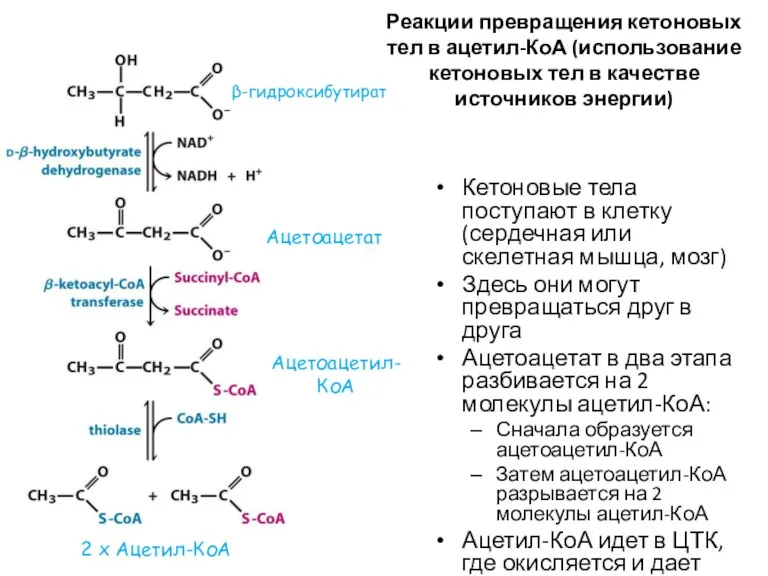
- 56. Реакции превращения кетоновых тел в ацетил-КоА (использование кетоновых тел в качестве источников энергии) Кетоновые тела поступают
- 57. СИНТЕЗ ГЛИЦЕРОФОСФОЛИПИДОВ И ТРИАЦИЛГЛИЦЕРОЛОВ
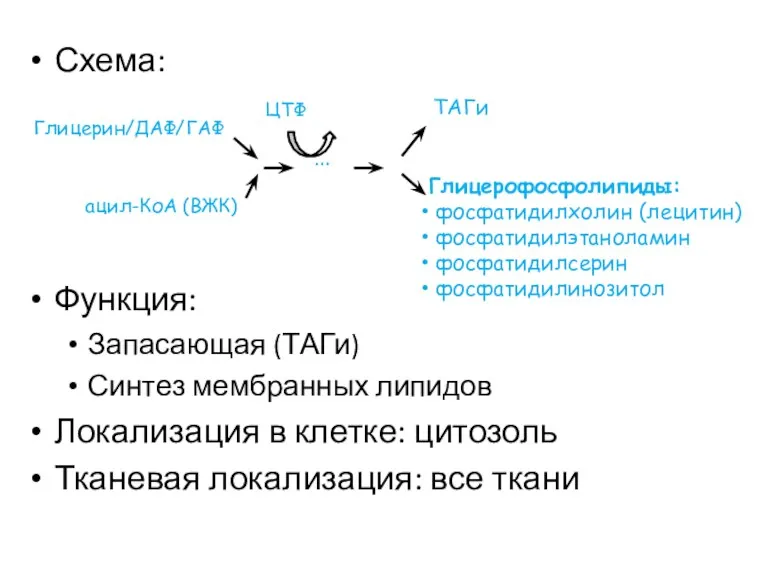
- 58. Схема: Функция: Запасающая (ТАГи) Синтез мембранных липидов Локализация в клетке: цитозоль Тканевая локализация: все ткани ацил-КоА
- 59. Источники глицериновой части в молекулах глицеролипидов: Глицерин (только в печени, где он может быть фосфорилирован глицеролкиназой)
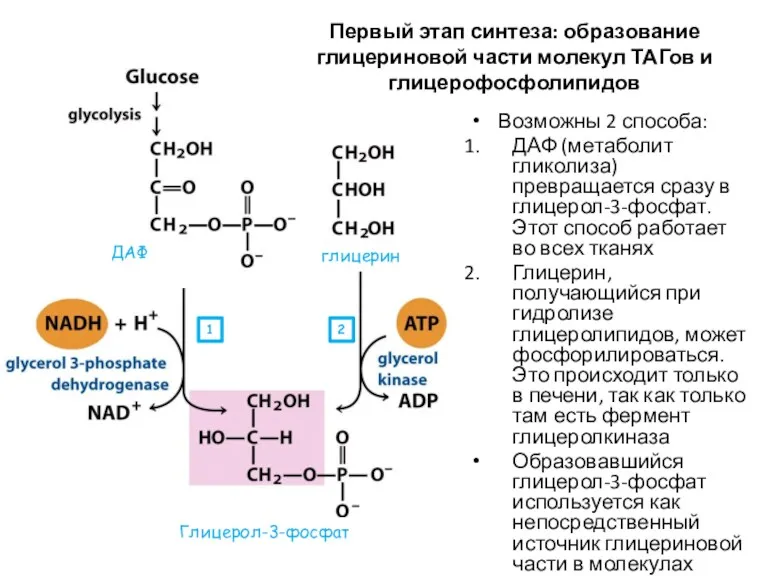
- 60. Первый этап синтеза: образование глицериновой части молекул ТАГов и глицерофосфолипидов Возможны 2 способа: ДАФ (метаболит гликолиза)
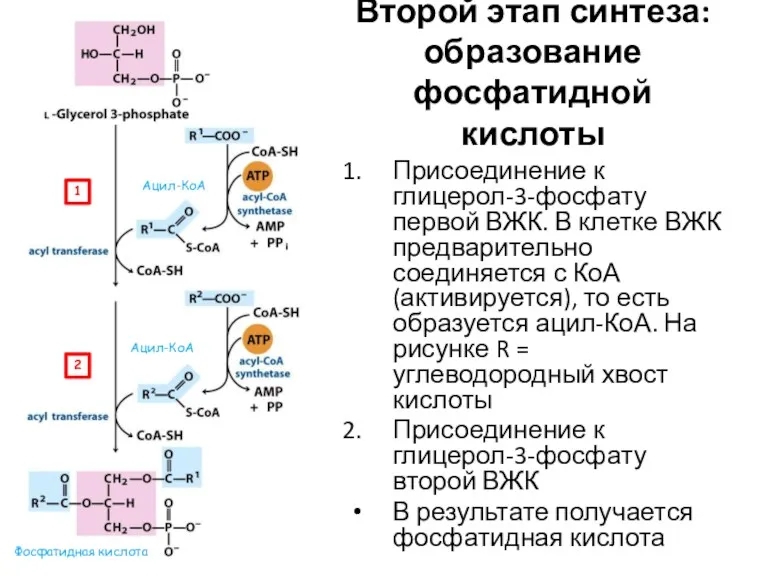
- 61. Второй этап синтеза: образование фосфатидной кислоты Присоединение к глицерол-3-фосфату первой ВЖК. В клетке ВЖК предварительно соединяется
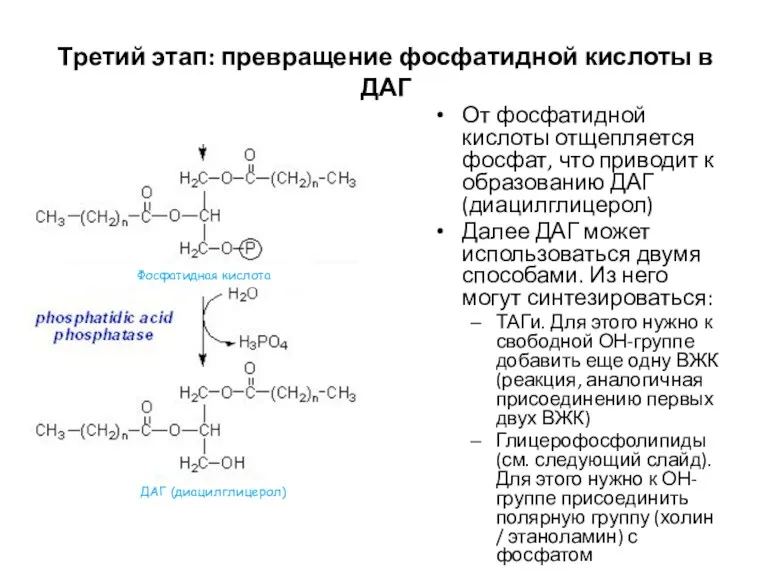
- 62. Третий этап: превращение фосфатидной кислоты в ДАГ От фосфатидной кислоты отщепляется фосфат, что приводит к образованию
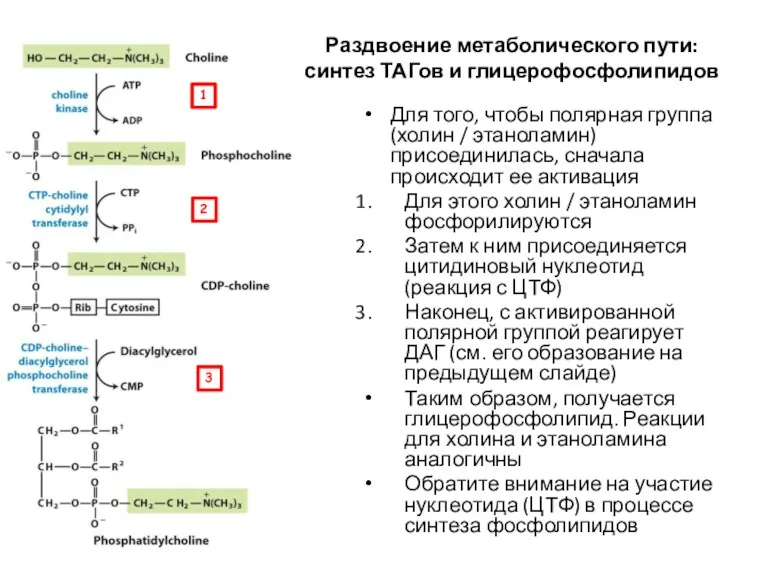
- 63. Раздвоение метаболического пути: синтез ТАГов и глицерофосфолипидов Для того, чтобы полярная группа (холин / этаноламин) присоединилась,
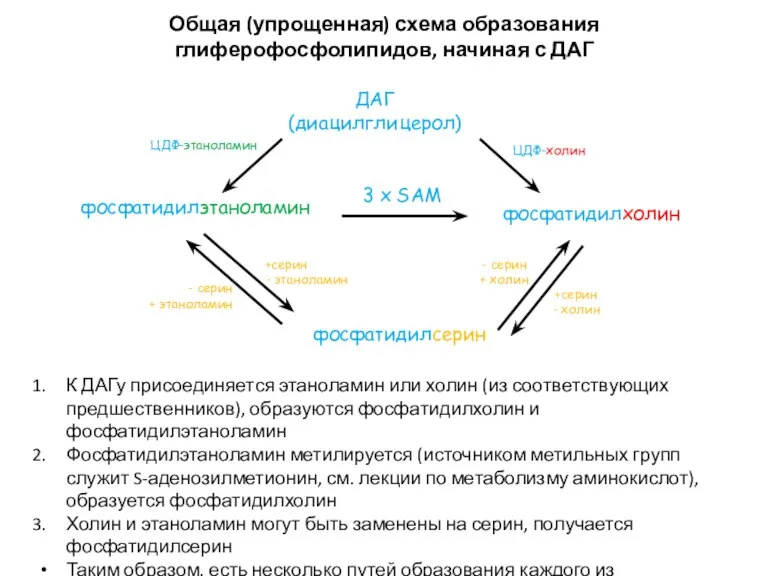
- 64. - серин + этаноламин - серин + холин +серин - холин +серин - этаноламин Общая (упрощенная)
- 65. ТРАНСПОРТ ЛИПИДОВ В ОРГАНИЗМЕ
- 66. Липопротеины (ЛП) Простые липиды, например ВЖК, могут транспортироваться в крови в комплексе с альбумином. Но для
- 67. Структура ЛП По форме – везикулы (пузырьки, шарики) Снаружи – оболочка из одного слоя фосфолипидов (полярная
- 68. Липопротеин – другая форма транспорта ВЖК (и вообще липидов) в крови Внутри липопротеина находятся ВЖК и
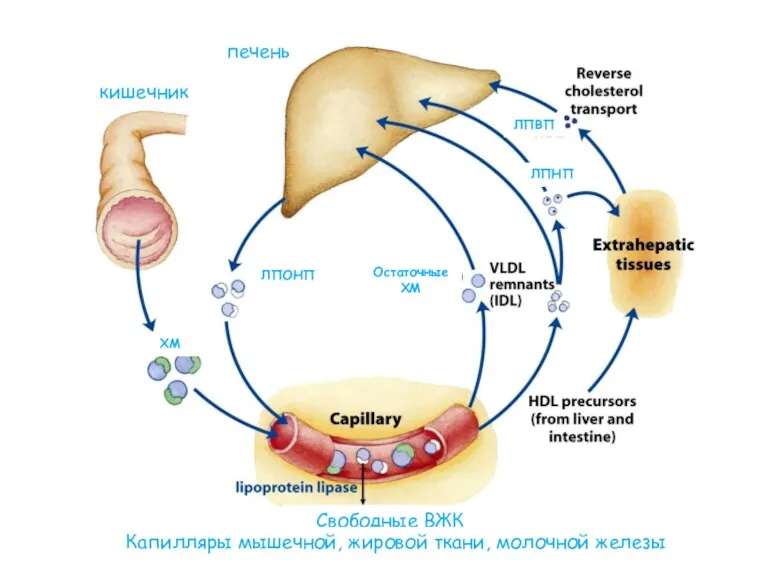
- 69. Типы ЛП ХМ (хиломикроны): транспорт липидов из кишечника в ткани (прежде всего, жировую и мышечную). Образуются
- 70. печень кишечник Свободные ВЖК Капилляры мышечной, жировой ткани, молочной железы ХМ ЛПОНП Остаточные ХМ ЛПНП ЛПВП
- 71. Роль в развитии атеросклероза Атерогенные («плохой холестерин»): ЛПОНП и ЛПНП. При увеличении их концентрации увеличивается вероятность
- 72. ЭЙКОЗАНОИДЫ
- 73. Гормоноподобные вещества, синтезируемые из арахидоновой кислоты (С20:4). В структуре есть атом О, циклы и двойные связи
- 74. Синтез Арахидоновая кислота не содержится в клетках в свободном виде, а входит в состав фософлипидов мембраны.
- 76. Скачать презентацию
































 Красная Книга Ростовской области
Красная Книга Ростовской области Механизмы биоэлектрогенеза
Механизмы биоэлектрогенеза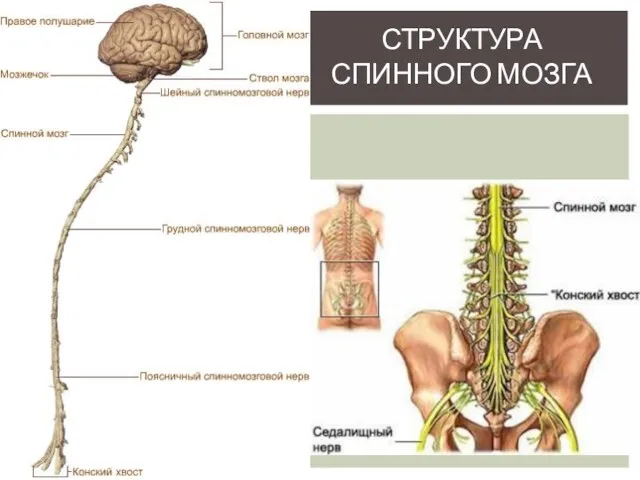 Структура спинного мозга
Структура спинного мозга Обеспечение клеток энергией
Обеспечение клеток энергией Строение и жизнедеятельность бактерий
Строение и жизнедеятельность бактерий Бактериология. Классификация бактерий. Морфология бактерий и методы её изучения. (Лекция 9)
Бактериология. Классификация бактерий. Морфология бактерий и методы её изучения. (Лекция 9) Физиология сердца. (Лекция 5.1)
Физиология сердца. (Лекция 5.1) Отряд Киты
Отряд Киты Межвидовые отношения организмов
Межвидовые отношения организмов Эволюция ОДС (опорно-двигательной системы)
Эволюция ОДС (опорно-двигательной системы) Строение семян однодольных и двудольных растений. Морфология проростка. Прорастание семян
Строение семян однодольных и двудольных растений. Морфология проростка. Прорастание семян Предмет и структура ихтиологической науки
Предмет и структура ихтиологической науки Цветы в легендах, поэзии, музыке
Цветы в легендах, поэзии, музыке ВНД человека. Вторая сигнальная система
ВНД человека. Вторая сигнальная система Морфология. Общие понятия
Морфология. Общие понятия Конструкции, обогрев и эксплуатация сооружений защищенного грунта
Конструкции, обогрев и эксплуатация сооружений защищенного грунта Жизнедеятельность клетки
Жизнедеятельность клетки Natural selection of human population. Darwin’s theory of evolution by natural selection
Natural selection of human population. Darwin’s theory of evolution by natural selection Антропогенез. Расы. Расизм. Часть 4
Антропогенез. Расы. Расизм. Часть 4 Бактерии
Бактерии Потребности и интересы. Уровень развития способностей человека
Потребности и интересы. Уровень развития способностей человека Динозавры
Динозавры Пищеварительная система
Пищеварительная система Физиология спорта. Физиологические основы классификации физических упражнений
Физиология спорта. Физиологические основы классификации физических упражнений Презентация к выступлению на научной конференции Совершенствование естественнонаучного школьного образования
Презентация к выступлению на научной конференции Совершенствование естественнонаучного школьного образования Клубеньковые долгоносики. Гороховая зерновка
Клубеньковые долгоносики. Гороховая зерновка Типы кожи лица. Уход за сухой кожей
Типы кожи лица. Уход за сухой кожей Как животные пустынь получают воду
Как животные пустынь получают воду