Молекулярные механизмы регуляции поведения. Аминокислоты как медиаторы. Ацетилхолин. (Лекция 4) презентация
Содержание
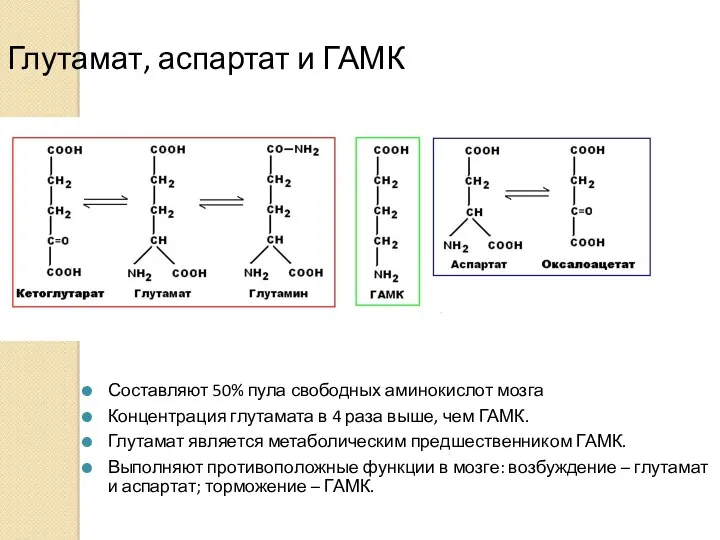
- 2. Глутамат, аспартат и ГАМК Составляют 50% пула свободных аминокислот мозга Концентрация глутамата в 4 раза выше,
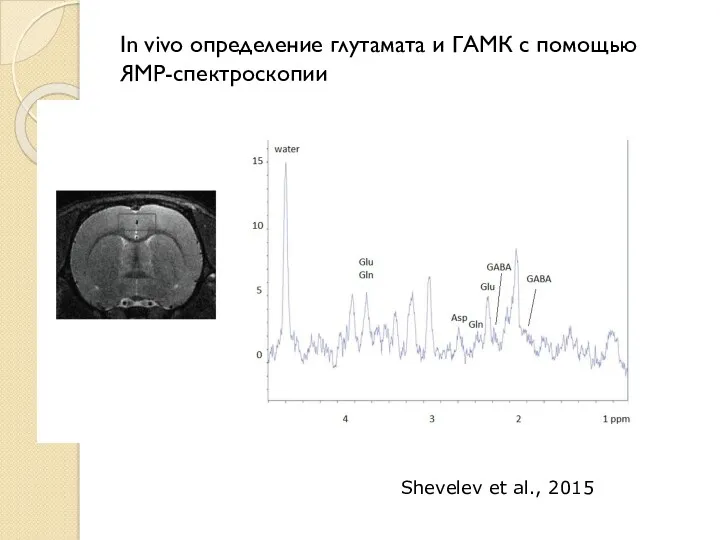
- 3. In vivo определение глутамата и ГАМК с помощью ЯМР-спектроскопии Shevelev et al., 2015
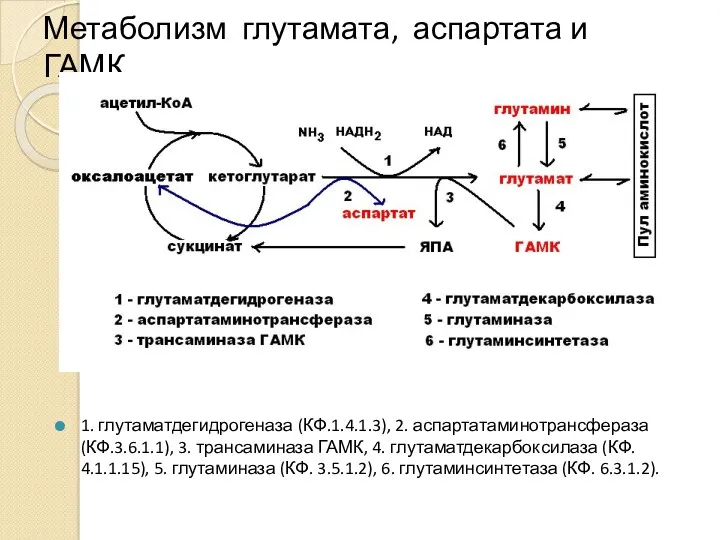
- 4. Метаболизм глутамата, аспартата и ГАМК 1. глутаматдегидрогеназа (КФ.1.4.1.3), 2. аспартатаминотрансфераза (КФ.3.6.1.1), 3. трансаминаза ГАМК, 4. глутаматдекарбоксилаза
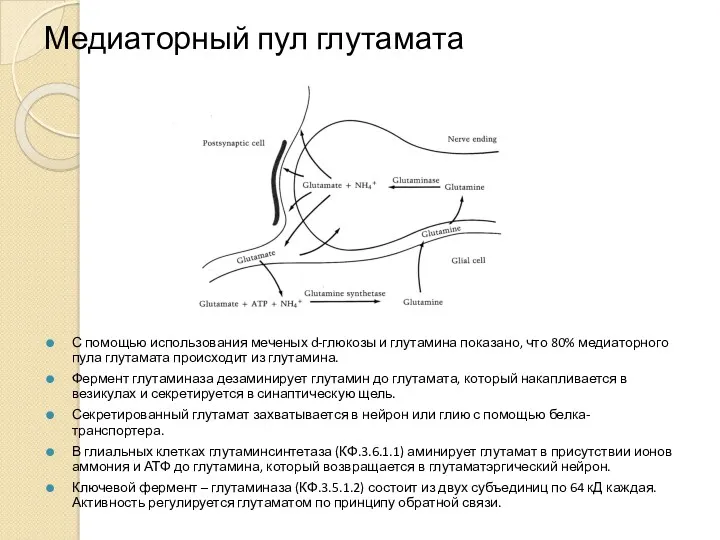
- 5. Медиаторный пул глутамата С помощью использования меченых d-глюкозы и глутамина показано, что 80% медиаторного пула глутамата
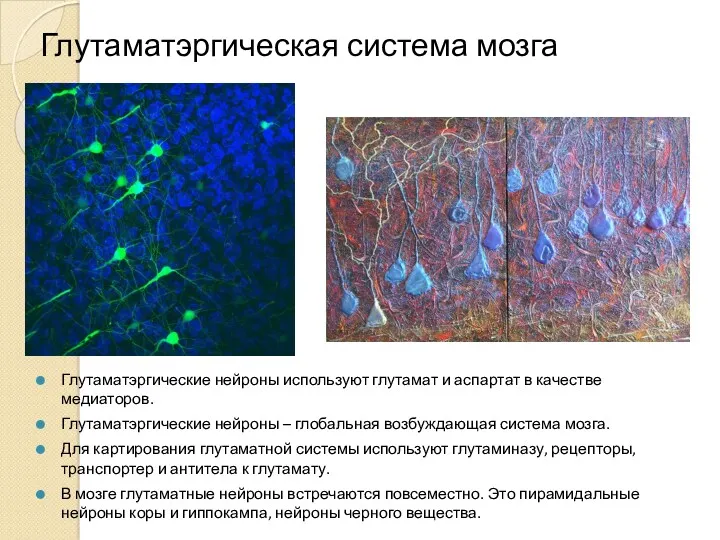
- 6. Глутаматэргическая система мозга Глутаматэргические нейроны используют глутамат и аспартат в качестве медиаторов. Глутаматэргические нейроны – глобальная
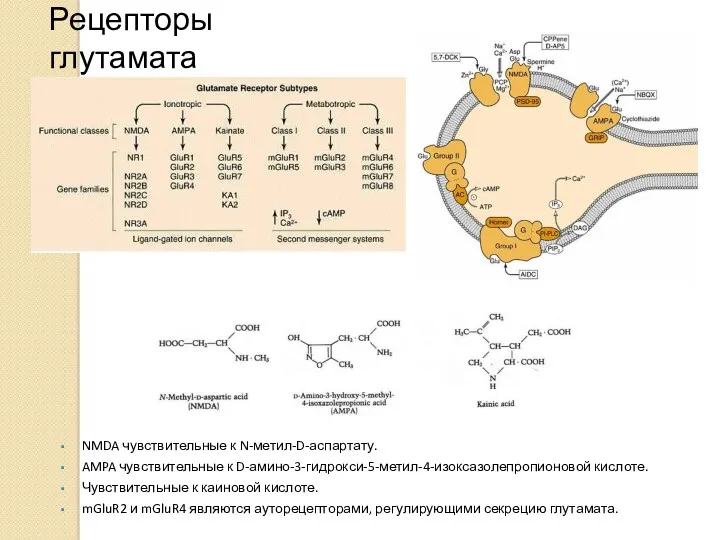
- 7. Рецепторы глутамата NMDA чувствительные к N-метил-D-аспартату. AMPA чувствительные к D-амино-3-гидрокси-5-метил-4-изоксазолепропионовой кислоте. Чувствительные к каиновой кислоте. mGluR2
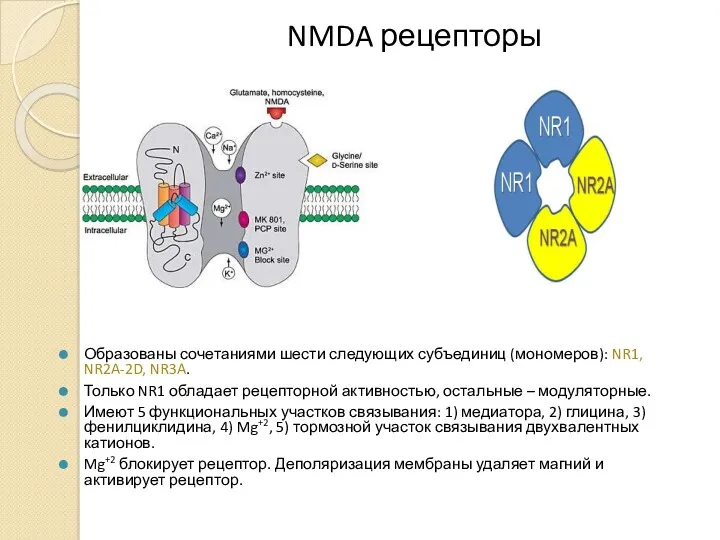
- 8. NMDA рецепторы Образованы сочетаниями шести следующих субъединиц (мономеров): NR1, NR2A-2D, NR3A. Только NR1 обладает рецепторной активностью,
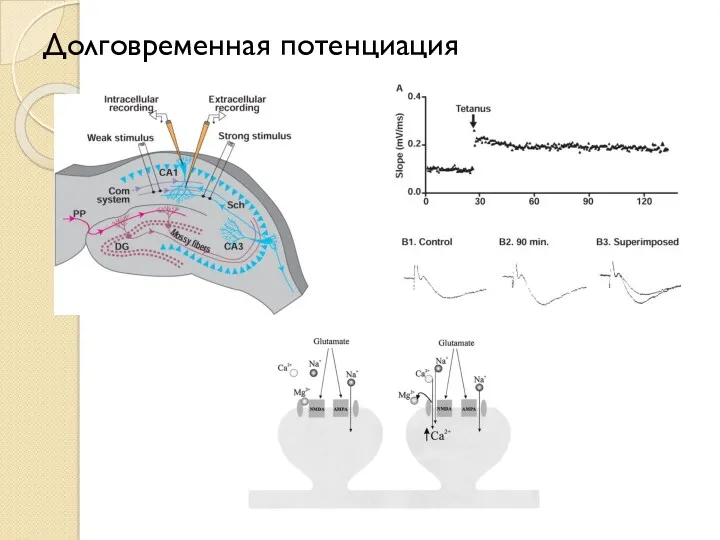
- 9. Долговременная потенциация
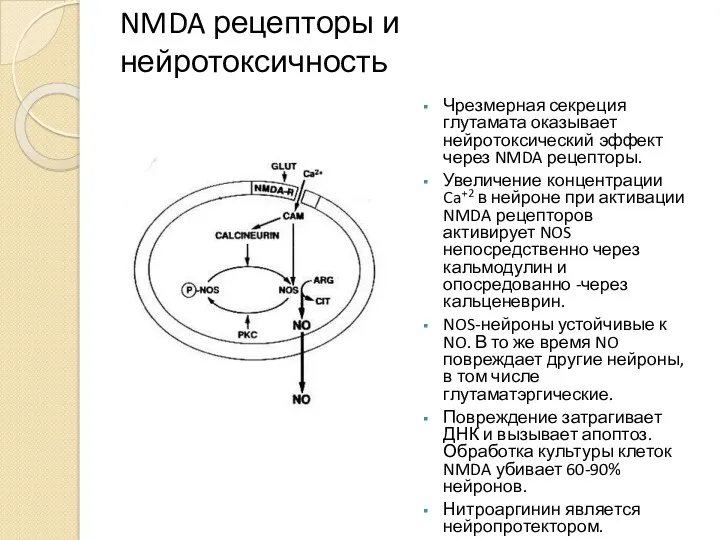
- 10. NMDA рецепторы и нейротоксичность Чрезмерная секреция глутамата оказывает нейротоксический эффект через NMDA рецепторы. Увеличение концентрации Ca+2
- 11. Выводы Глутаматные нейроны – глобальная активирующая система мозга. Вызывает активацию нейронов через NMDA и AMPA рецепторы.
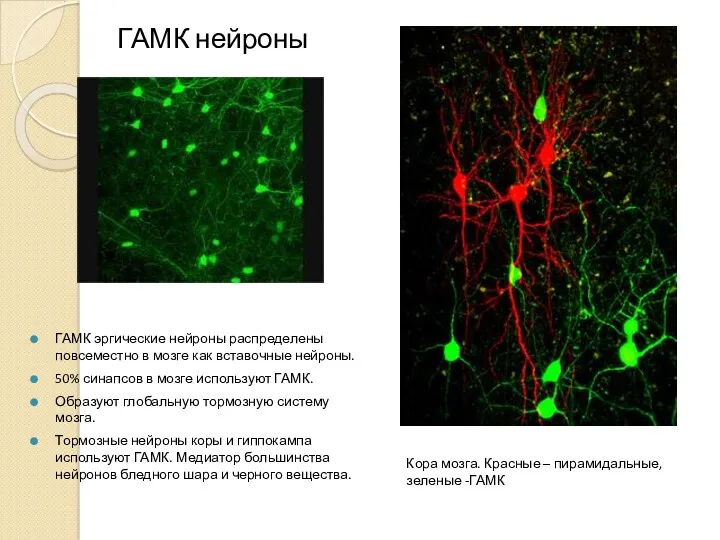
- 12. ГАМК нейроны ГАМК эргические нейроны распределены повсеместно в мозге как вставочные нейроны. 50% синапсов в мозге
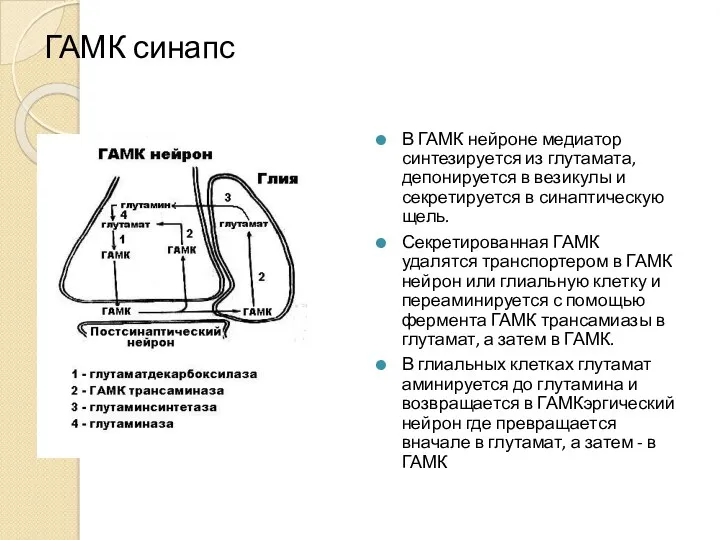
- 13. ГАМК синапс В ГАМК нейроне медиатор синтезируется из глутамата, депонируется в везикулы и секретируется в синаптическую
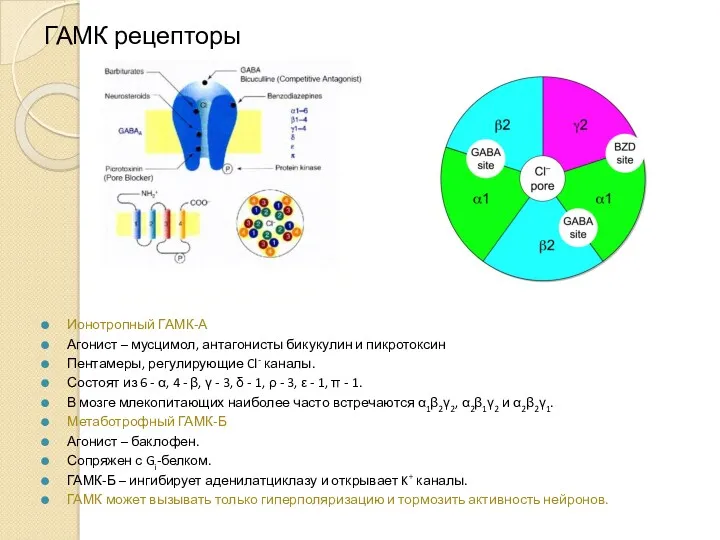
- 14. ГАМК рецепторы Ионотропный ГАМК-А Агонист – мусцимол, антагонисты бикукулин и пикротоксин Пентамеры, регулирующие Cl- каналы. Состоят
- 15. Бензодиазепины Бензодиазепины большая группа веществ с успокаивающим, анксиолитическим и седативным действием (диазепам, клоназепам, нитразепам). Соединяясь со
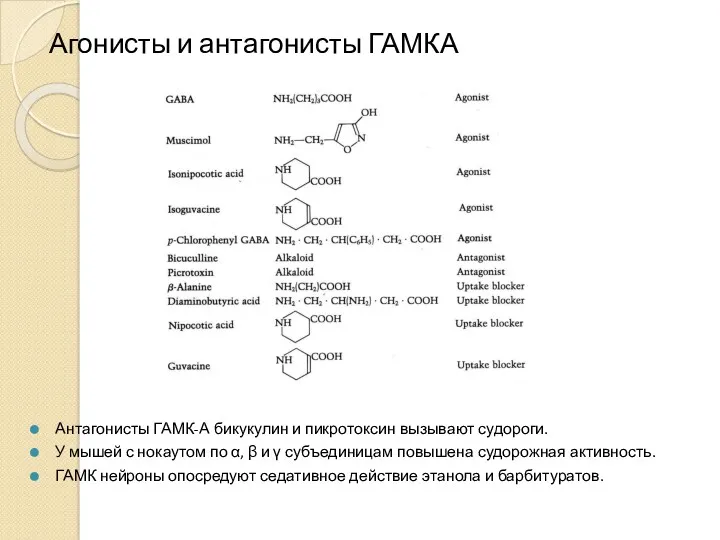
- 16. Агонисты и антагонисты ГАМКА Антагонисты ГАМК-А бикукулин и пикротоксин вызывают судороги. У мышей с нокаутом по
- 17. Выводы ГАМК система одна из самых экспансивных – 50% синапсов являются ГАМКэргическими. ГАМК нейроны осуществляют глобальное
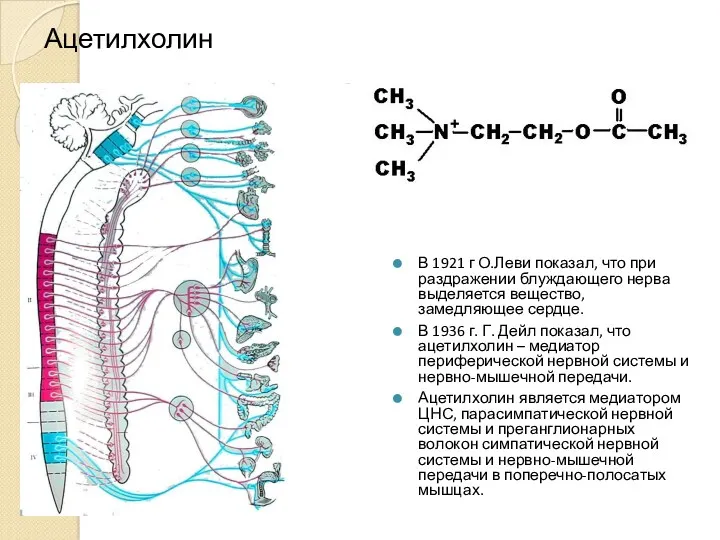
- 18. Ацетилхолин В 1921 г О.Леви показал, что при раздражении блуждающего нерва выделяется вещество, замедляющее сердце. В
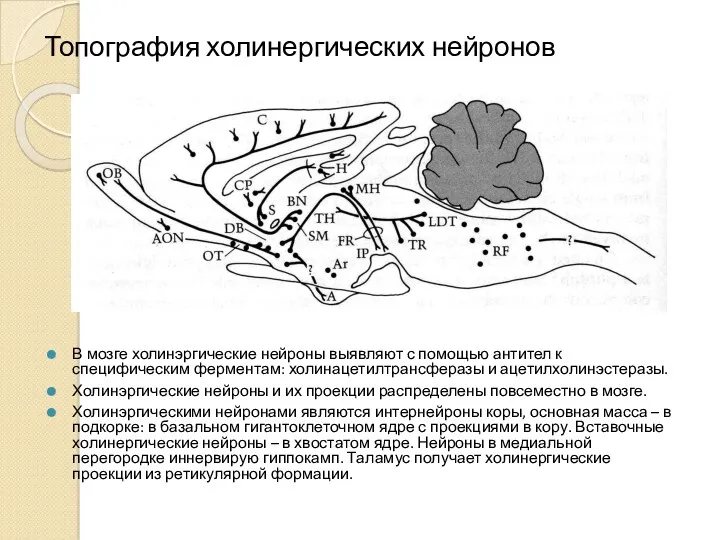
- 19. Топография холинергических нейронов В мозге холинэргические нейроны выявляют с помощью антител к специфическим ферментам: холинацетилтрансферазы и
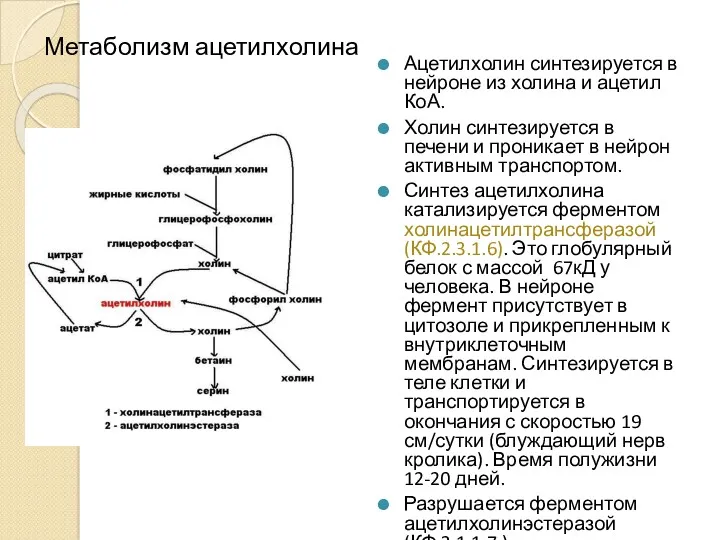
- 20. Метаболизм ацетилхолина Ацетилхолин синтезируется в нейроне из холина и ацетил КоА. Холин синтезируется в печени и
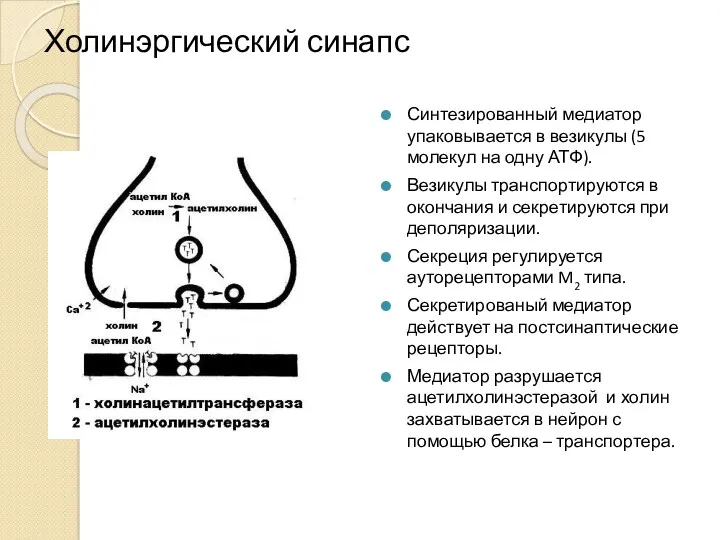
- 21. Холинэргический синапс Синтезированный медиатор упаковывается в везикулы (5 молекул на одну АТФ). Везикулы транспортируются в окончания
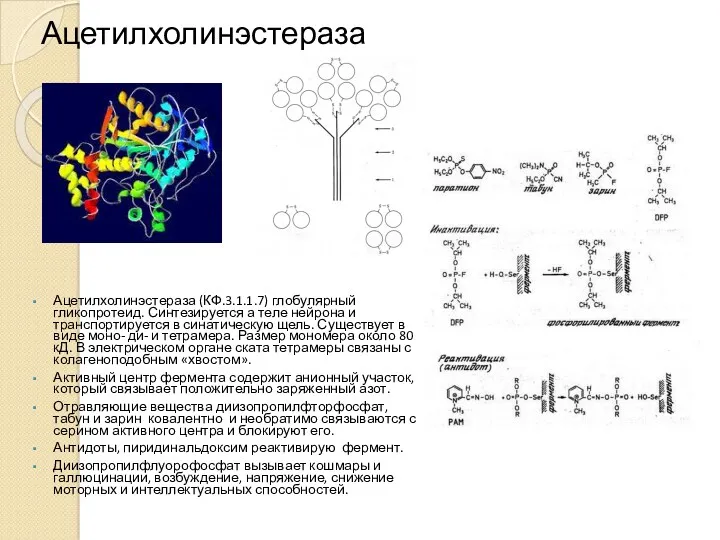
- 22. Ацетилхолинэстераза Ацетилхолинэстераза (КФ.3.1.1.7) глобулярный гликопротеид. Синтезируется а теле нейрона и транспортируется в синатическую щель. Существует в
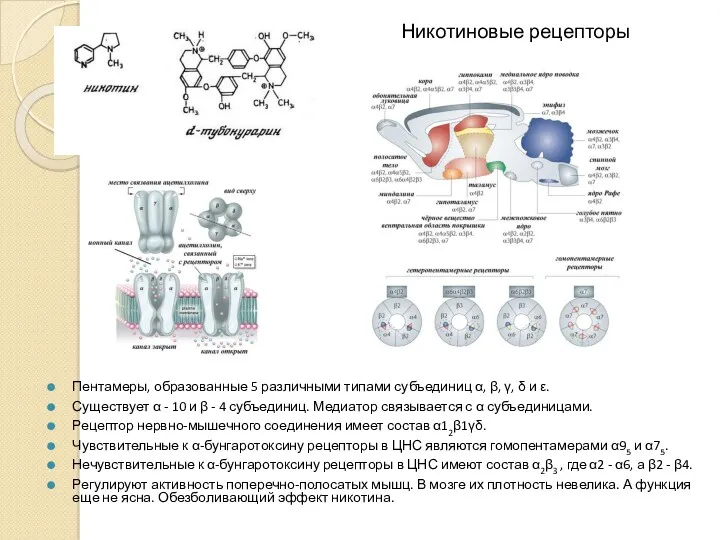
- 23. Никотиновые рецепторы Пентамеры, образованные 5 различными типами субъединиц α, β, γ, δ и ε. Существует α
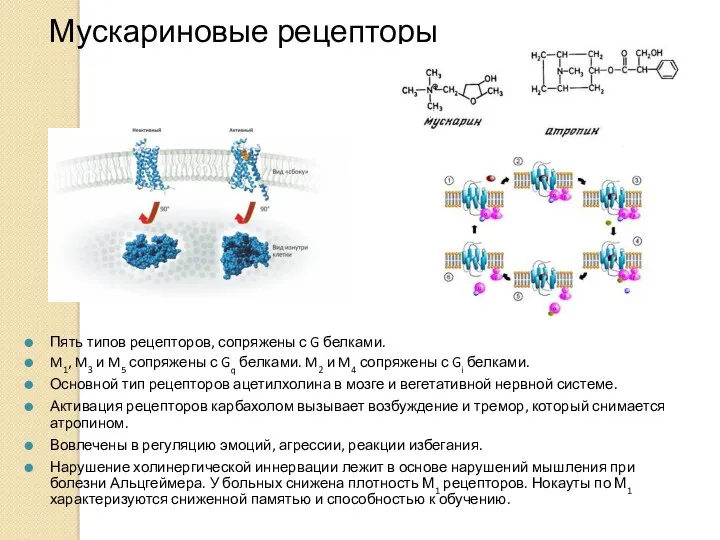
- 24. Мускариновые рецепторы Пять типов рецепторов, сопряжены с G белками. M1, M3 и M5 сопряжены с Gq
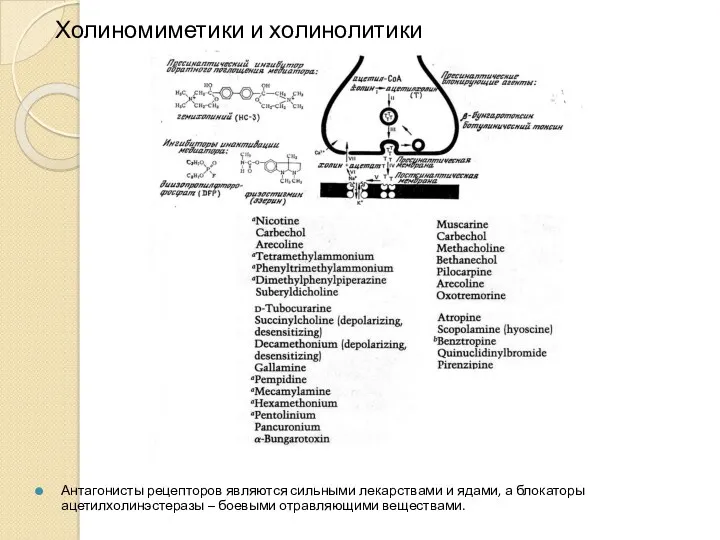
- 25. Холиномиметики и холинолитики Антагонисты рецепторов являются сильными лекарствами и ядами, а блокаторы ацетилхолинэстеразы – боевыми отравляющими
- 27. Скачать презентацию



 Клетка – элементарная биологическая система. Генетический материал и его характеристика
Клетка – элементарная биологическая система. Генетический материал и его характеристика Биомасса және. Фотосинтездің қолданылуы
Биомасса және. Фотосинтездің қолданылуы Зернобобові культури. Лекція 3
Зернобобові культури. Лекція 3 Общая морфология клеток прокариот
Общая морфология клеток прокариот Вплив електромагнітного випромінювання на рослини
Вплив електромагнітного випромінювання на рослини Черенкование комнатных растений
Черенкование комнатных растений Метаботропные рецепторы
Метаботропные рецепторы Растениеводство. Корнеплодные культуры
Растениеводство. Корнеплодные культуры Биохимия спорта
Биохимия спорта Типы развития насекомых
Типы развития насекомых Основы генетики
Основы генетики Роль комнатных растений в жизни человека
Роль комнатных растений в жизни человека Принципы зоологической систематики
Принципы зоологической систематики Неклеточные формы жизни. Вирусы
Неклеточные формы жизни. Вирусы Органы дыхания. Эволюция
Органы дыхания. Эволюция Адамның рефлекторлық реакциясын зерттеу
Адамның рефлекторлық реакциясын зерттеу Animales en el zoológico de Madrid
Animales en el zoológico de Madrid Влияние алкоголя на организм человека
Влияние алкоголя на организм человека Изучение сортов и линий яровой пшеницы в предварительном сортоиспытании 2017 года
Изучение сортов и линий яровой пшеницы в предварительном сортоиспытании 2017 года Сцепленное наследование признаков. Закон Томаса Моргана
Сцепленное наследование признаков. Закон Томаса Моргана Опорно - двигательная система животных
Опорно - двигательная система животных Презентация к уроку Строение цветка
Презентация к уроку Строение цветка Домашний доктор
Домашний доктор Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки В гостях у зимующих птиц
В гостях у зимующих птиц Технология подготовки территория под создание цветника. Правила выращивания георгин различных сортов
Технология подготовки территория под создание цветника. Правила выращивания георгин различных сортов презентация к урокам биологии и экологии Живые организмы как среда жизни
презентация к урокам биологии и экологии Живые организмы как среда жизни Плесневые грибы и дрожжи
Плесневые грибы и дрожжи