Слайд 2
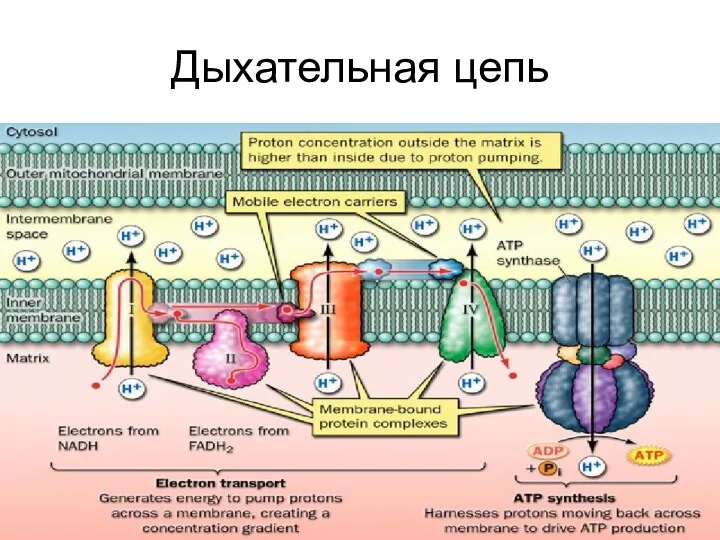
Слайд 3

В пище человека нет готовых первичных доноров водорода - субстратов для
дегидрогеназ.
Они образуются в ходе катаболизма пищевых веществ.
Слайд 4

Слайд 5
Слайд 6
Слайд 7

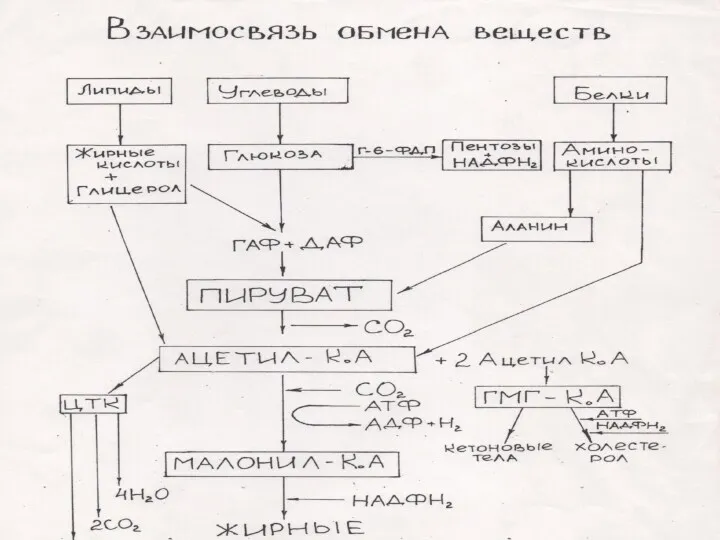
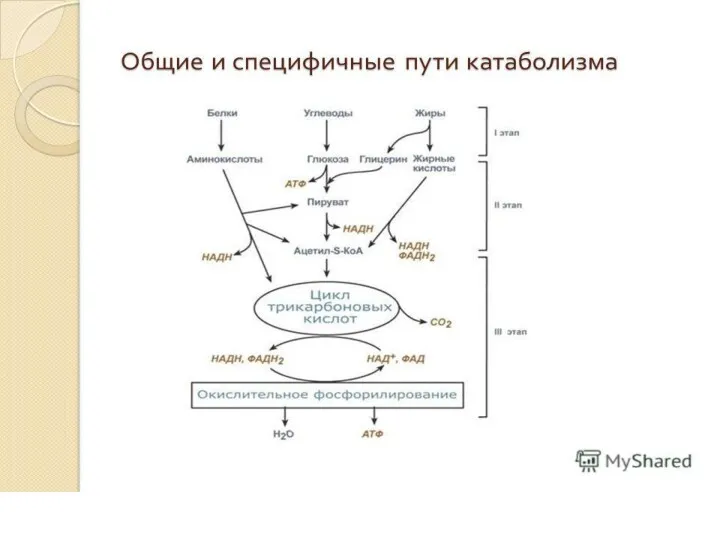
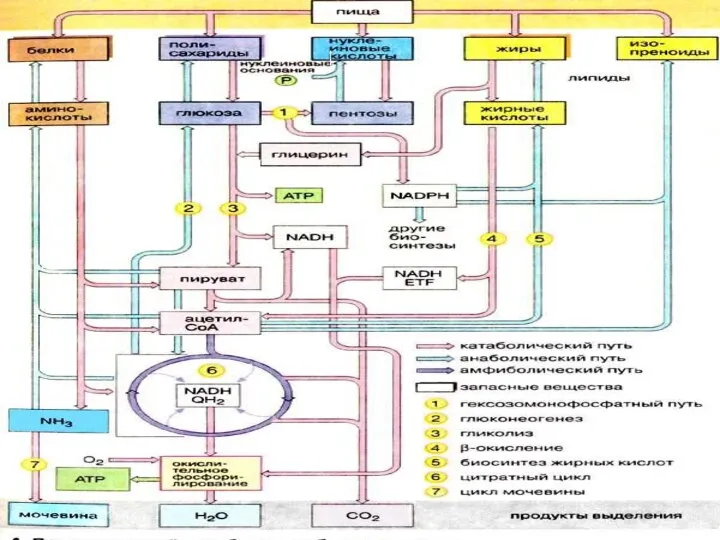
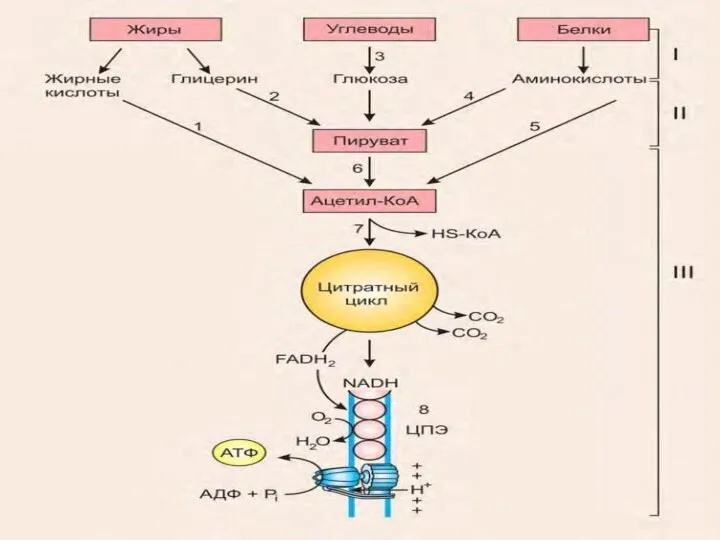
Различают специфические пути катаболизма и
Общие пути катаболизма, которые являются продолжением специфических
путей.
Слайд 8
Слайд 9

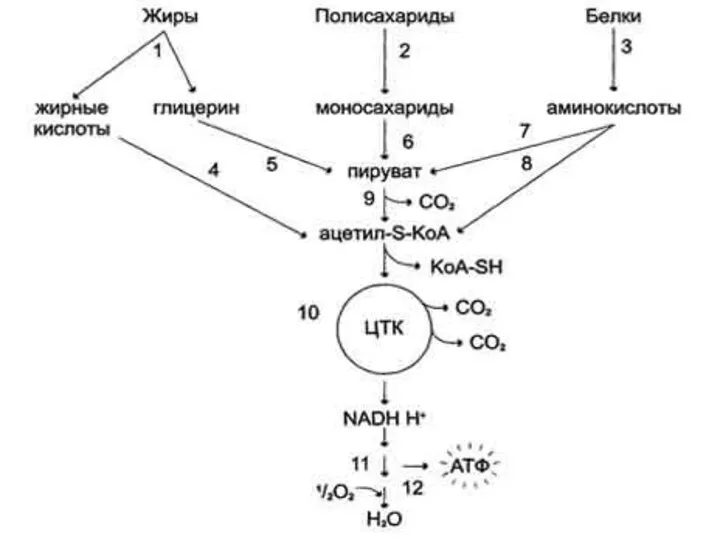
В ходе метаболизма У , Ж и Б образуются 2 центральных
метаболита:
1) ПВК (пировиноградная кислота) и
2) ацетил-КоА.
Слайд 10
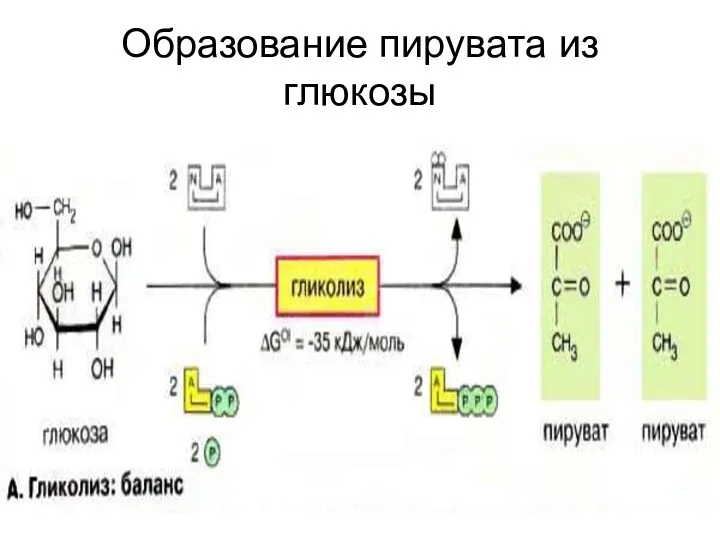
Образование пирувата из глюкозы
Слайд 11

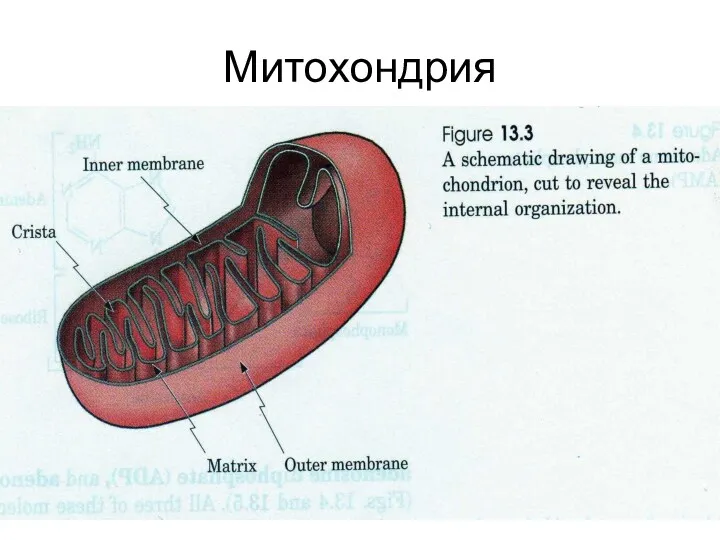
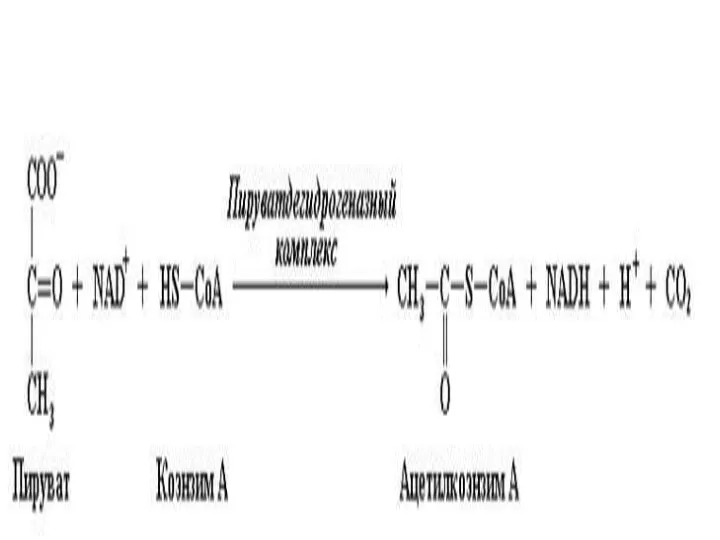
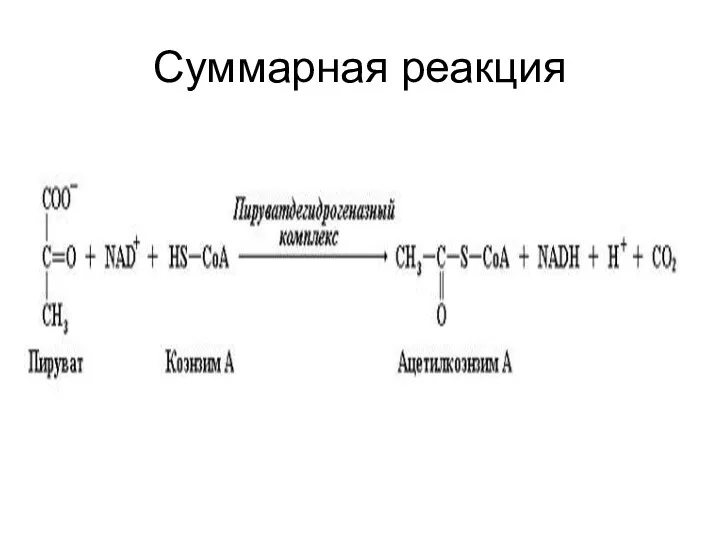
Окислительное декарбоксилирование пирувата
Окислению пируват подвергается в матриксе МХ. Транспорт ПВК через
вн. мембрану МХ осуществляется при помощи спец. белка-переносчика по механизму симпорта с Н+.
Слайд 12
Слайд 13
Слайд 14

Слайд 15
Слайд 16

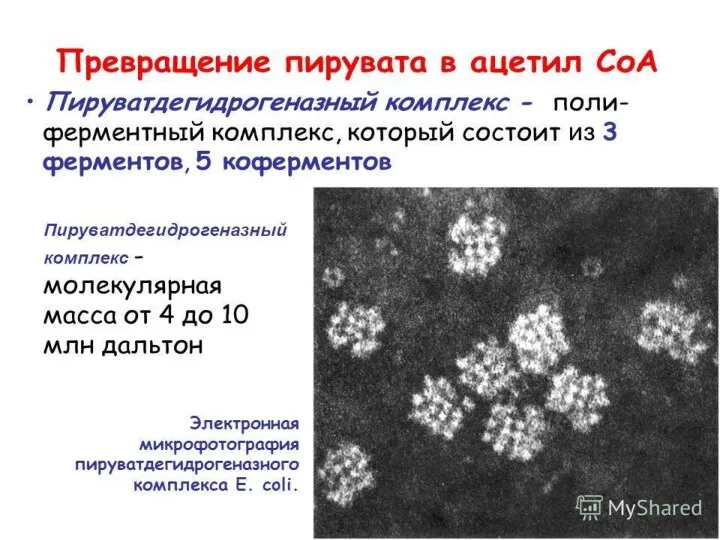
Полиферментный пируватдегидрогеназный комплекс
3 фермента:
1) ПИРУВАТДЕГИДРОГЕНАЗА (декарбоксилирующая) (Е1-ТДФ);
2) ДИГИДРОЛИПОИЛАЦЕТИЛ-ТРАНСФЕРАЗА (Е2-ЛК);
3) ДИГИДРОЛИПОИЛ-ДЕГИДРОГЕНАЗА (Е3-ФАД).
Слайд 17

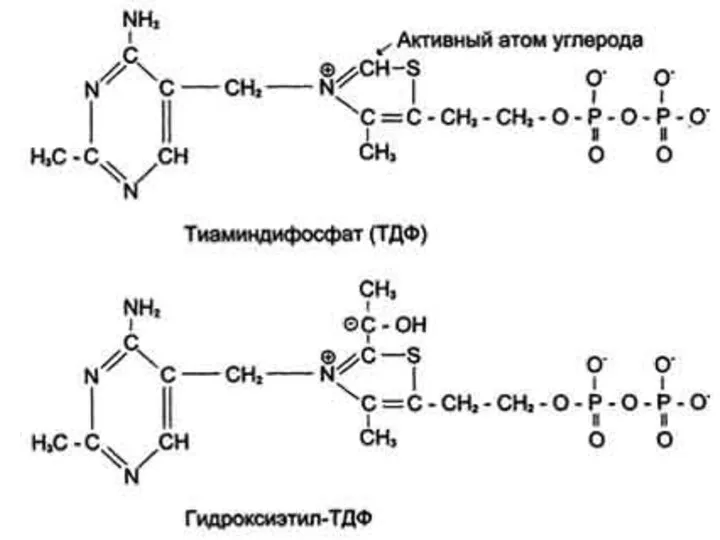
Коферменты
Пять коферментов ассоциированы с белковыми компонентами ферментов.
1)Тиаминдифосфат (ТДФ) связан
с Е1,
2) Липоевая кислота (ЛК) связана с остатком лизина Е2,
Слайд 18

3) ФАД в виде простетической группы Е3.
4) НАД+
и
5) кофермент А взаимодействуют с комплексом в виде растворимых коферментов.
Слайд 19

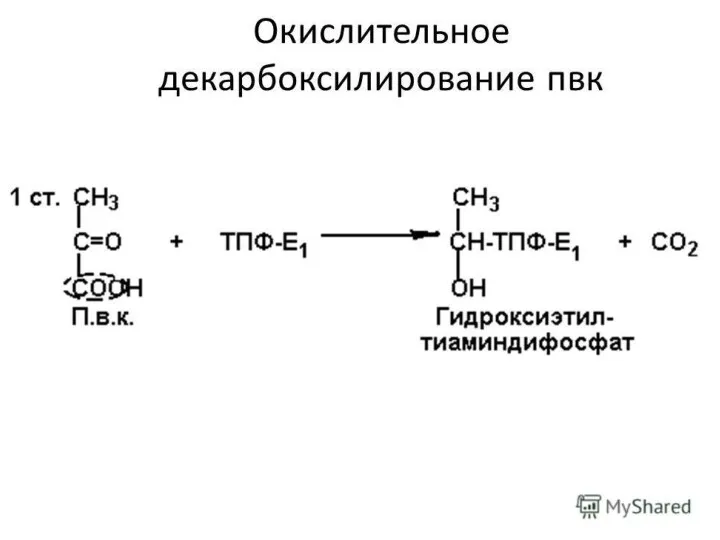
Пируватдегидрогеназа декарбоксилирующая
Пируватдегидрогеназа (Е1-ТДФ) катализирует:1) декарбоксилирование пирувата,
2)перенос образованного гидроксиэтильного остатка на
тиаминдифосфат,
3)окисление гидроксиэтильной группы с образованием ацетильного остатка.
Слайд 20
Слайд 21
Слайд 22
Слайд 23
Слайд 24

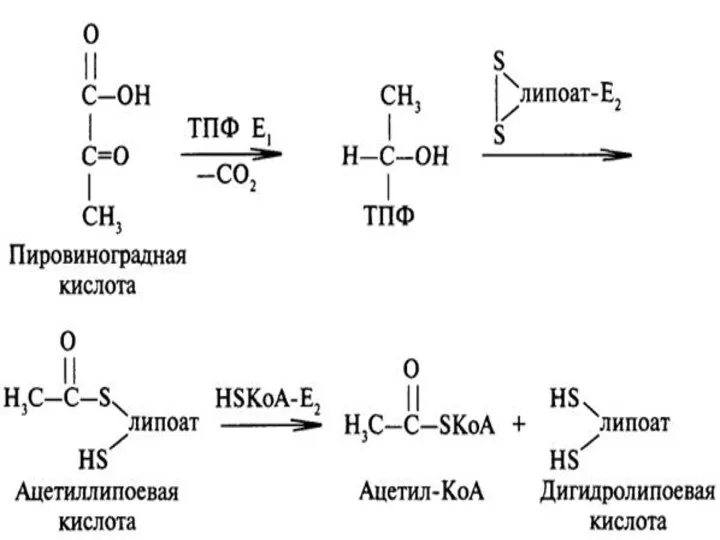
Восстановление липоата
Дигидролипоилацетилтрансфераза (Е2-ЛК) катализирует перенос атома водорода на ЛК и ацетильной
группы на кофермент А,
Слайд 25

Окисление дигидролипоата
Дигидролипоат окисляется до липоата третьим ферментом, дигидролипоилдегидрогеназой (Е3-ФАД) с образованием
НАДН2.
Слайд 26

Слайд 27
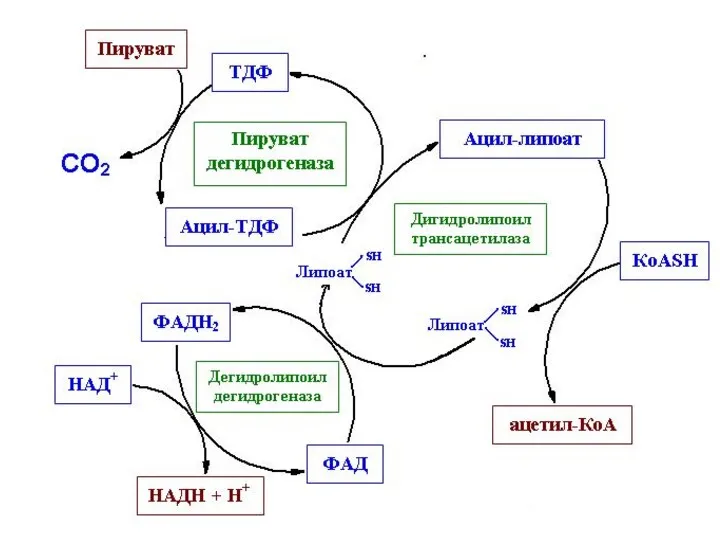
Пируватдегидрогеназный комплекс
Слайд 28

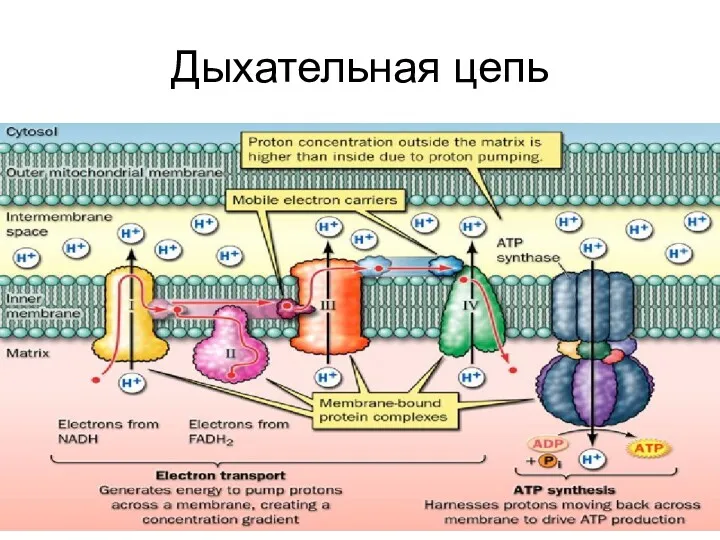
Сопряжение дыхания и фосфорилирования
Окисление НАДН + Н+ в ЦПЭ приведет к
образованию в процессе ОФ – 3 мол. АТФ.
Слайд 29
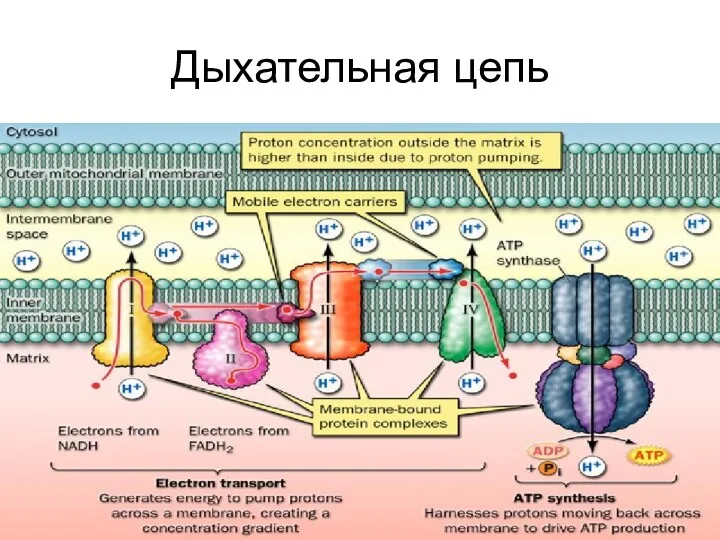
Слайд 30

Цикл трикарбоновых кислот
Слайд 31

Цикл трикарбоновых кислот
Полное «сгорание» как жирных кислот, так и углеводов требует
окисления до СО2 и Н2О ацетильного остатка, связанного с коферментом А.
Слайд 32

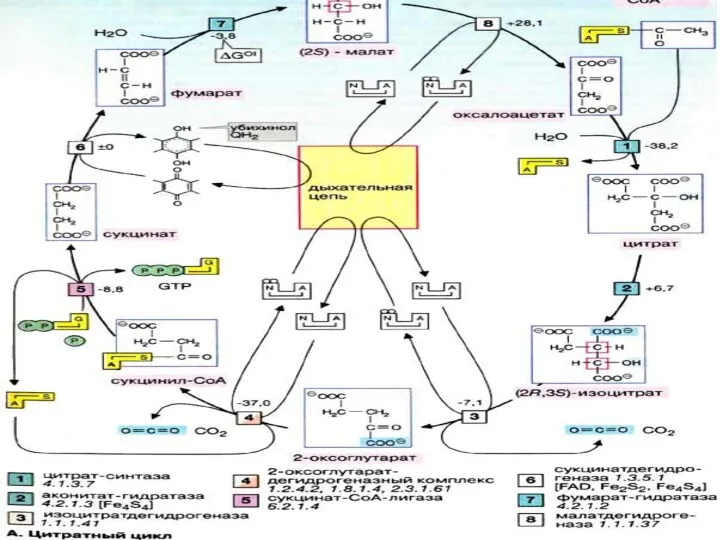
ЦТК – цикл Кребса
Сгорание происходит в системе 8 реакций, называемых циклом
трикарбоновых кислот или — циклом Кребса.
Слайд 33

Слайд 34

Слайд 35

ЦТК
Первая реакция: присоединение ацетильного остатка ацетилкофермента А к оксалоацетату с образованием
трикарбоновой лимонной кислоты — цитрата.
Слайд 36

ЦТК
Далее цитрат претерпевает ряд последовательных превращений, сопровождающихся двумя реакциями декарбоксилирования, т.
е. выделения СО2, и в конечном итоге приводящих к регенерации оксалоацетата.
Слайд 37

Первая стадия
Взаимодействие ацетилкофермента А с оксалоацетатом, катализируемое ферментом цитратсинтазой:
Слайд 38
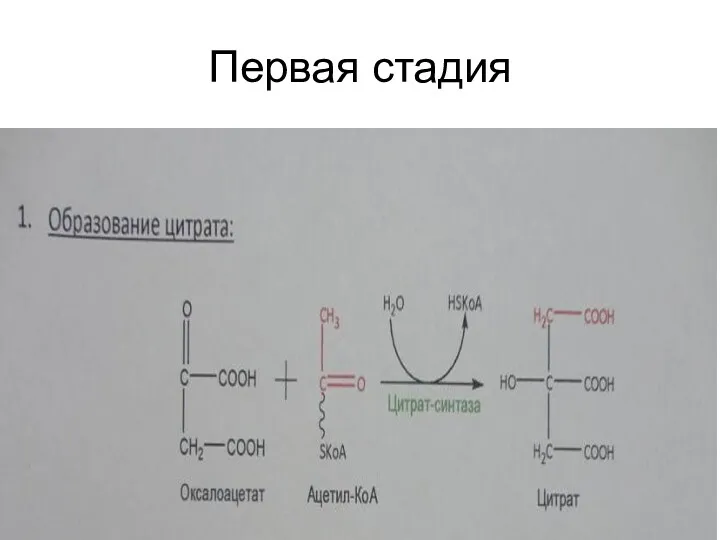
Слайд 39

Вторая стадия
2. Изомеризация цитрата в изоцитрат, катализируемая ферментом аконитазой и проходящая
через промежуточное образование аконитата путем дегидратации цитрата и последующей гидратации аконитата с превращением его в изоцитрат:
Слайд 40
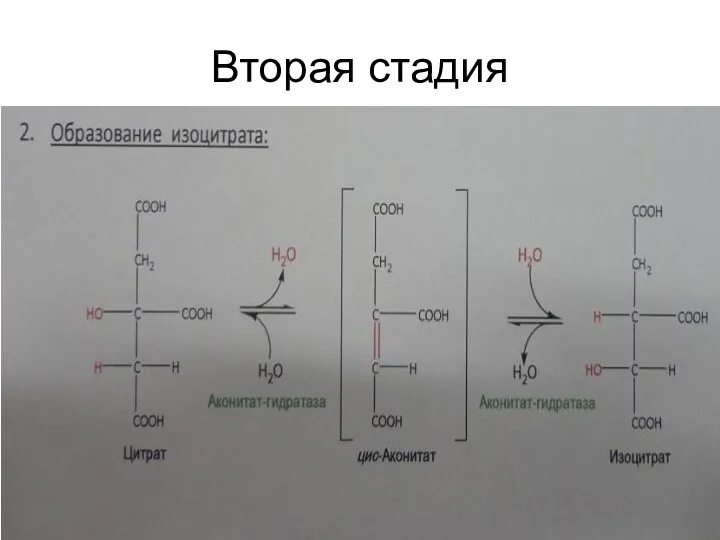
Слайд 41

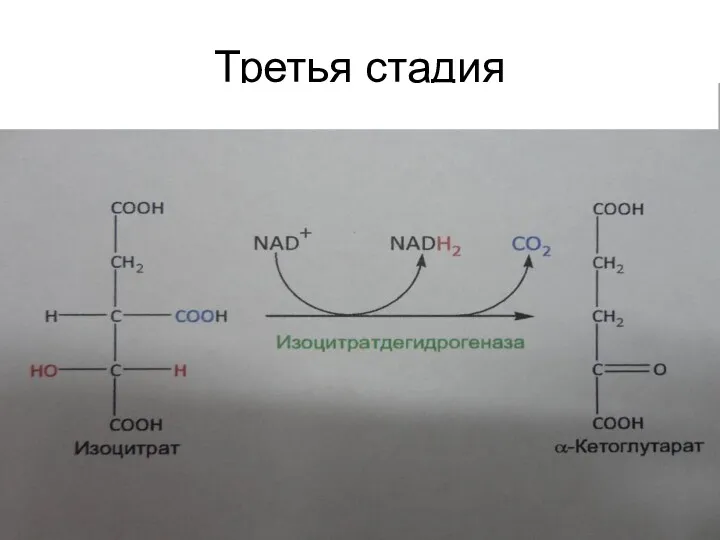
Третья стадия
3. Окисление гидроксигруппы изоцитрата до карбонильной группы с помощью НАД+,
сопровождающееся элиминацией карбоксильной группы в бета-положении, катализируемое изоцитратдегидрогеназой:
Слайд 42
Слайд 43

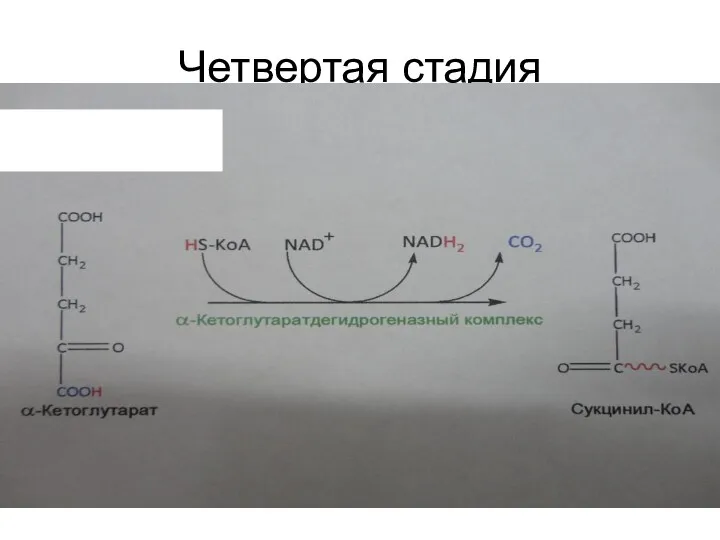
Четвертая стадия
4. Окислительное декарбоксилирование
aльфа-кетоглутарата, катализируемое aльфа‑кетоглутаратдегидрогеназным комплексом, приводит к образованию
сукцинилкофермента А и выделению второй молекулы CO2:
Слайд 44
Слайд 45

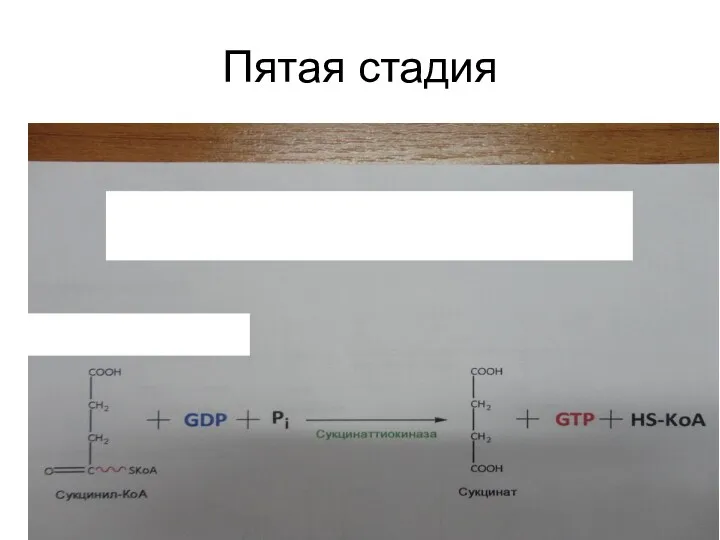
Пятая стадия
5. Фосфорилирование ГТФ, сопряженное с гидролизом макроэргической тиоэфирной связи в
сукцинилкоферменте А, катализируемое сукцинатСоА лиазой:
Слайд 46
Слайд 47

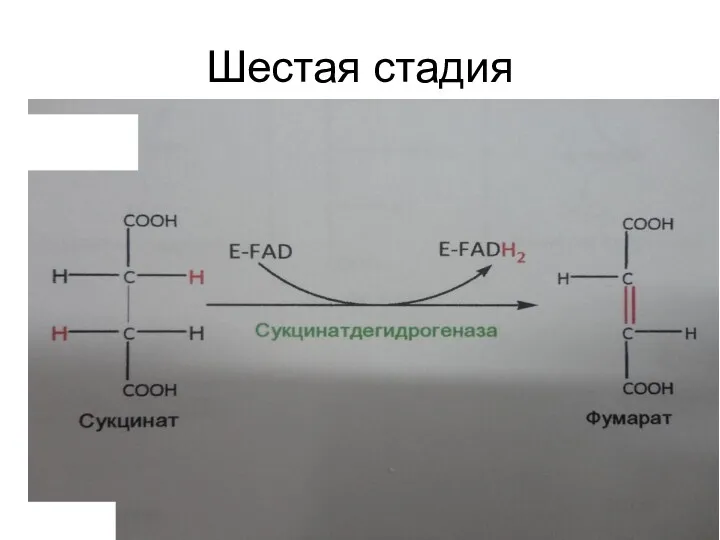
Шестая стадия
6. Превращение сукцината в фумарат, катализируемое сукцинатдегидрогеназой, входящей в состав
комплекса II ЦПЭ с коферментом Q в качестве акцептора электронов:
Слайд 48
Слайд 49

Седьмая стадия
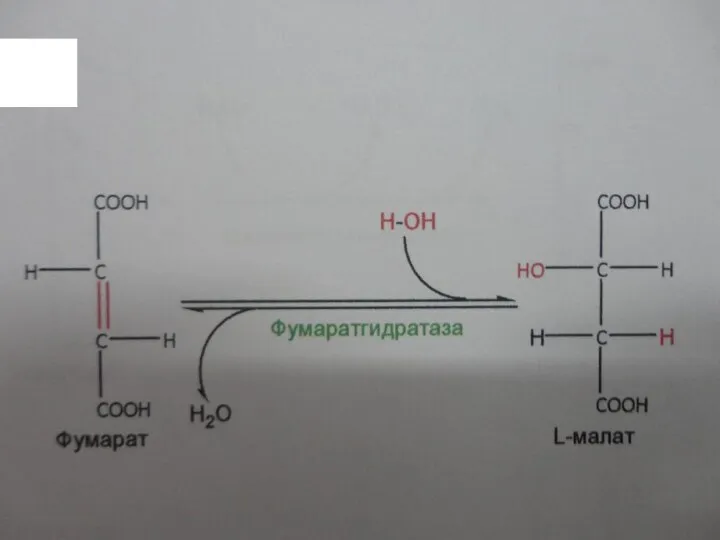
7. Гидратация двойной связи фумарата с образованием малата (соль яблочной
кислоты), катализируемая фумарат- гидратазой:
Слайд 50
Слайд 51

Восьмая стадия
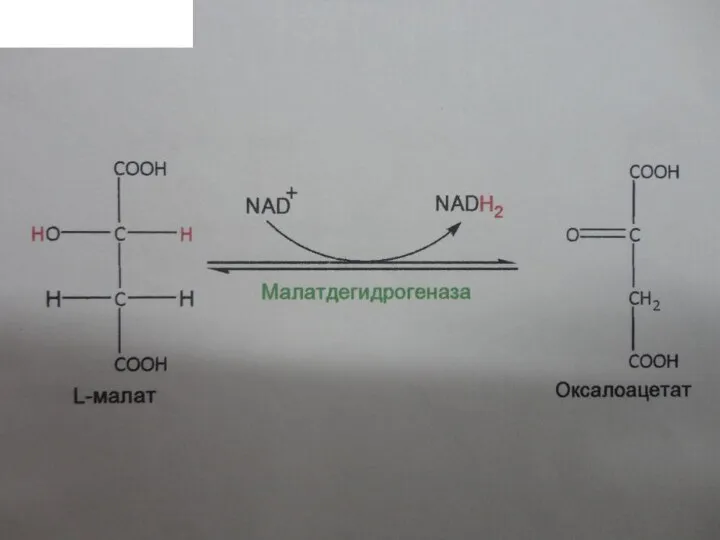
8. Окисление гидроксигруппы малата до кетогруппы, приводящее к регенерации оксалоацетата,
катализируемое малатдегидрогеназой:
Слайд 52
Слайд 53

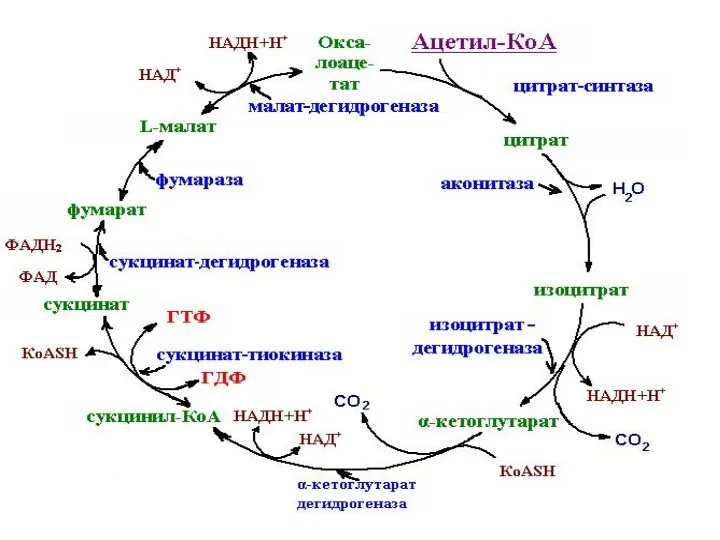
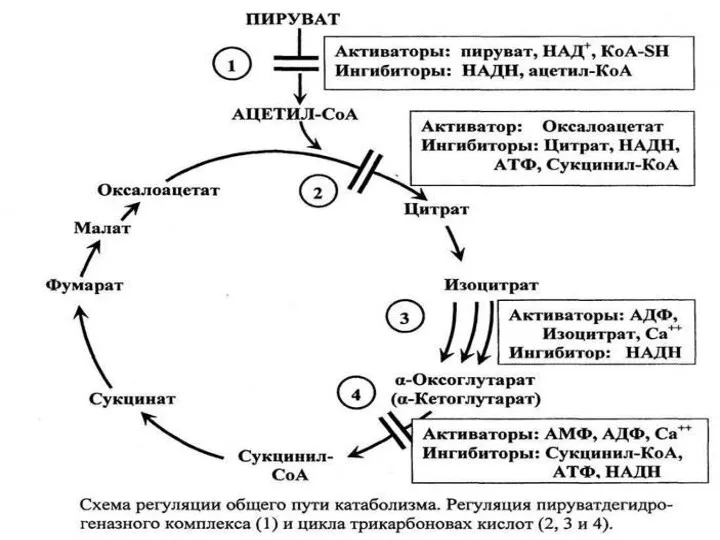
Энергетическое значение ЦТК
В ходе ЦТК восстанавливается до НАДH три молекулы НАД+,
пара электронов посылается в комплекс III от ФАДН2 через кофермент Q и образуется одна макроэргическая связь субстратным фосфорилированием в молекуле ГТФ.
Слайд 54
Слайд 55

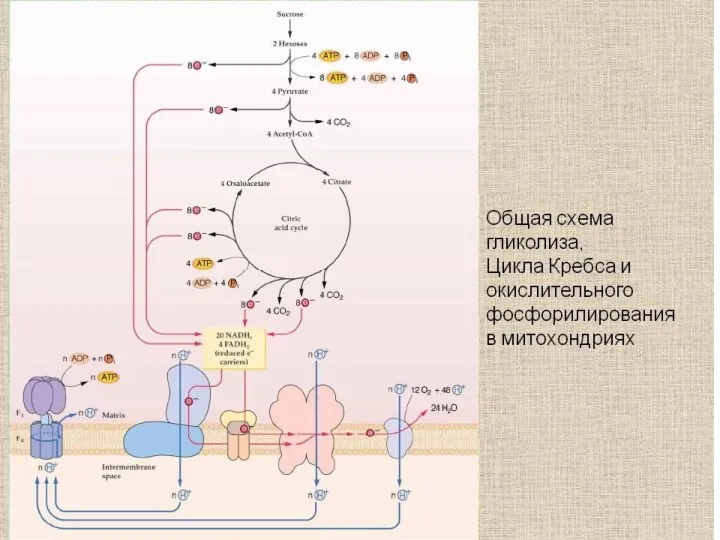
Энергетика ЦТК
С учетом АТР, образующихся в ЦПЭ при окислении НАДH и
ФАДH2, сгорание ацетильного остатка в ЦТК сопровождается образованием 11 молекул АТФ и одной ГТФ, т.е. образованием 12 макроэргических связей.
Слайд 56
Слайд 57

Роль ЦТК для анаболизма
Некоторые компоненты ЦТК: альфа-КГ, сукцинат и оксалоацетат
могут использоваться для синтеза заменимых АК и нуклеотидов.
Слайд 58
Слайд 59
Слайд 60
Слайд 61

Слайд 62
Слайд 63
Слайд 64































































 Эволюция (1 часть)
Эволюция (1 часть) Тонкий кишечник
Тонкий кишечник Пороговые концентрации при остром и хроническом воздействии. Сравнение пороговых концентраций для человека и животных
Пороговые концентрации при остром и хроническом воздействии. Сравнение пороговых концентраций для человека и животных Игра В мире животных
Игра В мире животных Презентация Интегративное обучение в изучении предметов географии и биологии
Презентация Интегративное обучение в изучении предметов географии и биологии биозеноз 9 класс
биозеноз 9 класс Витамин Е
Витамин Е В краю родном. Викторина о природе Ростовской области
В краю родном. Викторина о природе Ростовской области Воздействия тяжелых металлов на биологические показатели растений
Воздействия тяжелых металлов на биологические показатели растений Экзотические домашние животные
Экзотические домашние животные Биологические ресурсы пригородных лесов Владивостока
Биологические ресурсы пригородных лесов Владивостока Исторические этапы развития микробиологии
Исторические этапы развития микробиологии Human genetics
Human genetics Химия и еда
Химия и еда Запилення квіткових рослин
Запилення квіткових рослин Плауны, хвощи, папоротники - высшие споровые растения.
Плауны, хвощи, папоротники - высшие споровые растения. Методы изучения природы
Методы изучения природы Пищеварительная система
Пищеварительная система Морфологические особенности растений различных видов
Морфологические особенности растений различных видов Класс Птицы
Класс Птицы Копитні ссавці
Копитні ссавці Технологии возделывания ячменя
Технологии возделывания ячменя Фотосинтез – способ питания растений
Фотосинтез – способ питания растений ЕГЭ Биология. Новый формат заданий. 2022
ЕГЭ Биология. Новый формат заданий. 2022 Органоиды клетки
Органоиды клетки Тип Плоские черви
Тип Плоские черви Пищеварение в желудке жвачных
Пищеварение в желудке жвачных Презентация Тайны рождения
Презентация Тайны рождения