Содержание
- 2. Белки чрезвычайно разнообразны по своим свойствам, что определяется их пространственной структурой. Есть белки, растворимые (например, фибриноген)
- 3. Виды белков по функциям Ферменты (альдолаза, каталаза, пероксидаза и т. д.) Запасные белки (казеин) Гормоны (паратгормон,
- 4. Структурная Белки участвуют в образовании всех мембран и органоидов клетки. Составляют капсид вирусов. Кератин-компонент перьев, шерсти,
- 5. Структурная функция Структурные белки цитоскелета, как своего рода арматура, придают форму клеткам и многим органоидам и
- 6. Каталитическая В каждой клетке имеются сотни ферментов. Они помогают осуществлять биохимические реакции, действуя как биокатализаторы.
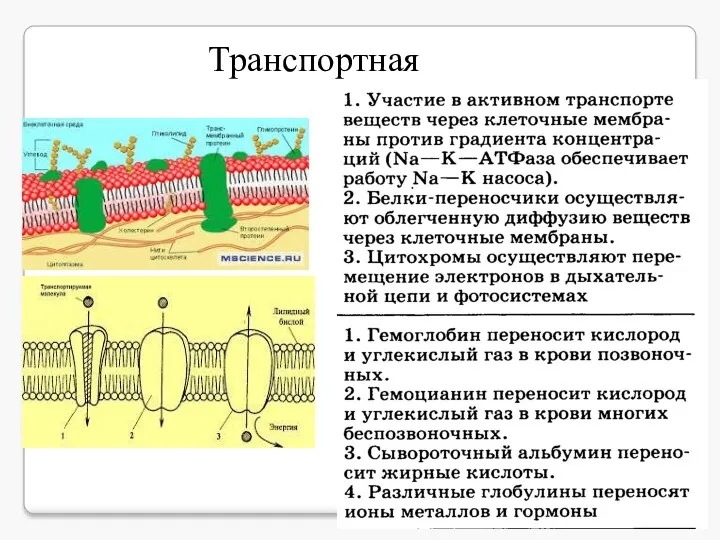
- 7. Транспортная Например, г е м о г л о б и н крови переносит кислород.
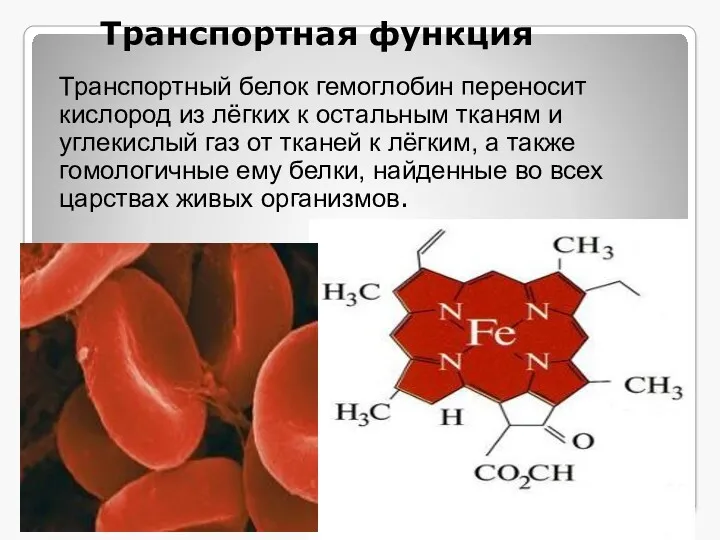
- 8. Транспортная функция Транспортный белок гемоглобин переносит кислород из лёгких к остальным тканям и углекислый газ от
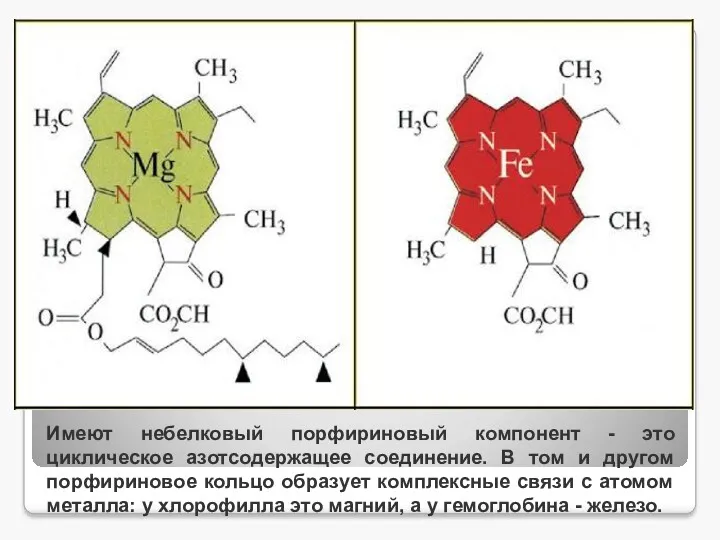
- 9. Имеют небелковый порфириновый компонент - это циклическое азотсодержащее соединение. В том и другом порфириновое кольцо образует
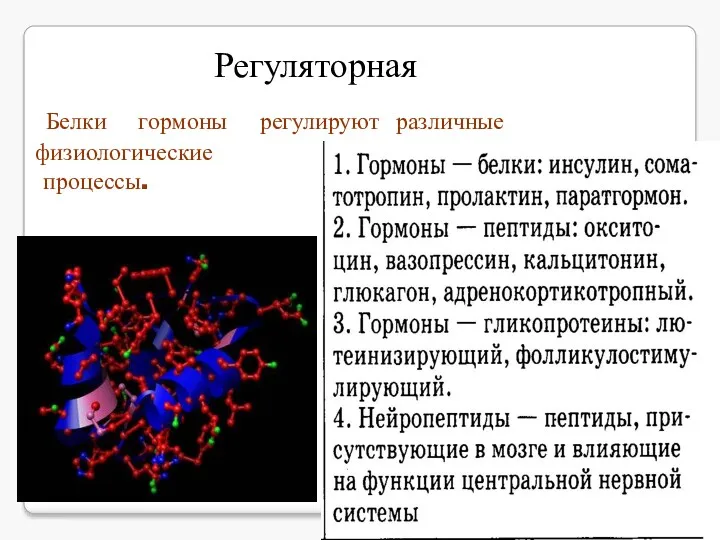
- 10. Регуляторная Белки гормоны регулируют различные физиологические процессы. Например, инсулин регулирует уровень углеводов в крови.
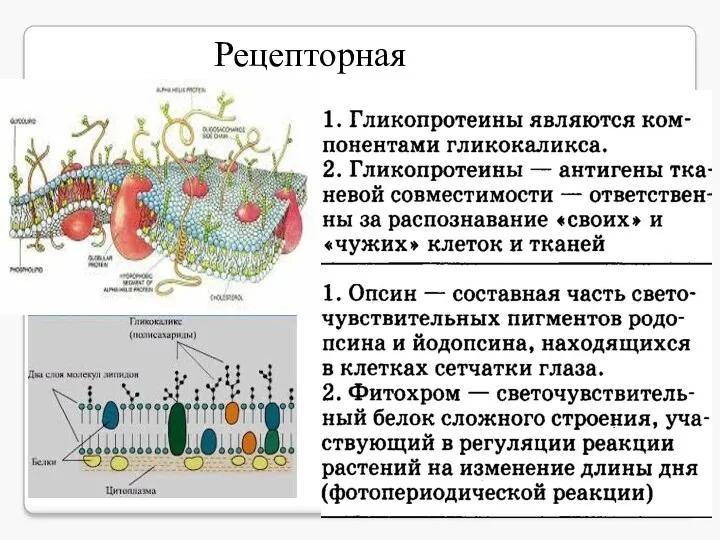
- 11. Рецепторная Например, инсулин регулирует уровень углеводов в крови.
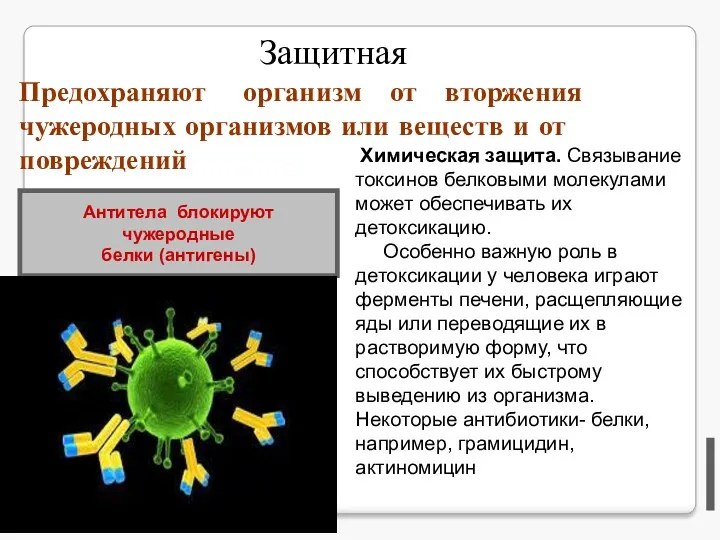
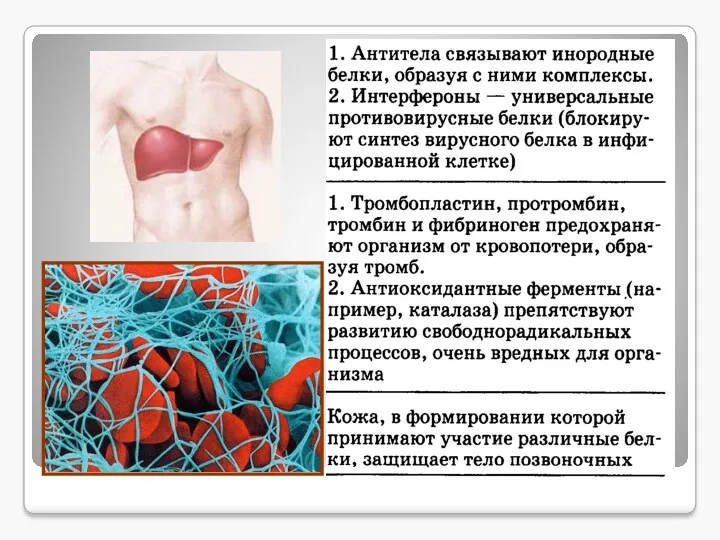
- 12. Защитная Антитела блокируют чужеродные белки (антигены) Предохраняют организм от вторжения чужеродных организмов или веществ и от
- 14. Сократительная . Актин и миозин – белки мышц
- 15. Энергетическая 1г белка - 17.6 кДж При недостатке углеводов или жиров окисляются молекулы белков. При полном
- 16. Энергетическая функция Сначала белки расщепляются до аминокислот, а затем до конечных продуктов — воды, углекислого газа
- 17. Пищевая функция Запасающая функция
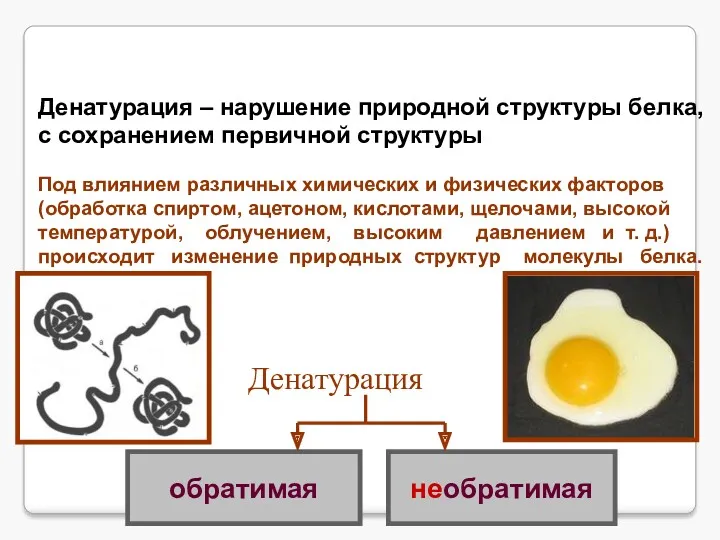
- 18. Денатурация – нарушение природной структуры белка, с сохранением первичной структуры. Денатурация Под влиянием различных химических и
- 19. Денатурация белка Высокие температуры, кислоты, яды, радиация
- 20. Ренатурация белка При нормальных условиях белок ренатурирует – восстанавливает свою структуру
- 22. Биуретовая реакция на белки
- 23. Ксантопротеиновая реакция Если к раствору белка прилить концентрированную азотную кислоту и нагреть, то образуется характерная желтая
- 24. Разрушение белка- денатурация. Действие серной кислоты на белок.
- 25. Денатурация белка сульфатом меди. Денатурация белка сульфатом меди
- 26. Денатурация белка сульфатом меди.
- 28. Скачать презентацию

















 Сходства и различия клеток растений, животных и грибов
Сходства и различия клеток растений, животных и грибов Использование дрожжевых грибов для производства разных групп продуктов
Использование дрожжевых грибов для производства разных групп продуктов Открытое мероприятие по профилактике вредных привычек
Открытое мероприятие по профилактике вредных привычек Бактерії - прокаріотичні одноклітинні мікроорганізми
Бактерії - прокаріотичні одноклітинні мікроорганізми Влияние ГМО на организм человека
Влияние ГМО на организм человека Общая физиология сенсорных систем
Общая физиология сенсорных систем Половое поведение животных
Половое поведение животных Дыхание растений
Дыхание растений Круговорот кислорода в природе
Круговорот кислорода в природе Звёздный час. Загадки о животных и растениях
Звёздный час. Загадки о животных и растениях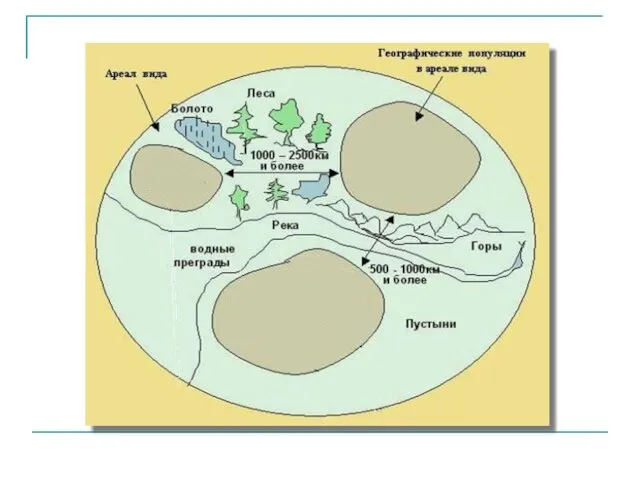 Популяция. Популяционная генетика
Популяция. Популяционная генетика Сахароза. Дисахариды (олигосахариды)
Сахароза. Дисахариды (олигосахариды) Клетки и их разнообразие в многоклеточном организме
Клетки и их разнообразие в многоклеточном организме Основы гистологии. Виды тканей
Основы гистологии. Виды тканей An introduction to metabolism
An introduction to metabolism Глюкоза. Молекулярна формула. Фізичні та хімічні властивості глюкози. Поширення в природі
Глюкоза. Молекулярна формула. Фізичні та хімічні властивості глюкози. Поширення в природі 20231101_vestniki_vesny_viktorina
20231101_vestniki_vesny_viktorina Глаз
Глаз Cattle breeds
Cattle breeds Как зимой помочь птицам (урок окружающего мира, 1 класс)
Как зимой помочь птицам (урок окружающего мира, 1 класс) Эффективный способ посадки картофеля
Эффективный способ посадки картофеля Мы говорим Нет алкоголю!
Мы говорим Нет алкоголю! Физиология растений. Механизмы поступления воды в растительную клетку. Дальний транспорт воды в растении
Физиология растений. Механизмы поступления воды в растительную клетку. Дальний транспорт воды в растении Презентация по биологии для 9 класса по теме:Метаболизм. Энергетический обмен.
Презентация по биологии для 9 класса по теме:Метаболизм. Энергетический обмен. Животные Антарктиды
Животные Антарктиды Красная книга Удмуртии. Животные
Красная книга Удмуртии. Животные Кератин в волосах и восстановление волос
Кератин в волосах и восстановление волос Катархей. Архей
Катархей. Архей