Содержание
- 2. Самопроизвольные процессы, протекающие на границе раздела двух фаз, называются поверхностными явлениями. Они протекают in vivo на
- 3. План 8.1 Поверхностная энергия и поверхностное натяжение. 8.2 Адсорбция ПАВ на границе жидкость-газ. 8.3 Адсорбция на
- 4. 8.1 Свободную поверхностную энергию Gs накапливают молекулы поверхностного слоя, что связано с различным энергетическим состоянием молекул
- 5. На молекулу воды, находящуюся в глубине жидкой фазы, действуют силы межмолекулярного взаимодействия (f1), причем их равнодействующая
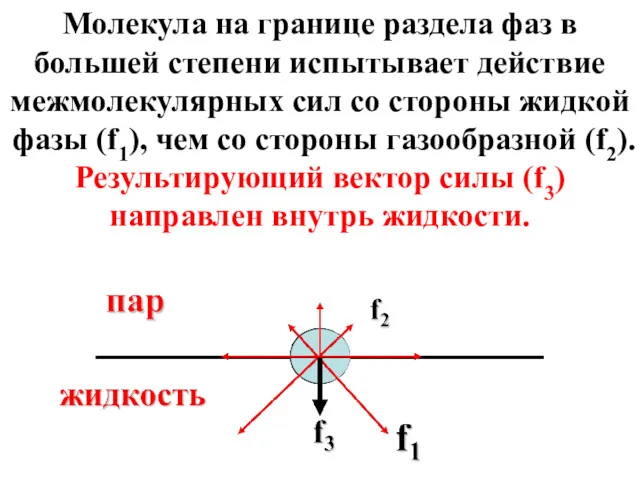
- 6. Молекула на границе раздела фаз в большей степени испытывает действие межмолекулярных сил со стороны жидкой фазы
- 7. Сила f3 создает внутреннее (межмолекулярное) давление жидкости, которое для воды составляет 14 000 атм/см2. Межмолекулярное давление-это
- 8. Вследствие нескомпенсированности сил межмолекулярного взаимодействия, поверхностный слой имеет избыточную свободную энергию Gs (по сравнению с объемом
- 9. Gs Дж Н σ = , = S м2 м Поверхностное натяжение – это поверхностная энергия
- 10. Поверхностное натяжение – важная характеристика жидкостей, зависящая а) от температуры, б) от полярности среды.
- 11. С увеличением температуры поверхностное натяжение жидкостей уменьшается, т.к. разрывается часть связей межмолекулярного взаимодействия. C увеличением полярности
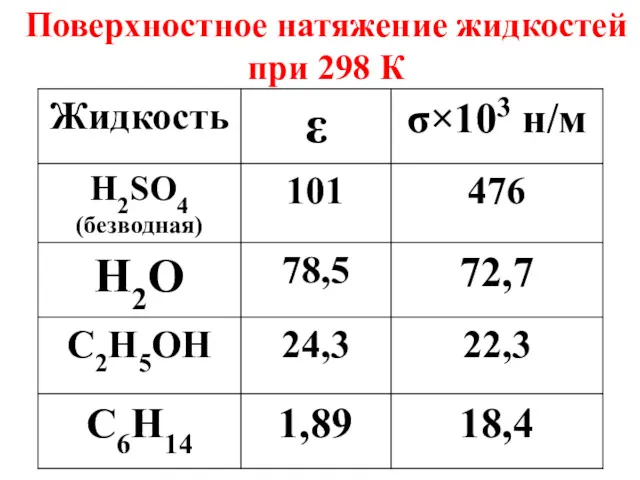
- 12. Поверхностное натяжение жидкостей при 298 К
- 13. Поверхностное натяжение – важная характеристика биологических жидкостей. В норме σ крови равно 45,4×10-3 н/м. Изменения σ
- 14. Согласно второму закону термодинамики Gs → min. Это стремление реализуется за счет уменьшения площади поверхности раздела
- 15. 8.2. Адсорбцией называется концентрирование какого-либо вещества в поверхностном слое в результате самопроизвольного перехода его из объема
- 16. Активирован-ный уголь Молекулы газа
- 17. Участниками сорбционного процесса являются адсорбент – вещество, на поверхности которого идет адсорбция, и адсорбат – вещество,
- 18. Адсорбция (Г) выражается в г/м2 или моль/м2 : Г = ν S m – масса адсорбата,
- 19. В зависимости от природы сил, действующих между адсорбентом и адсорбатом, различают физическую и химическую адсорбцию.
- 20. Физическая адсорбция обусловлена межмолекулярным взаимодействием адсорбата и адсорбента. Энергия такого взаимодействия составляет всего 4-40 кДж/моль.
- 21. Для физической адсорбции характерны: обратимость: одновременно с адсорбцией протекает десорбция, неспецифичность: она подчиняется правилу «подобное растворяется
- 22. Химическая адсорбция (хемосорбция) протекает тогда, когда между адсорбентом и адсорбатом образуются ковалентные связи. Энергия связи при
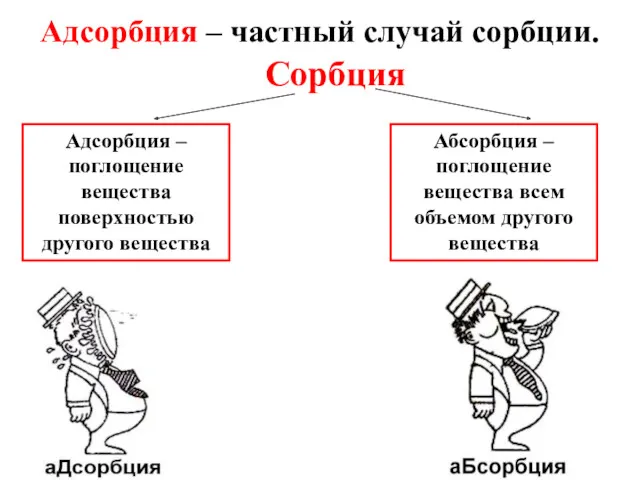
- 23. Адсорбция – частный случай сорбции. Сорбция Адсорбция – поглощение вещества поверхностью другого вещества Абсорбция – поглощение
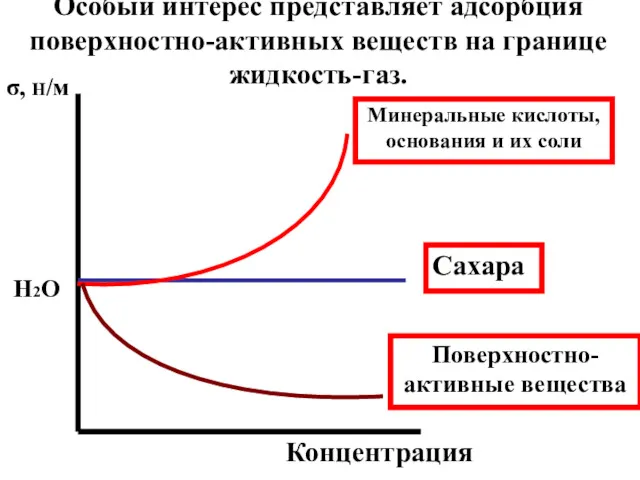
- 24. σ, Н/м Концентрация Особый интерес представляет адсорбция поверхностно-активных веществ на границе жидкость-газ. Минеральные кислоты, основания и
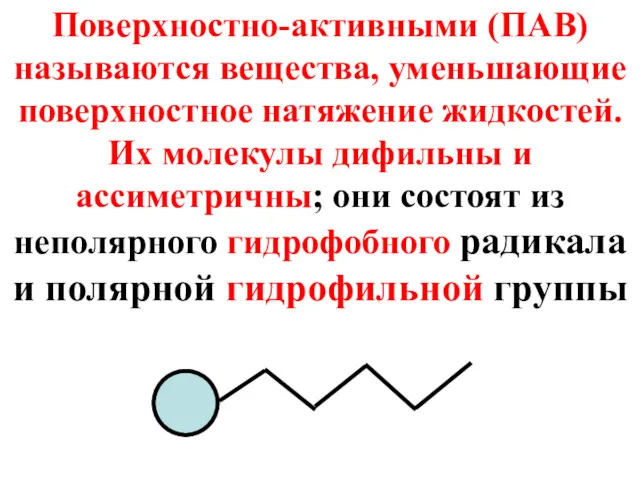
- 25. Поверхностно-активными (ПАВ) называются вещества, уменьшающие поверхностное натяжение жидкостей. Их молекулы дифильны и ассиметричны; они состоят из
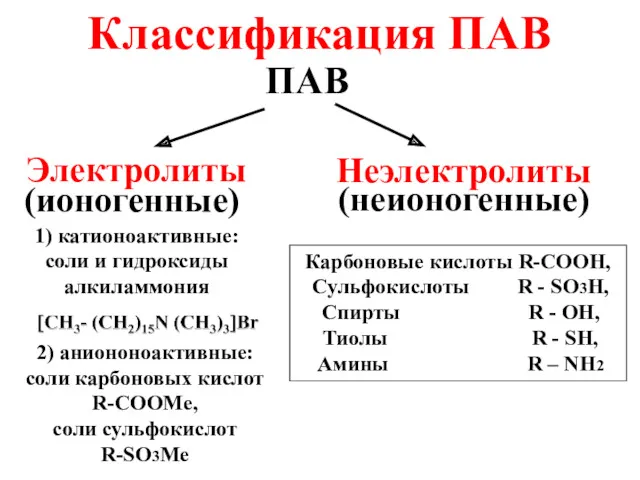
- 26. Классификация ПАВ ПАВ Электролиты Неэлектролиты (ионогенные) (неионогенные) 1) катионоактивные: соли и гидроксиды алкиламмония 2) аниононоактивные: соли
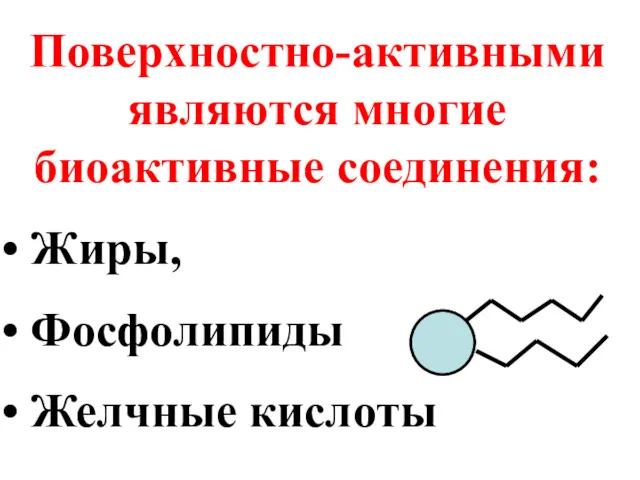
- 27. Поверхностно-активными являются многие биоактивные соединения: Жиры, Фосфолипиды Желчные кислоты
- 28. В соответствии с правилом «Подобное стремится к подобному», гидрофобные радикалы направлены в неполярную фазу (воздух), а
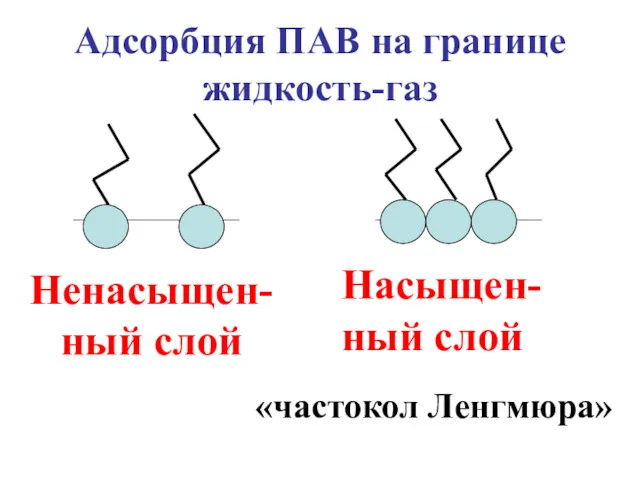
- 29. Насыщен-ный слой Ненасыщен-ный слой «частокол Ленгмюра» Адсорбция ПАВ на границе жидкость-газ
- 30. Поскольку молекулы ПАВ менее полярны, чем молекулы воды, силы поверхностного натяжения в поверхностном слое уменьшаются.
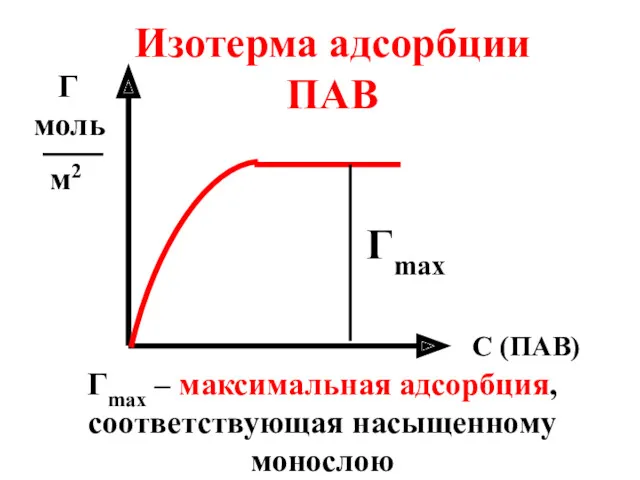
- 31. С (ПАВ) Г моль м2 Изотерма адсорбции ПАВ Гmax Гmax – максимальная адсорбция, соответствующая насыщенному монослою
- 32. Зная Гmax можно рассчитать а) длину молекулы ПАВ (ℓ) ℓ = Г max M ρ ρ
- 33. Важнейшей характеристикой ПАВ является их поверхностная активность (g): g = Δσ ΔC где Δσ – уменьшение
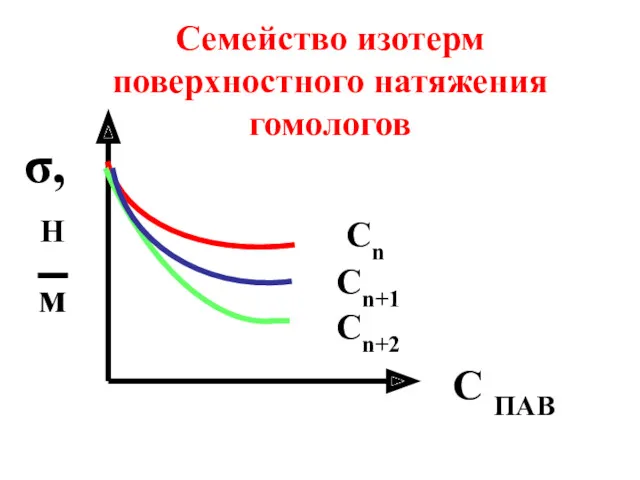
- 34. Для членов одного гомологического ряда (спиртов, аминов или карбоновых кислот) выполняется правило Дюкло-Траубе (1888): с увеличением
- 35. Сn Сn+1 Сn+2 C ПАВ σ, Н м Семейство изотерм поверхностного натяжения гомологов
- 36. Зависимость адсорбции ПАВ от их концентрации в растворе описывается уравнением Гиббса (1878): Г = dσ dс
- 37. Влияние концентрации ПАВ на поверхностное натяжение растворов описывается уравнением Шишковского (1909): σ = σо – а
- 38. Для расчета адсорбции ПАВ используется объединенное уравнение Гиббса-Шишковского: Г = a RT b×c 1 + b×c
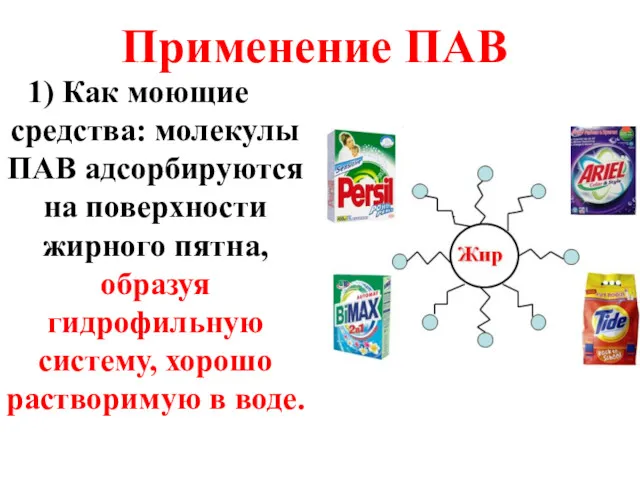
- 39. Применение ПАВ Как моющие средства: молекулы ПАВ адсорбируются на поверхности жирного пятна, образуя гидрофильную систему, хорошо
- 40. 2) Как антисептики в хирургии: антимикробная активность ионогенных ПАВ значительно выше (до 300 раз) активности традиционно
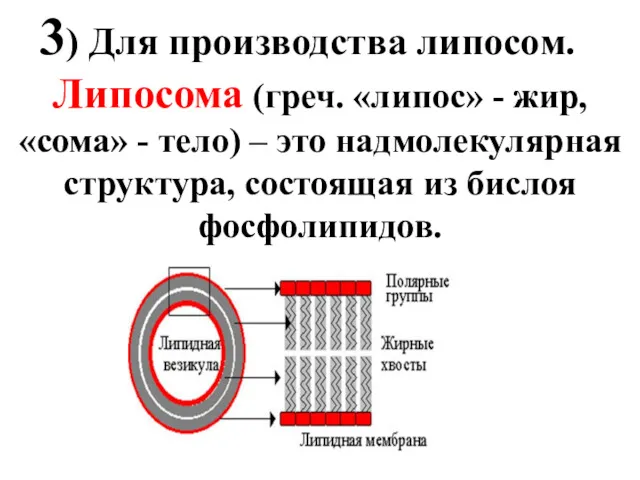
- 41. 3) Для производства липосом. Липосома (греч. «липос» - жир, «сома» - тело) – это надмолекулярная структура,
- 42. Липосомы применяются для направленной доставки лекарственного препарата к пораженным органам и тканям.
- 43. 8.3 Твердые адсорбенты – это природные или синтетические вещества с развитой внутренней или наружной поверхностью, на
- 44. Важнейшей характеристикой твердых адсорбентов является их активная (удельная) поверхность (Sa), выражаемая в м2/кг или м2/г. Sa
- 45. Классификация твердых адсорбентов 1) Углеродные сорбенты (активированный уголь); 2) алюмосиликаты – алюминиевые соли поликремневых кислот; Например,
- 46. 3) цеолиты – алюмосиликаты с высоким содержанием натрия и кальция; 4) силикагели – обезвоженный гель поликремневой
- 47. целлюлоза, пектин и лигнин, являющиеся важным компонентом питания человека. 6. Пищевые волокна -
- 48. Виды адсорбции на твердых адсорбентах Молекулярная адсорбция 2. Избирательная адсорбция электролитов из их растворов 3. Ионообменная
- 49. Молекулярной называют адсорбцию неэлектролитов и слабых электролитов из жидкой или газообразной фазы твердыми адсорбентами.
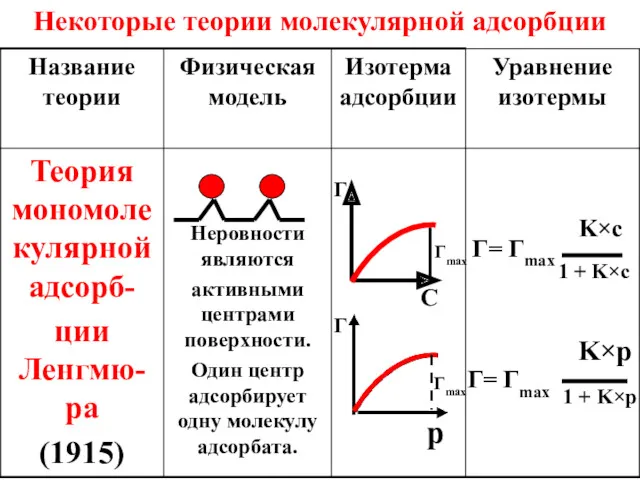
- 50. Некоторые теории молекулярной адсорбции Г= Гmax С Г K×c 1 + K×c Г= Гmax 1 +
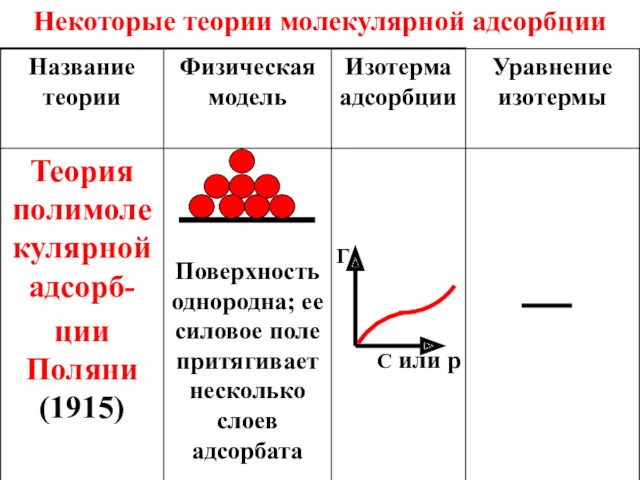
- 51. Некоторые теории молекулярной адсорбции С или p Г
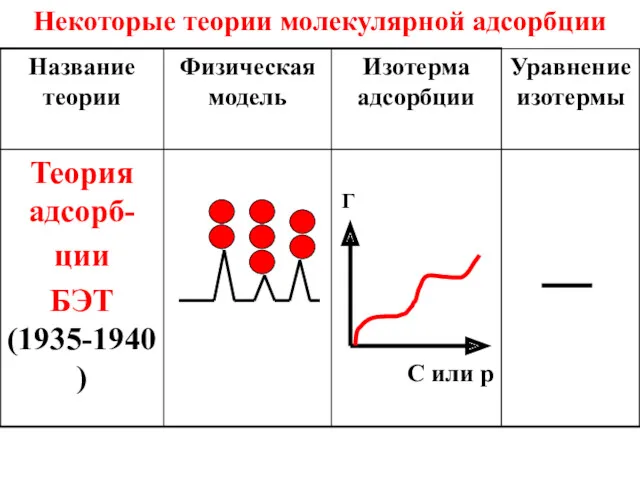
- 52. Некоторые теории молекулярной адсорбции С или p Г
- 53. Для вычисления молекулярной адсорбции используют эмпирическое уравнение Фрейндлиха: æ = kс1/n æ = kp1/n æ –
- 54. Избирательная адсорбция электролитов из растворов описывается правилами Панета-Фаянса.
- 55. Правило 1: на твердой поверхности адсорбируются преимущественно те ионы, которые входят в ее состав. Такую адсорбцию
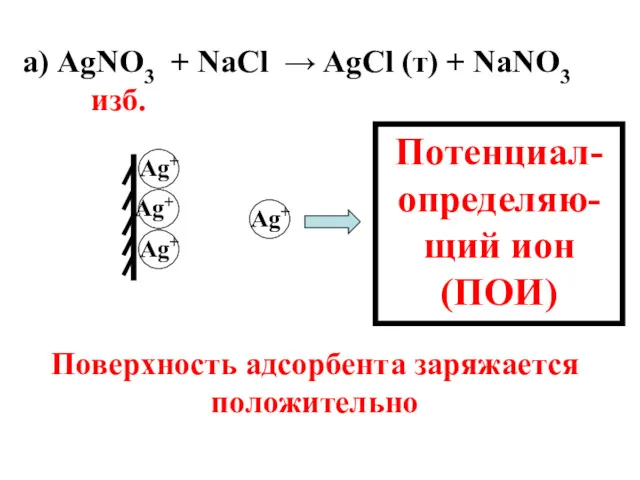
- 56. а) AgNО3 + NaCl → AgCl (т) + NaNO3 изб. Ag+ Ag+ Ag+ Ag+ Потенциал-определяю-щий ион
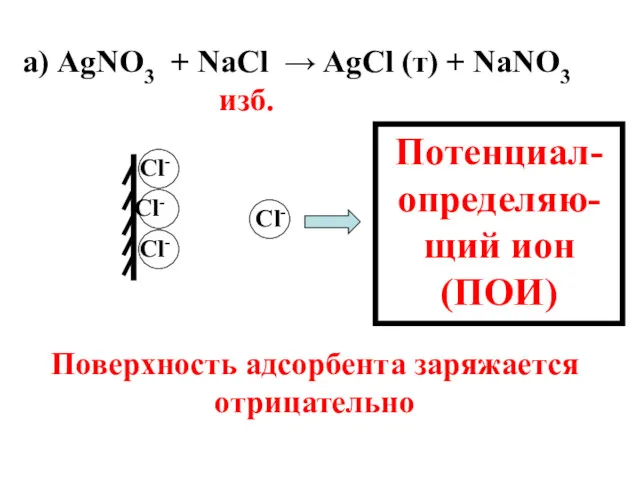
- 57. а) AgNО3 + NaCl → AgCl (т) + NaNO3 изб. Cl- Cl- Cl- Cl- Потенциал-определяю-щий ион
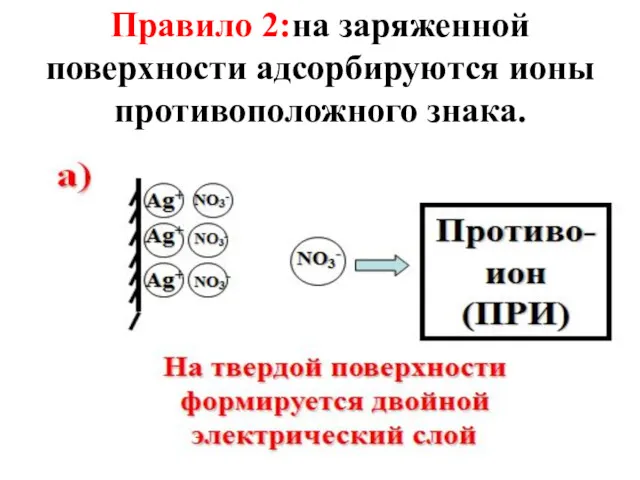
- 58. Правило 2:на заряженной поверхности адсорбируются ионы противоположного знака.
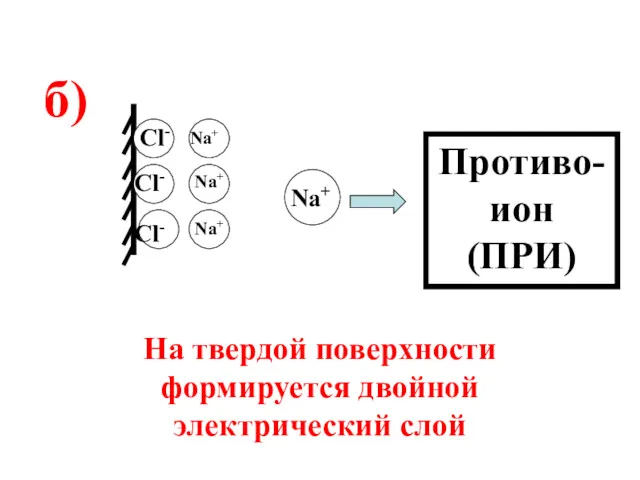
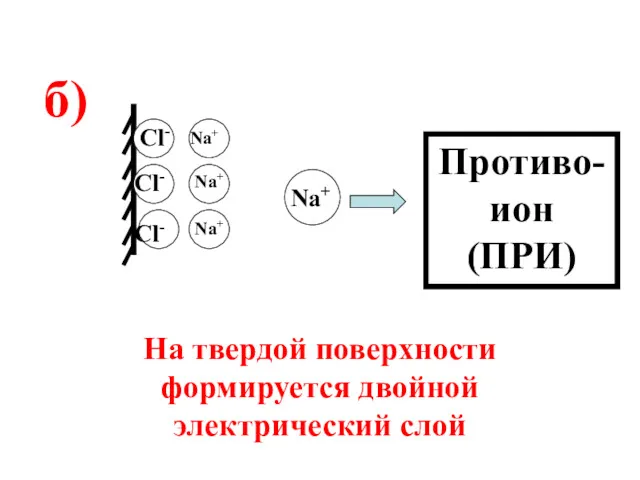
- 59. Cl- Cl- Cl- На твердой поверхности формируется двойной электрический слой Na+ Na+ Nа+ Na+ Противо-ион (ПРИ)
- 60. Cl- Cl- Cl- На твердой поверхности формируется двойной электрический слой Na+ Na+ Nа+ Na+ Противо-ион (ПРИ)
- 61. Ионообменная адсорбция - это процесс, в котором твердый адсорбент и раствор обмениваются одноименно заряженными ионами в
- 62. Сорбенты, способные к обмену ионов, называются ионообменниками или ионитами. Иониты Катиониты Аниониты
- 63. Адсорбционная терапия применяется для удаления токсинов и других вредных веществ из организма человека. В современной медицине
- 65. Энтеросорбция – это метод лечения, основанный на связывании и выведении из ЖКТ токсичных веществ и аллергенов.
- 66. «Будущее не за вводящей, а за выводящей медициной» проф. Ю.М. Лопухин
- 68. Скачать презентацию













































 Ядерные реакции, атомная энергия
Ядерные реакции, атомная энергия Исследование устойчивости САР с помощью программы VisSim
Исследование устойчивости САР с помощью программы VisSim Steering System
Steering System Методы зондирования окружающей среды. Радиорефракция
Методы зондирования окружающей среды. Радиорефракция Молекулярная физика и термодинамика
Молекулярная физика и термодинамика Гипотеза о световом давлении
Гипотеза о световом давлении презентация урока Закон Ома для участка цепи
презентация урока Закон Ома для участка цепи Внеклассное мероприятие Физика и кошка
Внеклассное мероприятие Физика и кошка Конденсатор - устройство, предназначенное для накопления заряда и энергии электрического поля
Конденсатор - устройство, предназначенное для накопления заряда и энергии электрического поля Термодинаміка. Внутрішня енергія
Термодинаміка. Внутрішня енергія Дисперсия света
Дисперсия света Реактивное движение
Реактивное движение Измерение давления в покоящейся жидкости
Измерение давления в покоящейся жидкости Система питания дизельного двигателя внутреннего сгорания. (Тема 10.2)
Система питания дизельного двигателя внутреннего сгорания. (Тема 10.2) Виды теплопередач
Виды теплопередач Електричний струм. Електрична провідність матеріалів. Дії електричного струму
Електричний струм. Електрична провідність матеріалів. Дії електричного струму Магические числа
Магические числа Молекулярная физика и термодинамика
Молекулярная физика и термодинамика Исаак Ньютон. Дисперсия
Исаак Ньютон. Дисперсия Механические колебания
Механические колебания Величины в рад защ и безоп
Величины в рад защ и безоп Проектирование масштабных моделей в технике простого занижения. (4 класс)
Проектирование масштабных моделей в технике простого занижения. (4 класс) Повторение темы Электростатика
Повторение темы Электростатика Интегрированные системы ходового мостика (ИСМ)
Интегрированные системы ходового мостика (ИСМ) Экситонные поляритоны в полупроводниковом микрорезонаторе
Экситонные поляритоны в полупроводниковом микрорезонаторе Презентация к уроку Увеличительные приборы
Презентация к уроку Увеличительные приборы Радиоактивность как свидетельство сложного строения атомов. α-, β- и γ- излучения. Правила смещения при α- и βраспадах
Радиоактивность как свидетельство сложного строения атомов. α-, β- и γ- излучения. Правила смещения при α- и βраспадах Ударно-тяговые приборы
Ударно-тяговые приборы