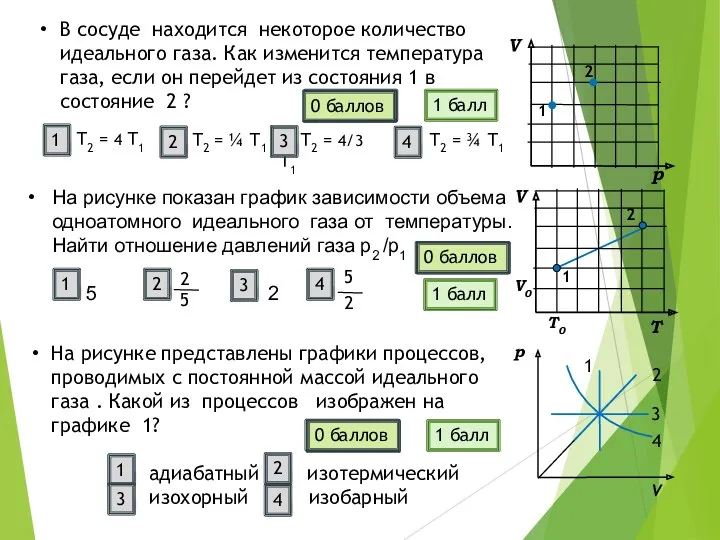
На рисунке показан график зависимости объема одноатомного идеального газа от температуры.
Найти отношение давлений газа р2 /р1
5 2
На рисунке представлены графики процессов, проводимых с постоянной массой идеального газа . Какой из процессов изображен на графике 1?
адиабатный изотермический
изохорный изобарный
2
1
3
4
1
2
1
2
V0
Т0
Т2 = 4 Т1
Т2 = ¾ Т1
Т2 = 4/3 Т1
Т2 = ¼ Т1
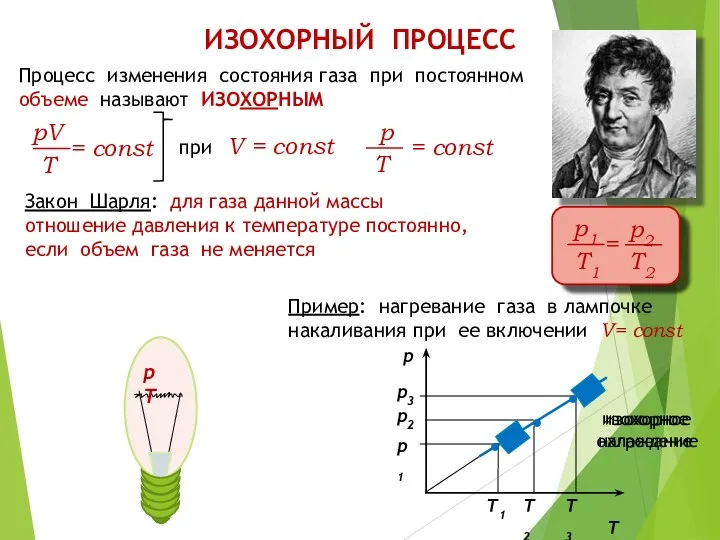
В сосуде находится некоторое количество идеального газа. Как изменится температура газа, если он перейдет из состояния 1 в состояние 2 ?
1
0 баллов
1 балл
2
3
4
1
4
3
2
0 баллов
1 балл
1 балл
0 баллов
1
3
2
4
0 баллов
0 баллов
0 баллов
0 баллов
0 баллов
0 баллов

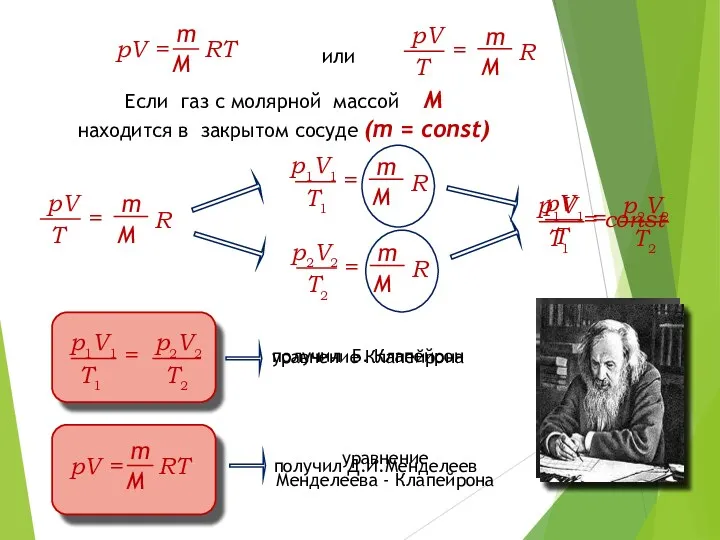
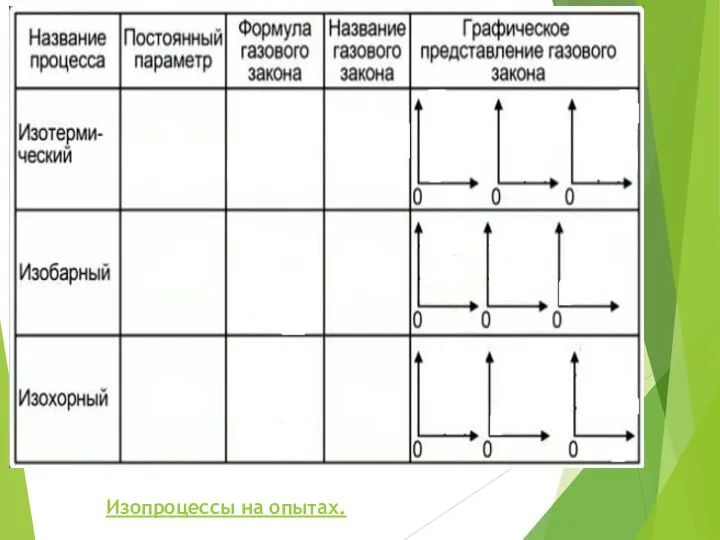


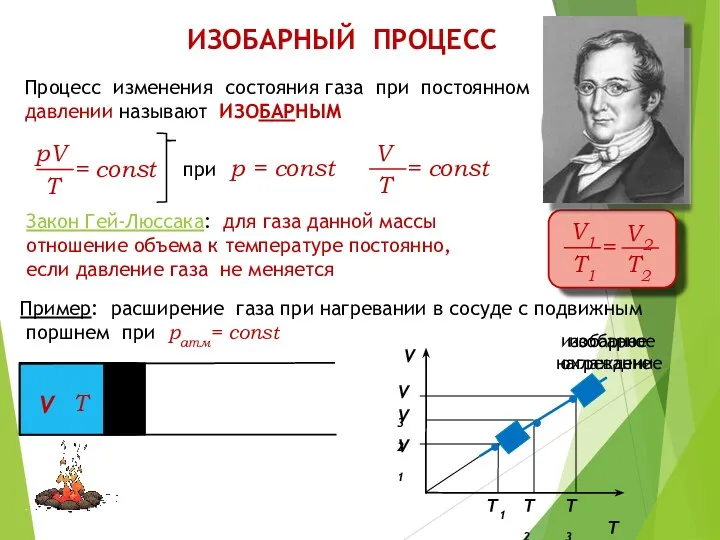
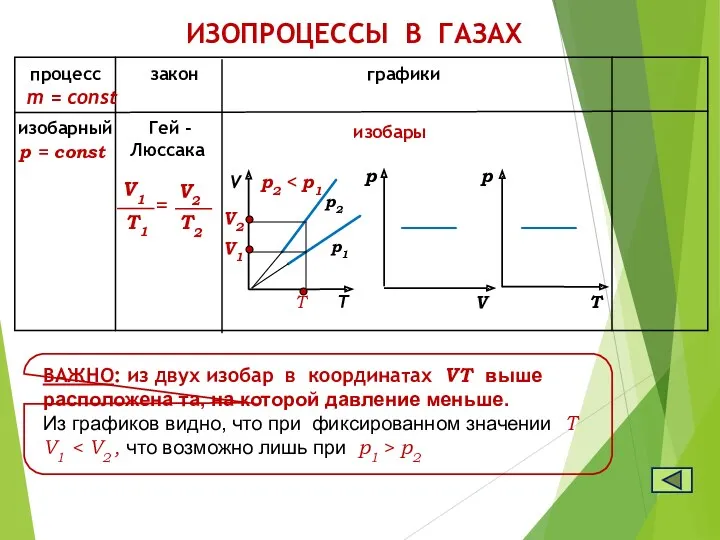

 Перший омнібус Д.Шилібіра
Перший омнібус Д.Шилібіра Система полного привода 4Motion Volkswagen. Трансмиссия
Система полного привода 4Motion Volkswagen. Трансмиссия Работа. Энергия. Механика
Работа. Энергия. Механика Физические основы механики
Физические основы механики Тепловые двигатели
Тепловые двигатели Источники света,Прямолинейное распространение света
Источники света,Прямолинейное распространение света Зубчатая передача
Зубчатая передача Сила трения. (7 класс)
Сила трения. (7 класс) Gas Dynamics (Introduction to Compressible Flow) Lecture 6a and 6b
Gas Dynamics (Introduction to Compressible Flow) Lecture 6a and 6b Основы трибофатики (трибофатика)
Основы трибофатики (трибофатика) Нанотехнологии и их применение
Нанотехнологии и их применение Проблемное обучение в преподавании физики
Проблемное обучение в преподавании физики Энтропия. Тепловые двигатели. (Лекция 10)
Энтропия. Тепловые двигатели. (Лекция 10) Система смазки и суфлирования
Система смазки и суфлирования Презентация. Обучение детей с учётом психофизиологии.
Презентация. Обучение детей с учётом психофизиологии. квантовая физика
квантовая физика Что изучает физика? Некоторые физические термины
Что изучает физика? Некоторые физические термины Урок физики в 8 классе Энергия топлива. Удельная теплота сгорания топлива
Урок физики в 8 классе Энергия топлива. Удельная теплота сгорания топлива методическая разработка урока
методическая разработка урока Internal combustion engine
Internal combustion engine презентация открытого урока: Строение атома
презентация открытого урока: Строение атома Физико-химические методы анализа
Физико-химические методы анализа Элементы машиноведения. Составные части машин
Элементы машиноведения. Составные части машин Проектирование зоны ТО-1 грузовых автомобилей с выделением шиномонтажного участка, технологический процесс ремонта колес
Проектирование зоны ТО-1 грузовых автомобилей с выделением шиномонтажного участка, технологический процесс ремонта колес Какие факторы влияют на испарение различных жидкостей
Какие факторы влияют на испарение различных жидкостей Радиационные методы контроля
Радиационные методы контроля Индикаторные и эффективные показатели ДВС. Тема 8
Индикаторные и эффективные показатели ДВС. Тема 8 игра инерция
игра инерция