Слайд 2

Жидкостная хроматография
метод разделения, в котором подвижная фаза представляет собой жидкость, а
неподвижная – твердую или жидкую фазу (не смешивающуюся с подвижной фазой).
Различают:
А. колоночную (низкого и высокого давления – ВЭЖХ или ЖХВД) и планарную (ТСХ) хроматографии.
Б. по полярности неподвижной/подвижной фаз и по механизму удерживания/разделения:
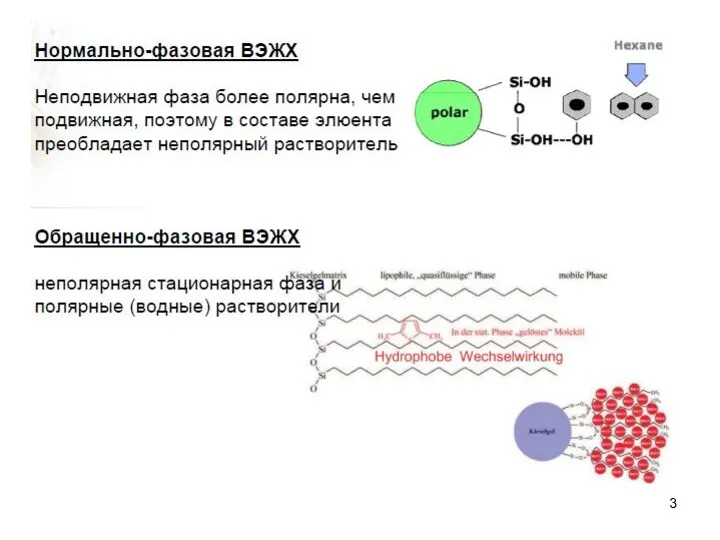
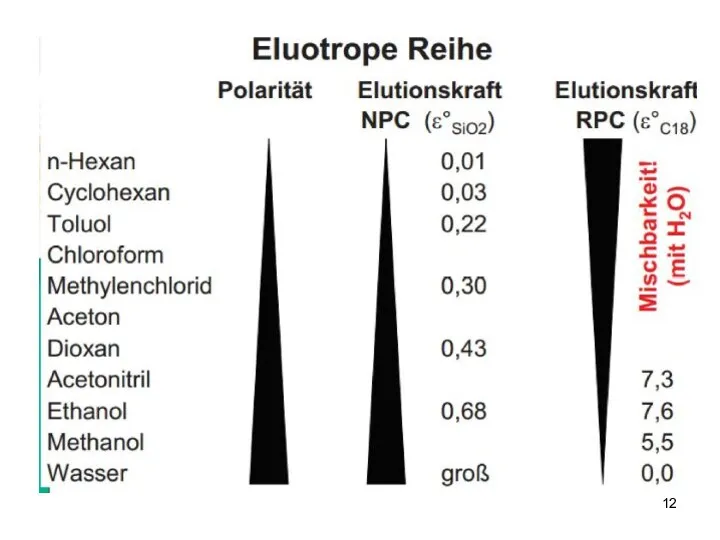
- прямо-фазовую ЖХ (НФ – полярная, ПФ – неполярные жидкости)
- обращенно-фазовую ЖХ (НФ – неполярная или среднеполярная, ПФ – полярные жидкости).
- ионообменная или ионная.
- эксклюзионная (гель-хроматография).
Слайд 3
Слайд 4
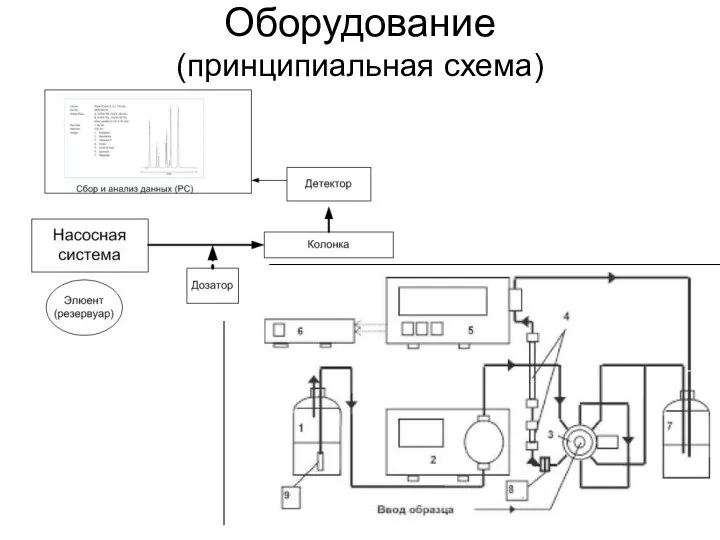
Оборудование
(принципиальная схема)
Слайд 5
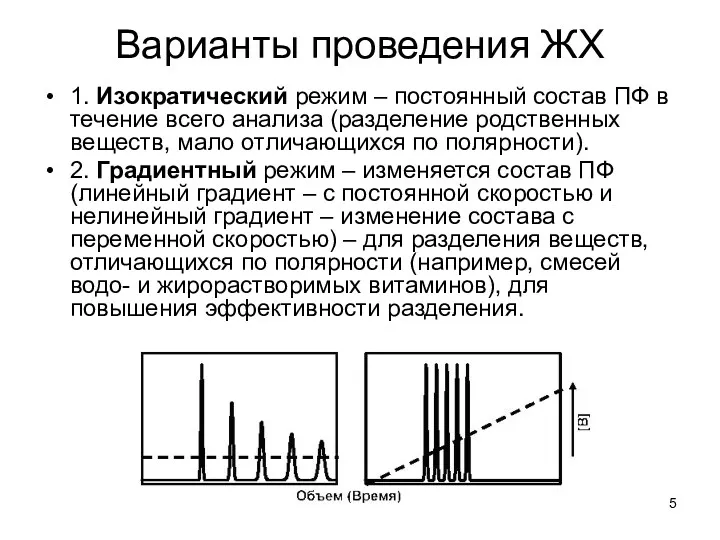
Варианты проведения ЖХ
1. Изократический режим – постоянный состав ПФ в течение
всего анализа (разделение родственных веществ, мало отличающихся по полярности).
2. Градиентный режим – изменяется состав ПФ (линейный градиент – с постоянной скоростью и нелинейный градиент – изменение состава с переменной скоростью) – для разделения веществ, отличающихся по полярности (например, смесей водо- и жирорастворимых витаминов), для повышения эффективности разделения.
Слайд 6

Хроматографические колонки
Стальные трубки внутренним диаметром 2-5 мм, длиной 5-30 см,
с пористыми фильтрами с обоих концов. Для защиты аналитической колонки используются сменные предколонки (длиной 1-2 см).
Слайд 7

Неподвижные фазы
Общие требования:
1. Для обеспечения высокой эффективности разделения – размер частиц
сорбента должен быть четко установленного размера (1,8 – 10 мкм), четко сферической формы.
2. Должен быть устойчивым к повышенному давлению (нехрупким), к химическим веществам (устойчивость при рН 2-8) и температуре (до 60-80оС).
3. Обладать высокой удельной поверхностью (60-300 м2/г) и определенным размером пор (10-300 нм).
4. Обратимая сорбция разделенных соединений.
Слайд 8
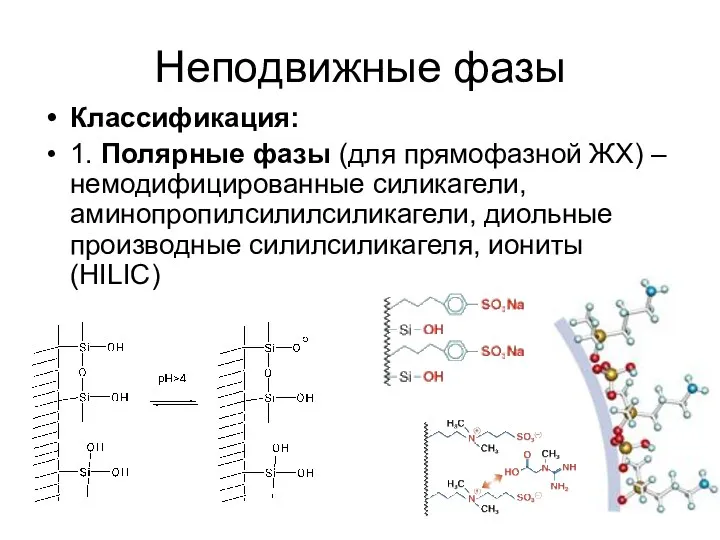
Неподвижные фазы
Классификация:
1. Полярные фазы (для прямофазной ЖХ) – немодифицированные силикагели, аминопропилсилилсиликагели,
диольные производные силилсиликагеля, иониты (HILIC)
Слайд 9
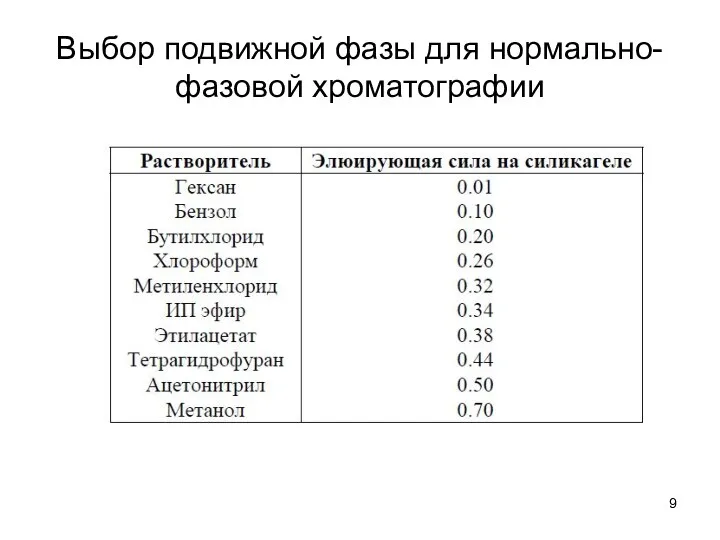
Выбор подвижной фазы для нормально-фазовой хроматографии
Слайд 10
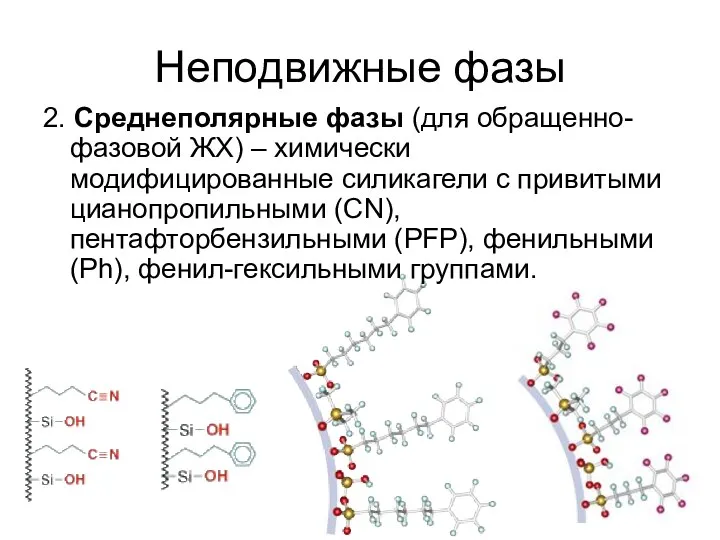
Неподвижные фазы
2. Среднеполярные фазы (для обращенно-фазовой ЖХ) – химически модифицированные силикагели
с привитыми цианопропильными (СN), пентафторбензильными (PFP), фенильными (Ph), фенил-гексильными группами.
Слайд 11

Неподвижные фазы
3. Неполярные фазы (для обращенно-фазовой ЖХ) – химически модифицированные силикагели
с привитыми октильными (С8), октадецильными (С18), фенильными и октадецильными (С18-Ph), и др.
Слайд 12
Слайд 13

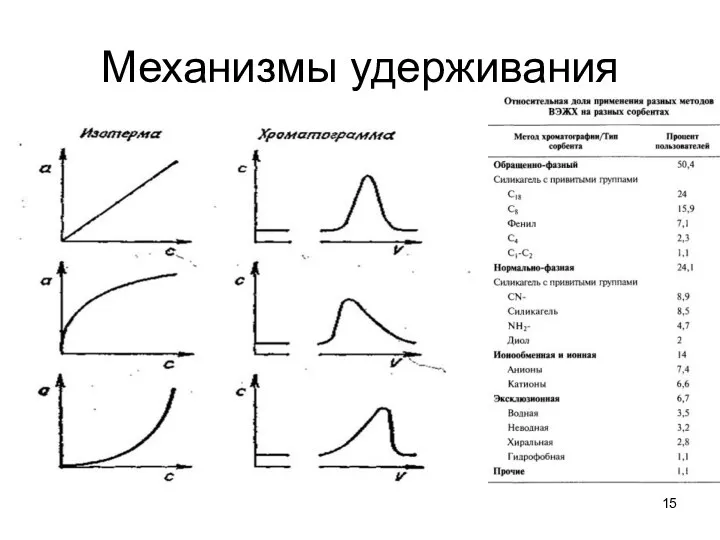
Принципы разделения
1. Полярные фазы –
1.1. для разделения неполярных и малополярных
веществ (слабо адсорбируются НФ) – малополярные элюенты (гексан (гептан) + низкая доля полярного растворителя, дихлорметан + низкая доля полярного растворителя).
1.2. для разделения полярных веществ (сильно адсорбируются НФ) – высокая доля полярных растворителей (метанол, ацетонитрил, вода), необходимо устанавливать рН (от 2 до 9), добавлять буферный раствор (ионная сила).
Слайд 14

Принципы разделения
2. Средне- и неполярные фазы:
2.1. Для разделения неполярных веществ используются
ПФ с высоким (40-100%) содержанием органического растворителя (ацетонитрил, метанол, тетрагидрофуран).
2.2. Для разделения ионизируемых органических веществ (кислот, оснований, амфолитов, ионов) необходимо использовать буферные растворы (рН 2-8 или для ряда колонок – 1-10).
2.3. Для разделения органических ионов и сильнополярных веществ – прибавляют ион-парные реагенты (алкилсульфонаты, четвертичные аммониевые соли).
Слайд 15
Слайд 16
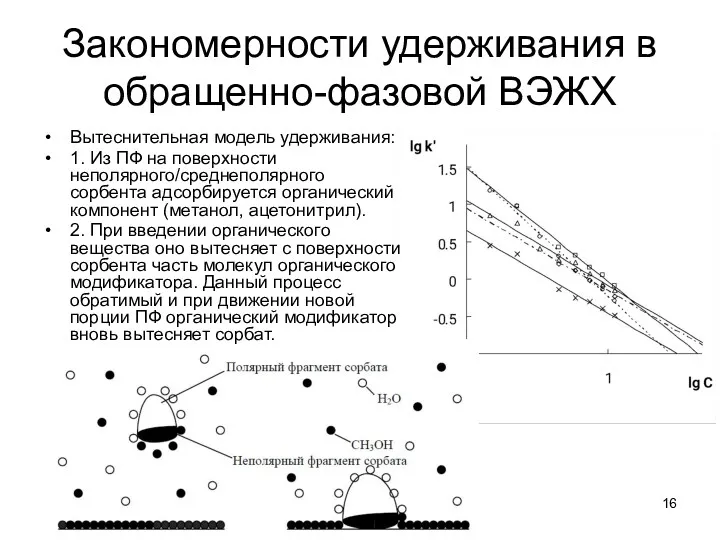
Закономерности удерживания в обращенно-фазовой ВЭЖХ
Вытеснительная модель удерживания:
1. Из ПФ на
поверхности неполярного/среднеполярного сорбента адсорбируется органический компонент (метанол, ацетонитрил).
2. При введении органического вещества оно вытесняет с поверхности сорбента часть молекул органического модификатора. Данный процесс обратимый и при движении новой порции ПФ органический модификатор вновь вытесняет сорбат.
Слайд 17

Влияние рН ПФ и температуры
На неполярных фазах за счет дисперсионных взаимодействий
лучше удерживаются неионизированные молекулы. При ионизации молекул удерживание при прочих равных условиях уменьшается.
Температура незначительно влияет на удерживание органических молекул в водно-органических фазах. При повышении температуры уменьшается вязкость ПФ и давление на колонке (возможно работать на более высоких скоростях ПФ).
Слайд 18
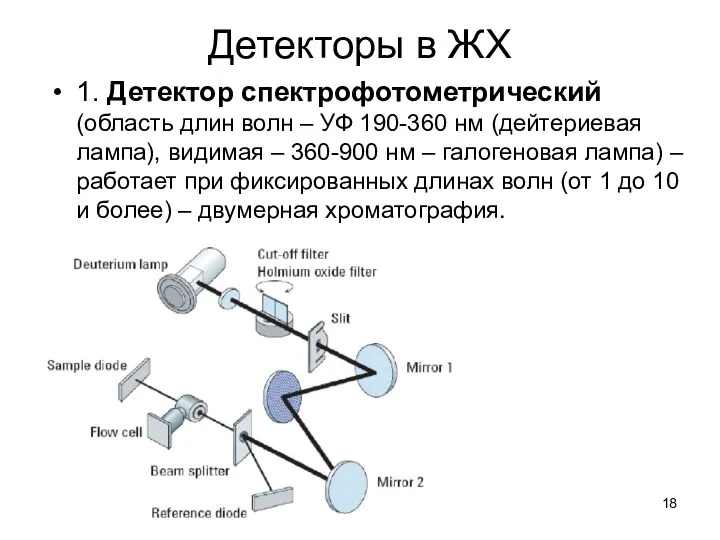
Детекторы в ЖХ
1. Детектор спектрофотометрический (область длин волн – УФ 190-360
нм (дейтериевая лампа), видимая – 360-900 нм – галогеновая лампа) – работает при фиксированных длинах волн (от 1 до 10 и более) – двумерная хроматография.
Слайд 19
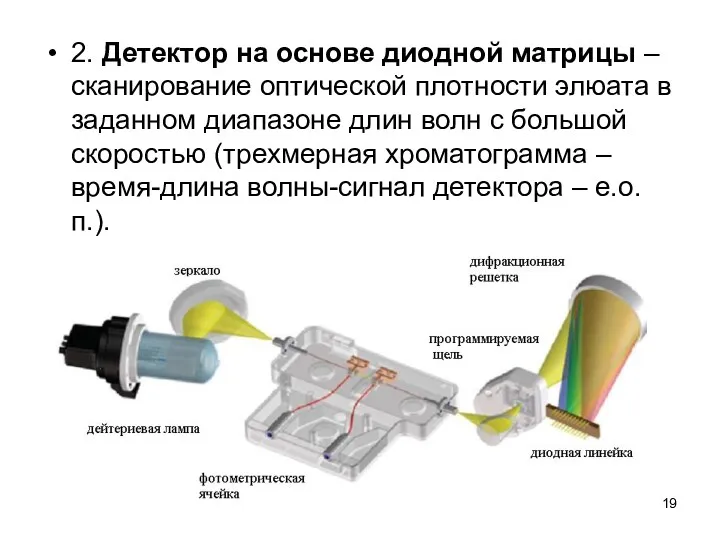
2. Детектор на основе диодной матрицы – сканирование оптической плотности элюата
в заданном диапазоне длин волн с большой скоростью (трехмерная хроматограмма – время-длина волны-сигнал детектора – е.о.п.).
Слайд 20
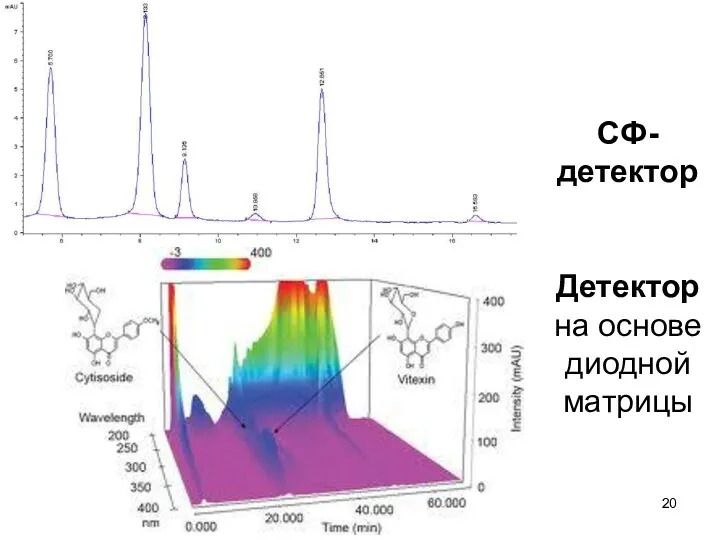
СФ-детектор
Детектор на основе диодной матрицы
Слайд 21
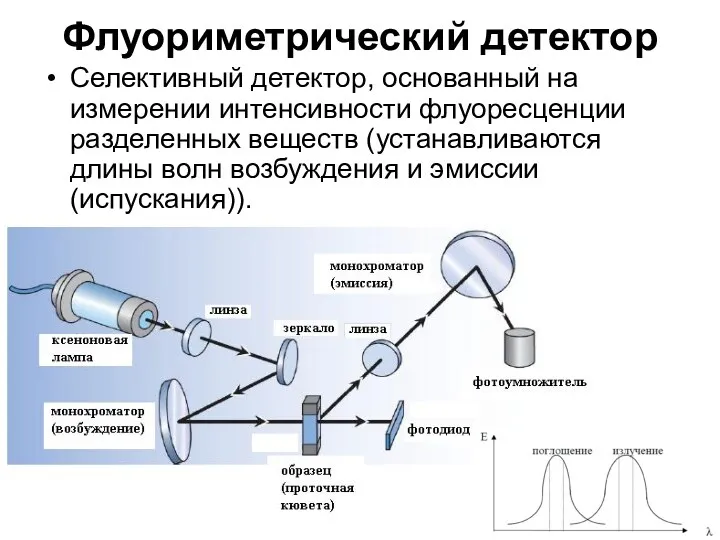
Флуориметрический детектор
Селективный детектор, основанный на измерении интенсивности флуоресценции разделенных веществ (устанавливаются
длины волн возбуждения и эмиссии (испускания)).
Слайд 22
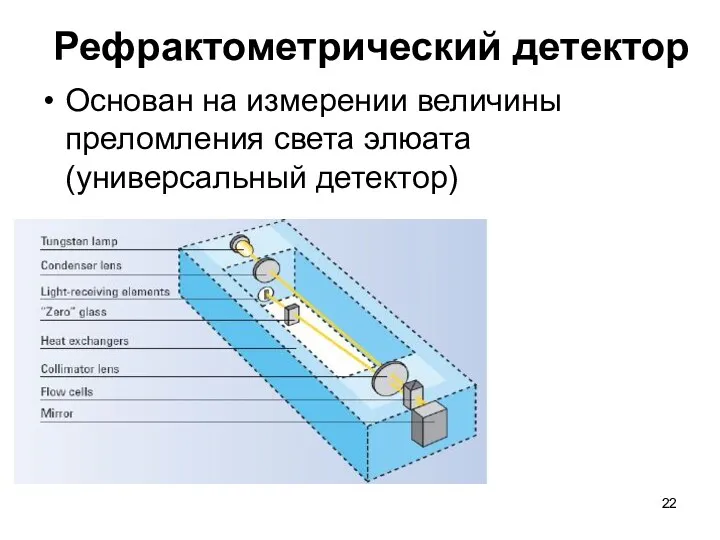
Рефрактометрический детектор
Основан на измерении величины преломления света элюата (универсальный детектор)
Слайд 23
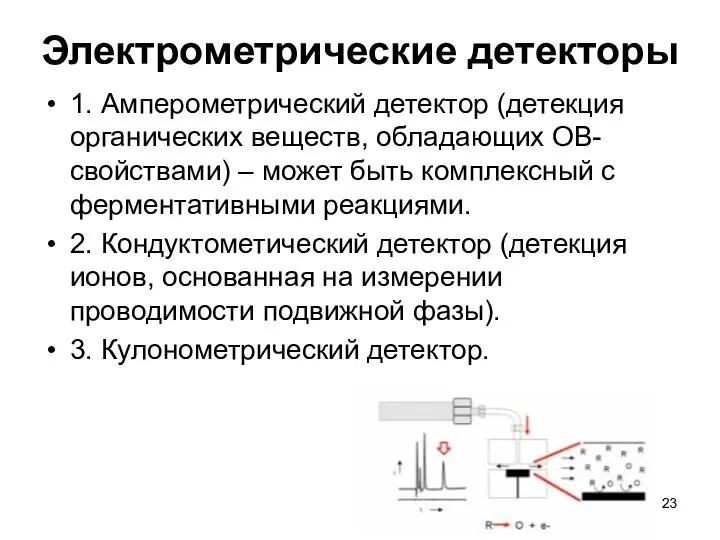
Электрометрические детекторы
1. Амперометрический детектор (детекция органических веществ, обладающих ОВ-свойствами) – может
быть комплексный с ферментативными реакциями.
2. Кондуктометический детектор (детекция ионов, основанная на измерении проводимости подвижной фазы).
3. Кулонометрический детектор.
Слайд 24
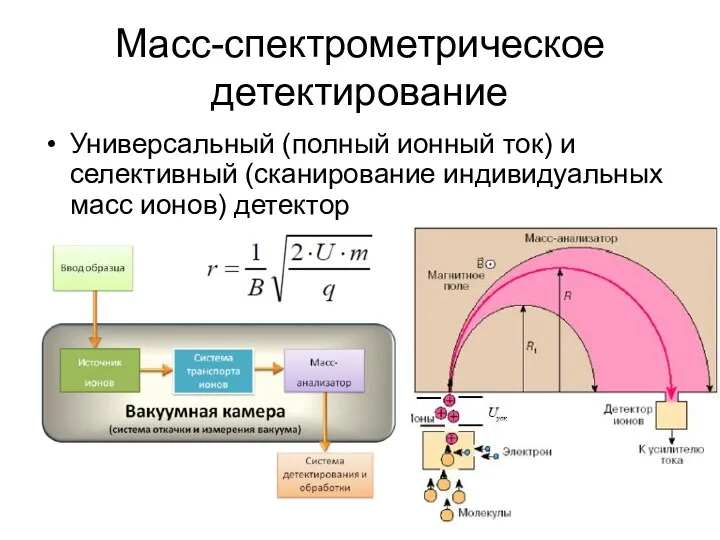
Масс-спектрометрическое детектирование
Универсальный (полный ионный ток) и селективный (сканирование индивидуальных масс ионов)
детектор
Слайд 25

Слайд 26
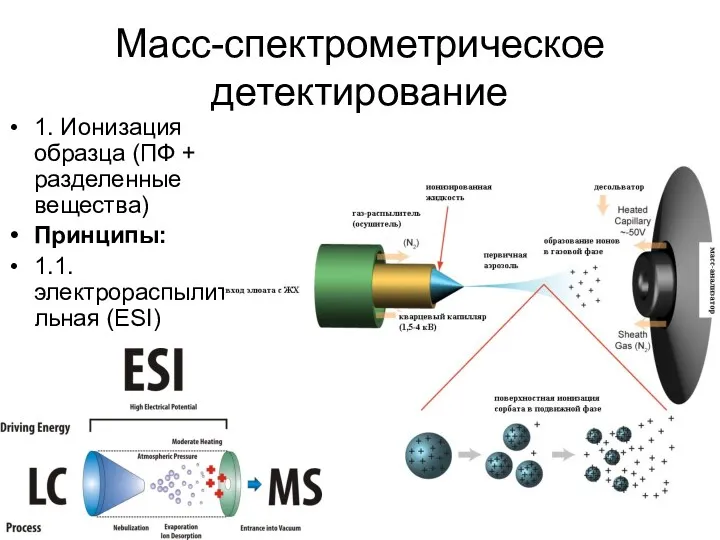
Масс-спектрометрическое детектирование
1. Ионизация образца (ПФ + разделенные вещества)
Принципы:
1.1. электрораспылительная (ESI)
Слайд 27
Слайд 28
Слайд 29
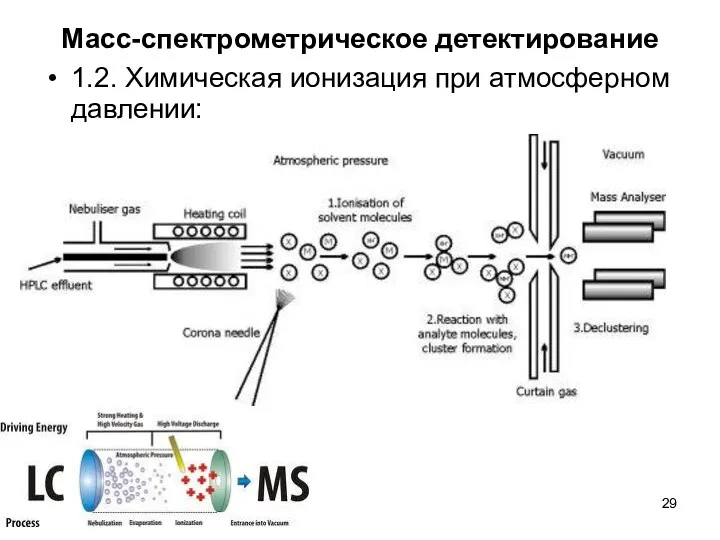
Масс-спектрометрическое детектирование
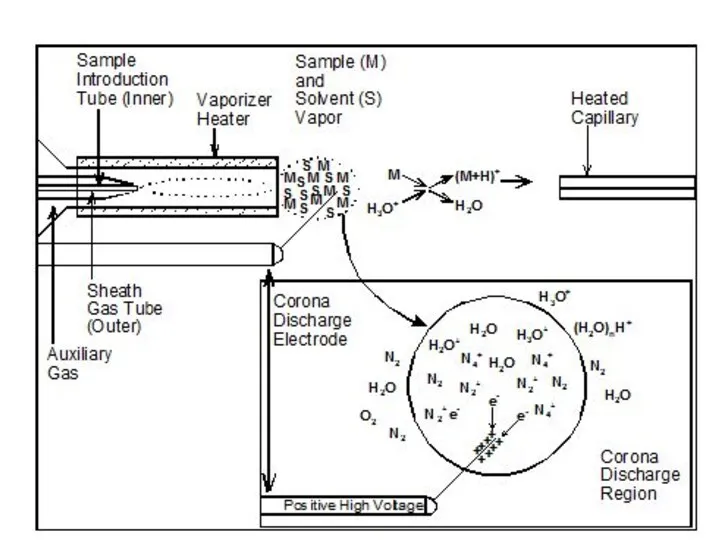
1.2. Химическая ионизация при атмосферном давлении:
Слайд 30
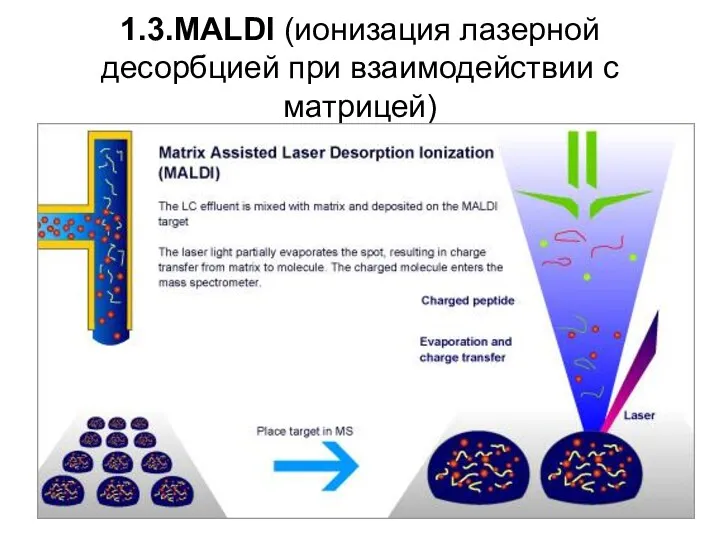
1.3.MALDI (ионизация лазерной десорбцией при взаимодействии с матрицей)
Слайд 31
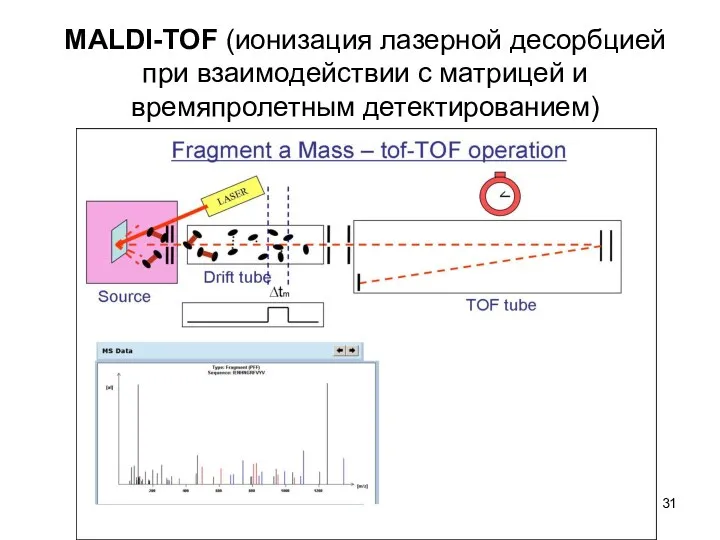
MALDI-TOF (ионизация лазерной десорбцией при взаимодействии с матрицей и времяпролетным детектированием)
Слайд 32

Масс-анализаторы
А. непрерывные масс-анализаторы
1. Магнитный и электростатический секторный масс-анализатор (Sector)
2. Квадрупольный масс-анализатор (Quadrupole mass
analyzer)
Б. импульсные масс-анализаторы
1. Времяпролётный масс-анализатор (Time-of-flight mass spectrometry)
2. Ионная ловушка (Ion trap)
3. Квадрупольная линейная ловушка (Quadrupole ion trap)
4. Масс-анализатор ионно-циклотронного резонанса с Фурье-преобразованием (Fourier transform ion cyclotron resonance)
5. Орбитрэп (Orbitrap)
Слайд 33

Масс-спектрометрическое детектирование
Достоинства:
1. Высочайшая чувствительность органических веществ, биополимеров (10-15 г/пробе).
2. Высокая специфичность
детекции (последовательная масс-спектрометрия (дочерних ионов)).
3. Метод сбора информации о структуре молекул (точность установления молярных масс – до 0,0001-0,000001 а.е.м.).
4. Широкий линейный диапазон – 106-107.
5. Наличие баз данных по масс-спектрам огромного числа органических веществ (для ГХ/МС).
6. Основной детектор при проведении биоэквивалентных испытаний, допинг-контроля, судебно-химической экспертизы, исследования метаболизма, генеза БАВ и др.
Недостатки:
1. Сложность и высокая стоимость оборудования и расходных материалов.
2. Необходимо дополнительное обучение непосредственно масс-спектрометрии и интерпретации спектров.
Слайд 34
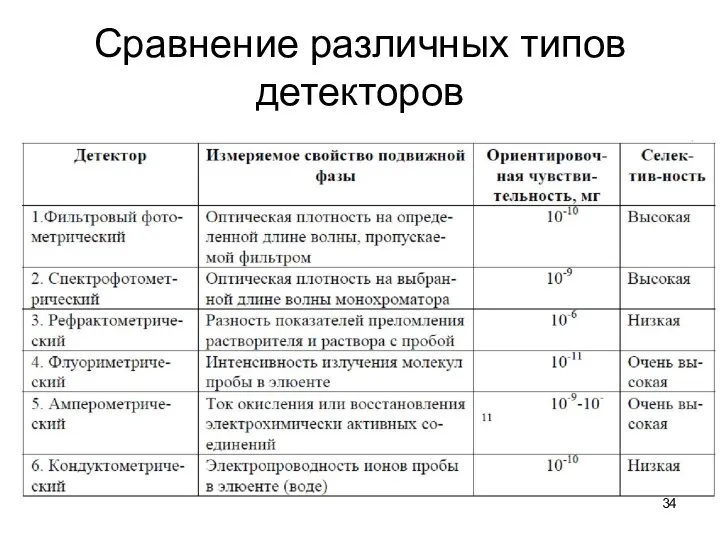
Сравнение различных типов детекторов
Слайд 35
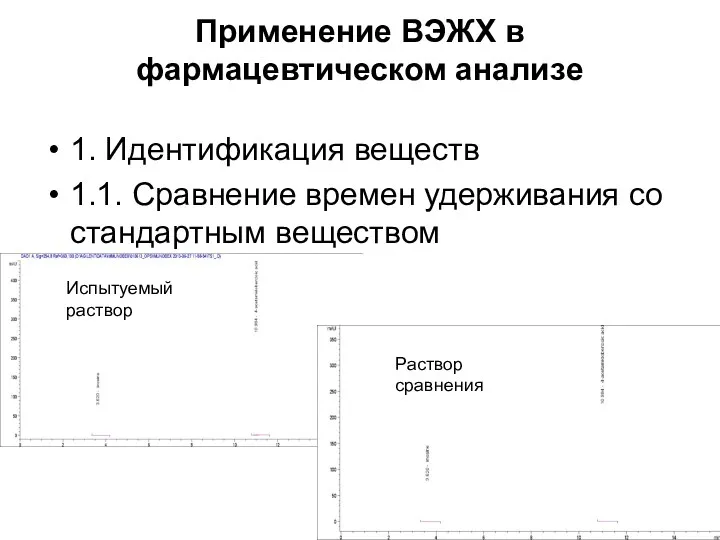
Применение ВЭЖХ в фармацевтическом анализе
1. Идентификация веществ
1.1. Сравнение времен удерживания со
стандартным веществом
Раствор сравнения
Испытуемый раствор
Слайд 36
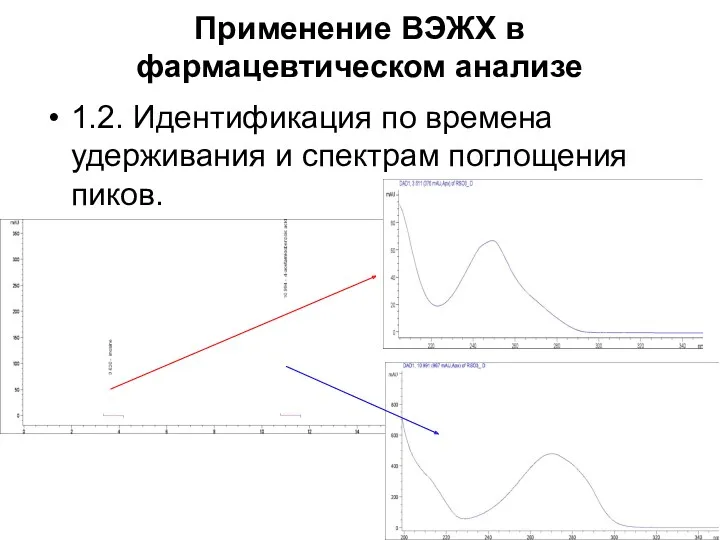
Применение ВЭЖХ в фармацевтическом анализе
1.2. Идентификация по времена удерживания и спектрам
поглощения пиков.
Слайд 37
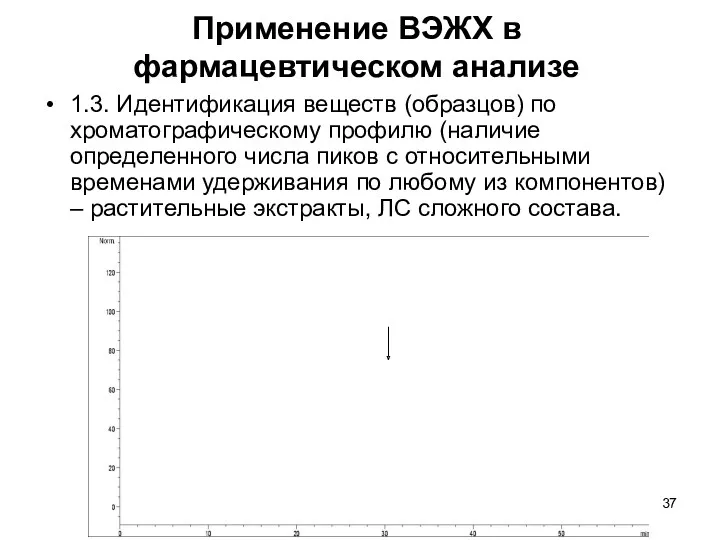
Применение ВЭЖХ в фармацевтическом анализе
1.3. Идентификация веществ (образцов) по хроматографическому профилю
(наличие определенного числа пиков с относительными временами удерживания по любому из компонентов) – растительные экстракты, ЛС сложного состава.
Слайд 38
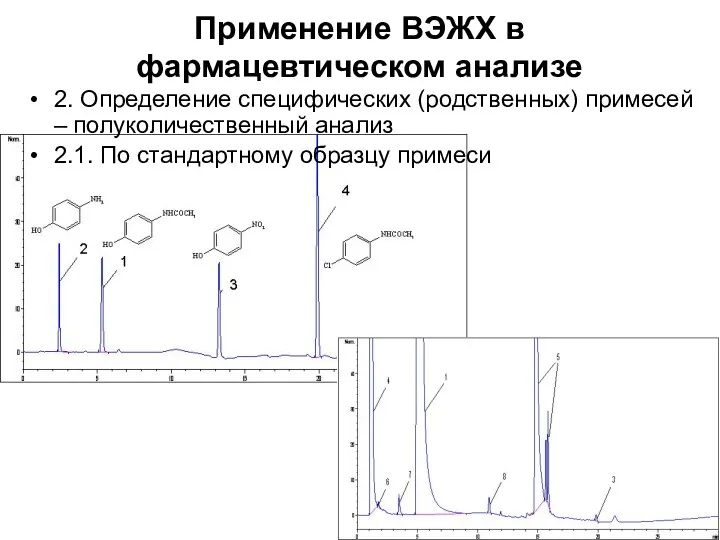
Применение ВЭЖХ в фармацевтическом анализе
2. Определение специфических (родственных) примесей – полуколичественный
анализ
2.1. По стандартному образцу примеси
Слайд 39
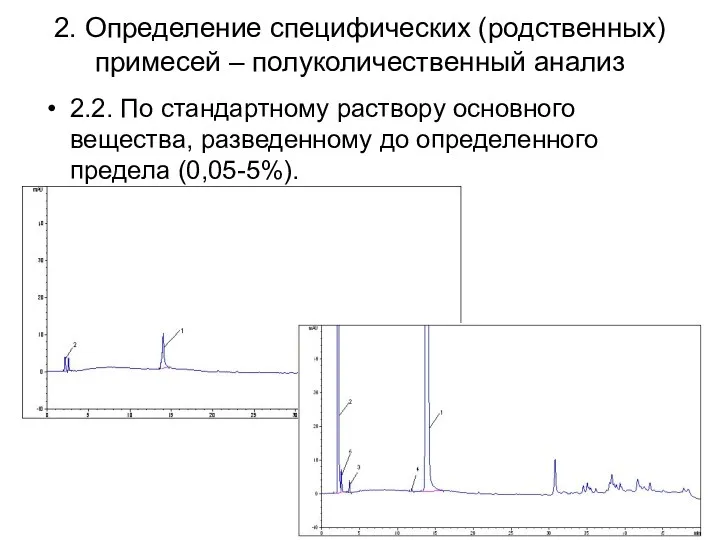
2. Определение специфических (родственных) примесей – полуколичественный анализ
2.2. По стандартному раствору
основного вещества, разведенному до определенного предела (0,05-5%).
Слайд 40
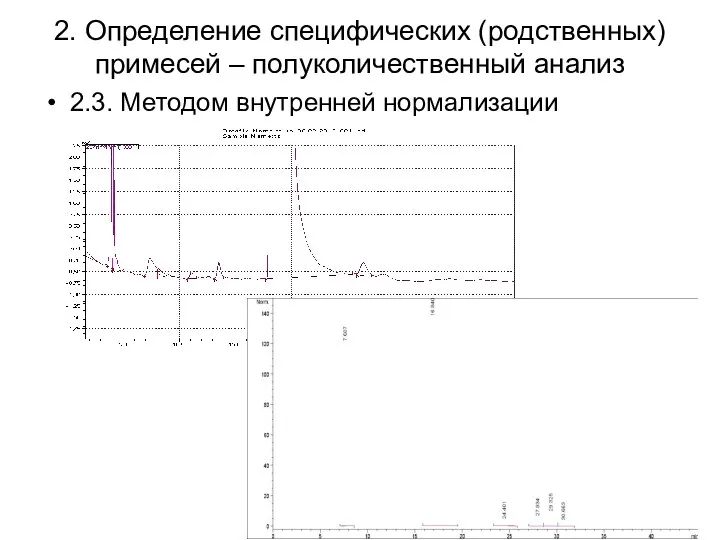
2. Определение специфических (родственных) примесей – полуколичественный анализ
2.3. Методом внутренней нормализации
Слайд 41
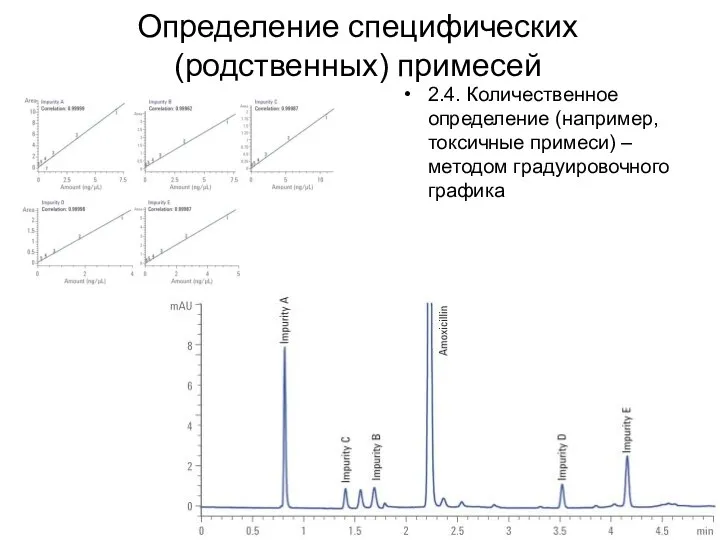
Определение специфических (родственных) примесей
2.4. Количественное определение (например, токсичные примеси) – методом
градуировочного графика
Слайд 42
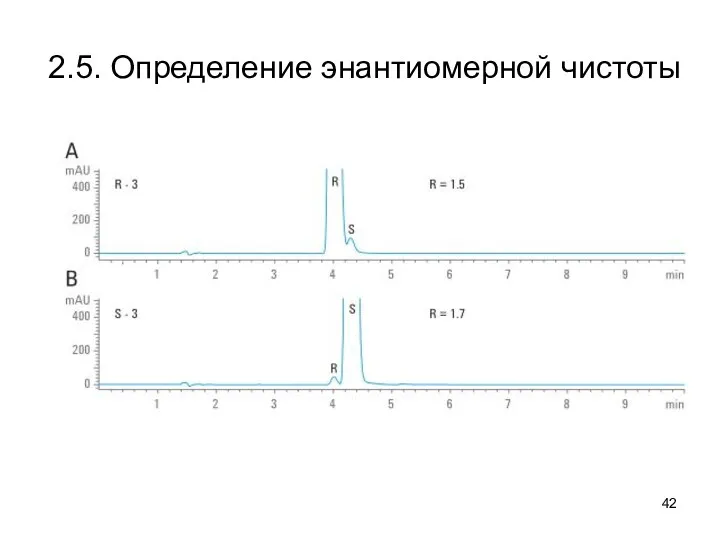
2.5. Определение энантиомерной чистоты
Слайд 43

Применение ВЭЖХ в фармацевтическом анализе
3. Определение основных показателей готовых лекарственных средств
– однородность дозированных единиц, тест «Растворение», количественное определение стабилизаторов, консервантов, красителей и др.
4. Определение пластификаторов в упаковочных материалах.
5. Определение остаточных количеств пестицидов (гербицидов, инсектицидов) в ЛРС, продуктах из ЛРС.
6. Определение остаточных количеств активных фармацевтических ингредиентов на оборудовании (контроль отмывки оборудования), в сточных водах.
Слайд 44

Капиллярный электрофорез
Метод капиллярного электрофореза (КЭ) основан на разделении заряженных компонентов сложной
смеси в кварцевом капилляре под действием приложенного электрического поля за счёт подачи высокого напряжения к концам капилляра.
Наиболее распространёнными вариантами метода КЭ являются: 1 капиллярный зонный электрофорез (КЗЭ)
2. мицеллярная электрокинетическая хроматография (МЭКХ).
КЗЭ - метод разделения, реализуемый в капиллярах и основанный на различии в электрокинетических подвижностях заряженных частиц как в водных, так и в неводных электролитах.
Слайд 45

Капиллярный электрофорез
МЭКХ - вариант капиллярного электрофореза, который позволяет проводить разделение соединений
ионного и нейтрального характера при использовании ПАВ. Разделение электро-нейтральных соединений осуществляется благодаря введению в состав ведущего электролита поверхностно-активных веществ - мицеллообразователей. Чаще всего используют анионный ПАВ (например, ДДС) в концентрациях, превышающих критическую концентрацию мицелообразования, что приводит к формированию так называемой «псевдостационарной фазы», и аналиты распределяются между мицеллой и буферным электролитом согласно их гидрофобности.
Слайд 46
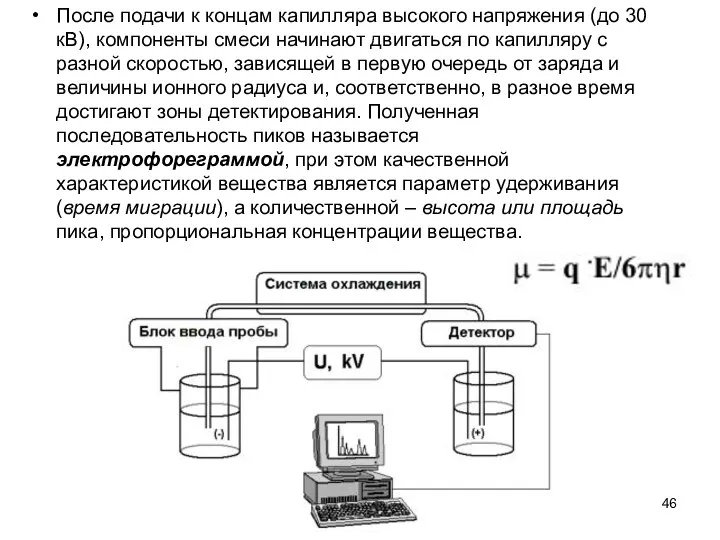
После подачи к концам капилляра высокого напряжения (до 30 кВ), компоненты
смеси начинают двигаться по капилляру с разной скоростью, зависящей в первую очередь от заряда и величины ионного радиуса и, соответственно, в разное время достигают зоны детектирования. Полученная последовательность пиков называется электрофореграммой, при этом качественной характеристикой вещества является параметр удерживания (время миграции), а количественной – высота или площадь пика, пропорциональная концентрации вещества.
Слайд 47

Основные параметры КЭ
1. Время миграции (tм) - время, необходимое компоненту для
прохождения им эффективной длины капилляра (Lэфф) от зоны ввода пробы (начала капилляра) до зоны детектирования;
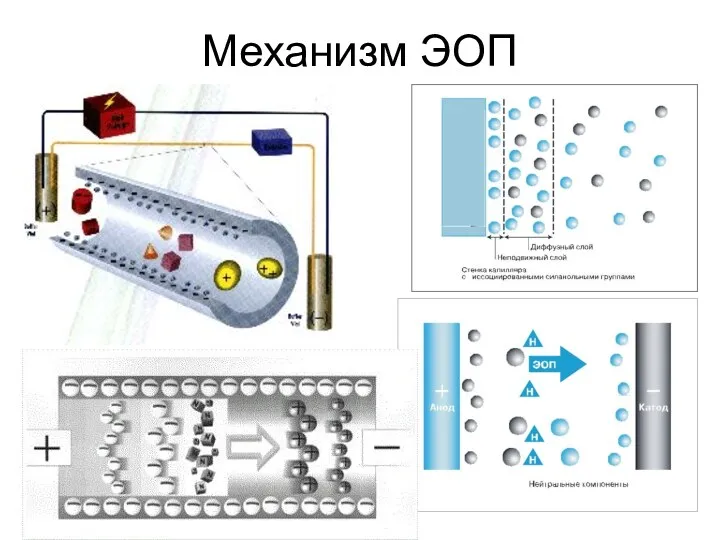
2. Электроосмотический поток (ЭОП) - течение жидкости в капилляре под действием приложенного электрического поля. Время, необходимое жидкости для преодоления эффективной длины капилляра вследствие возникающего ЭОП, называют временем ЭОП (tэоп) и экспериментально определяют из электрофореграммы по времени миграции нейтрального компонента – маркера ЭОП.
3. Подвижность ЭОП (μэоп) - представляет собой отношение скорости ЭОП к напряженности электрического поля. Скорость ЭОП положительна при направлении движения жидкости от входного участка капилляра к детектору и отрицательна при обратном направлении. В свою очередь, скорость ЭОП вычисляют по формуле:
νэоп= Lэфф / tэоп.
Слайд 48
Слайд 49
Слайд 50

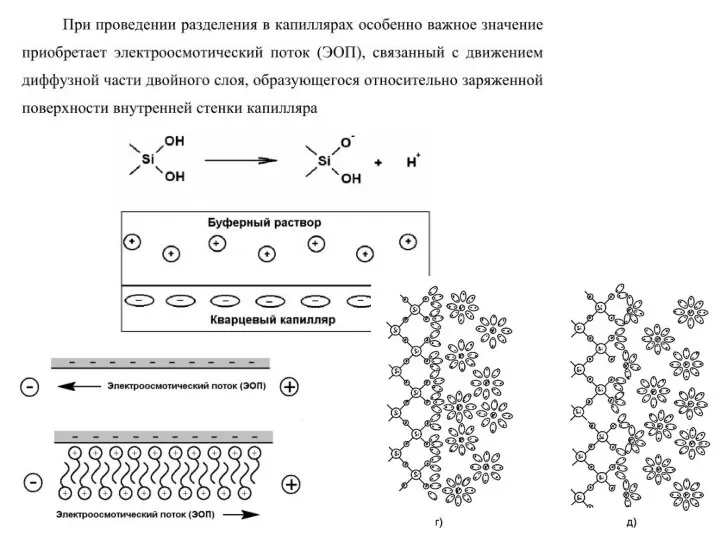
Электроосмотический поток
Уникальной особенностью ЭОП является плоский профиль потока в капилляре. Такой
профиль выгоден, поскольку уменьшается размывание зон разделяемых веществ. Следует отметить, что эффективность разделения в капиллярном электрофорезе прямо пропорциональна, а время анализа – обратно пропорционально напряжению, приложенному к электродам. Разделение в КЭ может быть выполнено как с положительной, так и отрицательной полярностью электродов. Зная значения рКа для компонентов пробы, можно выбрать буфер с подходящим значением рН и полярность электродов, чтобы образец двигался в сторону детектора. Скорость миграции зависит от напряженности электрического поля, которая обычно составляет 200-400 В/см.
Слайд 51

Капилляры для разделения
Подавляющее большинство разделений в КЭ проводят с использованием кварцевых
капилляров имеющих внешнее полимерное покрытие, обычно - полиимидное, улучшающее их механическую прочность, и значительно реже полимерные капилляры, например из тефлона. Внутренний диаметр капилляров колеблется в пределах от 25 до 200 микрон, а длина капилляра в зависимости от поставленной задачи – от нескольких сантиметров до 1 метра. Поскольку внешнее полиимидное покрытие непрозрачно в УФ-области, то участок покрытия удаляют и создают окно для УФ-детектирования. Капилляр закрепляется в специальной пластиковой кассете.
Надежное термостатирование капилляра является основным условием получения воспроизводимых времен миграции определяемого соединения и площади результирующего пика, что важно для количественного анализа. Используют капилляры с внутренним диаметром 25-50 мкм, что является компромиссным решением между достаточно высокой чувствительностью и эффективностью разделения.
Слайд 52

Ввод образца
Проба может быть введена в капилляр электрофоретическим, электрокинетическим или вытеснительным
способом. Объем вводимой пробы не превышает 2 нл, относительное стандартное отклонение составляет 0,03-0,04. При электрофоретическом вводе пробы, к концам капилляра прикладывается высокое напряжение на фиксированный промежуток времени, при этом входной конец капилляра погружают в раствор пробы. Ионы пробы перемещаются в капилляр пропорционально их электрофоретической подвижности. В случае электрокинетического ввода, компоненты пробы попадают в капилляр за счет комбинации электроэндоосмотического давления и электрофоретической подвижности. Вытеснительный ввод пробы достигается либо за счет создания избыточного внешнего давления инертного газа, приложенного к резервуару с образцом, либо за счет создания вакуума на выходе из капилляра или путем изменения уровня/высоты резервуара, содержащего образец, относительно резервуара с буферным раствором на выходе из капилляра (так называемое гравитационное введение пробы).
Слайд 53

Слайд 54
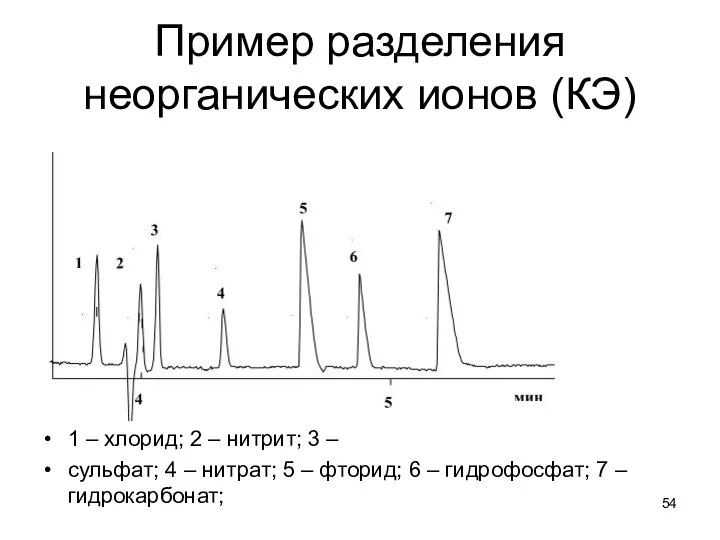
Пример разделения неорганических ионов (КЭ)
1 – хлорид; 2 – нитрит; 3
–
сульфат; 4 – нитрат; 5 – фторид; 6 – гидрофосфат; 7 – гидрокарбонат;
Слайд 55

Слайд 56

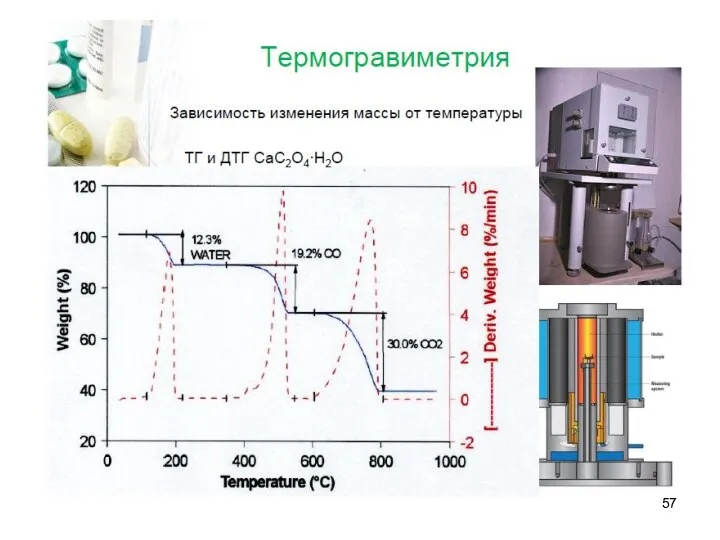
Термические методы анализа
Основаны на установлении зависимостей различных физических или физико-химических свойств
веществ от температуры (градиента температуры).
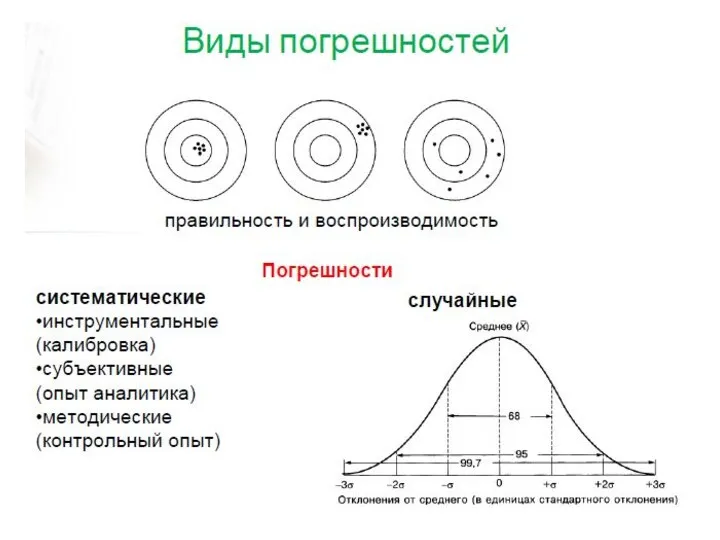
А – Термогравиметрия
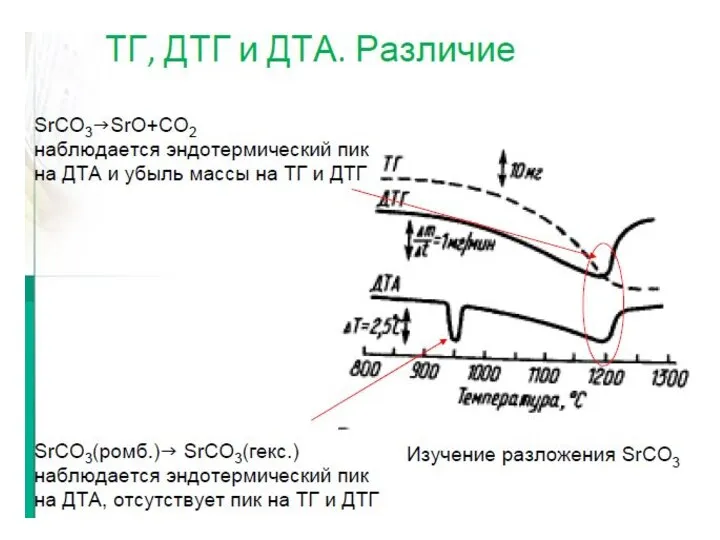
Б – Дифференциальный термический анализ
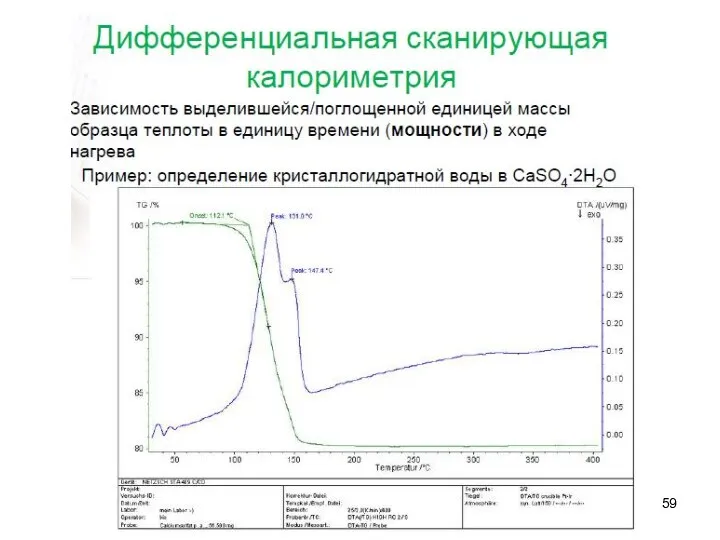
В – Дифференциальная сканирующая калориметрия
Слайд 57
Слайд 58

Слайд 59
Слайд 60

Слайд 61
Слайд 62
Слайд 63

Слайд 64

Слайд 65

Слайд 66

Слайд 67

Слайд 68




































































 Закон радиоактивного распада. Период полураспада
Закон радиоактивного распада. Период полураспада Ядерный магнитный резонанс
Ядерный магнитный резонанс Сила тока
Сила тока Камера-обскура. Интересные факты
Камера-обскура. Интересные факты Thermal Energy, Chemical Energy
Thermal Energy, Chemical Energy Система мащення охолодження та пуску ДВЗ
Система мащення охолодження та пуску ДВЗ ФИЗИКА 8 класс Изменение агрегатных состояний вещества
ФИЗИКА 8 класс Изменение агрегатных состояний вещества Методическое пособие по теме Геометрическая оптика
Методическое пособие по теме Геометрическая оптика Вантажопідйомні машини. Держгірпромнагляд
Вантажопідйомні машини. Держгірпромнагляд Электростатика
Электростатика Управляемый термоядерный синтез. Данные
Управляемый термоядерный синтез. Данные Люминесцентные лампы
Люминесцентные лампы Сила трения
Сила трения Жарықтың интерференциясы
Жарықтың интерференциясы Викторина на тему: Дисперсия света
Викторина на тему: Дисперсия света Рулевое управление
Рулевое управление открытый урок тепловые машины
открытый урок тепловые машины Методы и средства измерения частоты, временных интервалов и фазового сдвига
Методы и средства измерения частоты, временных интервалов и фазового сдвига Ғажайып ұяшықтар
Ғажайып ұяшықтар Семинарское занятие Основы электростатики. 10 класс.
Семинарское занятие Основы электростатики. 10 класс. Виды спектров и спектральный анализ. Тема №48
Виды спектров и спектральный анализ. Тема №48 Принципы построения системы допусков и посадок (СДП
Принципы построения системы допусков и посадок (СДП Своя игра. Простые механизмы
Своя игра. Простые механизмы Внутреннняя энергия
Внутреннняя энергия Выяснение условия равновесия рычага
Выяснение условия равновесия рычага Урок физики в 7 классе Инерция
Урок физики в 7 классе Инерция Структурный анализ плоских механизмов
Структурный анализ плоских механизмов Электричество и Магнетизм
Электричество и Магнетизм