Содержание
- 2. Пирогов Андрей Владимирович (д.х.н., профессор) Тел. ком.
- 3. Рассмотрим: Определение хроматографии и история метода Причины широкого распространения хроматографии в современной аналитической химии Основные понятия
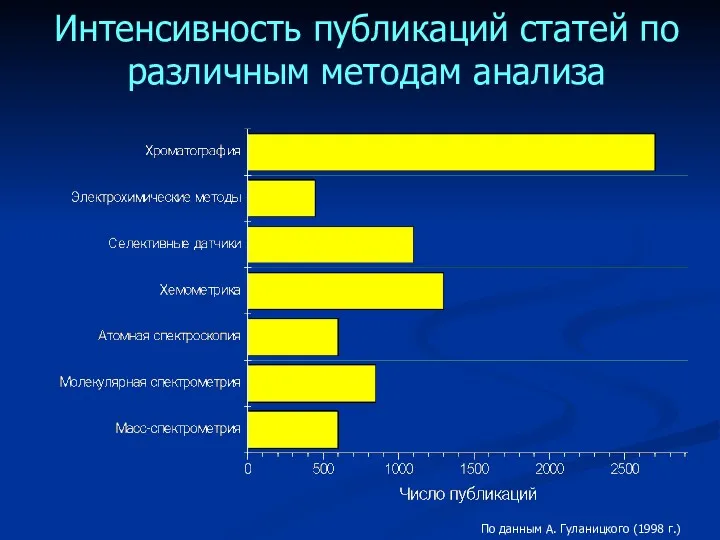
- 4. Интенсивность публикаций статей по различным методам анализа По данным А. Гуланицкого (1998 г.)
- 6. В чем причины? Создание новых веществ, типов лекарств, красителей и т.п. Расширение списка контролируемых соединений Снижение
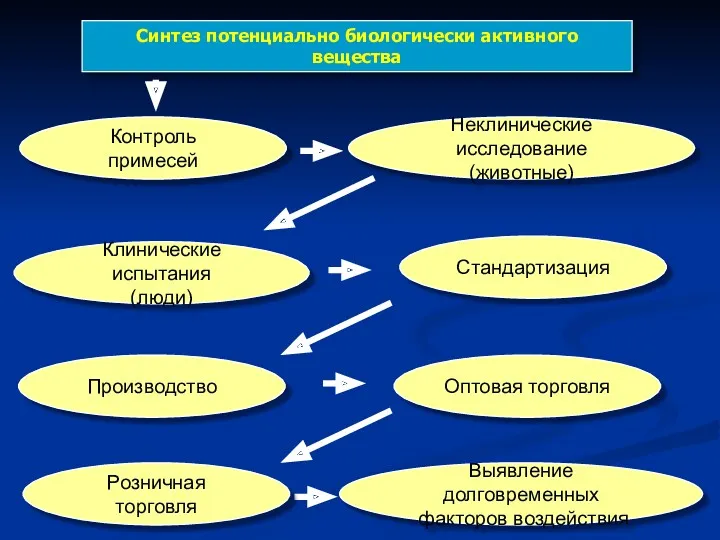
- 7. Синтез потенциально биологически активного вещества
- 8. Решаемые с помощью хроматографии фундаментальные задачи Изучение термодинамики и кинетики распределения неорганических веществ в двухфазной системе
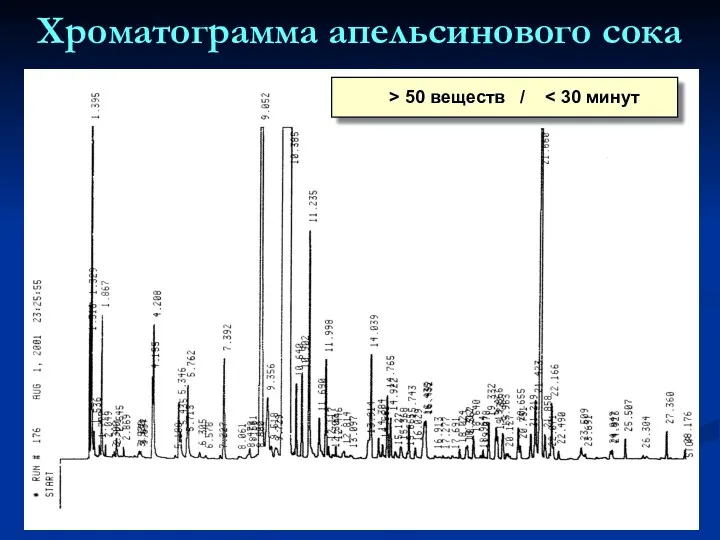
- 9. Хроматограмма апельсинового сока
- 10. Михаил Семенович Цвет
- 11. Здесь была открыта хроматография
- 12. Этапы развития хроматографии 1903 г. Открытие хроматографии (Цвет М.С.) 1931 г. Повторение опытов Цвета (Кун Р.)
- 13. Этапы развития хроматографии (продолжение) 1956 г. Капиллярная газовая хр-фия (Golay M.) 1960е гг. Высокоэффективная жидкостная хр-фия
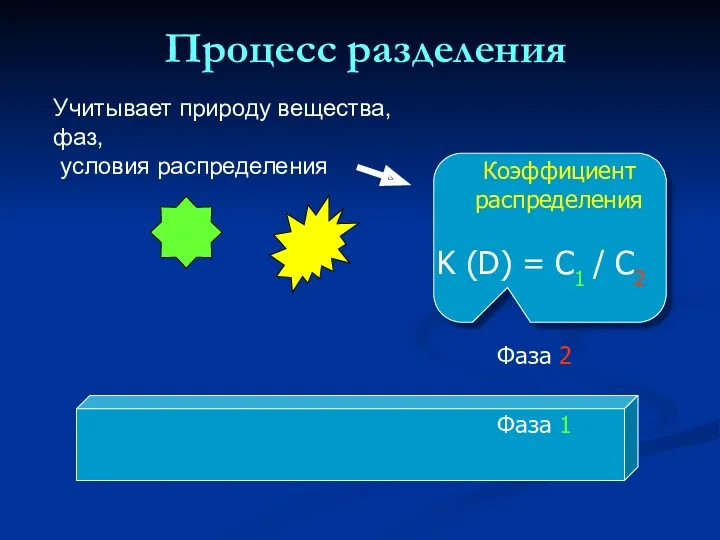
- 14. Процесс разделения Фаза 2
- 15. Динамический процесс разделения
- 16. ХРОМАТОГРАФИЯ Определение (Научный совет по хроматографии и адсорбции РАН) НАУКА О межмолекулярных взаимодействиях и переносе молекул
- 17. Процесс разделения Элюент Элюат
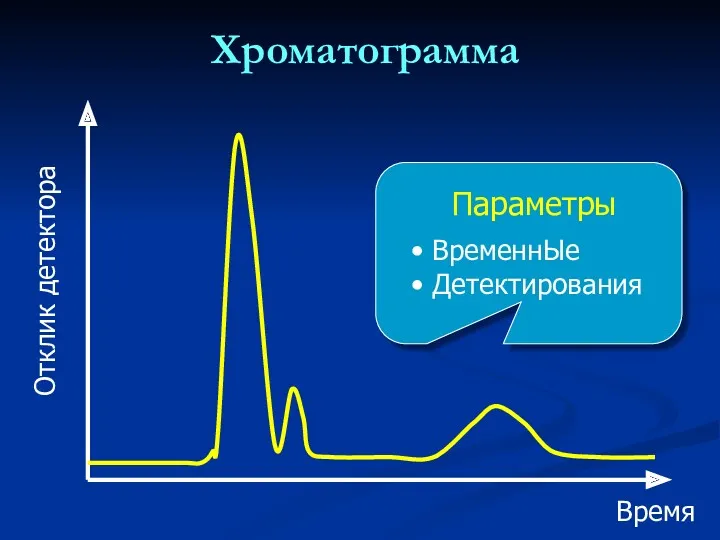
- 18. Хроматограмма Время Отклик детектора
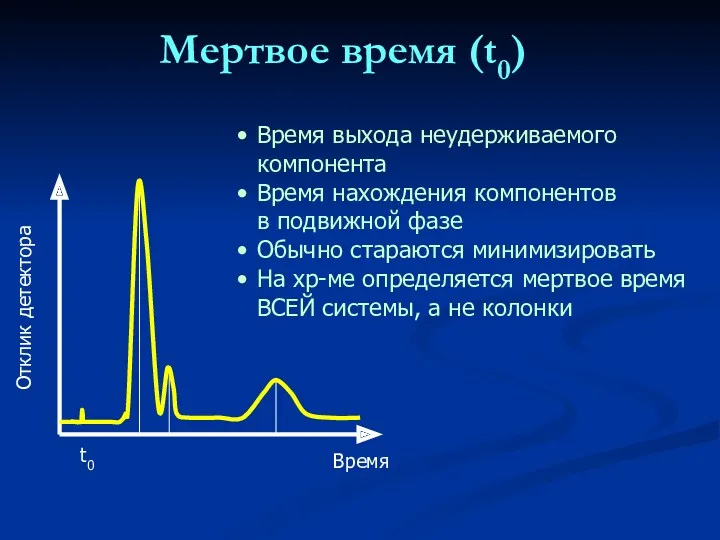
- 19. Мертвое время (t0) Время выхода неудерживаемого компонента Время нахождения компонентов в подвижной фазе Обычно стараются минимизировать
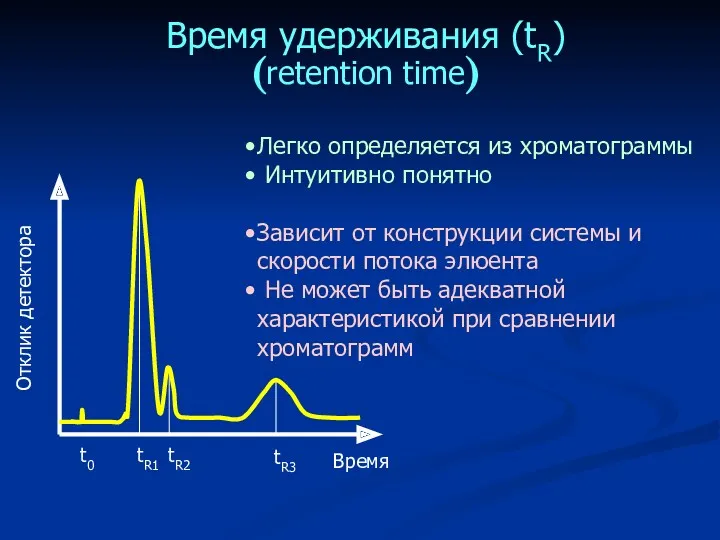
- 20. Время удерживания (tR) (retention time) Легко определяется из хроматограммы Интуитивно понятно Зависит от конструкции системы и
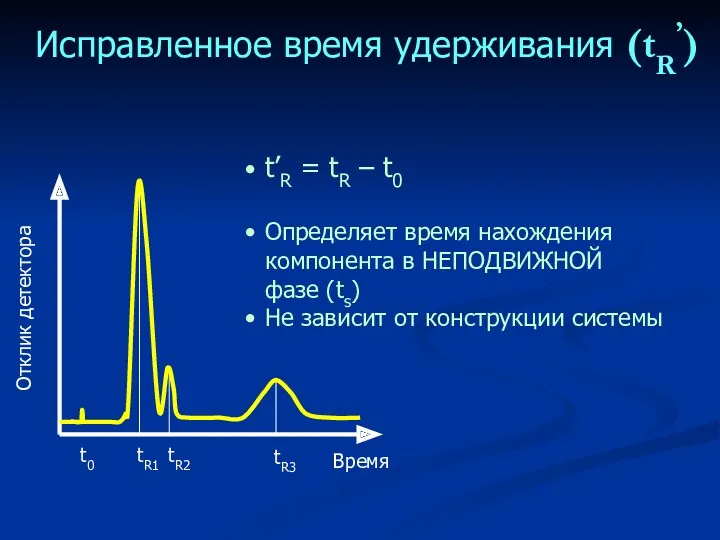
- 21. Исправленное время удерживания (tR’) t’R = tR – t0 Определяет время нахождения компонента в НЕПОДВИЖНОЙ фазе
- 22. Удерживаемый объем (Vx) Исправленный удерживаемый объём (V’x) V’R = t’Rx * F V’R = VR –
- 23. Фактор удерживания К (коэффициент емкости) Коэффициент емкости К = (tRx − t0) /t0 - отношение исправленного
- 24. Индекс удерживания I (индекс Ковача) где tRn−1 и tRn+1 — время удерживания н-алканов с n и
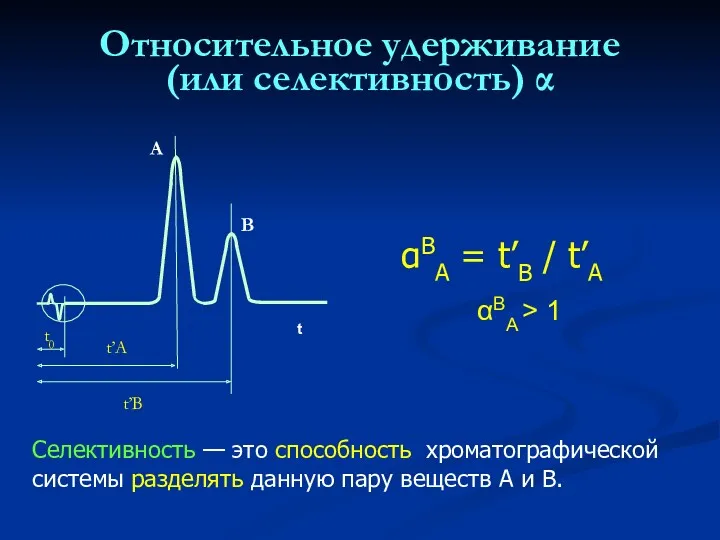
- 25. Относительное удерживание (или селективность) α Cелективность — это способность хроматографической системы разделять данную пару веществ А
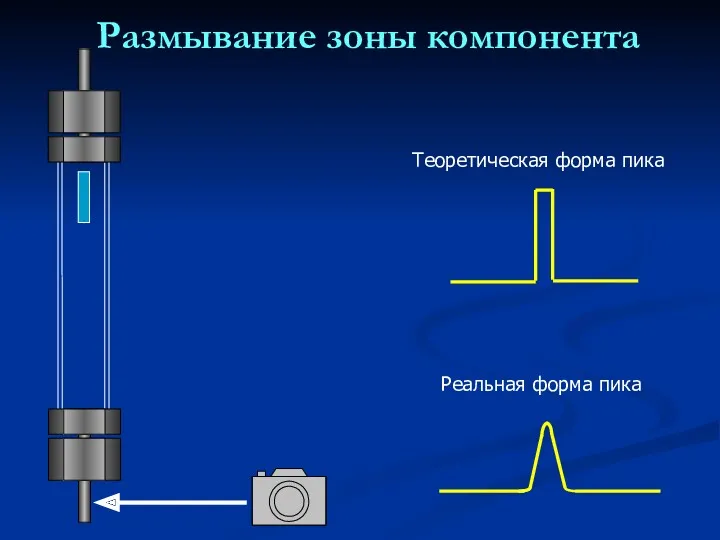
- 26. Размывание зоны компонента
- 27. Теория теоретических тарелок
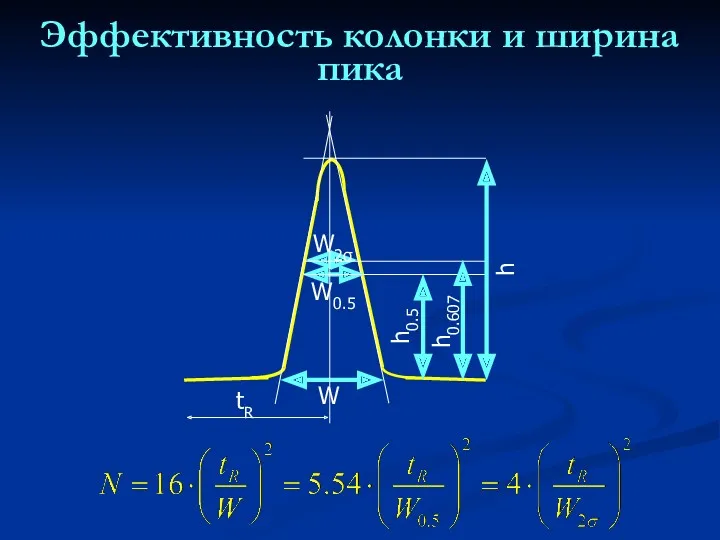
- 28. Эффективность колонки и ширина пика tR
- 29. Допущения теории теоретических тарелок Колонка состоит из ступеней (тарелок), на которых происходит разделение Равновесие на каждой
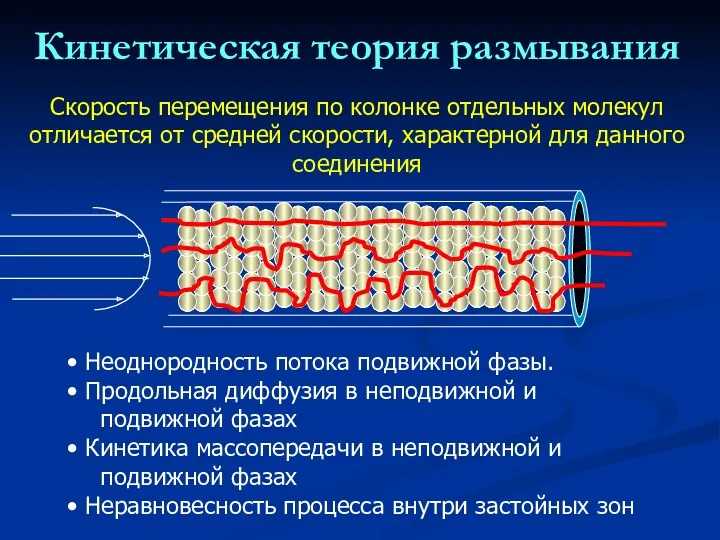
- 30. Кинетическая теория размывания Скорость перемещения по колонке отдельных молекул отличается от средней скорости, характерной для данного
- 31. Кинетическая теория размывания Эффективность зависит от: Диаметра зерен сорбента, их геометрии и монодисперсности Качества набивки колонки
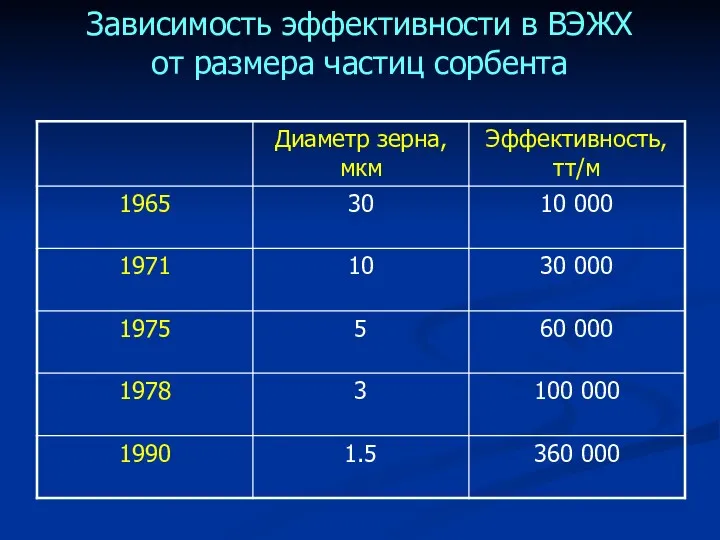
- 32. Зависимость эффективности в ВЭЖХ от размера частиц сорбента
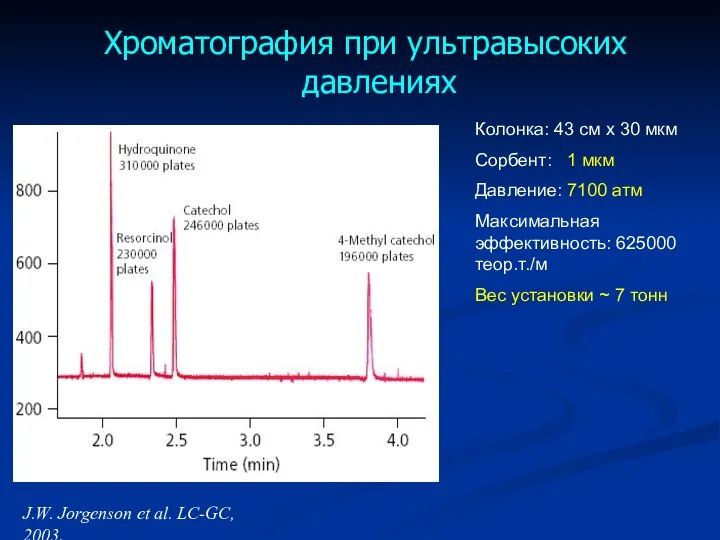
- 33. Хроматография при ультравысоких давлениях Колонка: 43 см х 30 мкм Сорбент: 1 мкм Давление: 7100 атм
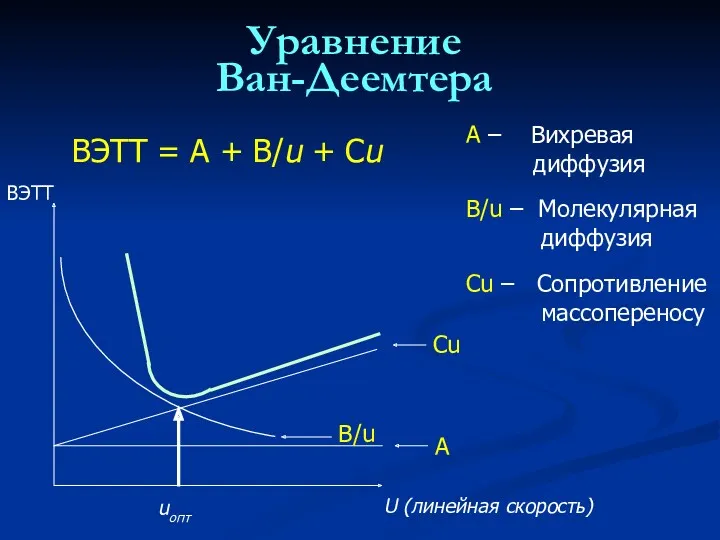
- 34. Уравнение Ван-Деемтера ВЭТТ = A + B/u + Cu U (линейная скорость) ВЭТТ А – Вихревая
- 35. Что есть что в уравнении Ван-Деемтера ВЭТТ = A + B/u + Cu
- 36. Критерий разделения Rs W1 W2 Rs ≈ 0.7 Продолжает увеличиваться при увеличении времени второго пика и
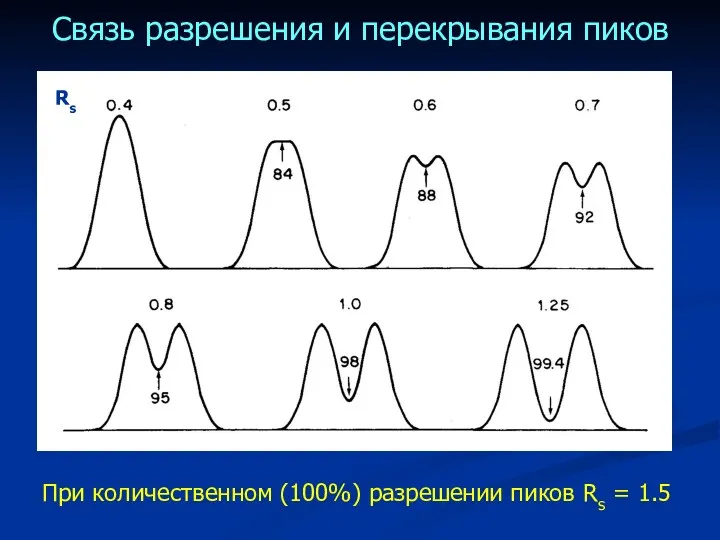
- 37. Связь разрешения и перекрывания пиков Rs При количественном (100%) разрешении пиков Rs = 1.5
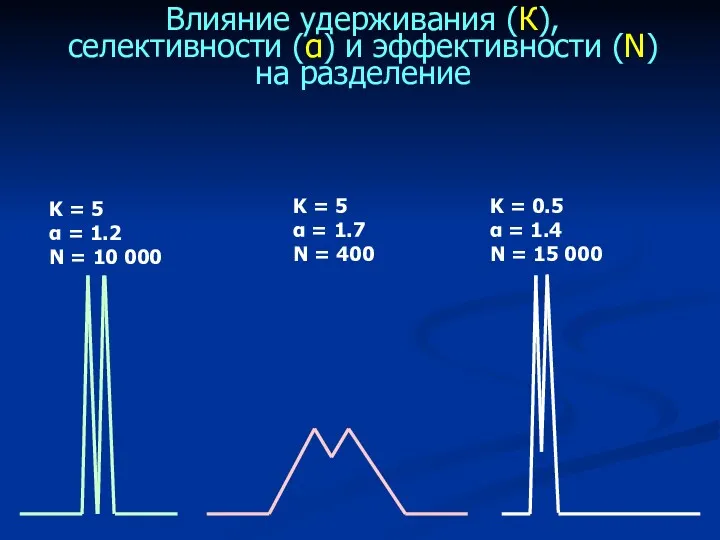
- 38. Влияние удерживания (К), селективности (α) и эффективности (N) на разделение
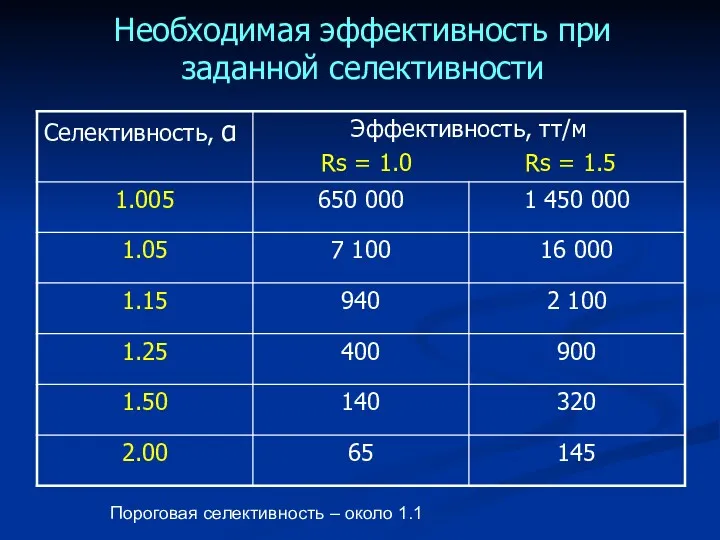
- 39. Необходимая эффективность при заданной селективности ? Пороговая селективность – около 1.1
- 40. Коэффициент асимметрии, Аs As = Wt(0.1) / Wf(0.1) Взаимодействие образца с силанольными группами сорбента Неоднородность сорбента
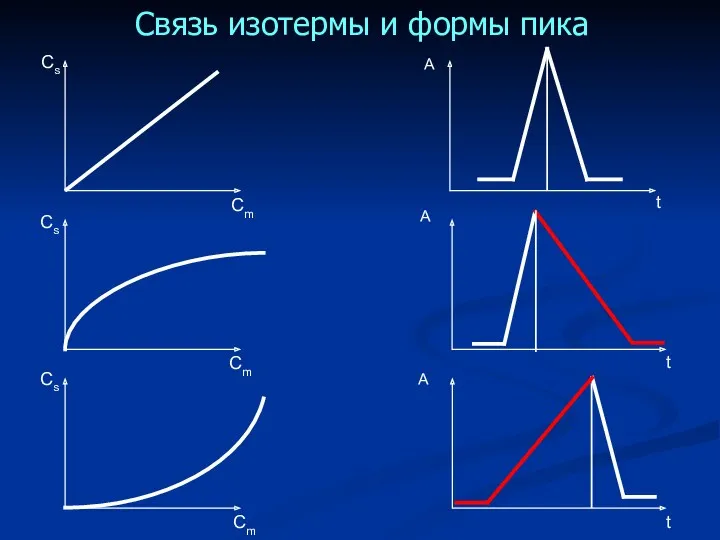
- 41. Связь изотермы и формы пика
- 42. Факторы, улучшающие разрешение пиков Увеличение длины колонки Уменьшение внутреннего диаметра колонки Оптимальная скорость потока элюента Однородность
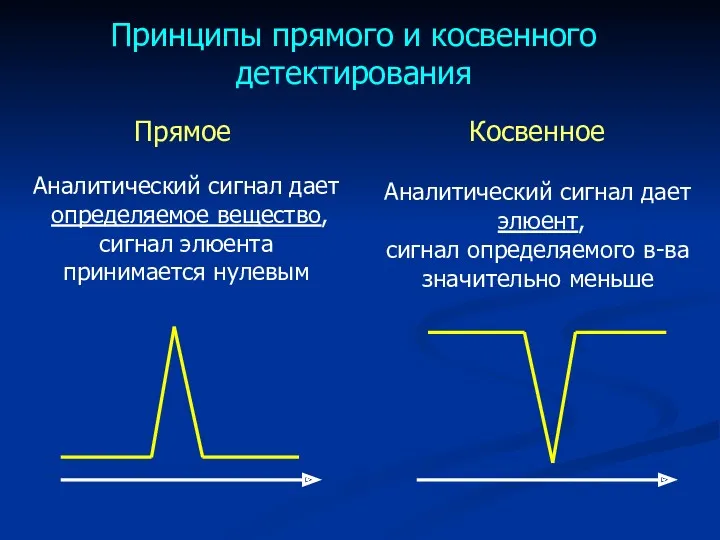
- 43. Принципы прямого и косвенного детектирования Прямое Косвенное Аналитический сигнал дает определяемое вещество, сигнал элюента принимается нулевым
- 44. Количественный анализ в хроматографии Количественной характеристикой является высота или площадь пика При наличии маленьких или несимметричных
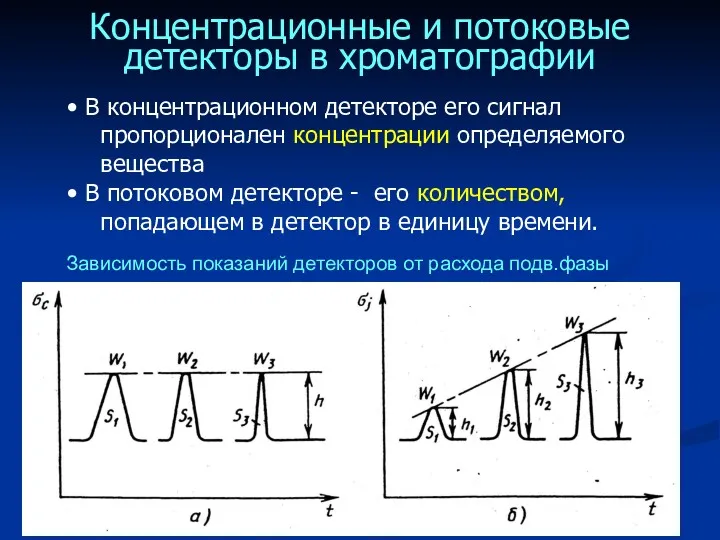
- 45. Концентрационные и потоковые детекторы в хроматографии В концентрационном детекторе его сигнал пропорционален концентрации определяемого вещества В
- 46. Методы количественного анализа в хроматографии Метод нормировки Метод внешнего стандарта Метод добавок Метод внутреннего стандарта
- 47. Метод внутренней нормальзации Sx Sy Sz
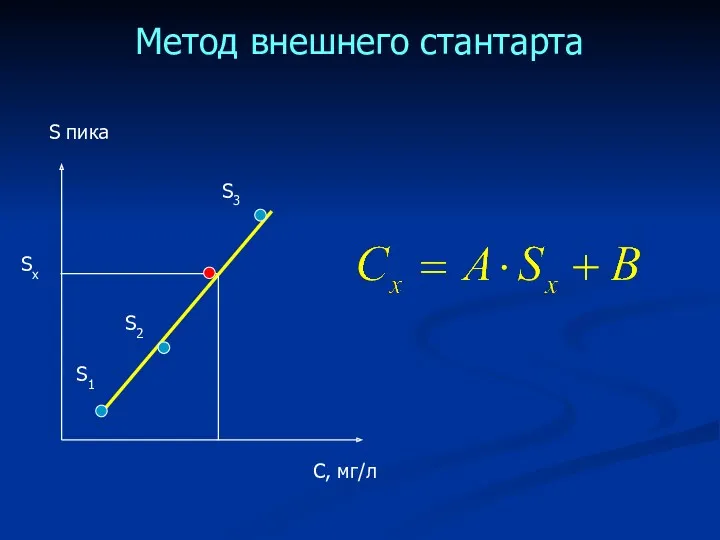
- 48. Метод внешнего стантарта
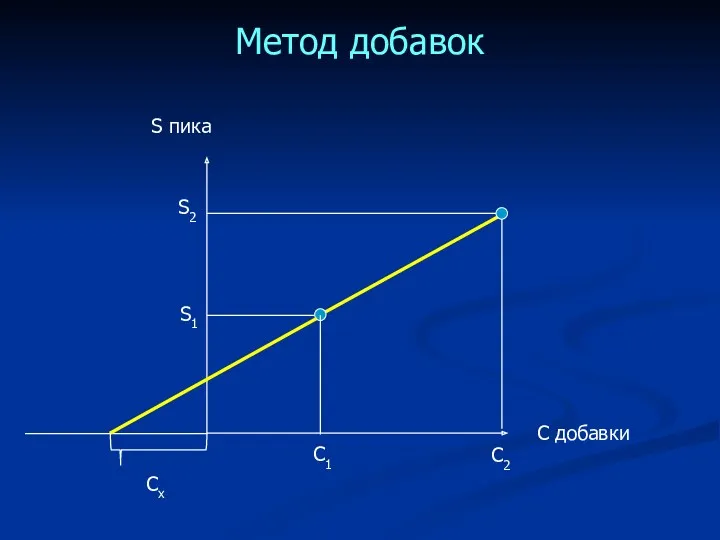
- 49. Метод добавок
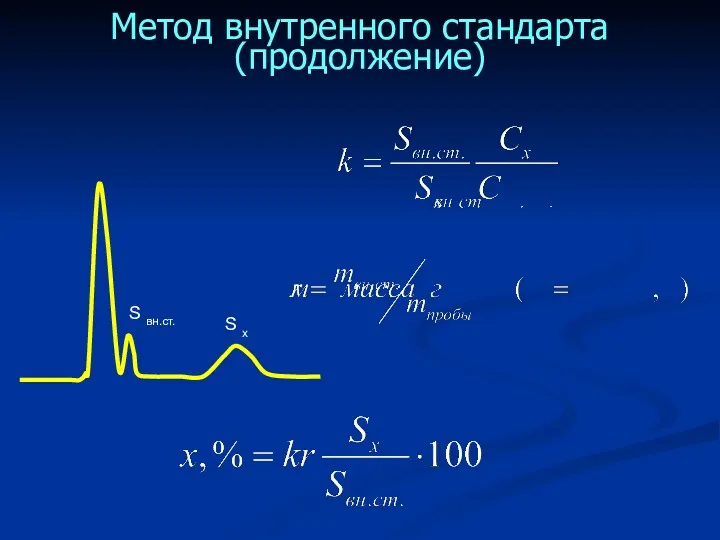
- 50. Метод внутренного стандарта Основан на введении в анализируемую смесь определенного количества постороннего вещества (внутреннего стандарта) отсутствовать
- 51. Метод внутренного стандарта (продолжение)
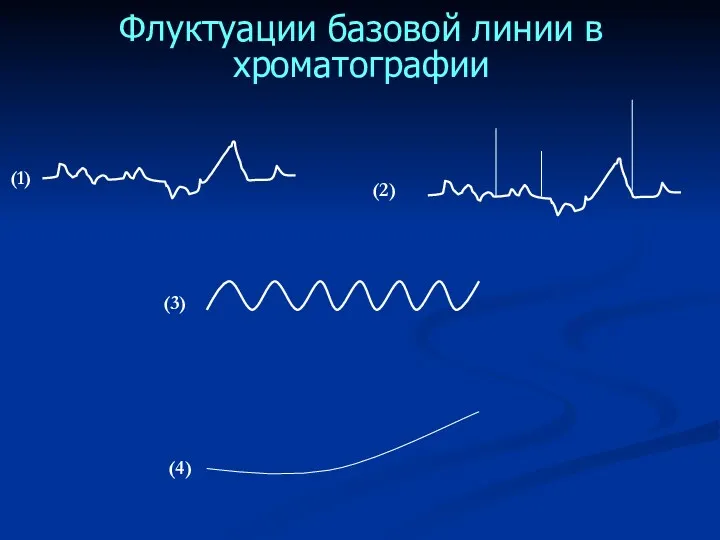
- 52. Флуктуации базовой линии в хроматографии (1) (2) (3) (4)
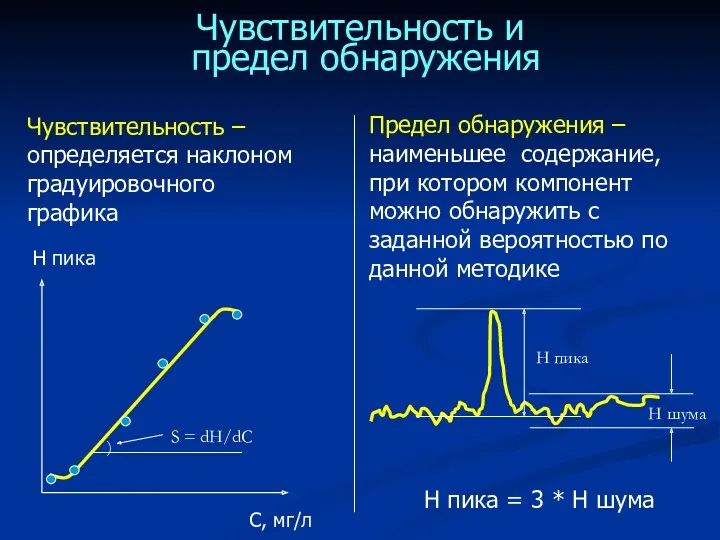
- 53. Чувствительность и предел обнаружения Чувствительность – определяется наклоном градуировочного графика
- 54. Российское хроматографическое приборостроение АКВИЛОН, Москва (жидкостная и ионная) ХИМАВТОМАТИКА, Москва (жидкостная, газовая, детекторы) ЛЕНХРОМ, Санкт-Петербург (тонкослойная)
- 55. Мировое хроматографическое приборостроение AGILENT (жидкостная, газовая, детекторы, электрофорез) ТHERMO (жидкостная, газовая, детекторы) WATERS (жидкостная) PERKIN-ELMER (жидкостная)
- 56. Основные журналы по хроматографии Журнал аналитической химии Журнал физической химии Заводская лаборатория Analytical Chemistry Journal of
- 57. Дополнительная литература по хроматографии Сакодынский К.И., Бражников В.В. и др. Аналитическая хроматография. М.: Химия. 1993, 464
- 58. Классификации хроматографических методов
- 59. Классификация хроматографических методов анализа По агрегатному состоянию подв. фазы (газовая, жидкостная) По механизму разделения (распределительная, адсорбционная,
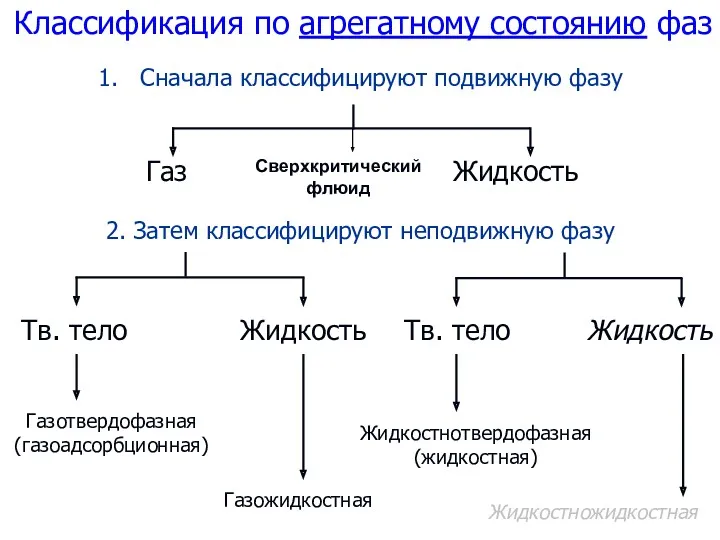
- 60. Классификация по агрегатному состоянию фаз Сначала классифицируют подвижную фазу 2. Затем классифицируют неподвижную фазу
- 61. Классификация по механизму взаимодействия Распределительная Адсорбционная Ионообменная Комплексообразовательная Лигандообменная Эксклюзионная Аффинная
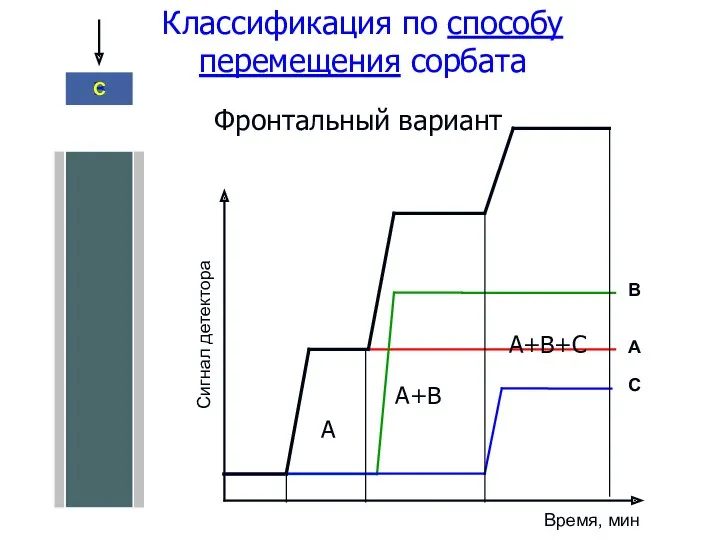
- 62. Фронтальный вариант Классификация по способу перемещения сорбата А В C А А+В А+В+С
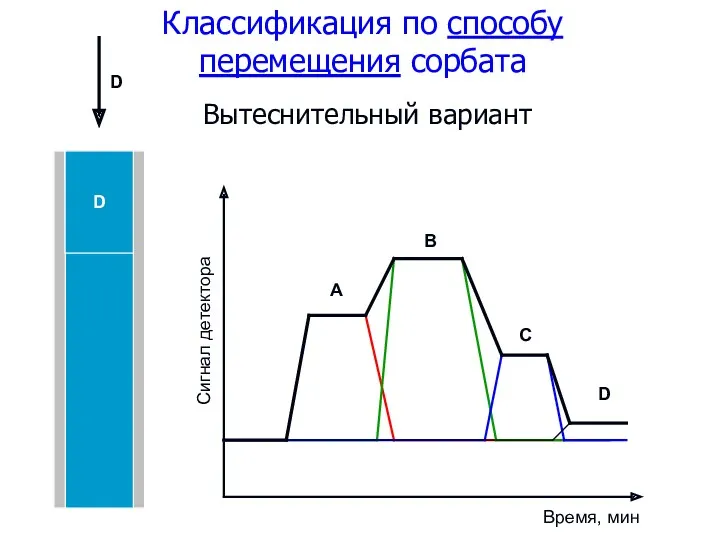
- 63. Классификация по способу перемещения сорбата Вытеснительный вариант A B C D
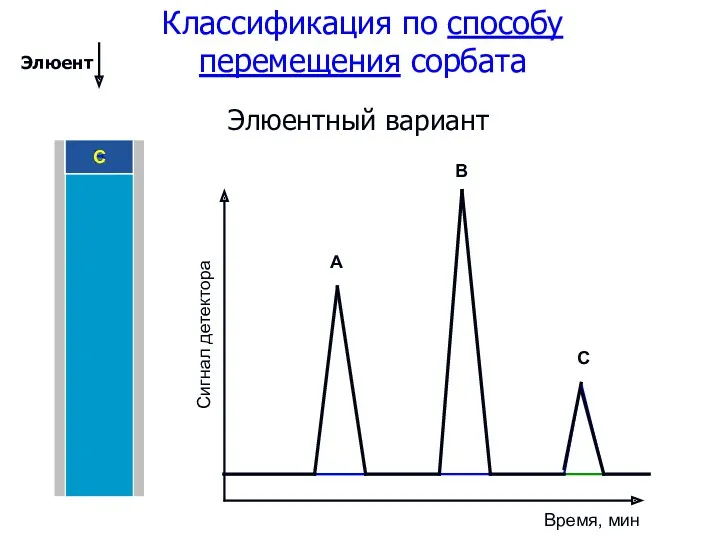
- 64. Элюентный вариант Классификация по способу перемещения сорбата А В C A B C
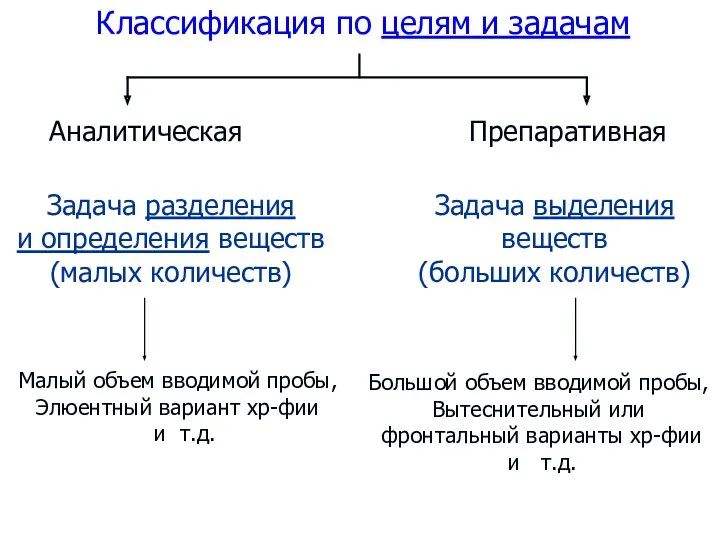
- 65. Классификация по целям и задачам Задача разделения и определения веществ (малых количеств) Задача выделения веществ (больших
- 66. Аналитические и препаративные колонки
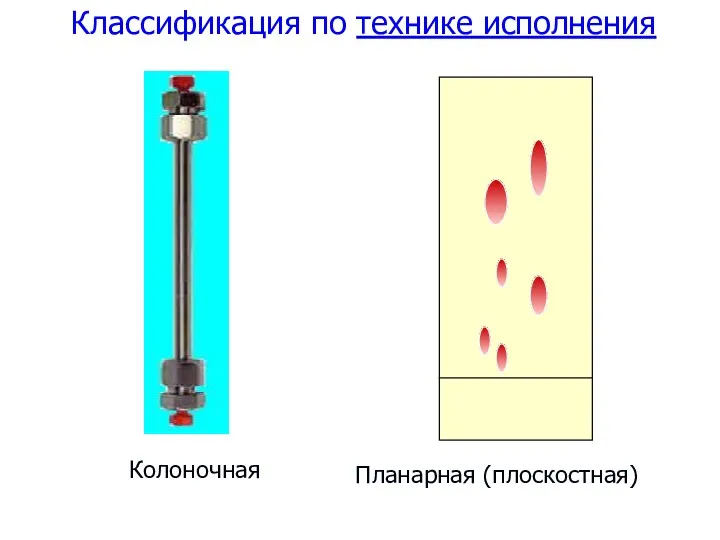
- 67. Классификация по технике исполнения
- 68. Подходы к поиску оптимальных условий хроматографического анализа
- 69. Поиск условий, которые годны для целей анализа… … и ВСЁ!!!
- 70. Не пренебрегайте поиском литературы, информации в Интернете, чтобы не «изобретать колесо»
- 71. Выбор варианта хроматографии в зависимости от задачи
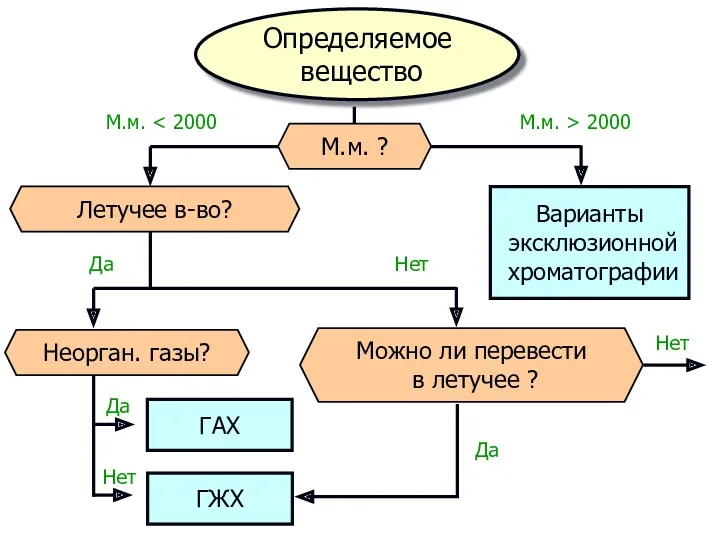
- 72. Определяемое вещество Варианты эксклюзионной хроматографии Летучее в-во? Можно ли перевести в летучее ? Неорган. газы? ГАХ
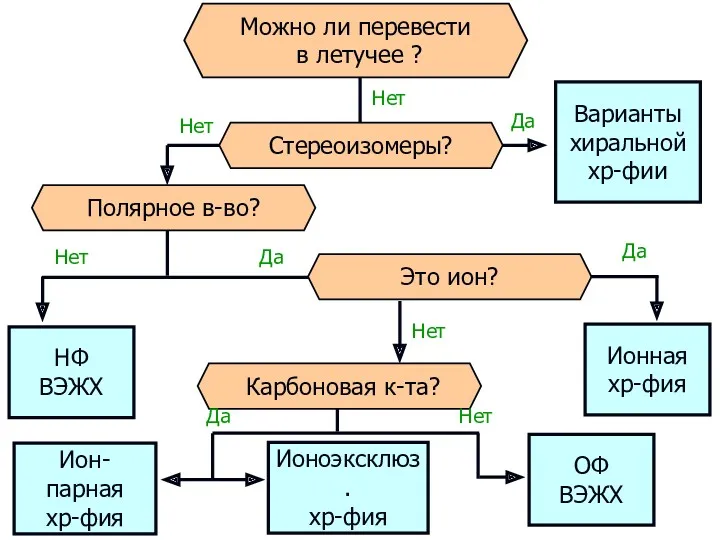
- 73. Полярное в-во? Стереоизомеры? Варианты хиральной хр-фии НФ ВЭЖХ Это ион? Карбоновая к-та? Ионная хр-фия
- 74. Изменение параметров
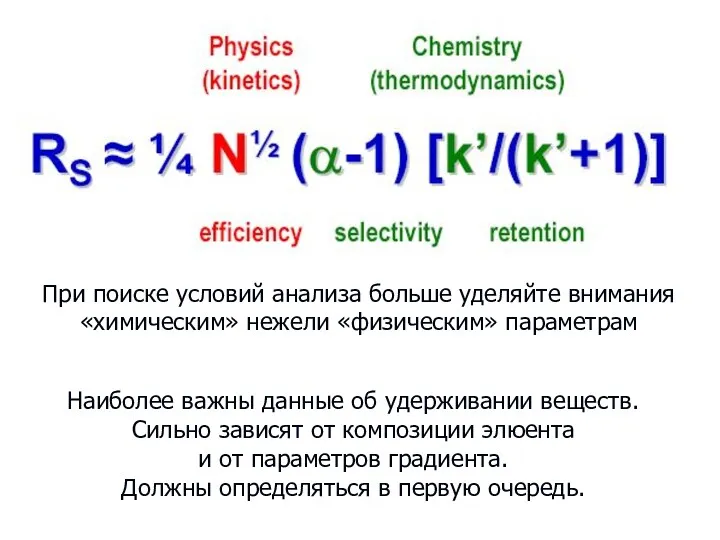
- 75. При поиске условий анализа больше уделяйте внимания «химическим» нежели «физическим» параметрам Наиболее важны данные об удерживании
- 76. Параметры, обычно варьируемые в ВЭЖХ Содержание ацетонитрила (метанола) рН Содержание специальных добавок Время и скорость изменения
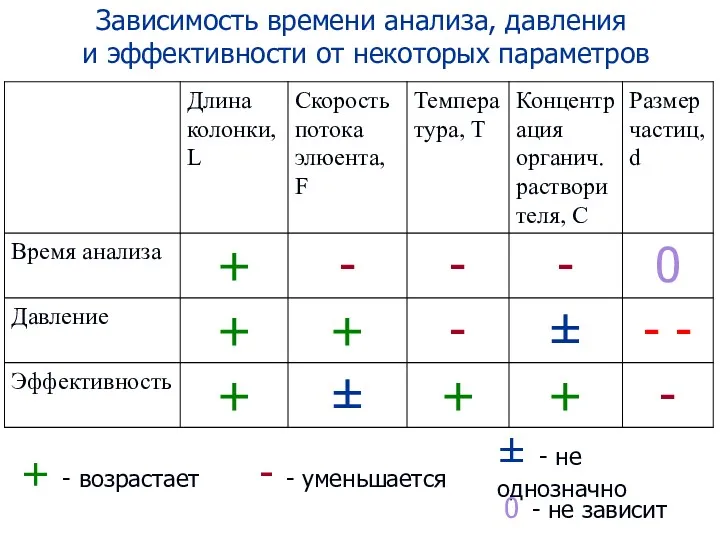
- 77. Зависимость времени анализа, давления и эффективности от некоторых параметров + - возрастает - - уменьшается ±
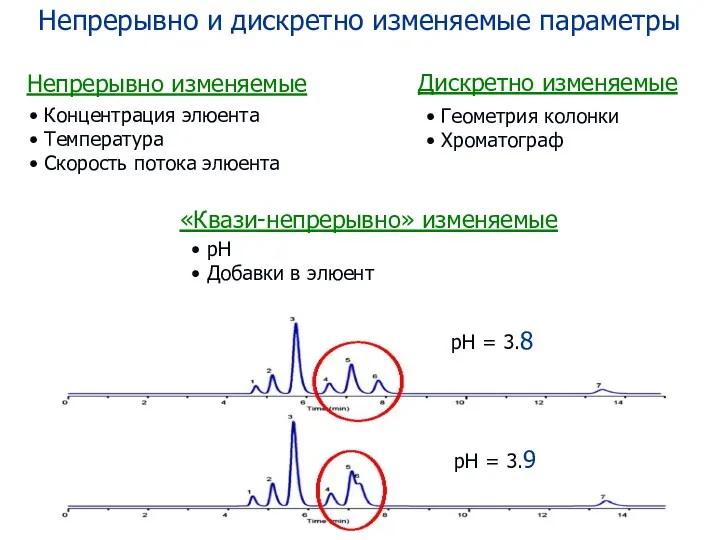
- 78. Непрерывно и дискретно изменяемые параметры
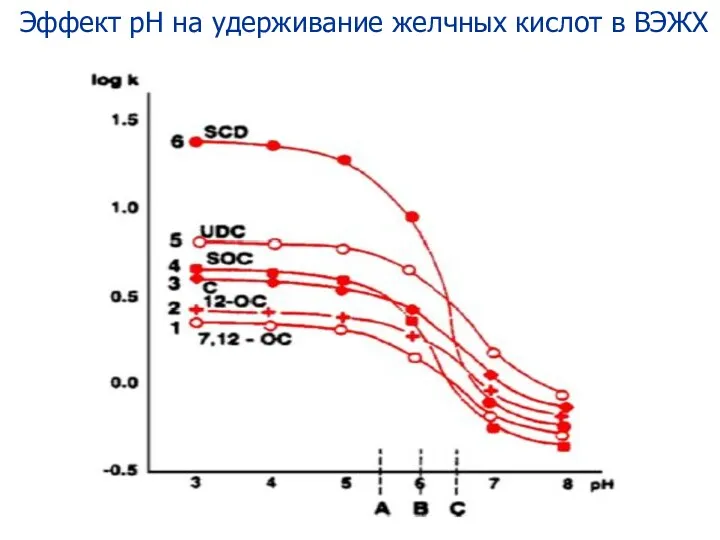
- 79. Эффект рН на удерживание желчных кислот в ВЭЖХ
- 80. Подходы к выбору условий
- 81. «Однопараметрические» подходы к поиску условий анализа Начните с ОФ варианта ВЭЖХ Проведите начальный градиент ацетонитрила (от
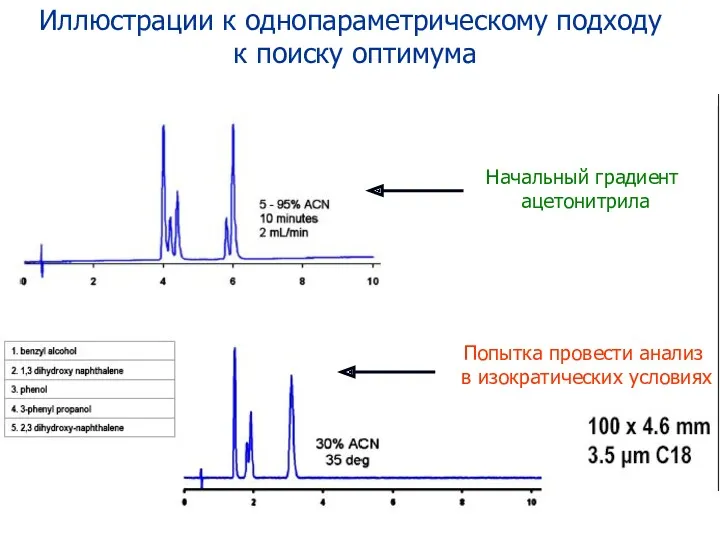
- 82. Иллюстрации к однопараметрическому подходу к поиску оптимума Начальный градиент ацетонитрила Попытка провести анализ в изократических условиях
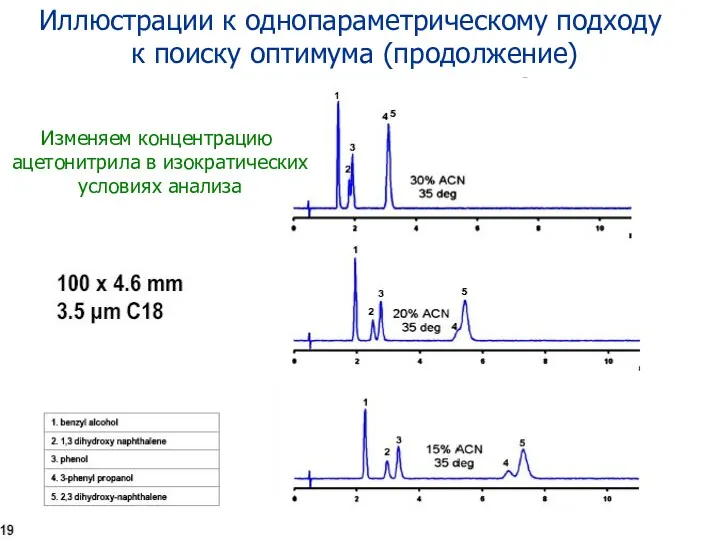
- 83. Иллюстрации к однопараметрическому подходу к поиску оптимума (продолжение) Изменяем концентрацию ацетонитрила в изократических условиях анализа
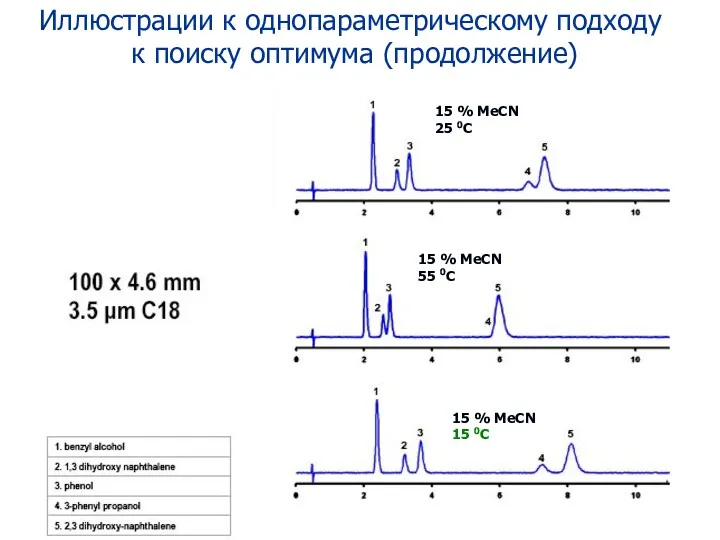
- 84. Иллюстрации к однопараметрическому подходу к поиску оптимума (продолжение) 15 % MeCN 25 0C 15 % MeCN
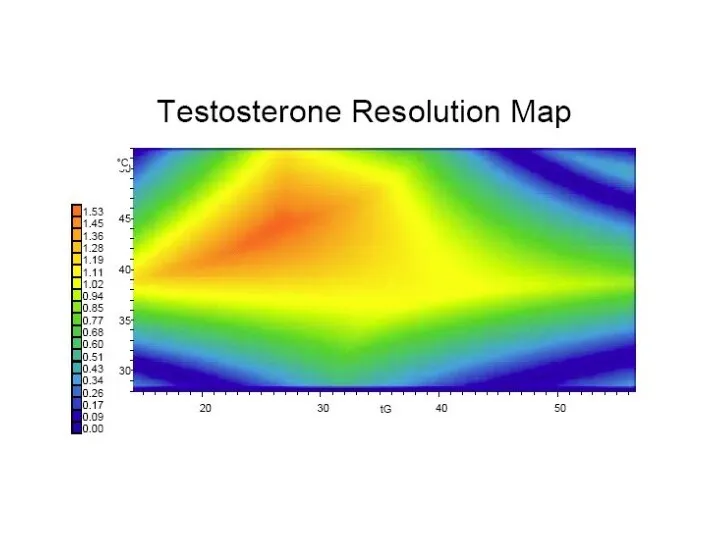
- 85. «Многопараметрические» подходы к поиску условий анализа Обычно совместно варьируемые параметры Температура и элюирующая сила легко автоматизировать
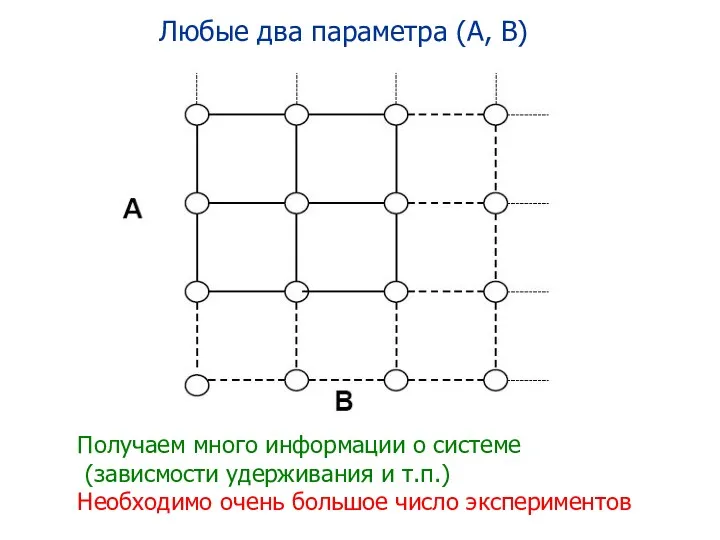
- 86. Получаем много информации о системе (зависмости удерживания и т.п.) Необходимо очень большое число экспериментов
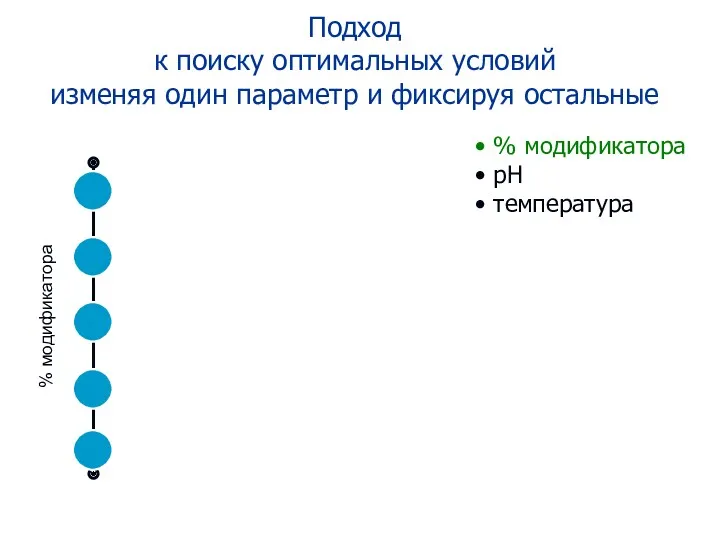
- 87. Подход к поиску оптимальных условий изменяя один параметр и фиксируя остальные % модификатора рН температура
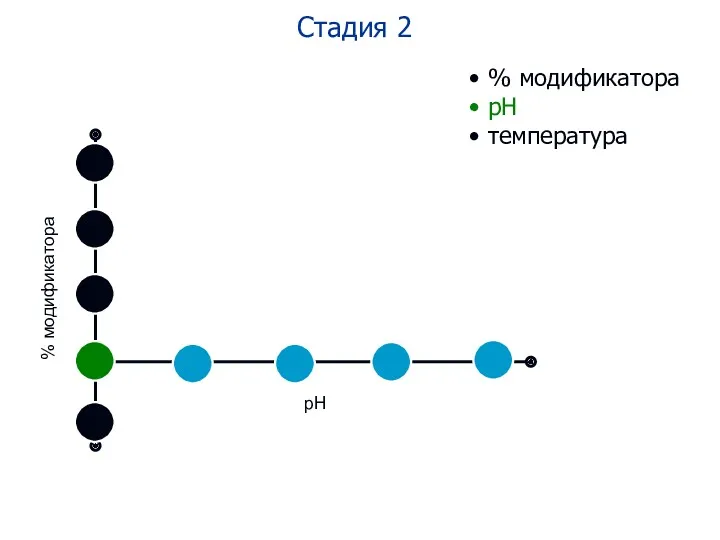
- 88. Стадия 2 % модификатора рН температура
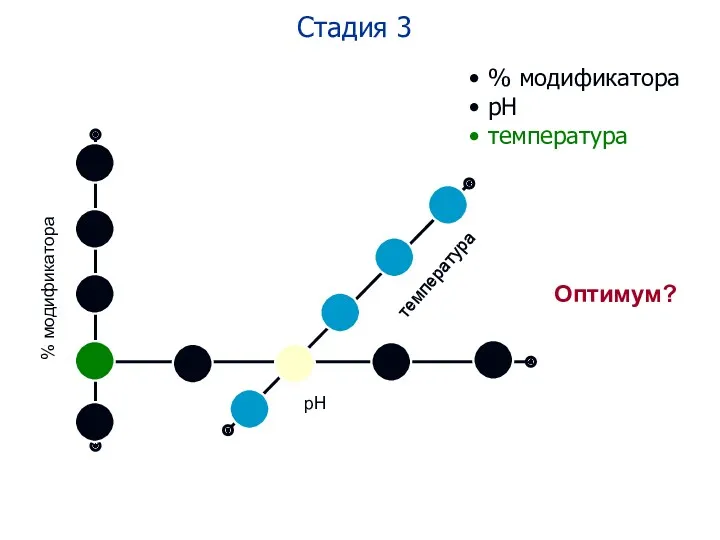
- 89. Стадия 3 % модификатора рН температура
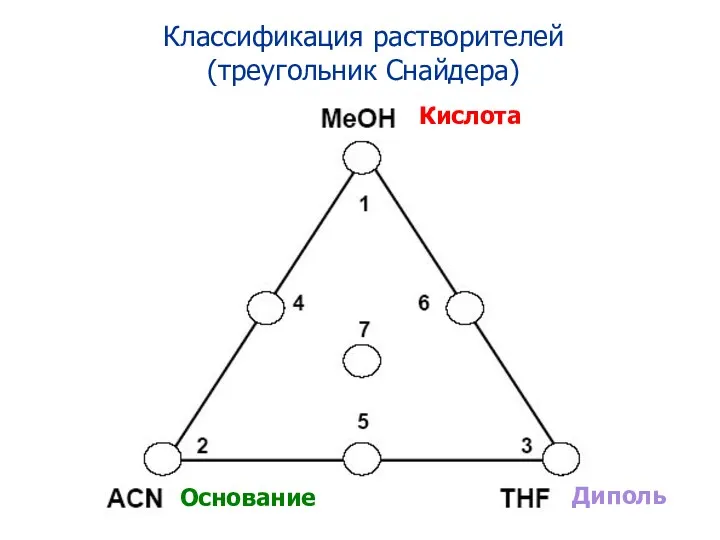
- 90. Классификация растворителей (треугольник Снайдера) Кислота Основание Диполь
- 91. Компьютеризированные подходы к поиску оптимальных условий анализа
- 92. Сущность подходов Применить математические методы поиска максимума функции нескольких переменных При этом варьируемые параметры называют параметрами
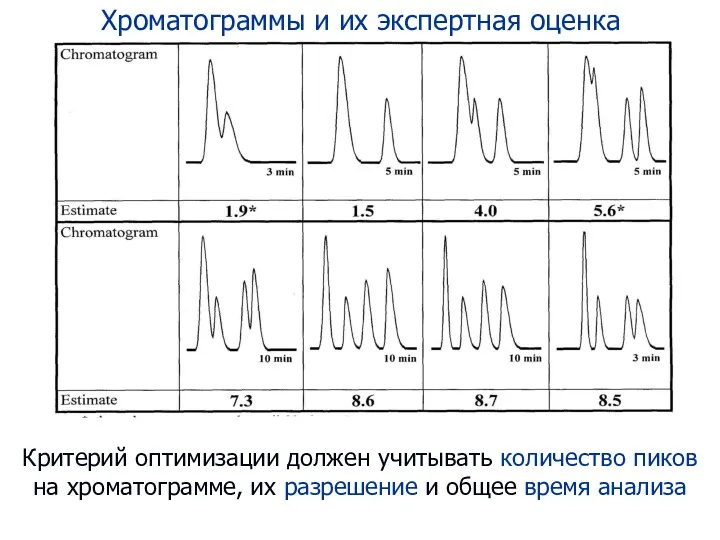
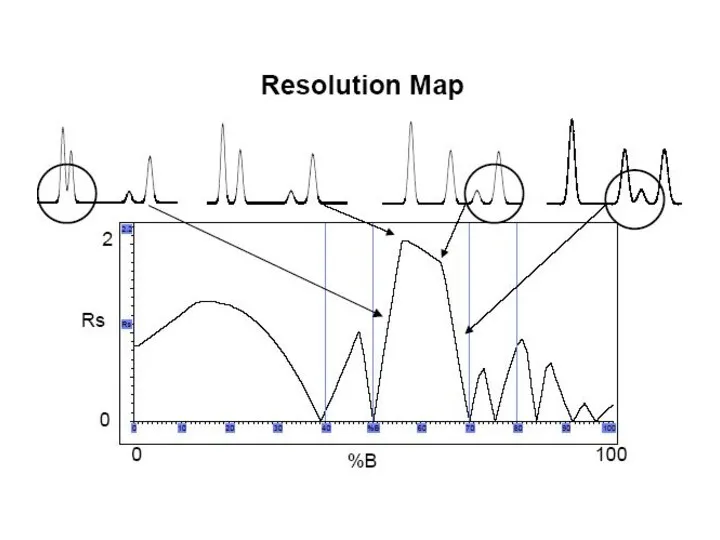
- 93. Хроматограммы и их экспертная оценка Критерий оптимизации должен учитывать количество пиков на хроматограмме, их разрешение и
- 94. Оконные диаграммы
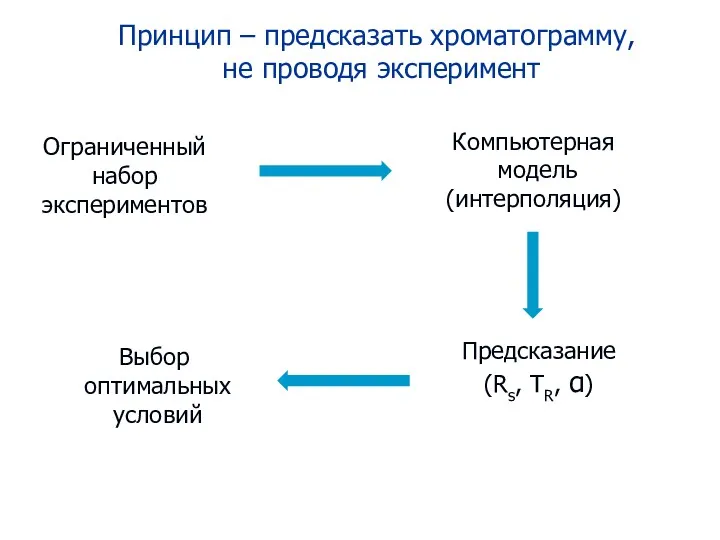
- 95. Принцип – предсказать хроматограмму, не проводя эксперимент
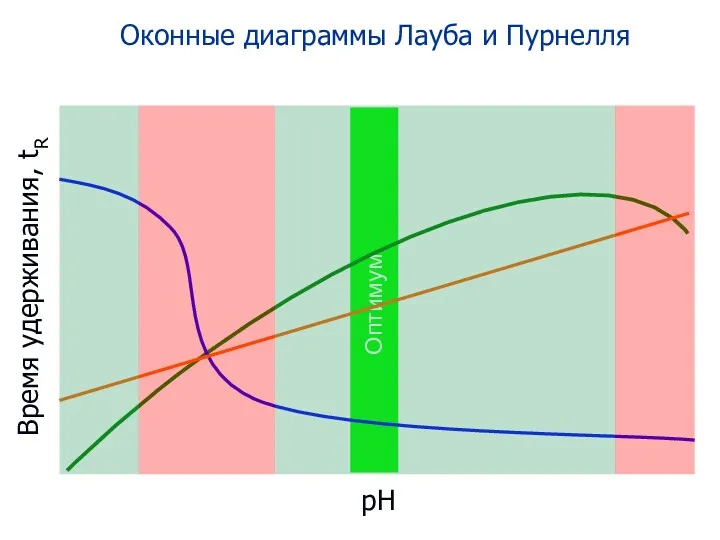
- 96. рН Время удерживания, tR Оконные диаграммы Лауба и Пурнелля
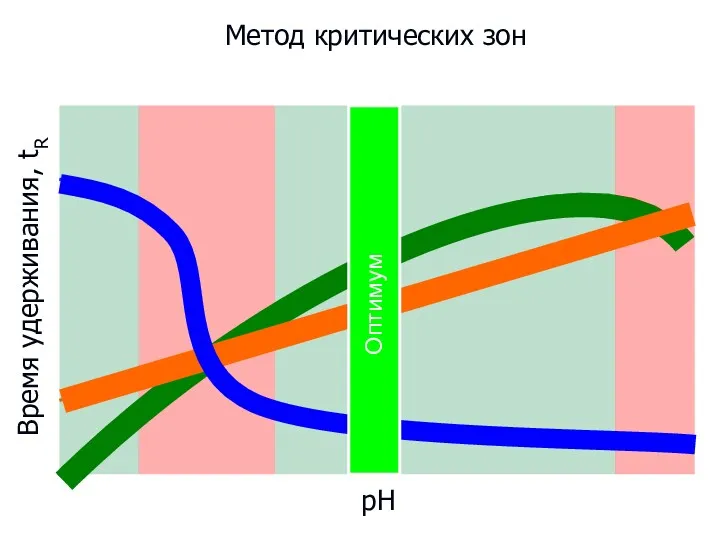
- 97. рН Время удерживания, tR Метод критических зон
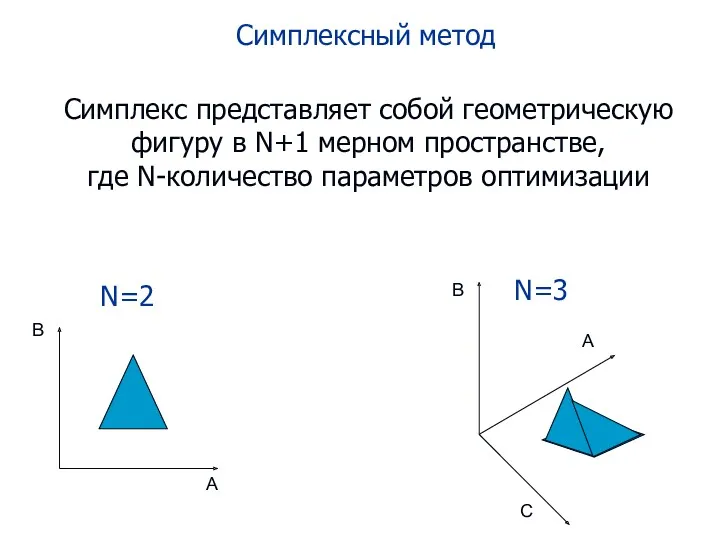
- 100. Симплексный метод
- 101. Симплексный метод Симплекс представляет собой геометрическую фигуру в N+1 мерном пространстве, где N-количество параметров оптимизации
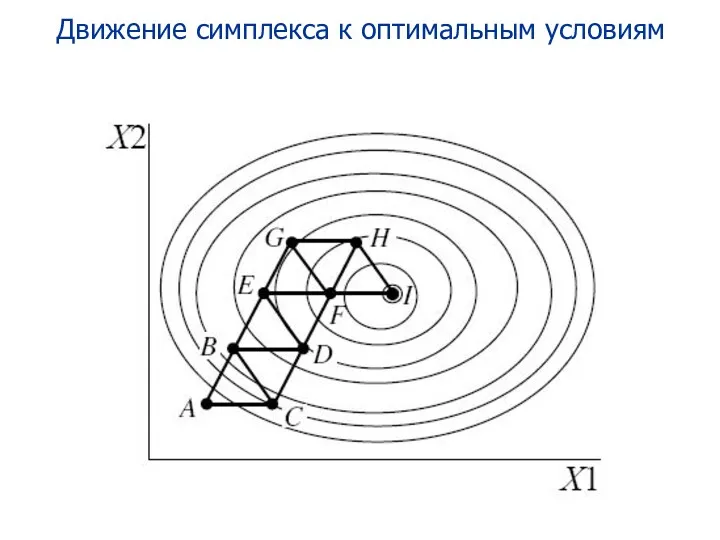
- 102. Движение симплекса к оптимальным условиям
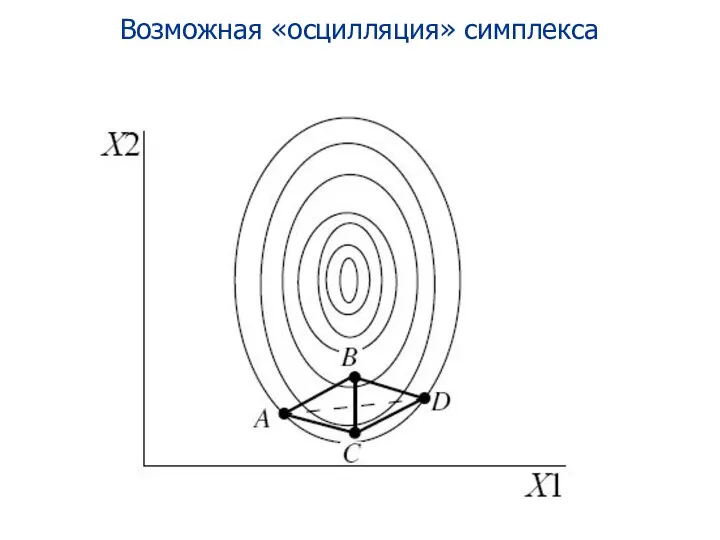
- 103. Возможная «осцилляция» симплекса
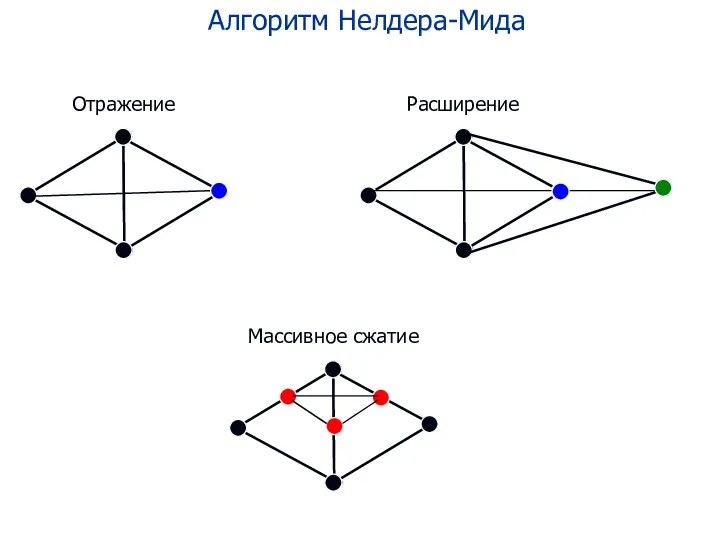
- 104. Алгоритм Нелдера-Мида
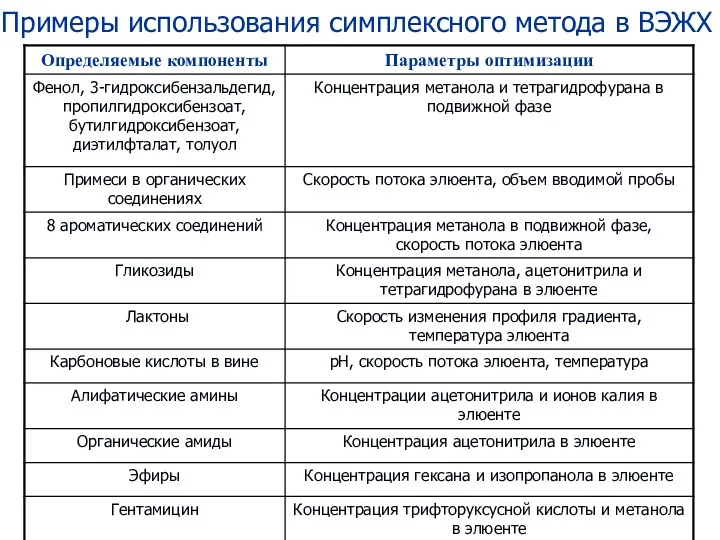
- 105. Примеры использования симплексного метода в ВЭЖХ
- 106. Достоинства и недостатки симплексного метода
- 107. Общие выводы Многие проблемы разделения веществ в ВЭЖХ можно решить с помощью варьирования ОДНОГО параметра Практически
- 108. Программное обеспечения для моделирования хроматограмм и/или поиска оптимальных условий ВЭЖХ анализа
- 109. Монолитные колонки, как альтернатива традиционным
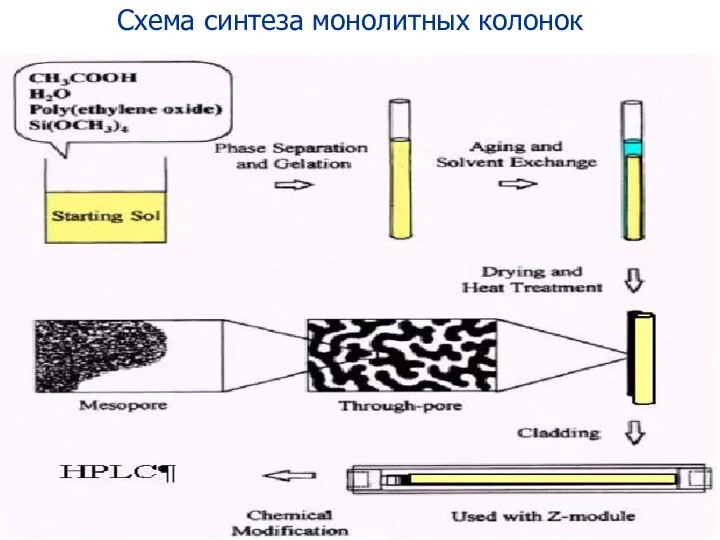
- 110. Схема синтеза монолитных колонок
- 111. Микрофотографии монолитных колонок
- 112. Различные форматы монолитных колонок
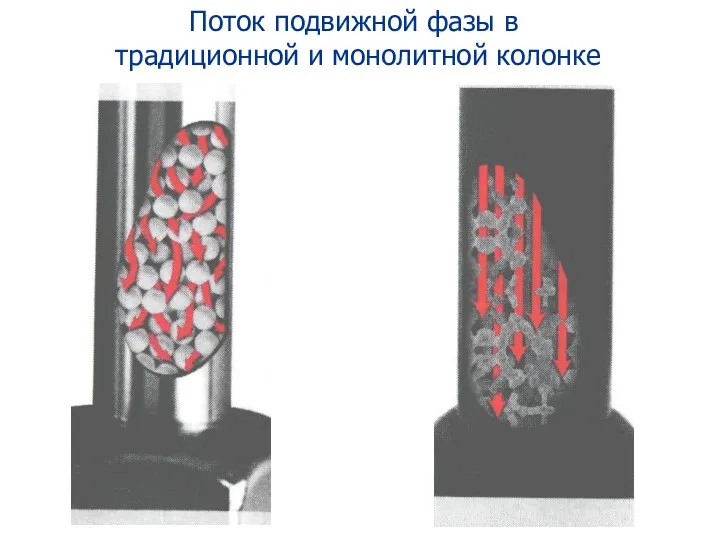
- 113. Поток подвижной фазы в традиционной и монолитной колонке
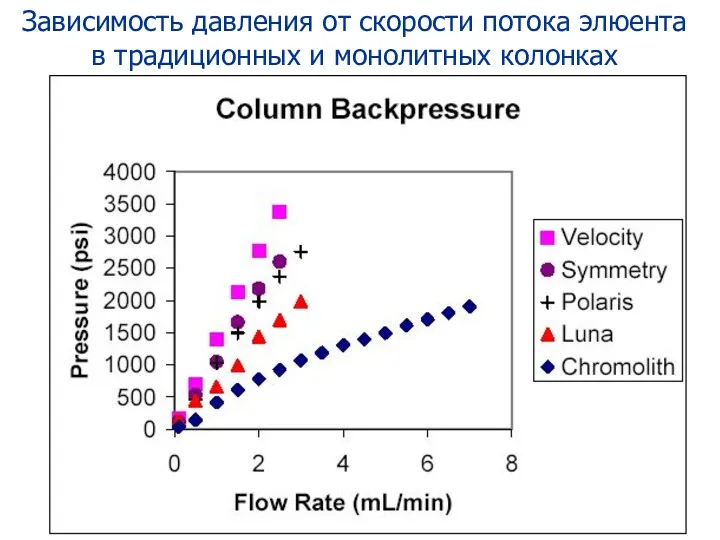
- 114. Зависимость давления от скорости потока элюента в традиционных и монолитных колонках
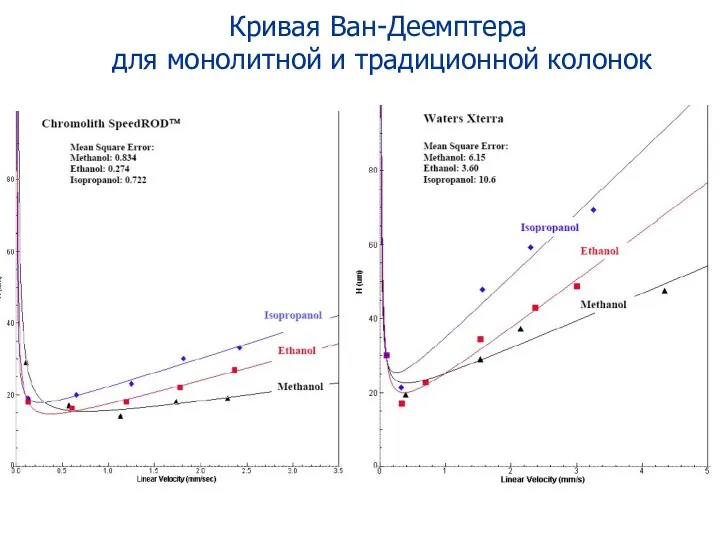
- 115. Кривая Ван-Деемптера для монолитной и традиционной колонок
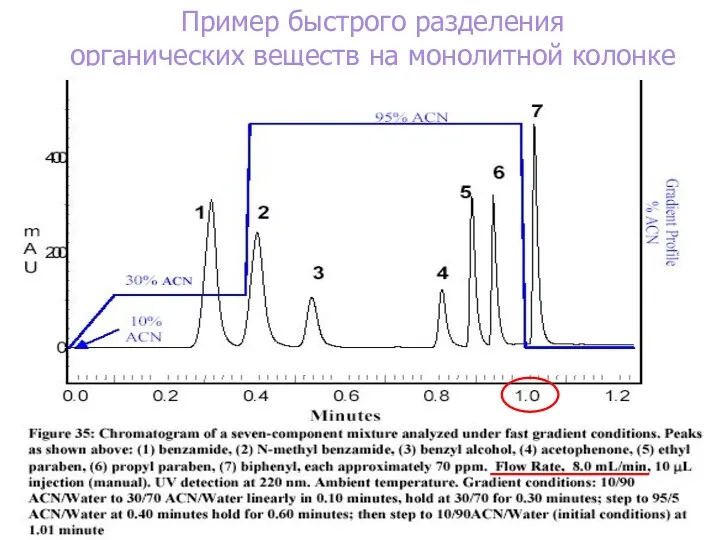
- 116. Пример быстрого разделения органических веществ на монолитной колонке
- 118. Скачать презентацию




















































 Паразитные эффекты в ИС при воздействии ИИ. Физика и особенности проявления тиристорных эффектов в КМОП ИС
Паразитные эффекты в ИС при воздействии ИИ. Физика и особенности проявления тиристорных эффектов в КМОП ИС Засоби аварійного покидання літального апарата
Засоби аварійного покидання літального апарата Көміртекті нанотүтікше
Көміртекті нанотүтікше MATIZ 0.8L. Учебное пособие. JATCO 4 AТ
MATIZ 0.8L. Учебное пособие. JATCO 4 AТ Трансформатор.
Трансформатор. Основы молекулярной и статистической физики
Основы молекулярной и статистической физики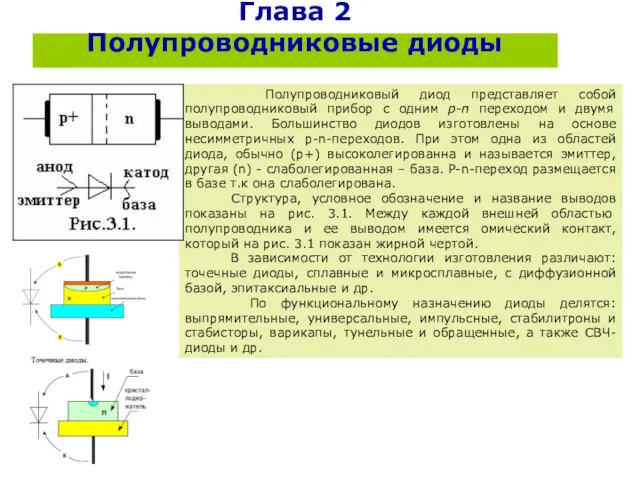 Полупроводниковые диоды
Полупроводниковые диоды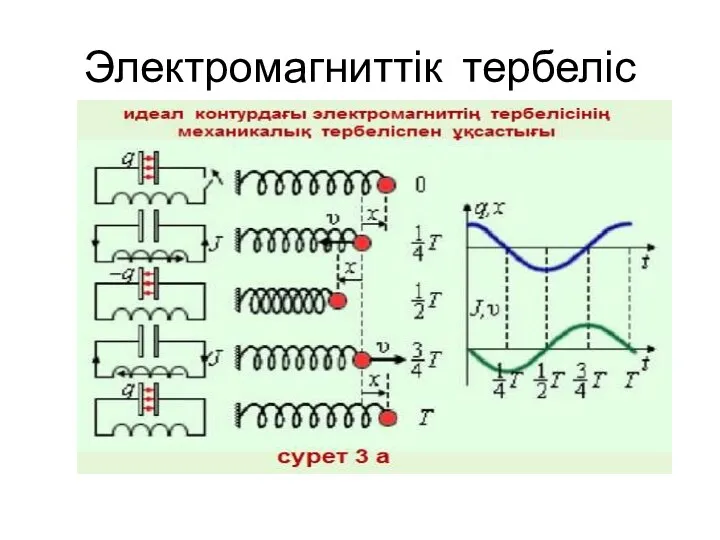 Электромагниттік тербеліс
Электромагниттік тербеліс Английский язык в механике
Английский язык в механике Экспериментальные методы исследования частиц
Экспериментальные методы исследования частиц Термоядерная реакция
Термоядерная реакция Электрический ток
Электрический ток Лекция № 8. Тема: Физические механизмы переноса веществ через мембрану
Лекция № 8. Тема: Физические механизмы переноса веществ через мембрану Лабораторные работы по физике для 8 класса к учебнику А.В.Перышкина Физика 8
Лабораторные работы по физике для 8 класса к учебнику А.В.Перышкина Физика 8 Внутрицентровое поглощение света на примесных уровнях в ИК-диапазоне
Внутрицентровое поглощение света на примесных уровнях в ИК-диапазоне Переходные процессы в цепях первого порядка
Переходные процессы в цепях первого порядка Электростатика. Электрические заряды
Электростатика. Электрические заряды Введение в динамику. Законы и аксиомы динамики материальной точки. Основное уравнение динамики
Введение в динамику. Законы и аксиомы динамики материальной точки. Основное уравнение динамики Расчет максимального отношения сигнал-шум на выходе оптимального приемника. Тема 4: Часть 3
Расчет максимального отношения сигнал-шум на выходе оптимального приемника. Тема 4: Часть 3 Источники и приемники оптического излучения
Источники и приемники оптического излучения Система питания двигателя
Система питания двигателя Сцепление. Назначение, конструкции
Сцепление. Назначение, конструкции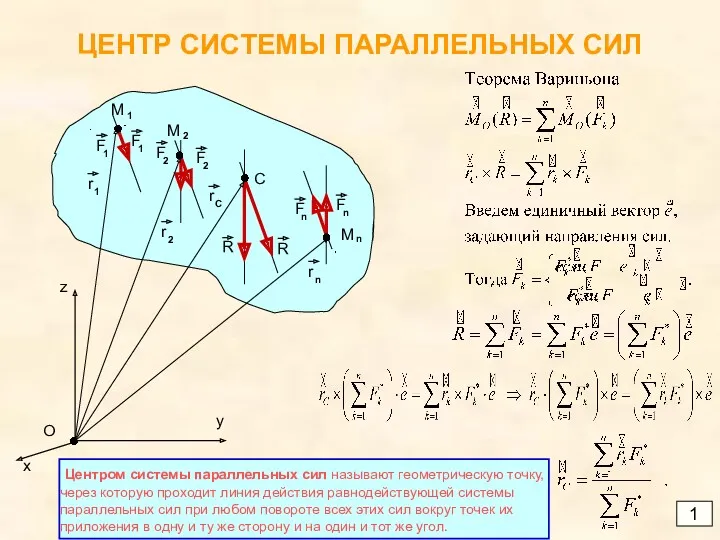 Центр системы параллельных сил
Центр системы параллельных сил Динамика. Законы Ньютона. (Лекция 2)
Динамика. Законы Ньютона. (Лекция 2) Обобщающий урок по физике 8 класс Тепловые явления.Агрегатные состояния вещества
Обобщающий урок по физике 8 класс Тепловые явления.Агрегатные состояния вещества Итоги работы опытной путевой машинной станции № 103 Московской дирекции по ремонту пути
Итоги работы опытной путевой машинной станции № 103 Московской дирекции по ремонту пути Методы и средства измерения полосы пропускания и дисперсии оптических волокон
Методы и средства измерения полосы пропускания и дисперсии оптических волокон презентация Векторы.Действия над векторами.Проекция вектора
презентация Векторы.Действия над векторами.Проекция вектора