Содержание
- 2. Уравнения движения классических частиц с потенциальным взаимодействием Движение системы классических частиц (материальных точек), взаимодействие которых характеризуется
- 3. Классический потенциал и сила взаимодействия Потенциальная энергия системы N атомов Сила, действующая на i-й атом Взаимодействие
- 4. Но атомы – квантовые объекты ! Строго говоря, взаимодействие атомов носит квантовый характер и осуществляется через
- 5. Уравнение Шредингера для N атомов полная волновая функция системы радиусы-векторы ядер системы радиусы-векторы электронов оператор Гамильтона
- 6. Адиабатическое приближение (Борн, Оппенгеймер, 1923) - ВФ ядер - ВФ электронов Не содержит операторов, воздействующих на
- 7. Адиабатическое приближение продолжение
- 8. Парные потенциалы U1 – одночастичный член (энергия частиц во внешнем поле или обусловленная граничными условиями (давлением
- 9. Потенциал Леннарда-Джонса Потенциал ЛД дает хорошее описание ван-дер-ваальсовских взаимодействий между атомами инертных газов и молекулами (Ar,
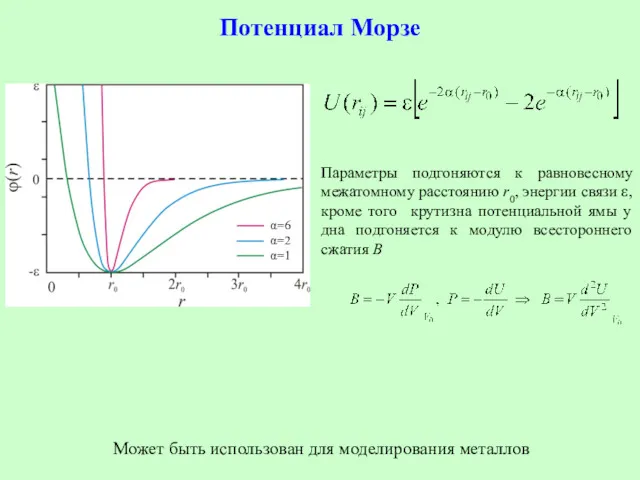
- 10. Потенциал Морзе Может быть использован для моделирования металлов Параметры подгоняются к равновесному межатомному расстоянию r0, энергии
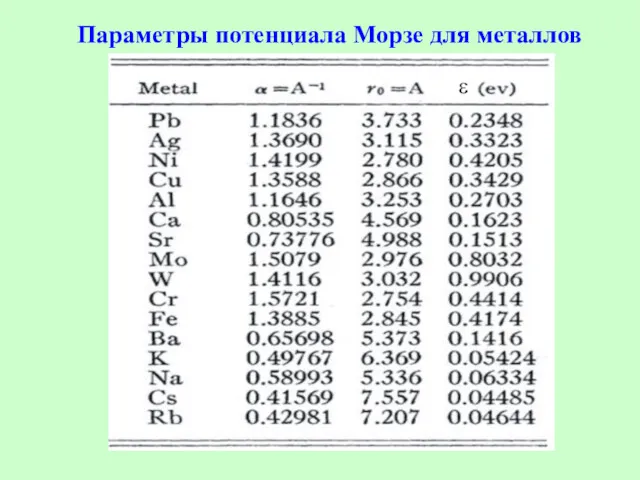
- 11. Параметры потенциала Морзе для металлов
- 12. Расчет силы для парных потенциалов Для потенциала ЛД
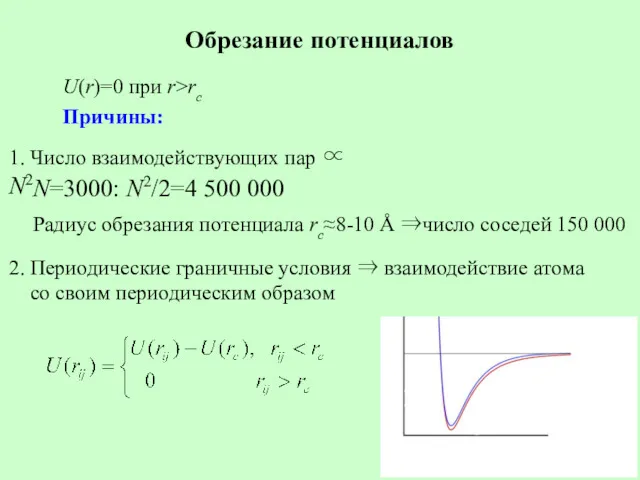
- 13. Обрезание потенциалов 1. Число взаимодействующих пар ∝ N2 N=3000: N2/2=4 500 000 Радиус обрезания потенциала rc≈8-10
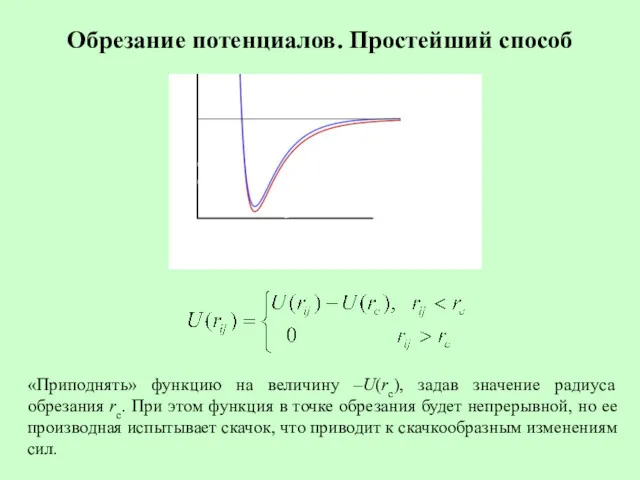
- 14. Обрезание потенциалов. Простейший способ «Приподнять» функцию на величину –U(rс), задав значение радиуса обрезания rс. При этом
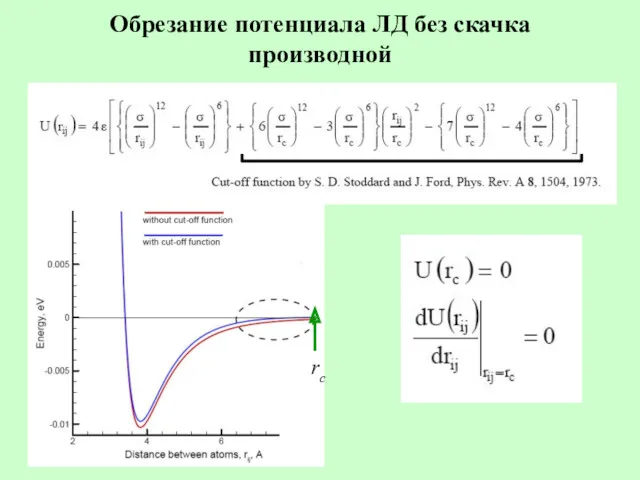
- 15. Обрезание потенциала ЛД без скачка производной rc
- 16. Недостатки парных потенциалов Не учитывают насыщение связей: энергия на одну связь в объеме меньше, чем на
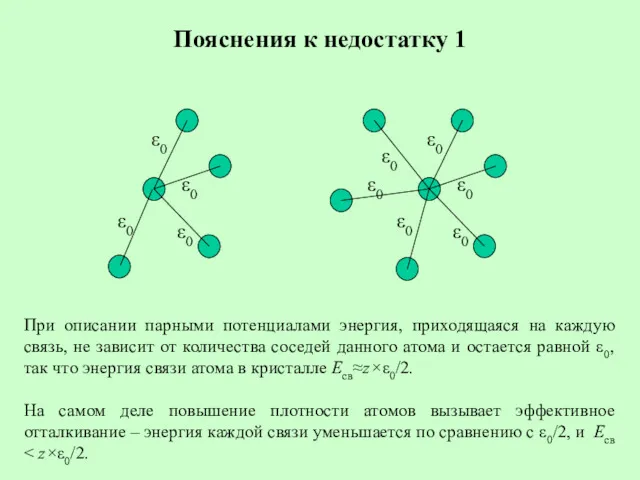
- 17. Пояснения к недостатку 1 При описании парными потенциалами энергия, приходящаяся на каждую связь, не зависит от
- 18. Тензор упругих постоянных кристаллов: основные формулы теории упругости
- 19. Тензор упругих постоянных кристаллов: независимые постоянные для кубической решетки
- 20. Понятие о теории функционала плотности Hohenberg P., Kohn W., 1964: Все аспекты электронной структуры системы взаимодействующих
- 21. Энергия связи твердого тела суммирование по i и j производится по ядрам твердого тела, ‑ заряд
- 22. Методы описания межатомного взаимодействия, основанные на теории функционала плотности Метод погруженного атома (Embedded atom method, EAM)
- 23. Метод погруженного атома плотность электронов в узле i энергия внедрения атома i в эту электронную плотность
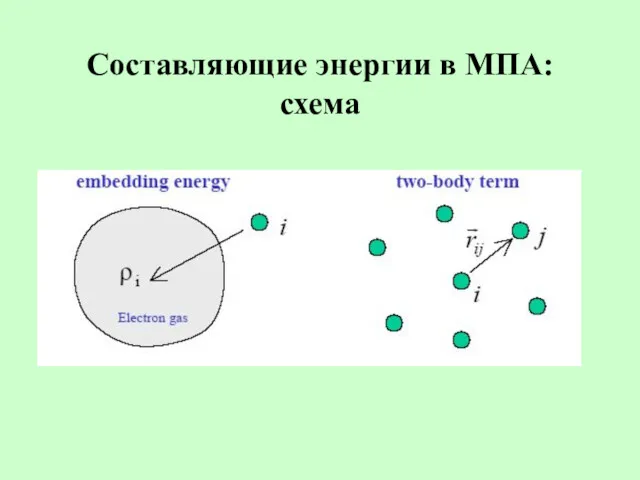
- 24. Составляющие энергии в МПА: схема
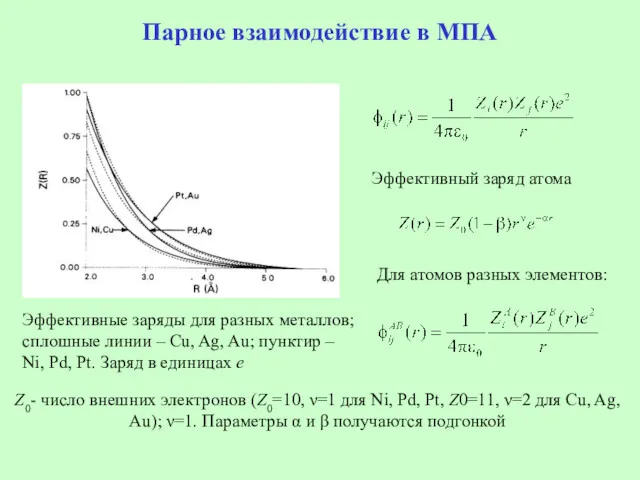
- 25. Парное взаимодействие в МПА Эффективный заряд атома Для атомов разных элементов: Эффективные заряды для разных металлов;
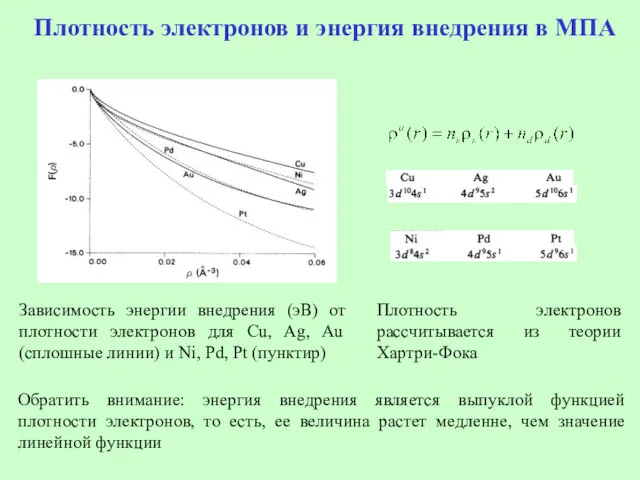
- 26. Плотность электронов и энергия внедрения в МПА Зависимость энергии внедрения (эВ) от плотности электронов для Cu,
- 27. Аналитический потенциал МПА Джонсона (1988) B‑ модуль всестороннего сжатия ‑ атомный объем -параметры, подгоняемые к параметру
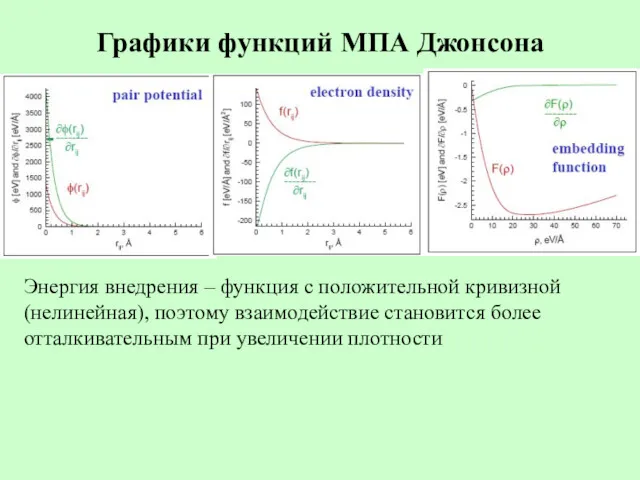
- 28. Графики функций МПА Джонсона Энергия внедрения – функция с положительной кривизной (нелинейная), поэтому взаимодействие становится более
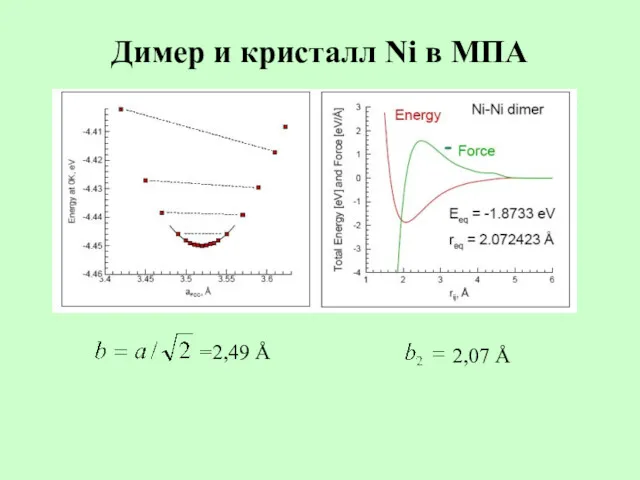
- 29. Димер и кристалл Ni в МПА =2,49 Å 2,07 Å
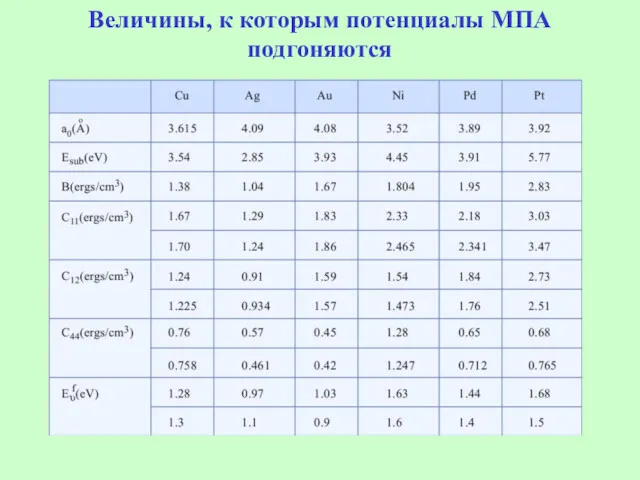
- 30. Величины, к которым потенциалы МПА подгоняются
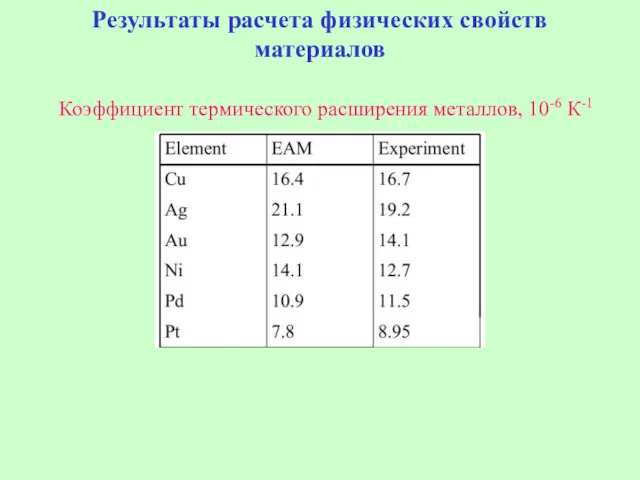
- 31. Результаты расчета физических свойств материалов Коэффициент термического расширения металлов, 10-6 К-1
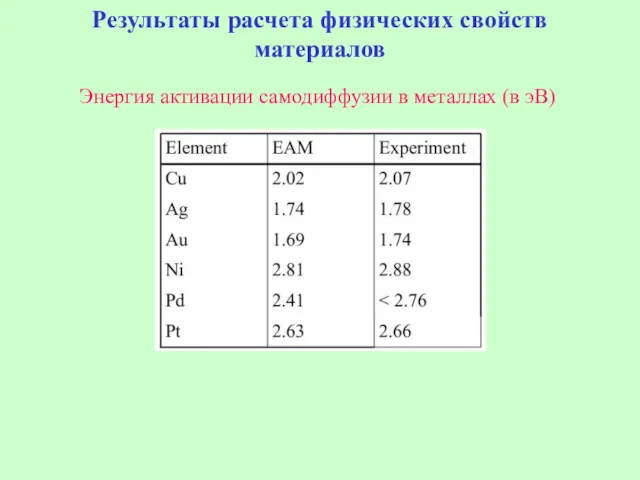
- 32. Результаты расчета физических свойств материалов Энергия активации самодиффузии в металлах (в эВ)
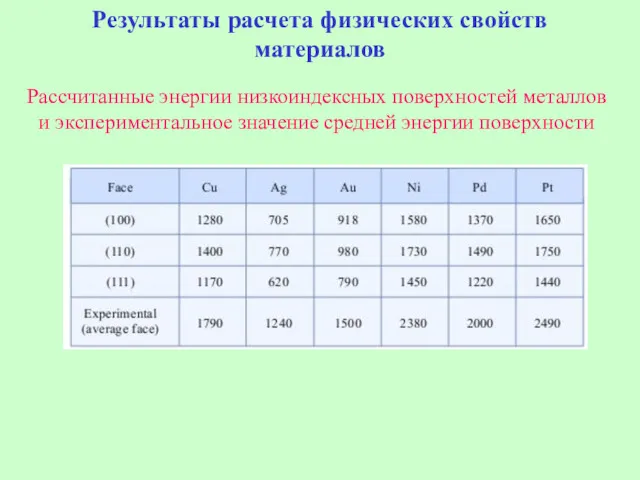
- 33. Результаты расчета физических свойств материалов Рассчитанные энергии низкоиндексных поверхностей металлов и экспериментальное значение средней энергии поверхности
- 34. Результаты расчета физических свойств материалов Температуры плавления металлов, К
- 35. Таблица потенциала niu3 для никеля eunit eV potential set eam 1 potential embed 1 500 0.000000
- 36. Потенциал метода МПА для титана При ρ>48 При ρ кубическим сплайном
- 37. Таблица потенциала метода МПА для титана # EAM potential for Ti, T. Hammerschmidt et al. PRB
- 38. Потенциал Клери-Росато (приближение второго момента модели сильной связи)
- 39. Потенциал Финниса-Синклера
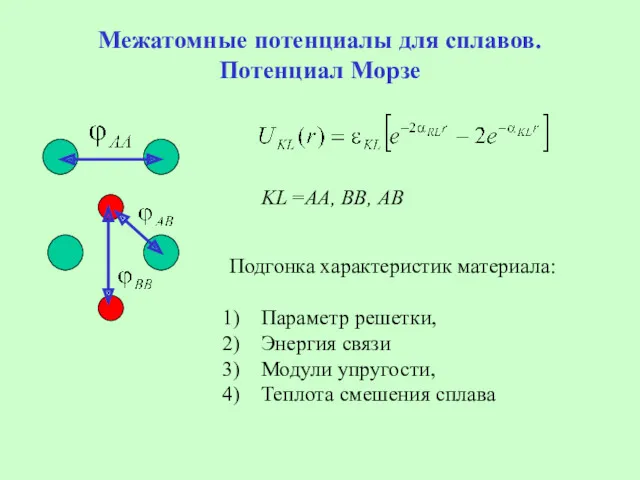
- 40. Межатомные потенциалы для сплавов. Потенциал Морзе KL =АА, ВВ, АВ Подгонка характеристик материала: Параметр решетки, Энергия
- 41. Потенциалы внедренного атома для сплавов. Энергия внедрения Fi(ρi) не зависит от того, какими атомами создается электронная
- 42. Потенциалы внедренного атома для сплавов. Энергия парного взаимодействия - эффективные заряды атомов А и В Z0,
- 43. Функции, необходимые для двухкомпонентного сплава Электронные плотности, создаваемые атомами А и В Энергии внедрения атомов А
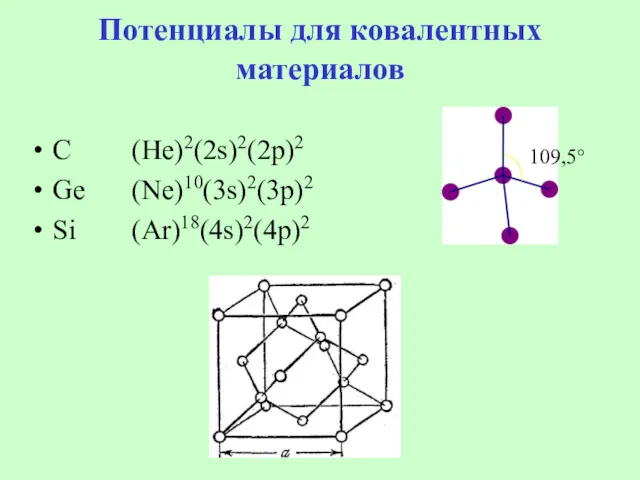
- 44. Потенциалы для ковалентных материалов C (He)2(2s)2(2p)2 Ge (Ne)10(3s)2(3p)2 Si (Ar)18(4s)2(4p)2
- 45. Потенциал Стиллингера-Вебера зависящий от угла член проводит к энергетически выгодной кристаллической структуре алмаза с тетраэдрическими углами
- 46. Недостатки потенциала Стиллингера-Вебера и другие потенциалы Трехчастичный член определяет только одну равновесную конфигурацию 109.47°, поэтому его
- 48. Скачать презентацию




























 Теория методов ГИС
Теория методов ГИС Электрический ток в биологических тканях. Основы реографии
Электрический ток в биологических тканях. Основы реографии Электромагнитные помехи
Электромагнитные помехи Колебания. Колебательные движения
Колебания. Колебательные движения Статически неопределимые системы. Лекция №5
Статически неопределимые системы. Лекция №5 Инфракрасное излучение
Инфракрасное излучение Эффект Доплера
Эффект Доплера Жарық толқындарының интерференциясы
Жарық толқындарының интерференциясы Элементы машиноведения
Элементы машиноведения Физика в ЛШ–2019
Физика в ЛШ–2019 Методы регистрации заряженных частиц
Методы регистрации заряженных частиц Статистический и термодинамический методы описания макроскопических тел. Лекция 10
Статистический и термодинамический методы описания макроскопических тел. Лекция 10 Рубка металла. Цель и назначение слесарной рубки
Рубка металла. Цель и назначение слесарной рубки Внутренняя энергия тела
Внутренняя энергия тела Молекулярная физика и термодинамика
Молекулярная физика и термодинамика Викторина по физике 9 класс
Викторина по физике 9 класс Енергія, робота та потужність.Закон збереження енергії. Лекція 5
Енергія, робота та потужність.Закон збереження енергії. Лекція 5 Расчет количества теплоты необходимого для нагревания тела или выделяемого им при охлаждении. Решение задач. Физика. 8 класс
Расчет количества теплоты необходимого для нагревания тела или выделяемого им при охлаждении. Решение задач. Физика. 8 класс Методы измерения газопроницаемости
Методы измерения газопроницаемости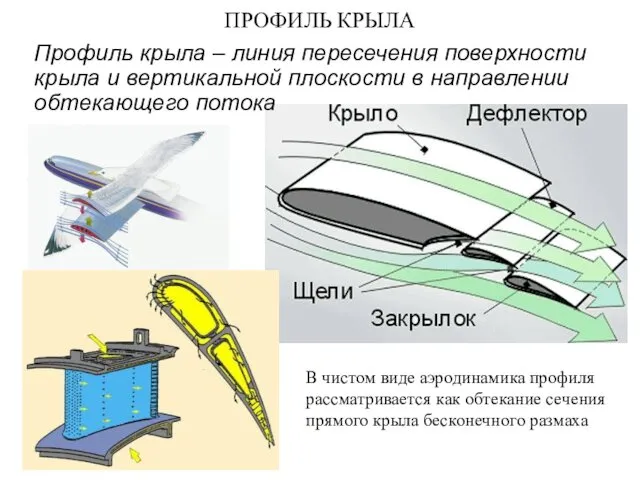 pr_Profil_kryla (3)
pr_Profil_kryla (3) Оптические приборы
Оптические приборы Состав поста Р300С4
Состав поста Р300С4 Системы питания и наддува ДВС. Тема 12
Системы питания и наддува ДВС. Тема 12 Создание телефона
Создание телефона электромагнитная природа света
электромагнитная природа света Динамика поступательного и вращательного движения твердого тела
Динамика поступательного и вращательного движения твердого тела ПЛАН-КОНСПЕКТ УРОКА Электроскоп. Проводники и непроводники электричества физика 8класс
ПЛАН-КОНСПЕКТ УРОКА Электроскоп. Проводники и непроводники электричества физика 8класс Тепловые явления (8 класс, урок-повторение)
Тепловые явления (8 класс, урок-повторение)