Содержание
- 2. изучает строение и свойства вещества, исходя из молекулярно-кинетических представлений: любое тело (твердое, жидкое или газообразное) состоит
- 3. Состояние системы. Термодинамические параметры и процессы Термодинамическими параметрами (или параметрами состояния) системы называются физические величины, служащие
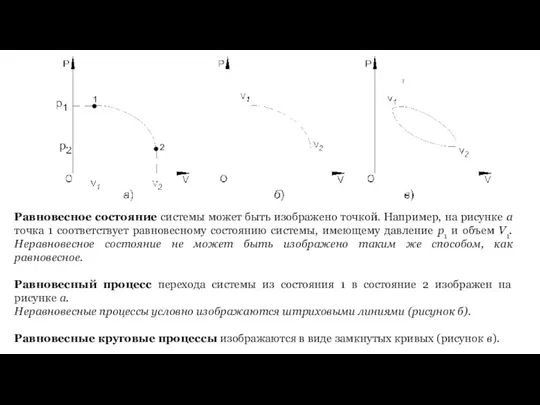
- 4. Равновесное состояние системы может быть изображено точкой. Например, на рисунке а точка 1 соответствует равновесному состоянию
- 5. Уравнение состояние. Основные положения МКТ Параметры состояния системы, находящейся в равновесном состоянии, связаны между собой определенной
- 6. Массы и размеры молекул Моль – единица измерения количества вещества. 1 моль любого вещества содержит одно
- 7. Идеальный газ Для описания свойств каких-либо объектов обычно пользуются модельными представлениями. Вид модели выбирается в зависимости
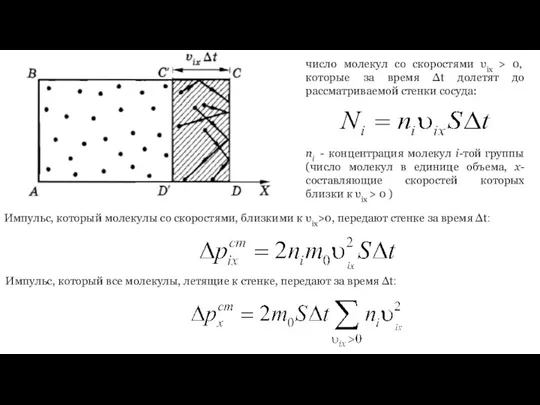
- 8. ОСНОВНОЕ УРАВНЕНИЕ МКТ. Давление идеального газа. Давление – результат столкновения молекул газа со стенками сосуда. При
- 9. ni - концентрация молекул i-той группы (число молекул в единице объема, x-составляющие скоростей которых близки к
- 10. Средний квадрат проекции скорости на ось Х: Все направления равновероятны:: Давление – импульс, переданный в единицу
- 12. ТЕМПЕРАТУРА Температура характеризует состояние теплового равновесия макроскопической системы: во всех частях системы, находящейся в состоянии теплового
- 13. Число степеней свободы молекулы Число степеней свободы – число независимых координат, с помощью которых можно однозначно
- 14. Теорема о равномерном распределении кинетической энергии по степеням свободы: в состоянии теплового равновесия на каждую степень
- 16. Уравнение состояния идеального газа. Газовые законы. Дж/моль∙К – универсальная газовая постоянная
- 17. ИЗОПРОЦЕССЫ: 1. Изотермический 2. Изобарический 3. Изохорический
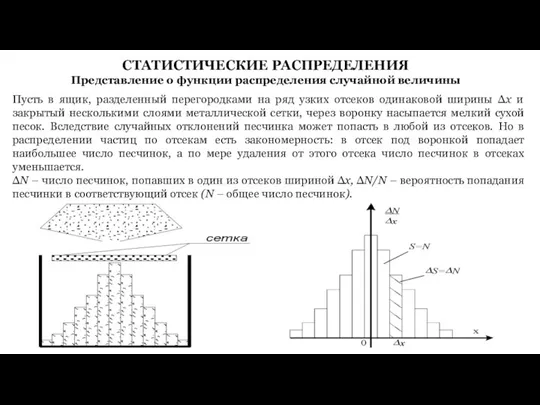
- 18. СТАТИСТИЧЕСКИЕ РАСПРЕДЕЛЕНИЯ Представление о функции распределения случайной величины Пусть в ящик, разделенный перегородками на ряд узких
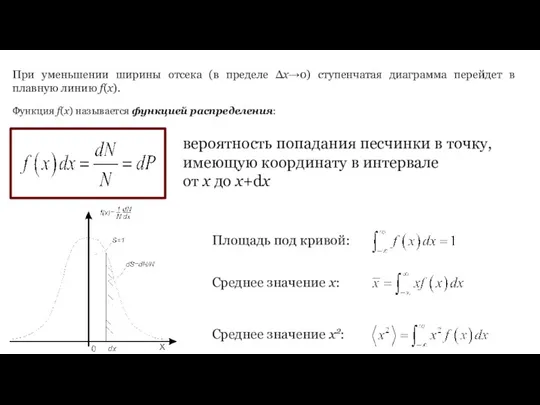
- 19. Функция f(x) называется функцией распределения: При уменьшении ширины отсека (в пределе Δx→0) ступенчатая диаграмма перейдет в
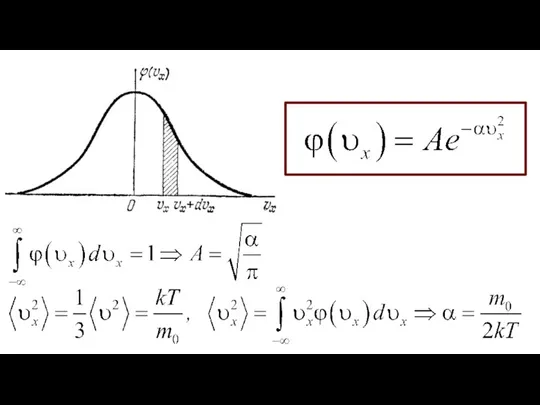
- 20. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО СКОРОСТЯМ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА) Молекулы газа, участвуя в непрерывном хаотическом движении, сопровождающемся многочисленными столкновениями
- 21. Идея Максвелла: попадания компонент скорости молекулы в интервалы (υx; υx +dυx), (υy; υy +dυy) и (υz;
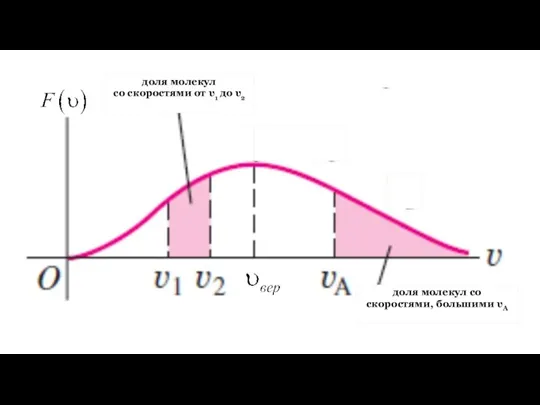
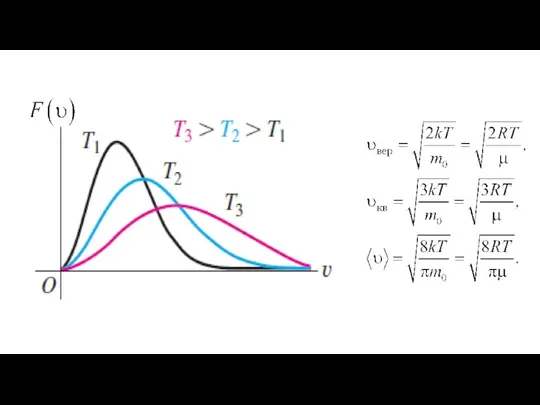
- 24. вероятность того, что модуль скорости наугад выбранной молекулы лежит в интервале от υ до υ+dυ
- 27. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ В ПОТЕНЦИАЛЬНОМ СИЛОВОМ ПОЛЕ (РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА) Выделим мысленно вертикальный столб воздуха с площадью основания
- 28. Тогда Интегрируя, получим: где n0 - концентрация на высоте h = 0. распределение Больцмана U –
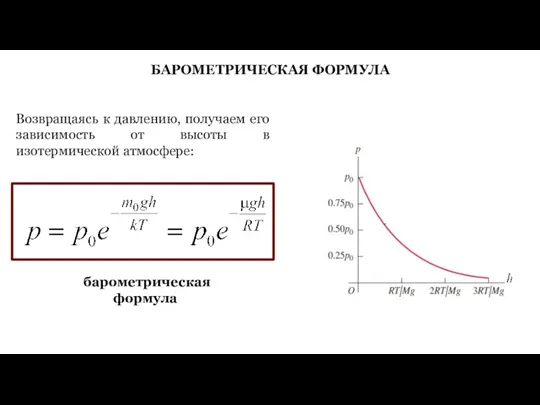
- 29. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА Возвращаясь к давлению, получаем его зависимость от высоты в изотермической атмосфере: барометрическая формула
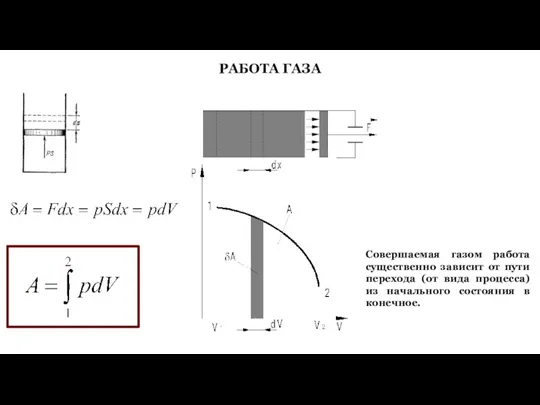
- 30. РАБОТА ГАЗА Совершаемая газом работа существенно зависит от пути перехода (от вида процесса) из начального состояния
- 31. Оболочка называется адиабатической, если состояние заключенной в ней системы остается неизменным при любых изменениях температуры окружающих
- 32. Внутренней энергией системы U называется функция состояния, приращение которой во всяком процессе, совершаемом системой в адиабатической
- 33. КОЛИЧЕСТВО ТЕПЛОТЫ Процесс обмена внутренними энергиями соприкасающихся тел, не сопровождающийся производством макроскопической работы, называется теплообменом. Энергия,
- 34. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Система (I+II) заключена в адиабатическую оболочку. Граница АВ – теплопроводящая. Оболочка системы II
- 35. Если U1 = U2 и Q = 0, то А = 0. Т.е. невозможен процесс, единственным
- 36. Стационарный переход теплоизолированного газа от одного давления к другому, происходящий в условиях, когда газ в процессе
- 37. внутренняя энергия идеального газа
- 38. ТЕПЛОЕМКОСТЬ отношение бесконечно малого количества тепла, полученного телом, к соответствующему приращению его температуры называется теплоемкостью тела
- 39. Молярные теплоемкости идеального газа при постоянном объеме и постоянном давлении
- 40. Для одного моля идеального газа: уравнение Майера
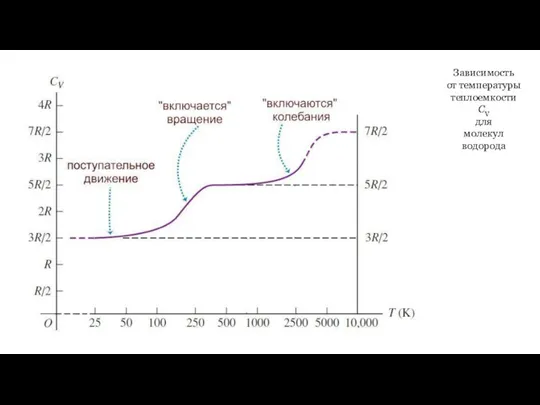
- 41. Зависимость от температуры теплоемкости СV для молекул водорода
- 42. АДИАБАТНЫЙ ПРОЦЕСС Процесс, происходящий без подвода и отвода тепла, называется адиабатным:
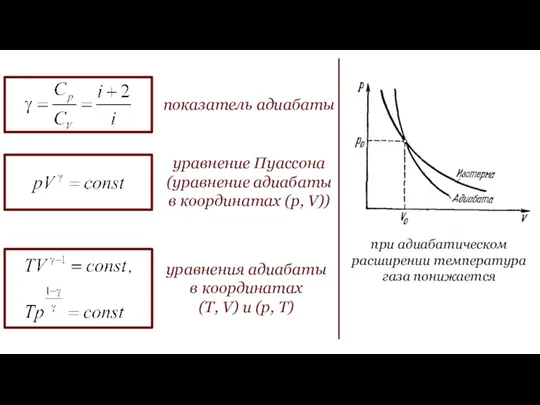
- 43. показатель адиабаты уравнение Пуассона (уравнение адиабаты в координатах (p, V)) уравнения адиабаты в координатах (T, V)
- 44. ПОЛИТРОПНЫЙ ПРОЦЕСС Процесс, в котором теплоемкость остается постояннной, называется адиабатным:
- 45. показатель политропы молярная теплоемкость идеального газа в политропном процессе уравнения политропы в координатах (p, V), (T,
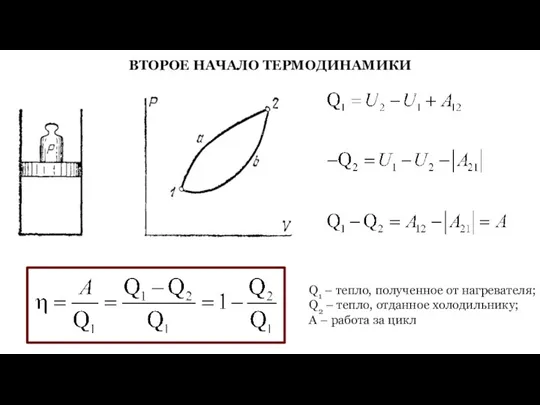
- 46. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q1 – тепло, полученное от нагревателя; Q2 – тепло, отданное холодильнику; A –
- 47. ? Можно ли построить периодически действующую тепловую машину без холодильника (перпетуум мобиле второго рода)? НЕВОЗМОЖНОСТЬ ПОСТРОЕНИЯ
- 48. ФОРМУЛИРОВКИ ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ Формулировка Планка: невозможно построить периодически действующую машину, единственным результатом которой было бы
- 49. ЦИКЛ КАРНО. ТЕОРЕМЫ КАРНО 1-ая теорема Карно: к.п.д. тепловой машины, работающей по циклу Карно, зависит только
- 50. НЕРАВЕНСТВО КЛАУЗИУСА (ЧАСТНЫЙ СЛУЧАЙ) 2-ая теорема Карно: к.п.д. всякой тепловой машины не может превосходить к.п.д. идеальной
- 51. НЕРАВЕНСТВО КЛАУЗИУСА (ОБЩИЙ СЛУЧАЙ). РАВЕНСТВО КЛАУЗИУСА. ЭНТРОПИЯ При окончательной формулировке неравенства можно пользоваться представлением о теплообмене
- 52. - элементарное приведенное количество тепла, полученное в бесконечно малом процессе; - приведенное количество тепла, полученное в
- 53. пути I и II перехода системы из состояния 1 в состояние 2 –квазистатические приведенное количество тепла,
- 54. ЭНТРОПИЯ Энтропия – функция состояния системы. Разность энтропий в двух равновесных состояниях равна приведенному количеству тепла,
- 55. :Приращение энтропии идеального газа:
- 56. ЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ Путь I – необратимый, путь II – квазистатический. Если система адиабатически изолирована:
- 57. СТАТИСТИЧЕСКИЙ СМЫСЛ ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ Состояние системы может быть задано с помощью макроскопических (то есть характеризующих
- 58. Вероятность того, что все N молекул соберутся в одной половине сосуда:
- 60. Скачать презентацию













































 Плавання тіл. Закон Архімеда
Плавання тіл. Закон Архімеда Решение задач на применение законов Ньютона
Решение задач на применение законов Ньютона Метод проектов на уроках физики
Метод проектов на уроках физики Атмосферное давление . Опыт Торричелли. Билет № 22. Нормальное атмосферное давление
Атмосферное давление . Опыт Торричелли. Билет № 22. Нормальное атмосферное давление Гидравлический расчет трубопроводов
Гидравлический расчет трубопроводов Презентация по физике Движение тела, брошенного вертикально вверх
Презентация по физике Движение тела, брошенного вертикально вверх Задачи на встречное движение
Задачи на встречное движение Механикалық энергия
Механикалық энергия Ремонт колёсных пар и буксовых узлов
Ремонт колёсных пар и буксовых узлов Лабораторная работа Изучение работы трансформатора
Лабораторная работа Изучение работы трансформатора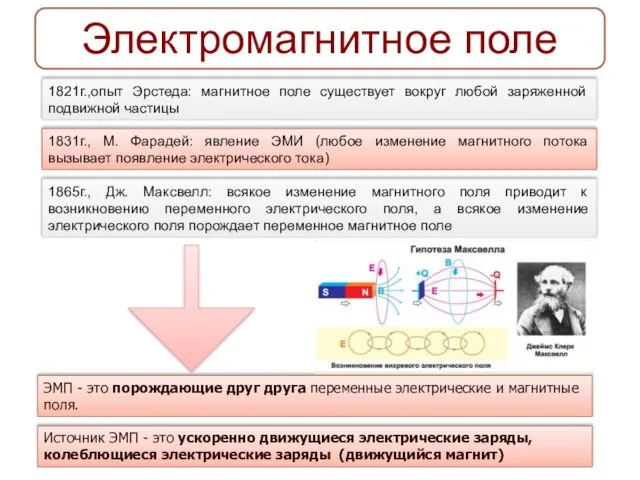 Электромагнитное поле
Электромагнитное поле Температурный режим воздуха и почвы
Температурный режим воздуха и почвы Оптические явления в природе
Оптические явления в природе Россыпь анограмм. Физика в мультфильмах
Россыпь анограмм. Физика в мультфильмах Свободное падение тел. Движение с ускорением свободного падения
Свободное падение тел. Движение с ускорением свободного падения Физические основы механики. Лекция 1
Физические основы механики. Лекция 1 Магнитное поле. Взаимодействие токов
Магнитное поле. Взаимодействие токов Сопротивление материалов: деформация, напряжение
Сопротивление материалов: деформация, напряжение Термоядерная реакция (9 класс)
Термоядерная реакция (9 класс) Основы теории двухполюсников. (Лекция 5)
Основы теории двухполюсников. (Лекция 5) Магнитное поле. 11 класс
Магнитное поле. 11 класс Электромагнитные волны. Электромагнитное поле как особый вид материи
Электромагнитные волны. Электромагнитное поле как особый вид материи Рулевое управление
Рулевое управление Световое загрязнение
Световое загрязнение Рівномірний рух по колу
Рівномірний рух по колу Физика атомного ядра и элементарных частиц
Физика атомного ядра и элементарных частиц Physical chemistry of nanostructured systems
Physical chemistry of nanostructured systems Газовые законы
Газовые законы