Содержание
- 2. Вопросы для повторения: В чём сущность явления радиоактивности? Кем оно было открыто и исследовано? Опишите опыт
- 3. Радиоактивность Радиоактивность – способность атомов некоторых химических элементов к самопроизвольному излучению.
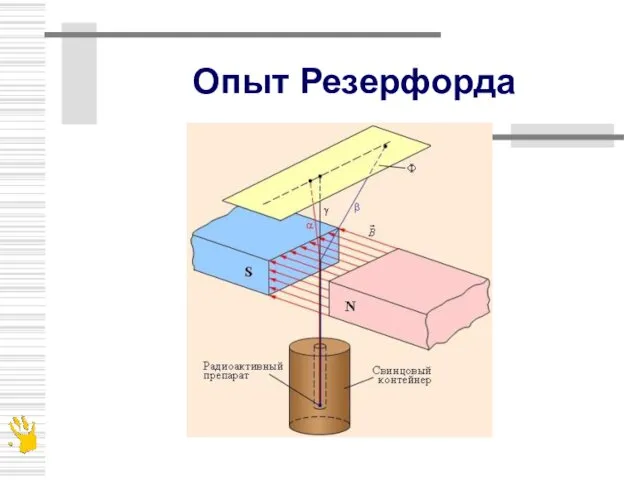
- 4. Опыт Резерфорда
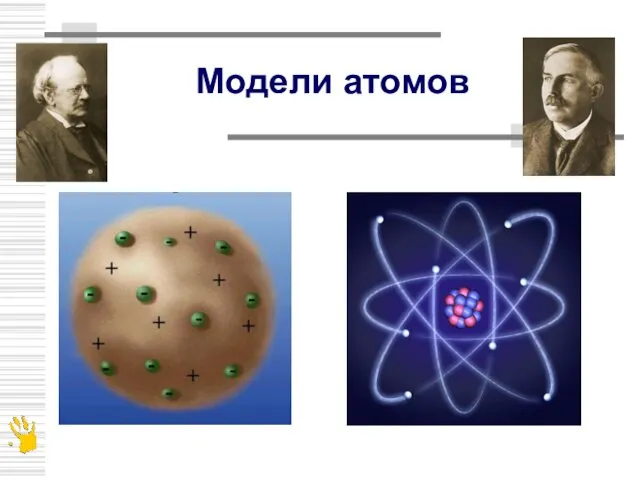
- 5. Модели атомов
- 6. Опыт Резерфорда по рассеянию альфа-частиц
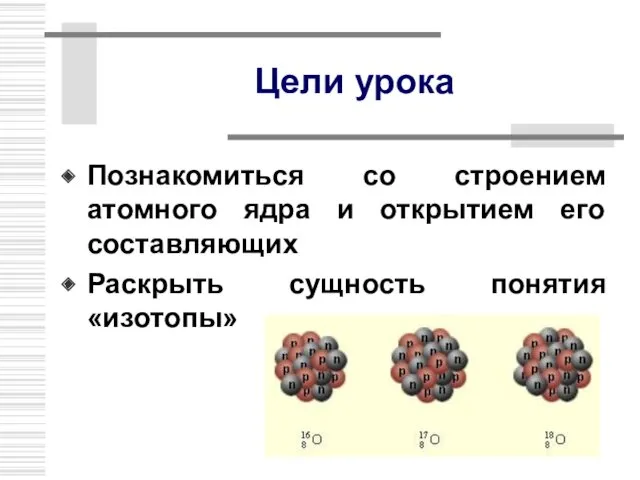
- 7. Цели урока Познакомиться со строением атомного ядра и открытием его составляющих Раскрыть сущность понятия «изотопы»
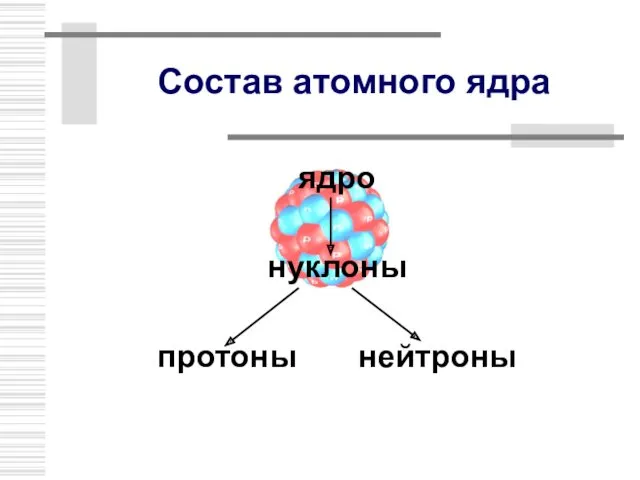
- 8. Состав атомного ядра ядро нуклоны протоны нейтроны
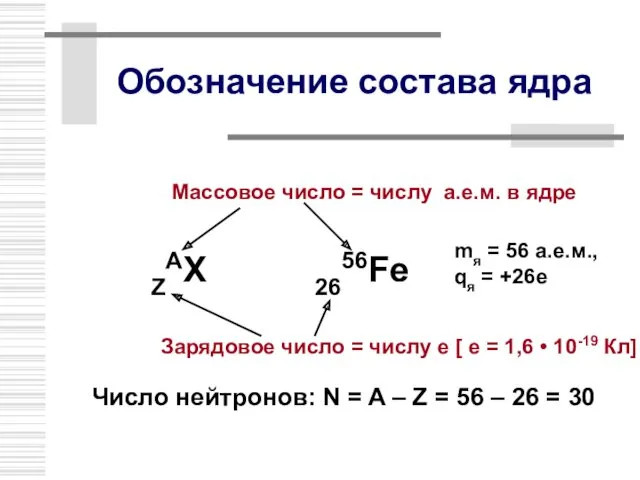
- 9. Обозначение состава ядра ZAX 2656Fe Зарядовое число = числу е [ е = 1,6 • 10-19
- 10. Радиоактивные превращения атомных ядер 88226Rd ? 86222Rn + 24He В 1903 г. Э.Резерфорд и Ф.Содди обнаружили
- 11. Открытие протона В 1919 г. Резерфорд поставил опыт по исследованию взаимодействия альфа-частиц с ядрами атомов азота,
- 12. Открытие протона 714N + 24He ? 817O + 11H Протоны входят в состав ядер атомов всех
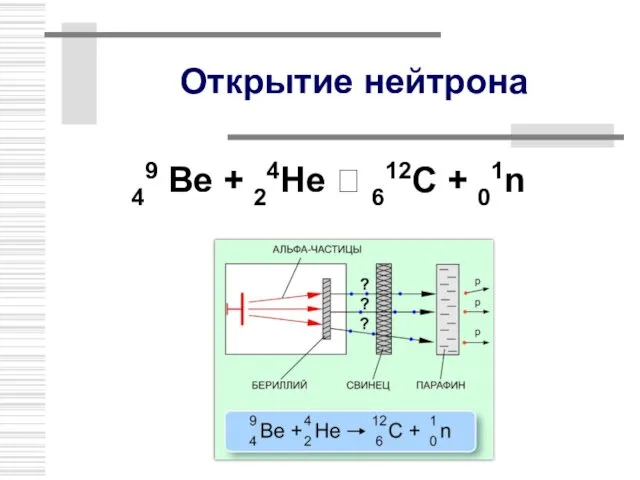
- 13. Открытие нейтрона В 1932 г. Дж. Чедвик , исследуя бериллиевое излучение,открыл нейтрон n0 или 01n mn
- 14. Открытие нейтрона 49 Ве + 24Не ? 612C + 01n
- 15. Протонно-нейтронная модель ядра В 1932 г. Д.Д.Иваненко и В.Г.Гейзенберг выдвинули гипотезу о протонно-нейтронном строении ядра: атомные
- 16. Протонно-нейтронная модель ядра Общее число нуклонов в ядре называется массовым и обозначается буквой А. Число протонов
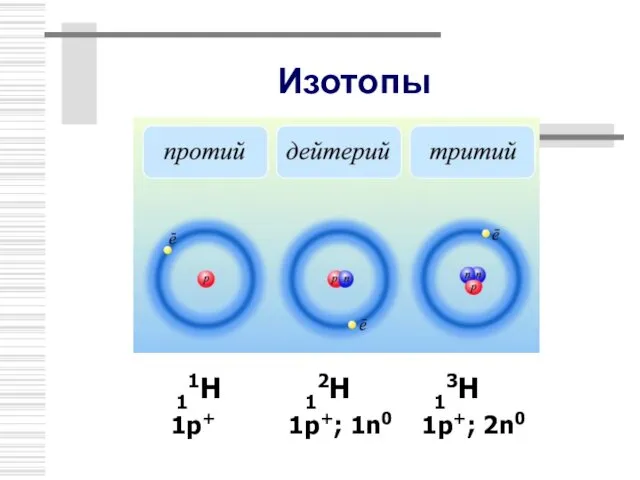
- 17. Изотопы В 1911 г. Ф.Содди предположил, что ядра с одинаковым числом протонов, но разным числом нейтронов
- 18. Изотопы 11Н 12Н 13Н 1р+ 1р+; 1n0 1p+; 2n0
- 19. Относительная атомная масса химического элемента 100 атомов Cl 75 атомов 25 атомов 1735Cl 1737Cl Ar=mср= 35
- 20. Закрепление изученного Сборник задач Лукашик № 1656 №1658 №1661 упр. 51 № 3-5, с. 234-235
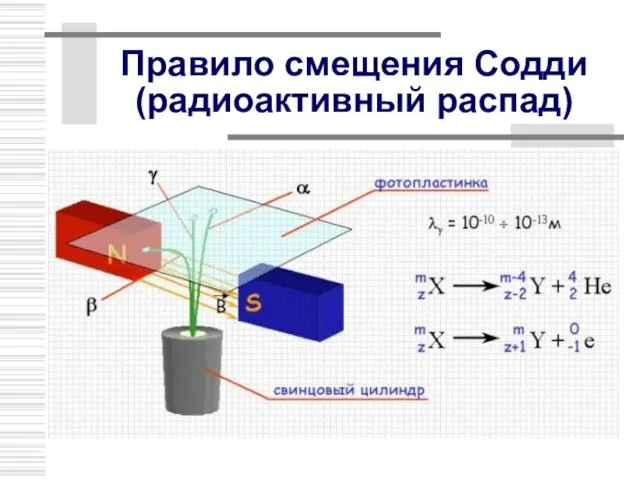
- 21. Правило смещения Содди (радиоактивный распад)
- 22. Правило смещения (α- распад)
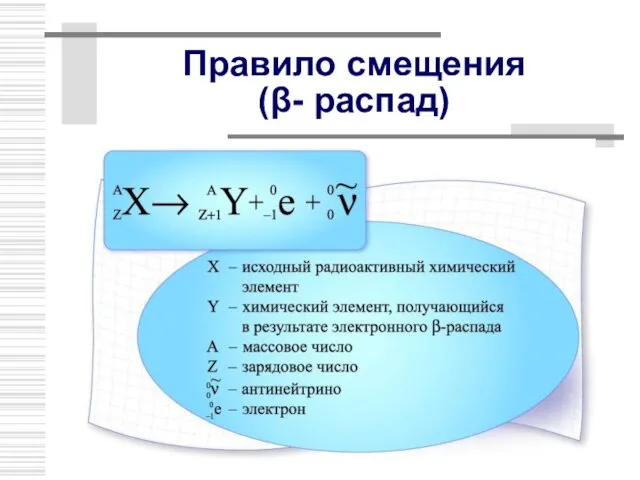
- 23. Правило смещения (β- распад)
- 25. Скачать презентацию













 Свойства уравнений Максвелла
Свойства уравнений Максвелла Физика – это интересно! Внеклассное мероприятие по физике. 7 класс
Физика – это интересно! Внеклассное мероприятие по физике. 7 класс Механическое движение. Что называют механическим движением?
Механическое движение. Что называют механическим движением? Основные понятия твердотельной электроники
Основные понятия твердотельной электроники Ходовая часть гусеничного трактора
Ходовая часть гусеничного трактора Электрическое явление
Электрическое явление Кинематическая схема станка СТД-120 м
Кинематическая схема станка СТД-120 м Лекция 3: Волновая оптика. Дифракция. Фурье оптика
Лекция 3: Волновая оптика. Дифракция. Фурье оптика Сила тяжести, вес тела
Сила тяжести, вес тела Управляемый термоядерный синтез (УТС)
Управляемый термоядерный синтез (УТС) Вечный двигатель
Вечный двигатель Паровая машина
Паровая машина Последние достижения в области нанотехнологий
Последние достижения в области нанотехнологий Lektsia_16_Fotoeffekt
Lektsia_16_Fotoeffekt Презентация по теме Сила трения
Презентация по теме Сила трения Зачем физика повару?
Зачем физика повару? Лазеры: строение, свойства, основные виды
Лазеры: строение, свойства, основные виды Hot charging area elevator chains
Hot charging area elevator chains Потенциал электростатического поля. Разность потенциалов
Потенциал электростатического поля. Разность потенциалов Статика. Равновесие тел
Статика. Равновесие тел Презентация Параллельное и последовательное соединение
Презентация Параллельное и последовательное соединение Теплообмен при омывании труб
Теплообмен при омывании труб Презентация-игра, 7-8 класс
Презентация-игра, 7-8 класс Импульсные сигналы и переходные процессы. Общие сведения об импульсных сигналах
Импульсные сигналы и переходные процессы. Общие сведения об импульсных сигналах Солнечная энергетика
Солнечная энергетика Подшипники качения
Подшипники качения КАБИНЕТ ФИЗИКИ
КАБИНЕТ ФИЗИКИ Сплошная среда
Сплошная среда