Содержание
- 2. Целью дисциплины является – изучение физических основ и разновидностей электронных приборов, их принципа действия, основных параметров
- 3. Компете́нция (от лат. competere — соответствовать, подходить) — способность применять знания, умения, успешно действовать на основе
- 4. Первым электронным переключающим прибором был вакуумный диод, запатентованный в 1904 году англичанином Д.А. Флемингом
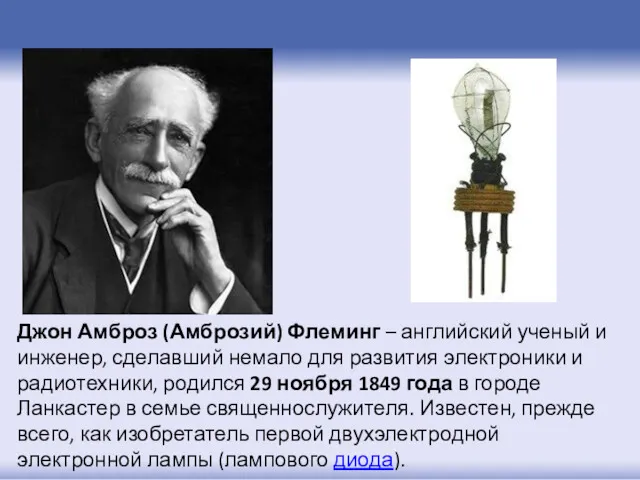
- 5. Джон Амброз (Амброзий) Флеминг – английский ученый и инженер, сделавший немало для развития электроники и радиотехники,
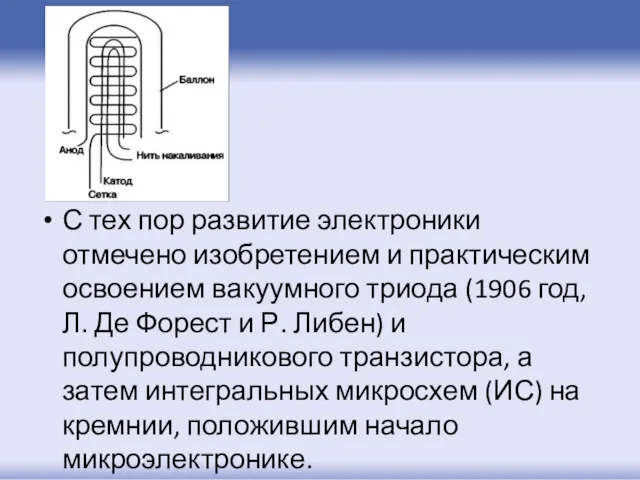
- 6. С тех пор развитие электроники отмечено изобретением и практическим освоением вакуумного триода (1906 год, Л. Де
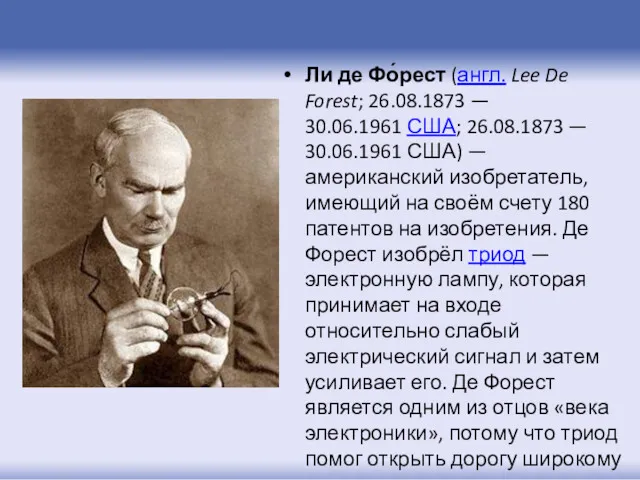
- 7. Ли де Фо́рест (англ. Lee De Forest; 26.08.1873 — 30.06.1961 США; 26.08.1873 — 30.06.1961 США) —
- 8. Р. Либен (Robert von Liben) (5.09.1878 –20.02.1913 in Vienna) – австрийский физик.
- 9. Создание первого транзистора 1947 год 1956 год. Вручение Бардину, Браттейну и Шокли Нобелевскую премию по физике
- 11. Создание Первой микросхемы с 5 транзисторами 12 сентября 1958 г. в компании Texas Instruments
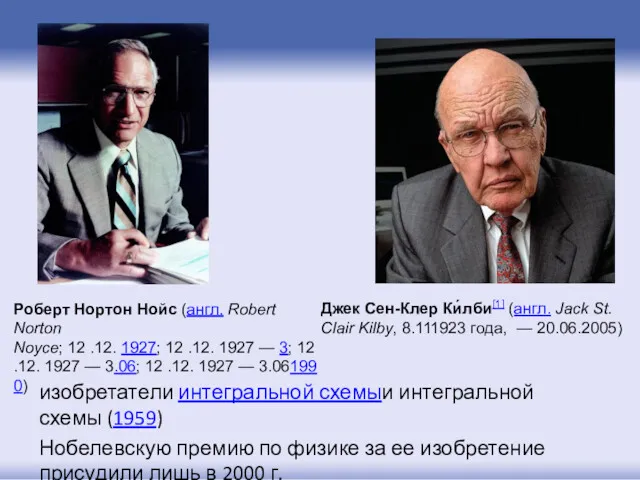
- 12. изобретатели интегральной схемыи интегральной схемы (1959) Нобелевскую премию по физике за ее изобретение присудили лишь в
- 13. Создание Первой коммерческой ИС с поликремниевым затвором 1968 г.
- 14. Сама возможность существования твердого состояния вещества обусловлена взаимодействием сил притяжения и отталкивания (взаимодействия) между частицами (атомами,
- 15. Выделяют несколько видов связи: Силы Ван-дер-Ваальса; Ковалентная; Ионная (полярная); Металлическая; Водородная
- 16. Кристаллы – это вещества, в которых составляющие их частицы (атомы, молекулы) расположены строго периодически, образуя геометрически
- 21. Движение электронов в атоме Все окружающие нас тела состоят из элементарных частиц (атомов) или из групп
- 24. 30.08.1871, Спринг Грув - 19.10.1937, Кембридж) – британский физик новозеландского происхождения. Известен как «отец» ядерной физикиИзвестен
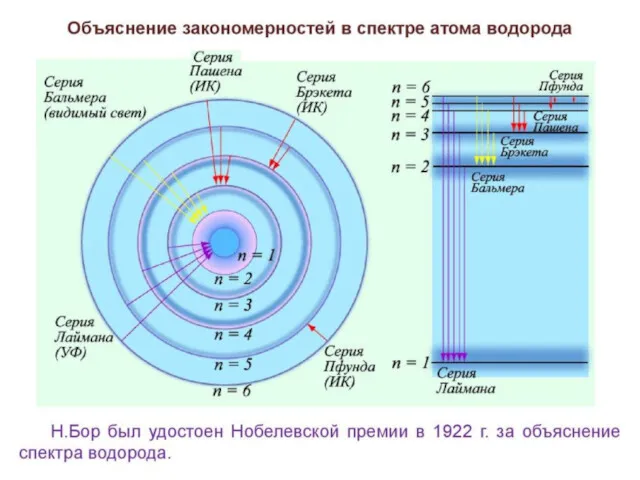
- 29. Постулаты Бора Нильс Хе́нрик Дави́д Бор (дат. Niels Henrik David Bohr; 7.10; 7.10. 1885; 7.10. 1885
- 31. Каждый атом или молекула может находиться в том или другом энергетическом состоянии. Иначе говоря, их внутренняя
- 33. Взаимодействие частиц в квантовой механике характеризуют потенциальной энергией, формула которой заимствуется из классической механики. Например, потенциальная
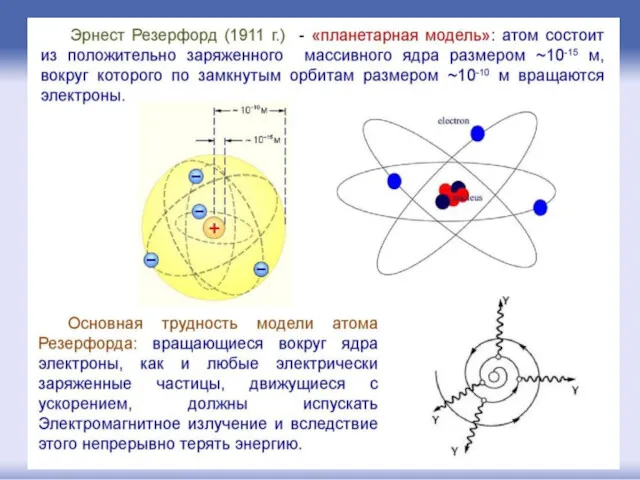
- 34. Квантование энергии атома Запишем условие вращения электрона массы по круговой орбите радиуса r под действием кулоновской
- 35. Решая эту систему уравнений, находим для радиусов стационарных орбит электрона в атоме водорода следующее выражение Вводя
- 36. Для скорости электрона на n-ой стационарной орбите получаем значение Полная энергия электрона, движущегося по n -ой
- 37. Полная энергия электрона в атоме оказалась отрицательной, так как отрицательна потенциальная электростатическая энергия взаимодействия электрона с
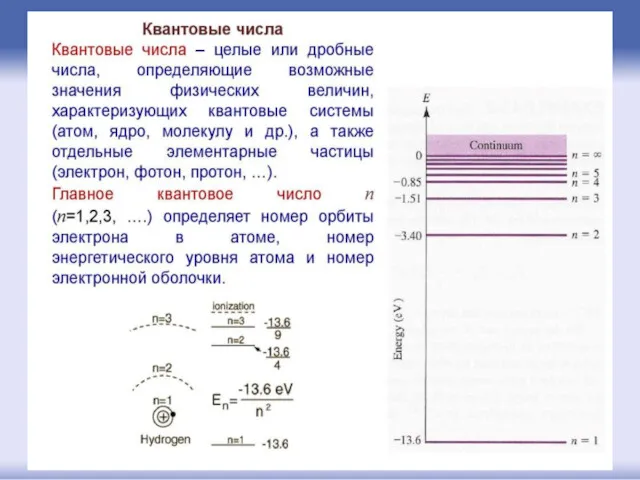
- 38. квантовые числа
- 40. Главное квантовое число n может принимать любые целые положительные значения от 1 до ∞. Оно определяет
- 41. Размеры атомной орбитали с увеличением атомного номера z уменьшаются приблизительно в z раз, а с увеличением
- 42. С увеличением n расстояние между энергетическими уровнями и энергия связи электронов с ядрами уменьшается, значение энергетического
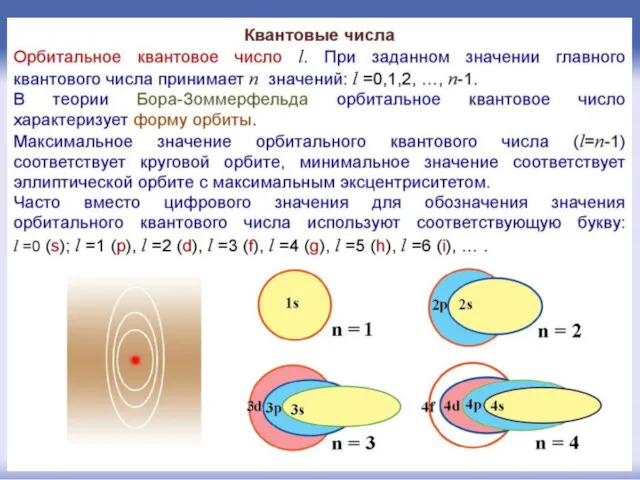
- 43. Орбитальное квантовое число l определяет форму орбитали. Значение орбитального числа l=(n-1)=0,1,2,3...(n-1). Также вводят буквенные обозначения: орбитали
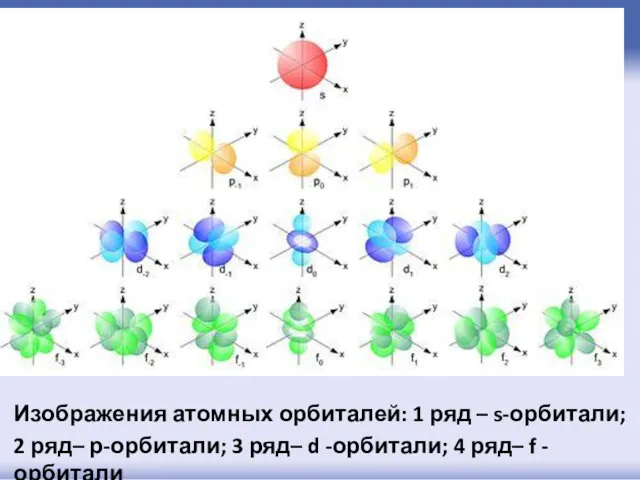
- 46. Изображения атомных орбиталей: 1 ряд – s-орбитали; 2 ряд– р-орбитали; 3 ряд– d -орбитали; 4 ряд–
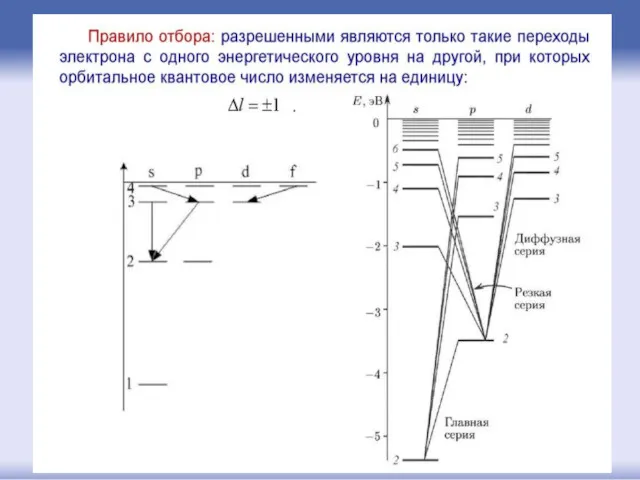
- 47. Каждому уровню энергии соответствует стоячая электронная волна, электрон колеблется вокруг и возле атомов и образует как
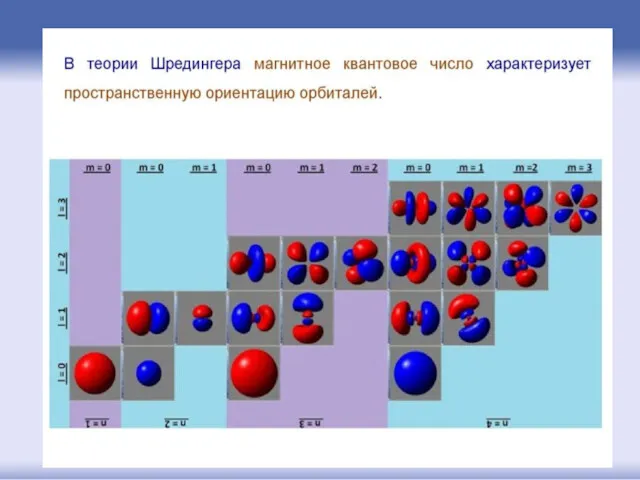
- 49. Магнитное квантовое число характеризует величину магнитного поля, создаваемого при вращении электрона вокруг ядра. Поэтому значение магнитного
- 54. – магнетон Бора (единица элементарного магнитного момента)
- 55. В 1925 г. голландец Ральф Кронинг и независимо Джордж Уленбек и Самюэль Гаудсмит предположили, что электрон
- 57. Спиновое квантовое число s Электрон помимо координат и импульса характеризуется вектором спина. Внутренний момент импульса, связанный
- 58. Спин – это одно из проявлений принципа тождественности частиц, который применительно к электронам звучит так: все
- 60. Скачать презентацию












































 Первый закон термодинамики
Первый закон термодинамики Повітряний транспорт
Повітряний транспорт Солнечные источники энергии. Солнечные батареи
Солнечные источники энергии. Солнечные батареи Теория деформаций. Лекция 4
Теория деформаций. Лекция 4 Термодинамика. Законы термодинамики
Термодинамика. Законы термодинамики Сопротивление. Закон Ома
Сопротивление. Закон Ома Техническая эксплуатация машинно-транспортного парка
Техническая эксплуатация машинно-транспортного парка Катушка Теслы
Катушка Теслы Посвящение в юные физики
Посвящение в юные физики Техническое обслуживание и диагностирование неисправностей сельскохозяйственных машин, ремонт отдельных деталей и узлов
Техническое обслуживание и диагностирование неисправностей сельскохозяйственных машин, ремонт отдельных деталей и узлов Источники звука. Звуковые волны. 9 класс
Источники звука. Звуковые волны. 9 класс Инструментальные методы исследования органических веществ. Лекция 11
Инструментальные методы исследования органических веществ. Лекция 11 Транспортная энергетика. Лекция 5. Термодинамика газового потока
Транспортная энергетика. Лекция 5. Термодинамика газового потока Законы Ньютона. 10 класс
Законы Ньютона. 10 класс Механическая работа
Механическая работа Решение краевых задач для уравнения теплопроводности
Решение краевых задач для уравнения теплопроводности Композитные материалы
Композитные материалы Методы разделения и концентрирования. Хроматография
Методы разделения и концентрирования. Хроматография Потенциал. Решение задач
Потенциал. Решение задач Детали машин и основы конструирования. Цепные передачи. (Лекция 6)
Детали машин и основы конструирования. Цепные передачи. (Лекция 6) Статистические и термодинамические свойства макросистем
Статистические и термодинамические свойства макросистем Расчет гармонических колебаний в электрических цепях
Расчет гармонических колебаний в электрических цепях Презентация Спектры (качественные задачи по теме Излучения и спектры)
Презентация Спектры (качественные задачи по теме Излучения и спектры) Презентация по физике Механические колебания
Презентация по физике Механические колебания Лекция 1-01 (2024)
Лекция 1-01 (2024) BRAIN-RING ФИЗИКИ
BRAIN-RING ФИЗИКИ Определение мощности. Лабораторная работа
Определение мощности. Лабораторная работа Энергия
Энергия