Слайд 2

Основные положения МКТ
Все вещества состоят из мельчайших частиц (атомов, молекул, электронов,
ионов).
Частицы вещества находятся в непрерывном хаотическом движении (броуновском движении).
Частицы вещества взаимодействуют друг с другом.
Слайд 3

Основная задача МКТ
Найти уравнение состояния вещества, установив связь между макроскопическими
и микроскопическими параметрами.
Слайд 4
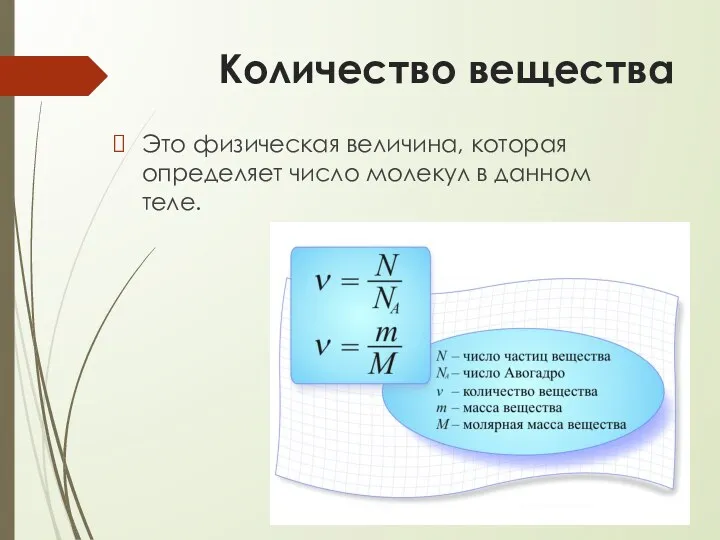
Количество вещества
Это физическая величина, которая определяет число молекул в данном теле.
Слайд 5

Постоянная Авогадро
Численно равна числу молекул в одном моле
NA = 6,02·1023 моль−1
Слайд 6

Молярная масса
M - это масса одного моля вещества
Слайд 7

Слайд 8

Концентрация частиц
это количество частиц в объеме
Слайд 9

Температура
характеризует состояние теплового равновесия: все тела, находящиеся в тепловом равновесии, имеют
одинаковую температуру
между абсолютной шкалой температур и шкалой Цельсия существует связь
Т = t °С + 273 (К)
Слайд 10
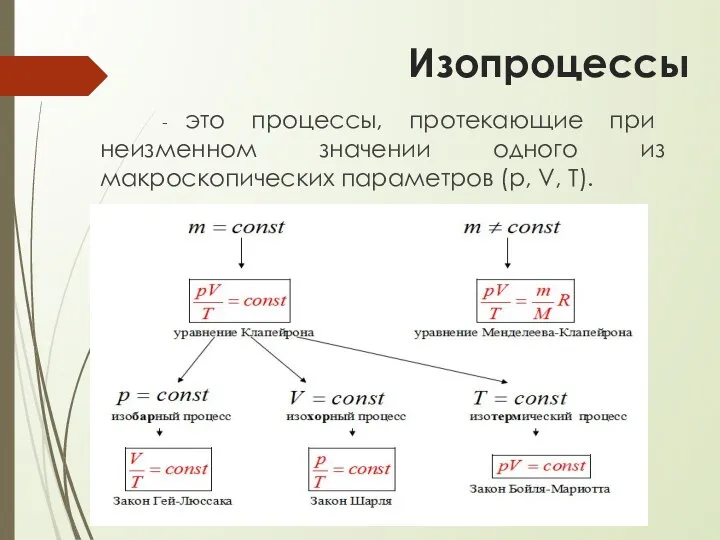
Изопроцессы
- это процессы, протекающие при неизменном значении одного из
макроскопических параметров (р, V, Т).
Слайд 11
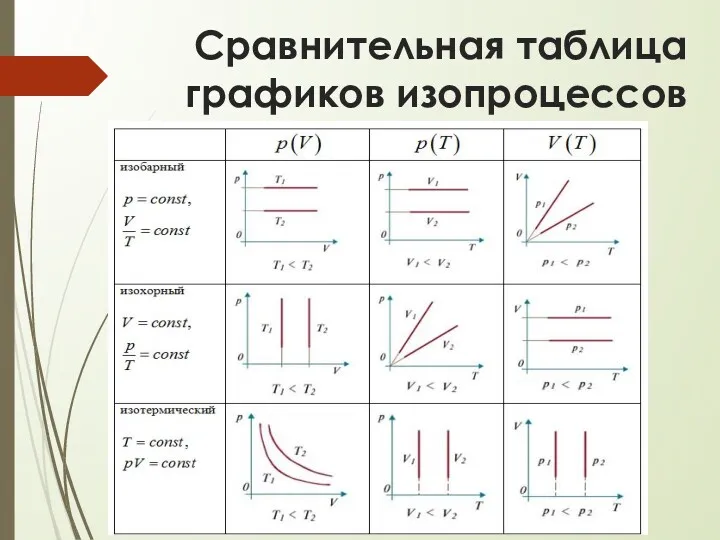
Сравнительная таблица
графиков изопроцессов
Слайд 12

Уравнение
состояния газа
Это уравнение, связывающее все три параметра – давление, объем
и температуру газа для данной его массы
Слайд 13

Уравнение Менделеева-Клапейрона
Слайд 14

Основное уравнение молекулярно-кинетической теории
Слайд 15
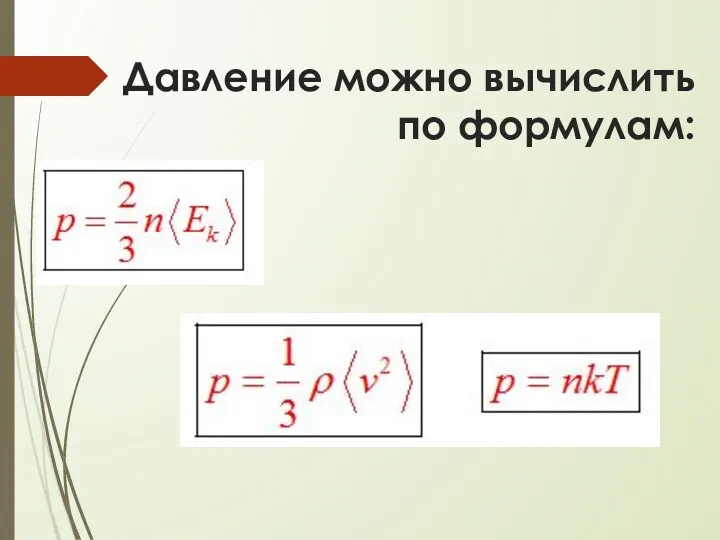
Давление можно вычислить по формулам:
Слайд 16
Слайд 17

















 Презентация по теме Деформация. Виды деформации
Презентация по теме Деформация. Виды деформации Турбомашиналардың паралель жұмыс істеуі бір
Турбомашиналардың паралель жұмыс істеуі бір Система сходящихся сил. Основные понятия статики
Система сходящихся сил. Основные понятия статики Импульс тела презентация к уроку физики
Импульс тела презентация к уроку физики Рулевое управление. Устройство автомобиля
Рулевое управление. Устройство автомобиля Законы геометрической оптики: отражение, преломление, полное внутреннее отражение, предельный угол преломления
Законы геометрической оптики: отражение, преломление, полное внутреннее отражение, предельный угол преломления техника философиясы
техника философиясы Механические свойства твердых тел
Механические свойства твердых тел Звук, инфразвук, ультразвук
Звук, инфразвук, ультразвук Разработка урока физики 10 класс
Разработка урока физики 10 класс Тиристор деп төрт деңгейлі жартылай өткізгіш құрылғылардын
Тиристор деп төрт деңгейлі жартылай өткізгіш құрылғылардын Проект От опытных фактов – к научной гипотезе или заглядывая вглубь Вселенной
Проект От опытных фактов – к научной гипотезе или заглядывая вглубь Вселенной Линзы. Построение изображений, даваемых линзой.
Линзы. Построение изображений, даваемых линзой. Сообщающиеся сосуды
Сообщающиеся сосуды Лекция №6 (6 ). Поле системы элементарных излучателей
Лекция №6 (6 ). Поле системы элементарных излучателей презентация Сила трения
презентация Сила трения Теоретические и правовые основы метрологического обеспечения
Теоретические и правовые основы метрологического обеспечения Авиационные преобразователи электрической энергии
Авиационные преобразователи электрической энергии Магнітне поле постійного струму
Магнітне поле постійного струму Cathode Ray Oscilloscope
Cathode Ray Oscilloscope Электрическая цепь и ее элементы
Электрическая цепь и ее элементы Электрический ток в металлах. Действия электрического тока
Электрический ток в металлах. Действия электрического тока Импульсные сигналы и переходные процессы. Общие сведения об импульсных сигналах
Импульсные сигналы и переходные процессы. Общие сведения об импульсных сигналах Жылу мөлшері. Заттың меншікті жылусыйымдылығы
Жылу мөлшері. Заттың меншікті жылусыйымдылығы Простые механизмы
Простые механизмы Конспект урока с презентацией по физике 7 класс Диффузия
Конспект урока с презентацией по физике 7 класс Диффузия Гидравлический пресс
Гидравлический пресс Уравнение динамики идеальной сплошной среды. Модель линий ток. Уравнение динамики при возмущении среды
Уравнение динамики идеальной сплошной среды. Модель линий ток. Уравнение динамики при возмущении среды