Содержание
- 2. ТЕРМОДИНАМИКА ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ СОДЕРЖАНИЕ КЛАССИЧЕСКАЯ ТЕРМОДИНАМИКА ИСТОРИЯ НАЧАЛ ТЕРМОДИНАМИКИ
- 3. Термодинамика Термодинамика — раздел физики,изучающий соотношения и превращения теплоты и других форм энергии. Термодинамика – наука
- 4. Классическая термодинамика: Главные законы термодинамики (иногда также называемые началами). Уравнения состояния и прочие свойства простых термодинамических
- 5. История начал термодинамики Первое установленное начало термодинамики, которое в конечном счете стало «Вторым законом», было сформулирован
- 6. Ю́лиус Ро́берт фон Ма́йер (1814 —1878) —немецкий врач и естествоиспытатель. Родился в семье немецкого зажиточного пивовара.
- 7. Джеймс Пре́скотт Джо́уль (1818— 1889) —английский физик. Родился в семье богатого пивовара. Получил домашнее образование. В
- 8. Герман Людвиг Фердинанд фон Гельмгольц (1821— 1894) —немецкий физик,врач, физиолог и психолог. В своих первых научных
- 9. КАРНО́ (Никола Леонар) Сади (1796—1832), французский физик и инженер. В 1824 году вышла его первая и
- 10. Лю́двиг Бо́льцман (1844— 1906) — австрийский физик-теоретик. Больцман родился в Вене в семье акцизного чиновника. Важное
- 11. Рудольф Юлиус Эммануэль Клаузиус (имя при рожд. — Рудольф Готтлиб (1822— 1888) — немецкий физик, механик
- 12. Начала термодинамики — совокупность постулатов, лежащих в основе термодинамики. Эти положения были установлены в результате научных
- 13. Первое начало термодинамики представляет собой закон сохранения энергии, один из всеобщих законов природы (наряду с законами
- 14. Приведем еще некоторые формулировки первого начала термодинамики: Полная энергия изолированной системы постоянна; Невозможен вечный двигатель первого
- 15. Внутренняя энергия это сумма энергий теплового движения молекул и межмолекулярных взаимодействий. В аксиоматической термодинамике движение молекул
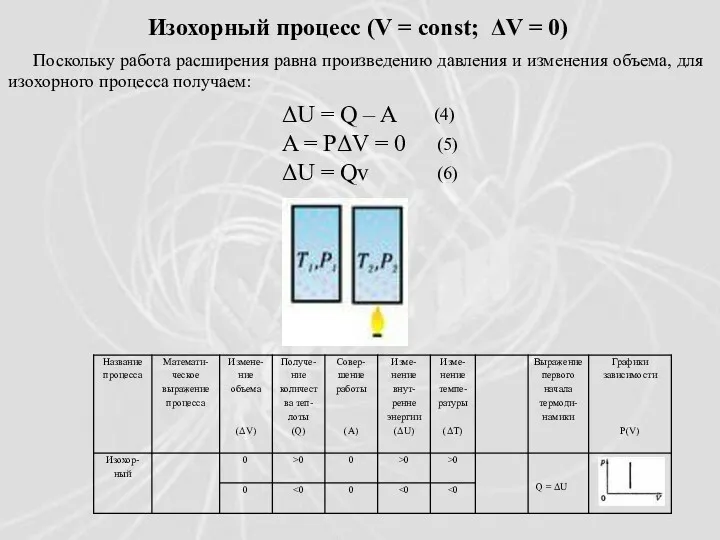
- 16. Изохорный процесс (V = const; ΔV = 0) Поскольку работа расширения равна произведению давления и изменения
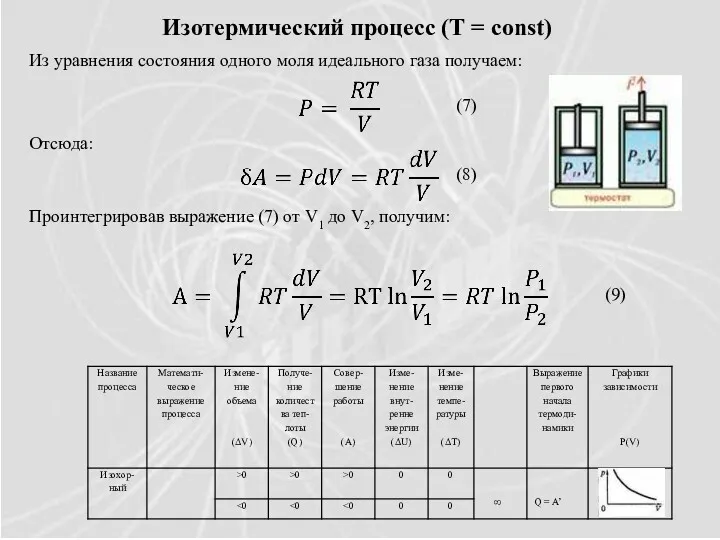
- 17. Изотермический процесс (Т = const) Из уравнения состояния одного моля идеального газа получаем: Отсюда: Проинтегрировав выражение
- 18. Изобарный процесс (Р = const) Подставляя полученные выражения для работы различных процессов в уравнение (4), для
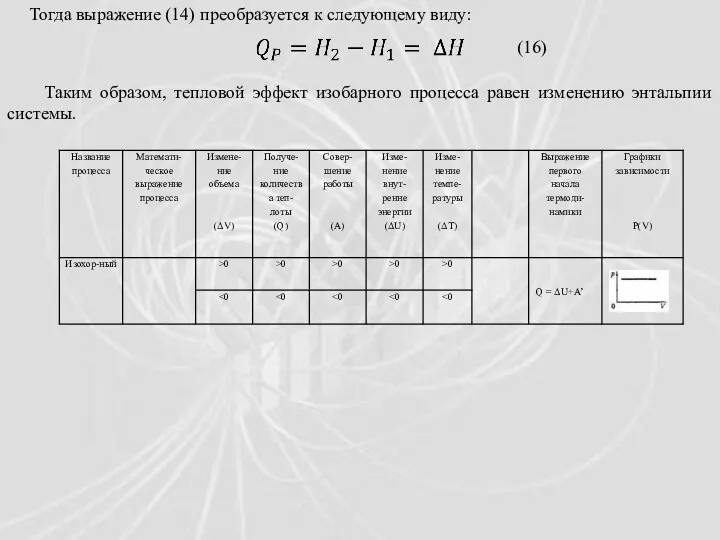
- 19. Тогда выражение (14) преобразуется к следующему виду: (16) Таким образом, тепловой эффект изобарного процесса равен изменению
- 20. Адиабатический процесс (Q = 0) Адиабати́ческий проце́сс— термодинамический процесс в макроскопической системе, при котором система не
- 21. К особенностям первого начала следует отнести то, что: первое начало термодинамики не указывает, в каком направлении
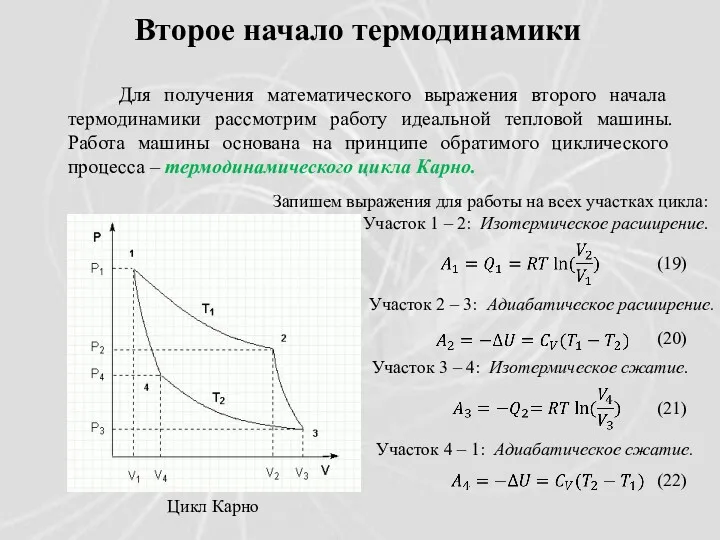
- 22. Второе начало термодинамики Для получения математического выражения второго начала термодинамики рассмотрим работу идеальной тепловой машины. Работа
- 23. Проведя ряд несложных преобразований, получим для КПД идеальной тепловой машины, работающей по циклу Карно: Общая работа
- 24. Для описания термодинамических процессов первого начала термодинамики недостаточно. Выражая общий закон сохранения и превращения энергии, первое
- 25. Отношение работы А, совершенной тепловой машиной, к количеству теплоты Q1, полученному от нагревателя, называется термодинамическим коэффициентом
- 26. Энтропия – понятие, введённое в термодинамике для определения меры необратимого рассеяния энергии. В статистической физике энтропия
- 27. (27) (28) (29) (30)
- 28. Первое и второе начала термодинамики в объединенной форме имеют вид: (31)
- 29. Количественная связь между энтропией S и термодинамической вероятностью W выражается формулой Больцмана: S = k ln
- 30. Заключение Термодинамика может быть применена в широком круге вопросов в области науки и техники, таких, как
- 31. Материалы сайта http://ru.wikipedia.org/ Материалы сайта http://gannalv.narod.ru/img/ Материалы сайта http://схемо.рф/shemy/fizika/orlov-v-a-fizika-shkolnaja-programa- v-tablicah-i-formulah-1998-g/4890.html Материалы сайта http://900igr.net/prezentatsii/fizika/Energija/003-Tema-4-PERVOE- NACHALO-TERMODINAMIKI.html Материалы сайта
- 33. Скачать презентацию

























 Линейные антенные решетки
Линейные антенные решетки Энергия электрического поля. Тема 6
Энергия электрического поля. Тема 6 Элементы гемодинамики
Элементы гемодинамики Метрология. Допуски и посадки шпоночных и шлицевых соединений
Метрология. Допуски и посадки шпоночных и шлицевых соединений Динамика механической системы
Динамика механической системы тепловые явления в юрте
тепловые явления в юрте Силовий трансформатор ЧС-4
Силовий трансформатор ЧС-4 Особливості будови систем та механізмів автомобіля ГАЗ-66
Особливості будови систем та механізмів автомобіля ГАЗ-66 Введение. Общие сведения о машинах и механизмах
Введение. Общие сведения о машинах и механизмах Зубчатые передачи
Зубчатые передачи Теоретическая механика. Статика абсолютно твердого тела
Теоретическая механика. Статика абсолютно твердого тела Diesel and petrol power
Diesel and petrol power Буксирное устройство судна и его техническая эксплуатация
Буксирное устройство судна и его техническая эксплуатация Пневмотранспорт, виды и применение. Достоинства и недостатки. Тема 14
Пневмотранспорт, виды и применение. Достоинства и недостатки. Тема 14 Методическая разработка для урока по теме Поперечность световых волн.
Методическая разработка для урока по теме Поперечность световых волн. Разборка и сборка тормозных колодок автобуса ЛИАЗ-5256
Разборка и сборка тормозных колодок автобуса ЛИАЗ-5256 Блок - разновидность простого механизма
Блок - разновидность простого механизма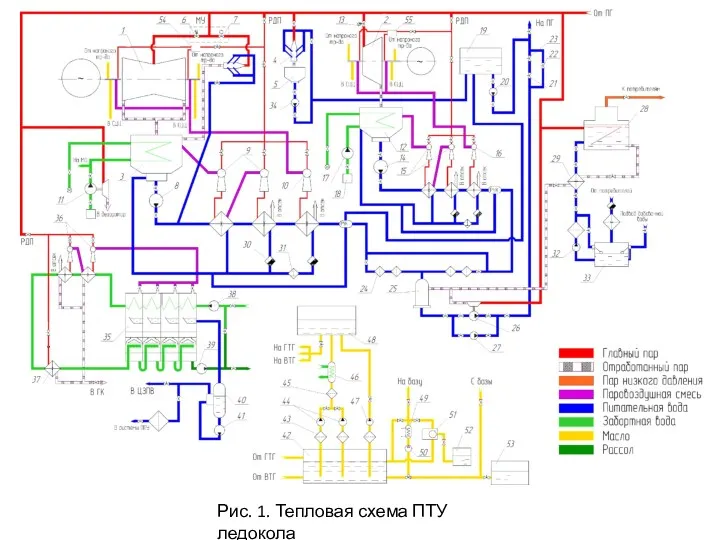 Системы ПТУ 2
Системы ПТУ 2 Гидродинамика. Поток жидкости и его основные понятия
Гидродинамика. Поток жидкости и его основные понятия Электрические цепи при гармоническом воздействии в установившемся режиме
Электрические цепи при гармоническом воздействии в установившемся режиме Уравнение Менделеева - Клапейрона
Уравнение Менделеева - Клапейрона Урок по физике в 7классе на тему Плотность вещества. Решение задач
Урок по физике в 7классе на тему Плотность вещества. Решение задач Tiristor GTO
Tiristor GTO Электротехника. Резонанс в электрических цепях. (Лекция 9)
Электротехника. Резонанс в электрических цепях. (Лекция 9) Измерение параметров инфракрасного и терагерцового излучения ч.2 Схемы измерения параметров
Измерение параметров инфракрасного и терагерцового излучения ч.2 Схемы измерения параметров Спектры. Виды спектров
Спектры. Виды спектров Инструментальные методы анализа
Инструментальные методы анализа Реализация проблемного метода обучения на уроках физики с помощью интерактивных компьютерных моделей
Реализация проблемного метода обучения на уроках физики с помощью интерактивных компьютерных моделей