Содержание
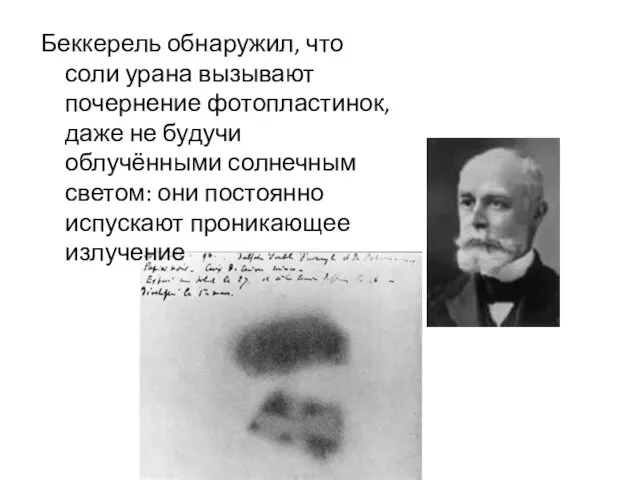
- 2. Беккерель обнаружил, что соли урана вызывают почернение фотопластинок, даже не будучи облучёнными солнечным светом: они постоянно
- 3. Историю возникновения самых общих представлений об атоме обычно ведут со времен греческого философа Демокрита (ок. 460
- 4. В 1897-1898 гг. французские учёные Пьер Кюри и Мария Склодовская –Кюри установили, что испускание уранового излучения
- 5. Строение атома Джозеф Джон Томсон в 1903 г. Предложил модель атома, согласно которой атомы представляют собой
- 6. Строение атома Резерфорд Внутри атома находится ядро, состоящее из протонов и нейтронов - нуклонов
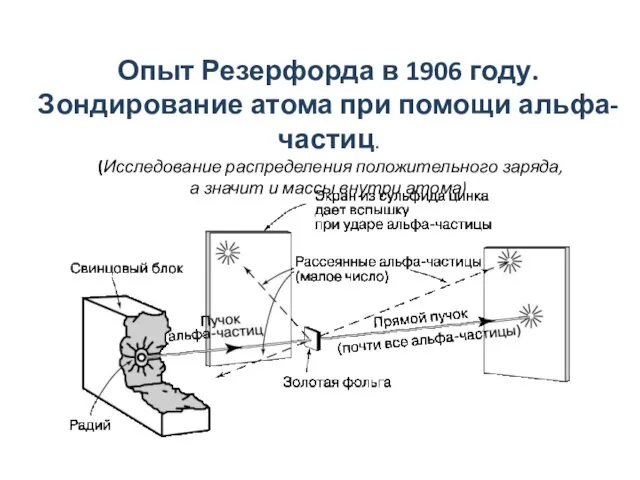
- 7. Опыт Резерфорда в 1906 году. Зондирование атома при помощи альфа-частиц. (Исследование распределения положительного заряда, а значит
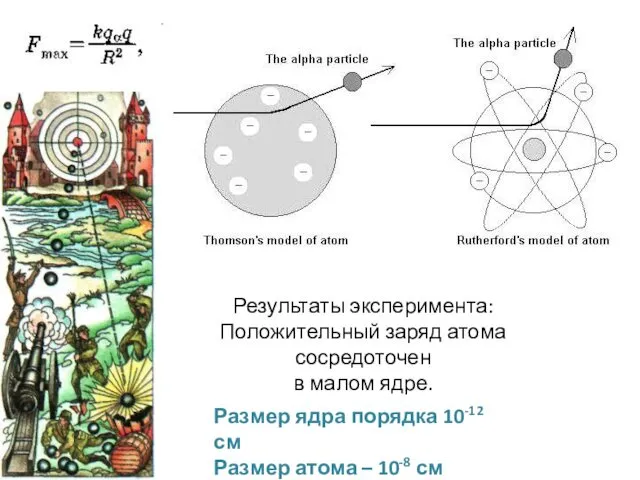
- 8. Результаты эксперимента: Положительный заряд атома сосредоточен в малом ядре. Размер ядра порядка 10-12 см Размер атома
- 9. Резерфорд предложил планетарную модель атома 1. атомы состоят из положительно заряженной части – ядра 2. В
- 10. Число протонов – зарядовое число Z Число нейтронов – N Число нуклонов A=Z+N – массовое число
- 11. Атом потерявший или приобретший один или несколько электронов уже не будет нейтральным и превратится в положительный
- 12. Атомы очень малы – их размеры порядка 10–10–10–9 м, а размеры ядра еще примерно в 100
- 13. http://www.youtube.com/watch?v=P7ojSW5pODk http://www.youtube.com/watch?v=OKnpPCQyUec
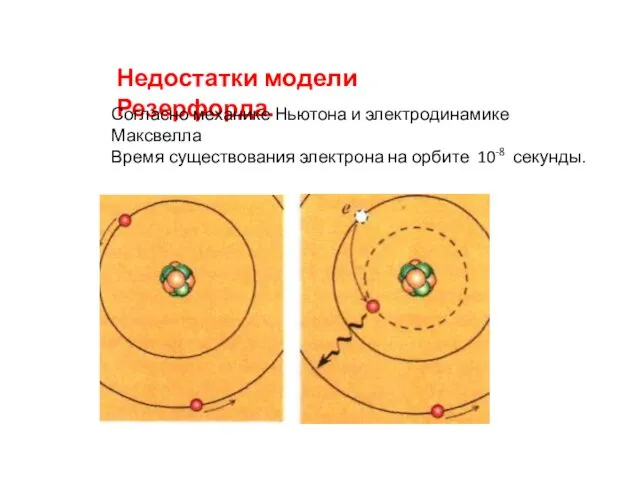
- 14. Недостатки модели Резерфорда. Согласно механике Ньютона и электродинамике Максвелла Время существования электрона на орбите 10-8 секунды.
- 15. Теория Бора Согласно классической механике, движущиеся с ускорением вокруг ядра электроны должны излучать электромагнитные волны и
- 16. Атомы движутся только по определенным стационарным орбитам При переходе с одной стационарной орбиты на другую атом
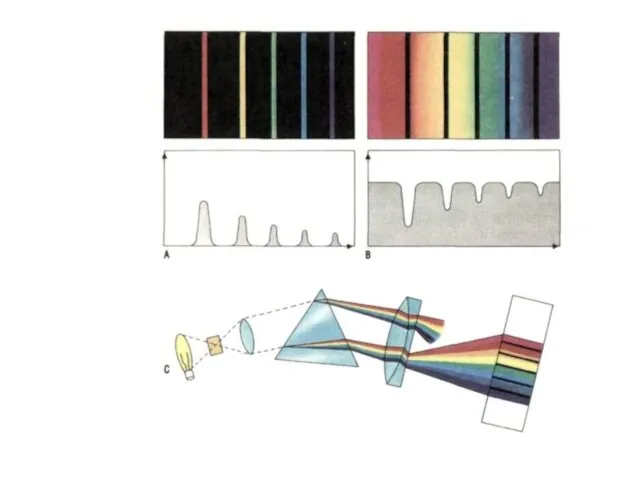
- 17. Спектры излучения и поглощения Каждому цвету соответствует электромагнитное излучение определенной частоты
- 18. Спектры бывают Сплошные – излучают раскаленные твердые и жидкие тела
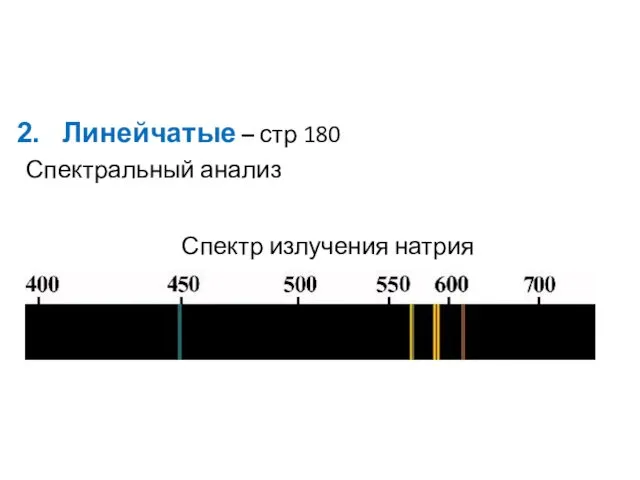
- 19. Спектр излучения натрия Линейчатые – стр 180 Спектральный анализ
- 20. 3. Полосатый- Состоит из отдельных цветных полос, разделенных темными промежутками. Эти полосы представляют собой совокупность большого
- 21. Спектры поглощения Стр 182 Йозеф Фраунгофер
- 23. Атомы любого химического элемента дают спектр, непохожий на спектры всех других элементов: они способны излучать и
- 24. Медики давно обратили внимание на то, что многие болезни связаны с недостаточностью поступления и содержания в
- 25. С учебником 1. С помощью каких приборов наблюдают спектры? 2. Почему спектры представляют собой линии, а
- 26. На основании каких опытов возникло предположение о сложном строении атома? Какие модели строения атома существовали 100
- 27. Атомное ядро. Радиоактивность 1. атомы состоят из положительно заряженной части – ядра 2. В состав ядра
- 28. Число протонов – зарядовое число Z Число нейтронов – N Число нуклонов A=Z+N – массовое число
- 29. Масса протона почти равна массе нейтрона Масса электрона Заряд протона равен заряду электрона
- 30. В 1897-1898 гг. французские учёные Пьер Кюри и Мария Склодовская –Кюри установили, что испускание уранового излучения
- 31. В 1899 г. английский физик Эрнест Резерфорд обнаружил неоднородность уранового излучения: в магнитном поле лучи разделяются
- 32. α-лучи представляют собой поток ядер гелия 2Не4 α-лучи обладают малой проникающей способностью. Даже лист бумаги толщиной
- 33. β-лучи – отрицательно заряженные частицы -1е0 Проникают сквозь алюминиевую фольгу толщиной несколько мм. Сильно отклоняются в
- 34. γ-лучи нейтральное излучение по свои свойствам схожее с рентгеновским Проникает сквозь слой свинца толщиной в 1
- 35. Атомное превращение при α- излучении NXM → N-2YM-4 + 2Не4 Где Х -начальное вещество У- вещество,
- 36. Письменно Запишите реакцию α-распада радия и объясните, что обозначает каждый символ Как называются верхние и нижние
- 37. Прочитайте параграф 18-19 и ответьте на вопросы Перечислите факты и явления подтверждающие сложное строение атома Как
- 38. Вопросы Чем отличаются друг от друга атомы разных химических элементов? Что является главной характеристикой определенного химического
- 40. Скачать презентацию






























 Основные положения молекулярно-кинетической теории
Основные положения молекулярно-кинетической теории Самоиндукция и взаимная индукция
Самоиндукция и взаимная индукция Физические и химические явления
Физические и химические явления Методическая разработка для урока по теме Поперечность световых волн.
Методическая разработка для урока по теме Поперечность световых волн. Щековые дробилки
Щековые дробилки Проекты АЭС с ВВЭР Российские реакторы 3-го поколения
Проекты АЭС с ВВЭР Российские реакторы 3-го поколения Анализ рабочих процессов и их влияние на формирование эксплуатационных свойств автомобиля
Анализ рабочих процессов и их влияние на формирование эксплуатационных свойств автомобиля Эксперимент. Принципы теории планирования эксперимента. Классификация и виды экспериментов
Эксперимент. Принципы теории планирования эксперимента. Классификация и виды экспериментов Свет. Источники света
Свет. Источники света Равновесие сил
Равновесие сил Задачи по квантовой механике
Задачи по квантовой механике Источники света,Прямолинейное распространение света
Источники света,Прямолинейное распространение света Квазикристаллы, аморфное состояние, жидкие кристаллы, жидкость
Квазикристаллы, аморфное состояние, жидкие кристаллы, жидкость Основные требования и допуски при финальной сборке. Виды и методики измерения
Основные требования и допуски при финальной сборке. Виды и методики измерения Загальна характеристика історичного розвитку фізики як науки
Загальна характеристика історичного розвитку фізики як науки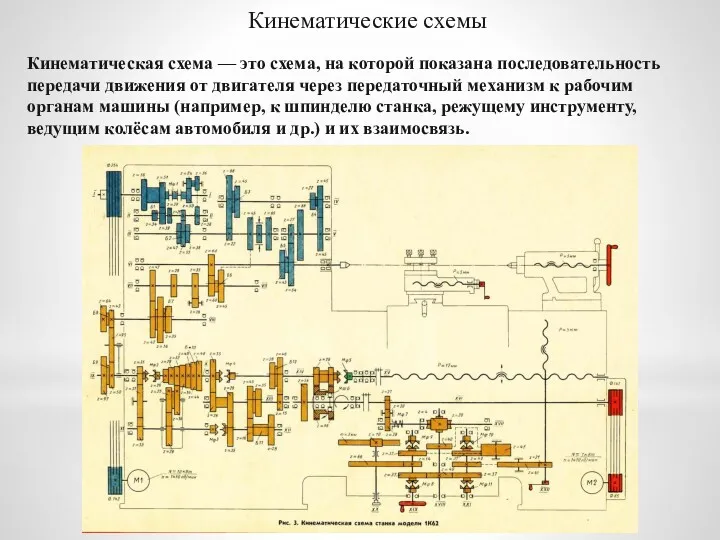 Кинематические схемы
Кинематические схемы Основные теоремы и методы анализа резистивных цепей
Основные теоремы и методы анализа резистивных цепей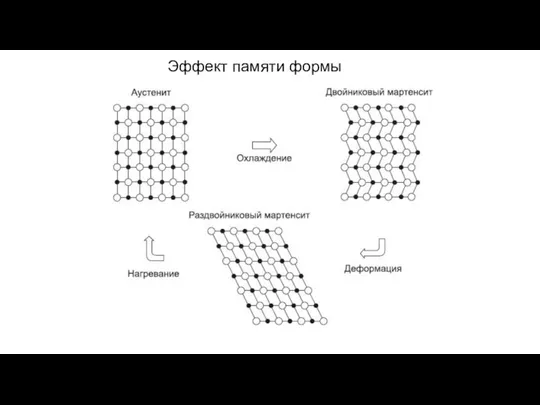 Эффект памяти формы
Эффект памяти формы Сили тертя. Коефіцієнт тертя ковзання
Сили тертя. Коефіцієнт тертя ковзання Условия плавания тел. Плавание судов
Условия плавания тел. Плавание судов Урок Атмосферное давление
Урок Атмосферное давление Определение скоростей и ускорений для различных видов движений
Определение скоростей и ускорений для различных видов движений интегрированный урок физика+математика
интегрированный урок физика+математика Филворд Тела для 7 класса по физике
Филворд Тела для 7 класса по физике Магнитное поле постоянного электрического тока
Магнитное поле постоянного электрического тока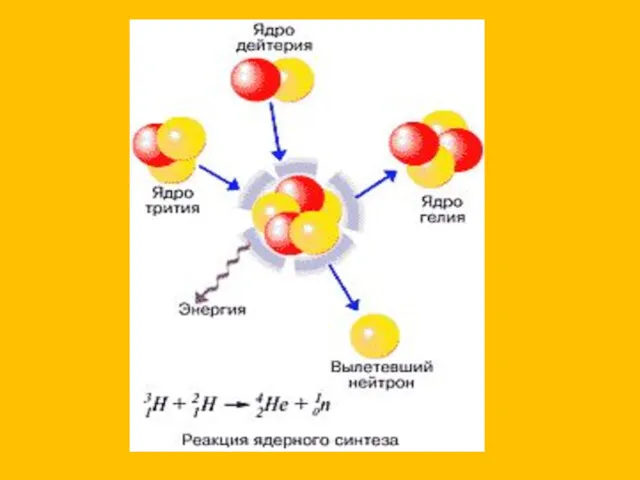 Термоядролық реакция
Термоядролық реакция Измерение мощности в трехфазной цепи
Измерение мощности в трехфазной цепи Закон сохранения энергии
Закон сохранения энергии