Содержание
- 2. ПОВТОРЕНИЕ 1. Назвать основные положения МКТ 2. Что называется диффузией и от чего она зависит? 3.
- 3. ТЕПЛОВОЕ РАВНОВЕСИЕ Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором
- 4. При тепловом равновесии в системе не меняются объем и давление, не изменяются агрегатные состояния вещества, концентрации
- 5. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ Для измерения температуры служат специальные приборы - термометры. Их действие основано на том факте,
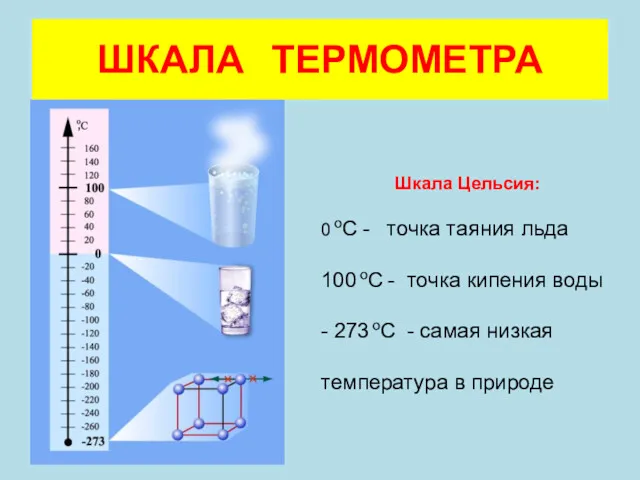
- 6. ШКАЛА ТЕРМОМЕТРА Шкала Цельсия: 0 оС - точка таяния льда 100 оС - точка кипения воды
- 7. Шведский ученый Андерс Цельсий Шведский естествоиспытатель Карл Линней создатели шкалы "Цельсия"
- 8. ГАЗОВЫЙ ТЕРМОМЕТР Особое место в физике занимают газовые термометры, в которых термометрическим веществом является разреженный газ
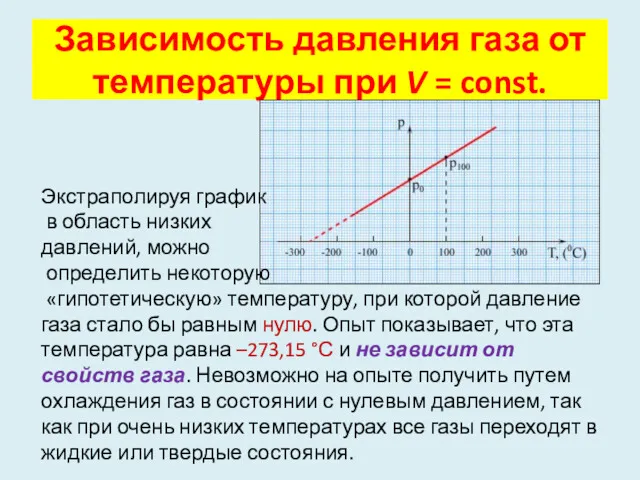
- 9. Зависимость давления газа от температуры при V = const. Экстраполируя график в область низких давлений, можно
- 10. ШКАЛА КЕЛЬВИНА Английский физик У. Кельвин в 1848 г. предложил использовать точку нулевого давления газа для
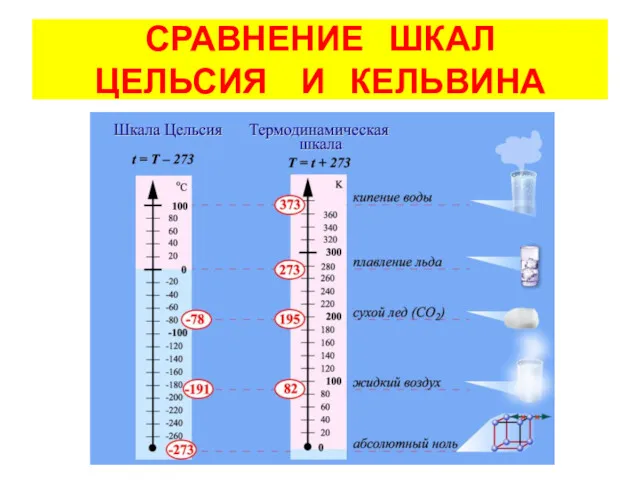
- 11. СРАВНЕНИЕ ШКАЛ ЦЕЛЬСИЯ И КЕЛЬВИНА
- 12. АБСОЛЮТНЫЙ НОЛЬ ТЕМПЕРАТУРЫ – предельная температура, при которой давление идеального газа обращается в ноль при данном
- 13. ТЕМПЕРАТУРА – МЕРА КИНЕТИЧЕСКОЙ ЭНЕРГИИ МОЛЕКУЛ Средняя кинетическая энергия движения молекул пропорциональна абсолютной температуре средняя кинетическая
- 14. р = nkT k = 1,38·10 Дж/К - постоянная Больцмана Следствия: 1. при одинаковых давлениях и
- 15. ЗАДАЧИ 1. Какова энергия теплового движения молекулы кислорода при температурах 60ºС и молекулы азота при –
- 16. Дано: Решение t1 = 60ºC Т1 = 60 + 273 = 333К t2 = - 60ºC
- 18. Скачать презентацию












 Высота, тембр и громкость звука
Высота, тембр и громкость звука Паразитные эффекты в ИС при воздействии ИИ. Физика и особенности проявления тиристорных эффектов в КМОП ИС
Паразитные эффекты в ИС при воздействии ИИ. Физика и особенности проявления тиристорных эффектов в КМОП ИС Физические основы термодинамики
Физические основы термодинамики Волновые свойства света
Волновые свойства света Деление ядер урана. Цепная реакция
Деление ядер урана. Цепная реакция Лекція №5. Закон збереження імпульсу
Лекція №5. Закон збереження імпульсу Основы атомно-эмиссионного спектрального анализа. Происхождение атомных спектров
Основы атомно-эмиссионного спектрального анализа. Происхождение атомных спектров Организация технического обслуживания и ремонта электрического и электромеханического оборудования
Организация технического обслуживания и ремонта электрического и электромеханического оборудования Способы преобразования энергии в полезную работу
Способы преобразования энергии в полезную работу Подготовка к контрольной работе по теме Механика 10 класс
Подготовка к контрольной работе по теме Механика 10 класс Самостоятельный разряд
Самостоятельный разряд Презентация к уроку физики Электромагниты
Презентация к уроку физики Электромагниты Количество теплоты. Количество теплоты при нагревании и охлаждении
Количество теплоты. Количество теплоты при нагревании и охлаждении Analysis of biological liquids by metal enhanced fluorescence from gold nanoparticles
Analysis of biological liquids by metal enhanced fluorescence from gold nanoparticles Радио. Принцип работы
Радио. Принцип работы тест по состояниям вещества 8 класс
тест по состояниям вещества 8 класс Проект паливної дільниці в міської СТО легкових автомобілів
Проект паливної дільниці в міської СТО легкових автомобілів урок физики в 7 классе
урок физики в 7 классе Химические реакторы. Гетерогенно-каталитические химические процессы. Лекция №11
Химические реакторы. Гетерогенно-каталитические химические процессы. Лекция №11 Измерение атмосферного давления
Измерение атмосферного давления Плавание судов
Плавание судов Нанокомпозиты
Нанокомпозиты Качество САУ. Точность работы САУ в установившихся режимах
Качество САУ. Точность работы САУ в установившихся режимах Спектрофотометрия и спектрофлуориметрия
Спектрофотометрия и спектрофлуориметрия Современные представления о структурных уровнях и формах окружающего мира
Современные представления о структурных уровнях и формах окружающего мира Коливальний рух у природі і техніці
Коливальний рух у природі і техніці Thermodynamics
Thermodynamics Подъемно-поворотные сварочные колонны
Подъемно-поворотные сварочные колонны