Содержание
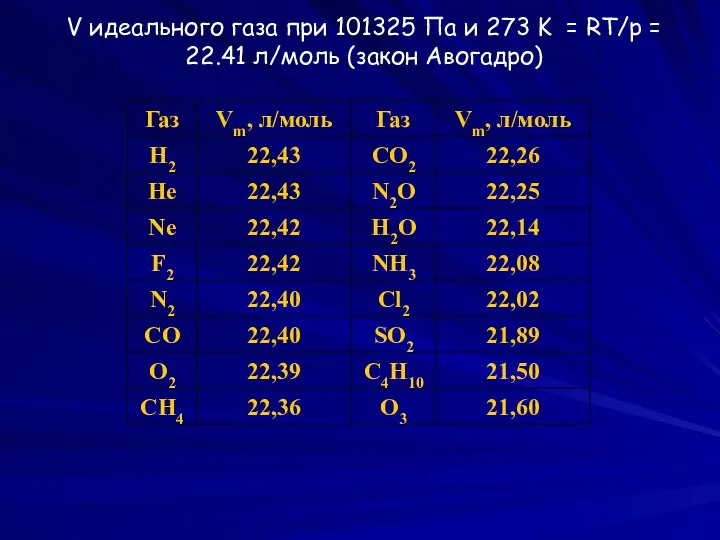
- 2. V идеального газа при 101325 Па и 273 K = RT/p = 22.41 л/моль (закон Авогадро)
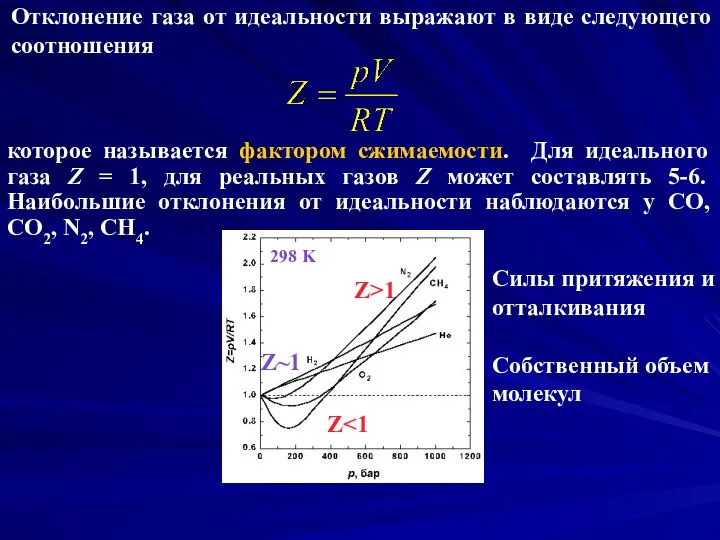
- 3. которое называется фактором сжимаемости. Для идеального газа Z = 1, для реальных газов Z может составлять
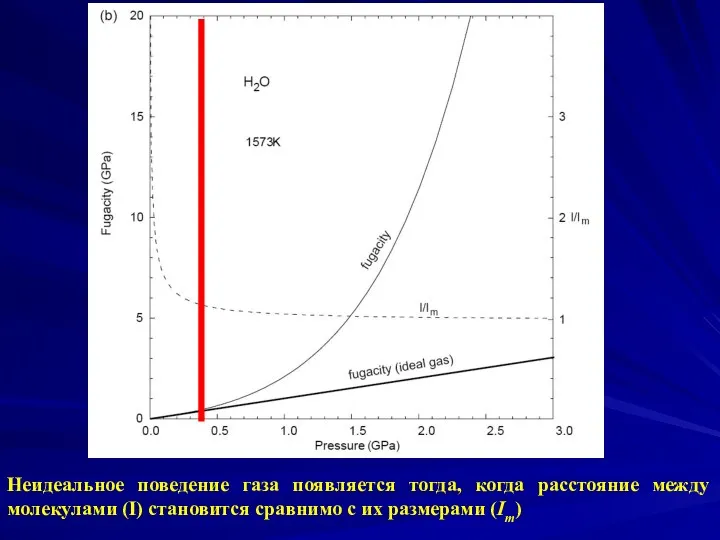
- 4. Неидеальное поведение газа появляется тогда, когда расстояние между молекулами (I) становится сравнимо с их размерами (Im)
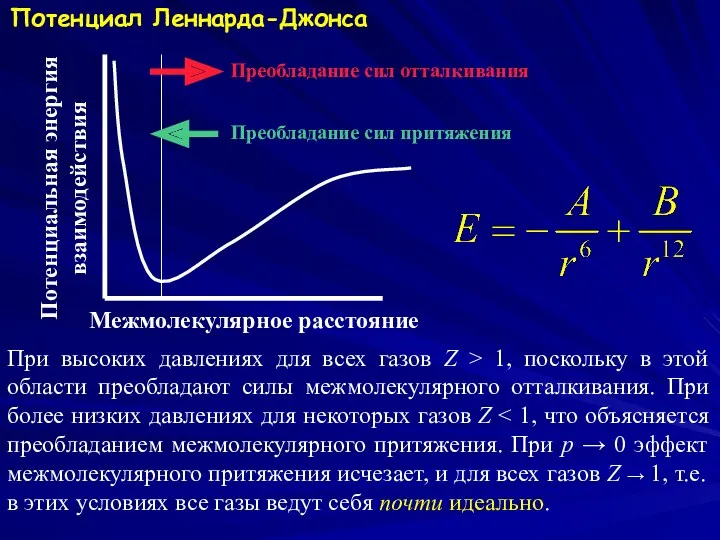
- 5. Потенциал Леннарда-Джонса Межмолекулярное расстояние Потенциальная энергия взаимодействия Преобладание сил отталкивания Преобладание сил притяжения При высоких давлениях
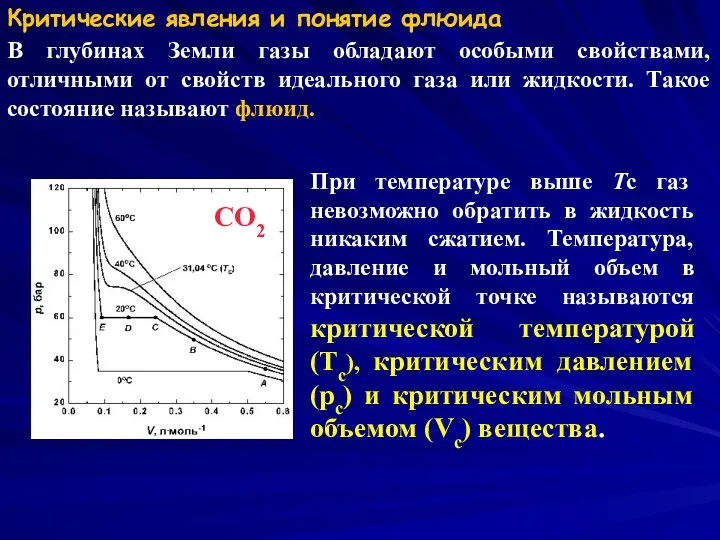
- 6. Критические явления и понятие флюида В глубинах Земли газы обладают особыми свойствами, отличными от свойств идеального
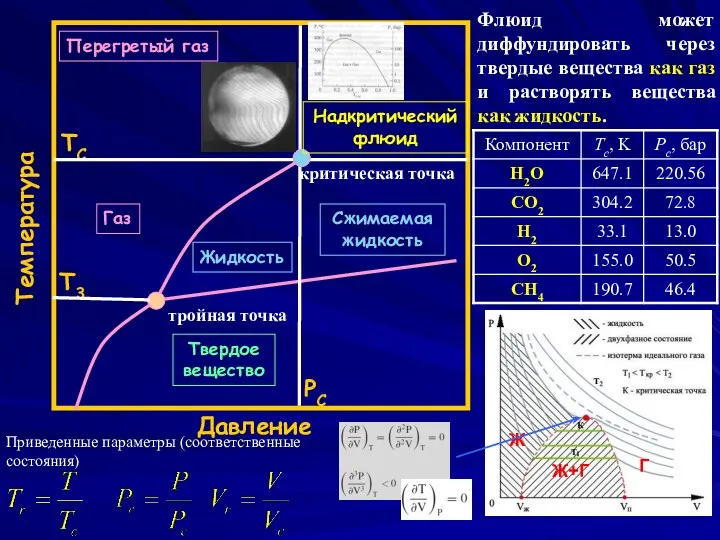
- 7. Давление Температура PC TC T3 Перегретый газ Надкритический флюид Газ Жидкость Сжимаемая жидкость Твердое вещество тройная
- 8. Для расчета молярной свободной энергии Гиббса (или химического потенциала) чистой фазы i при давлении P отличном
- 9. Обычно эти данные включают фугитивность (fi) или коэффициент фугитивности (Γi). Фугитивность представляет собой эффективное давление, которое
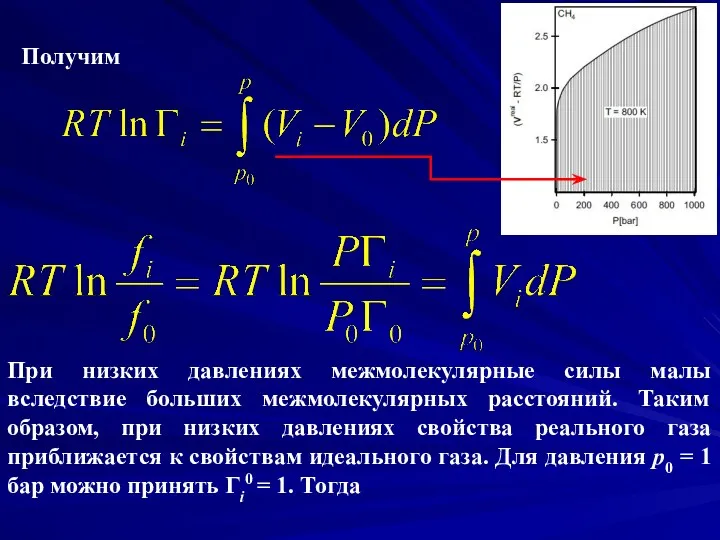
- 10. Получим При низких давлениях межмолекулярные силы малы вследствие больших межмолекулярных расстояний. Таким образом, при низких давлениях
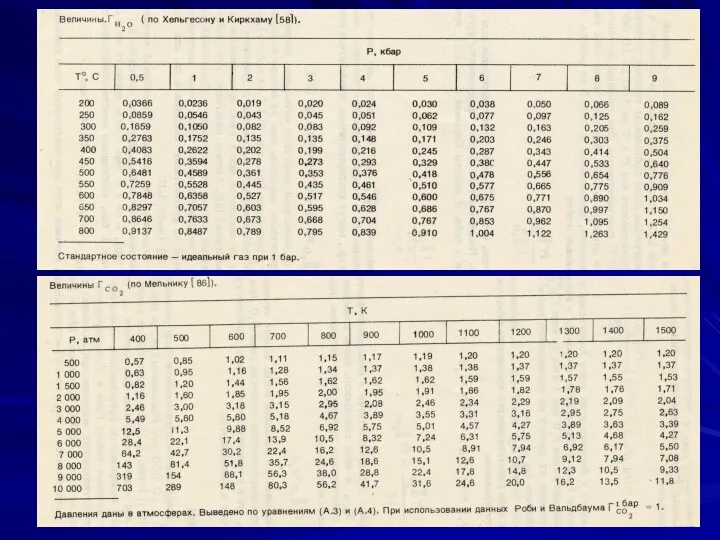
- 11. Таким образом, уравнение для свободной энергии Гиббса для реального газа i можно переписать следующим образом Значения
- 13. Уравнение состояния вещества (УС) – это аналитическая формулировка соотношений между объемом, температурой и давлением. Уравнения состояния
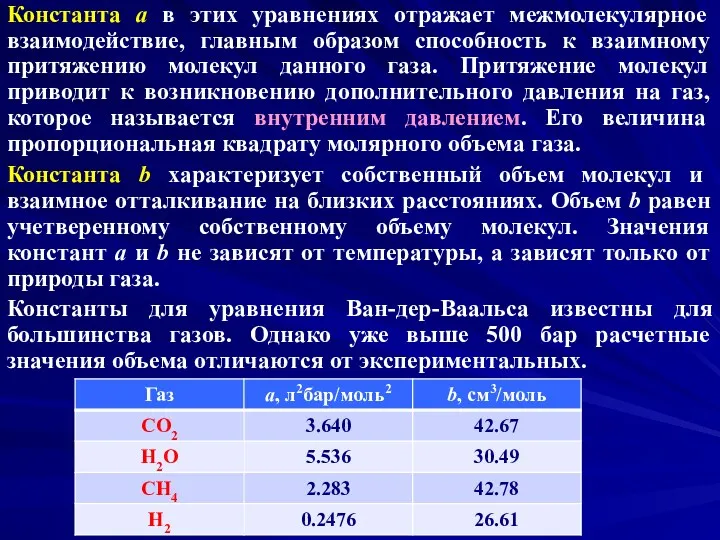
- 14. Константа a в этих уравнениях отражает межмолекулярное взаимодействие, главным образом способность к взаимному притяжению молекул данного
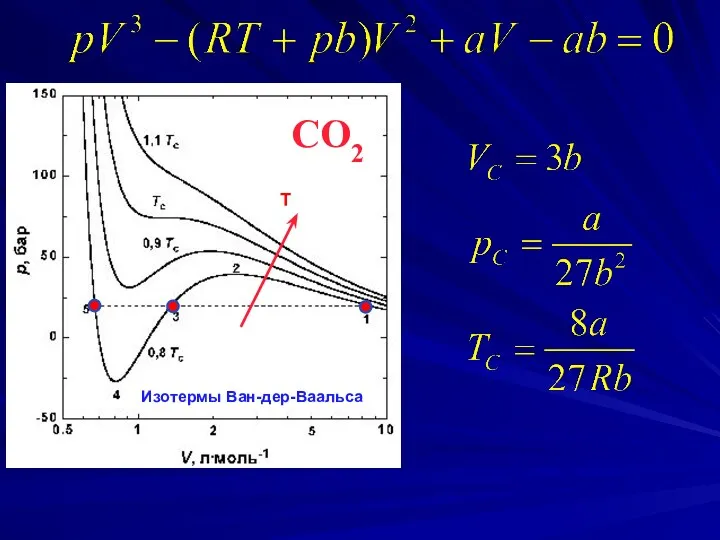
- 15. CO2 Изотермы Ван-дер-Ваальса T
- 16. Принципиальное значение уравнения Ван-дер-Ваальса определяется следующими обстоятельствами: 1) уравнение было получено из модельных представлений о свойствах
- 17. Вириальные уравнения где ρ - плотность, B, C, D – вириальные коэффициенты, зависящие от температуры и
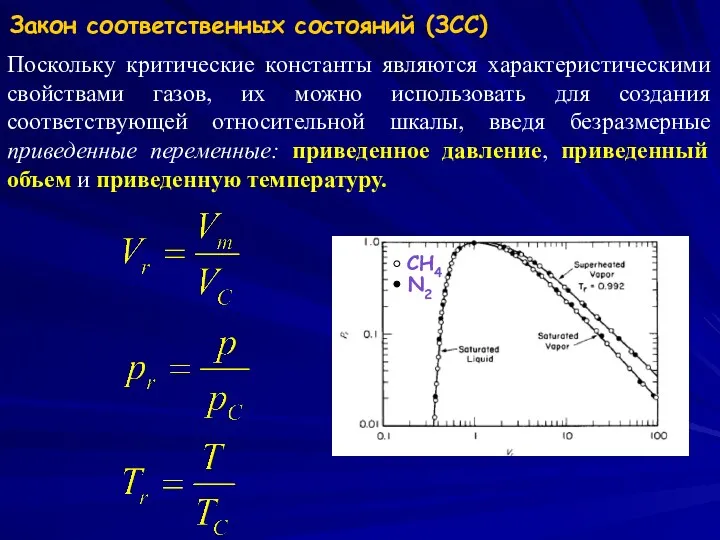
- 18. Закон соответственных состояний (ЗСС) Поскольку критические константы являются характеристическими свойствами газов, их можно использовать для создания
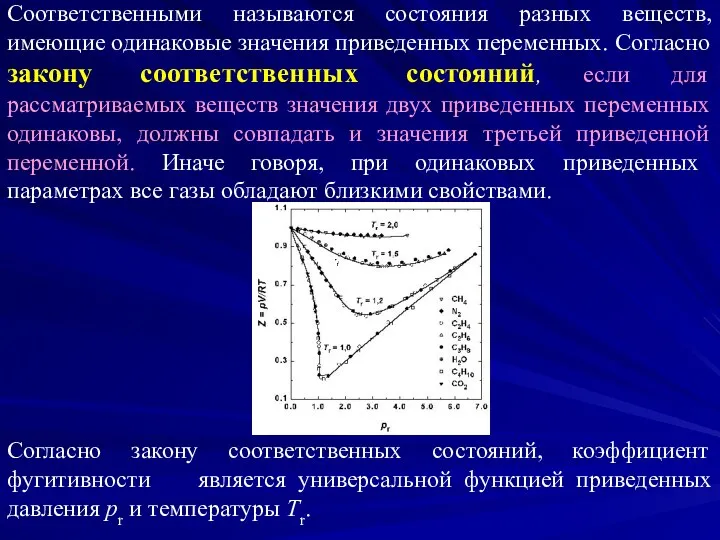
- 19. Соответственными называются состояния разных веществ, имеющие одинаковые значения приведенных переменных. Согласно закону соответственных состояний, если для
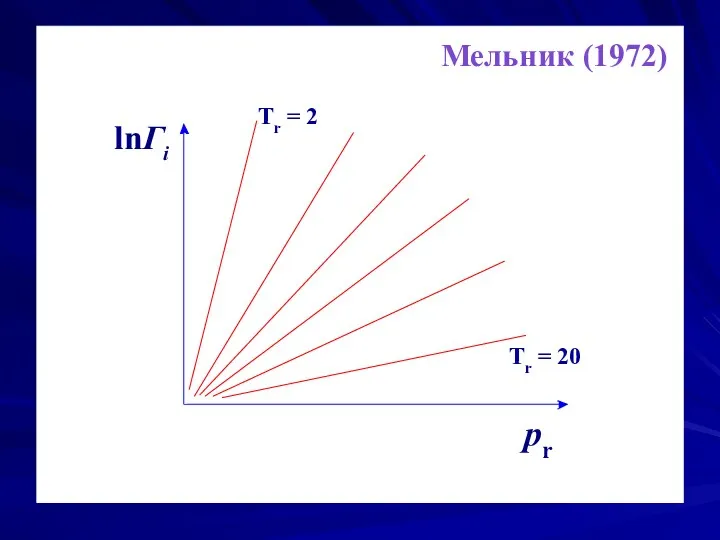
- 20. lnΓi τ=const pr Мельник (1972) Tr = 2 Tr = 20
- 21. О точности закона можно судить по значению критического коэффициента Если бы закон соответственных состояний выполнялся абсолютно
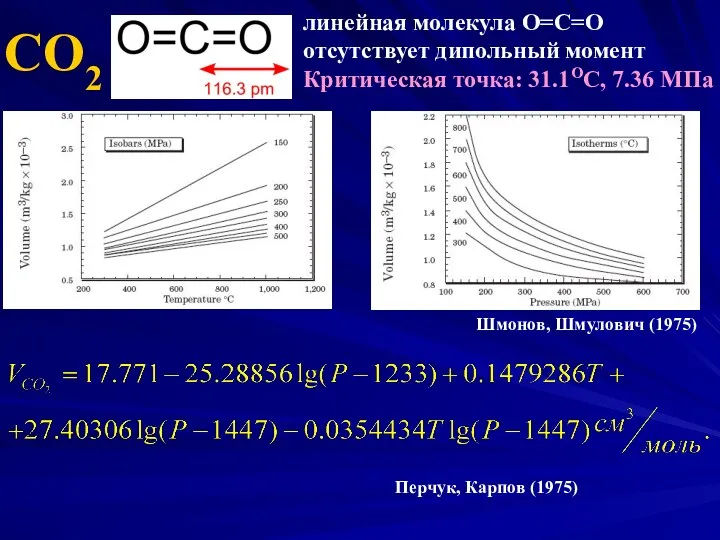
- 22. СО2 линейная молекула O=C=O отсутствует дипольный момент Критическая точка: 31.1ОС, 7.36 МПа Шмонов, Шмулович (1975) Перчук,
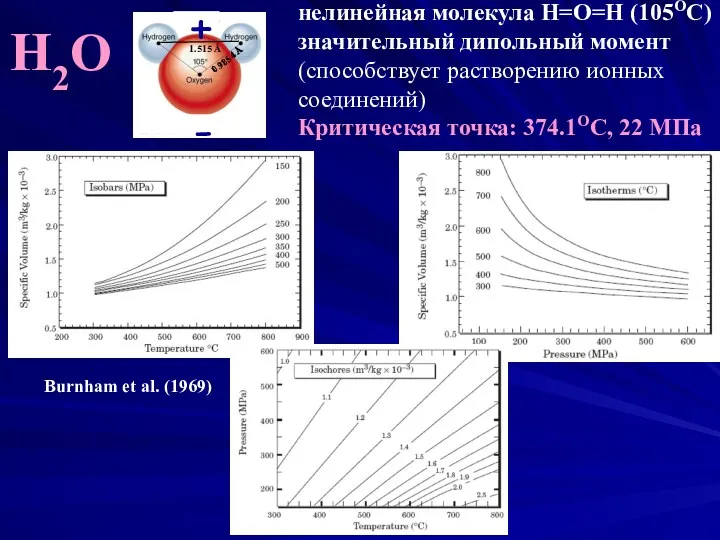
- 23. H2О нелинейная молекула H=O=H (105OC) значительный дипольный момент (способствует растворению ионных соединений) Критическая точка: 374.1ОС, 22
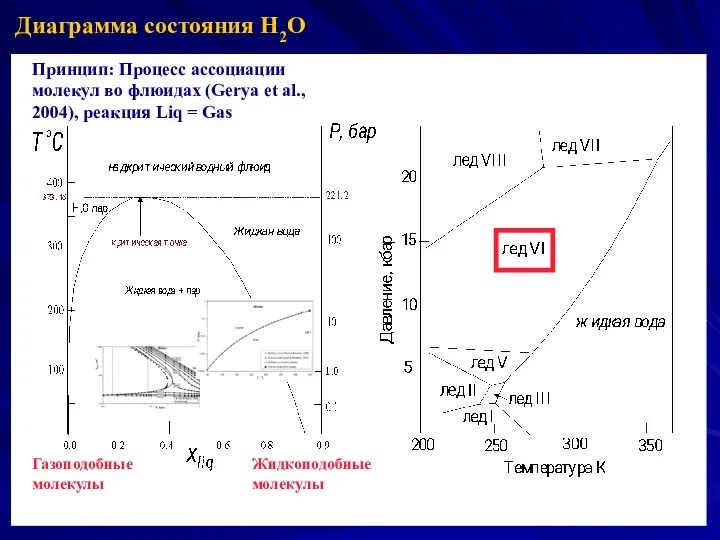
- 24. Диаграмма состояния H2O Принцип: Процесс ассоциации молекул во флюидах (Gerya et al., 2004), реакция Liq =
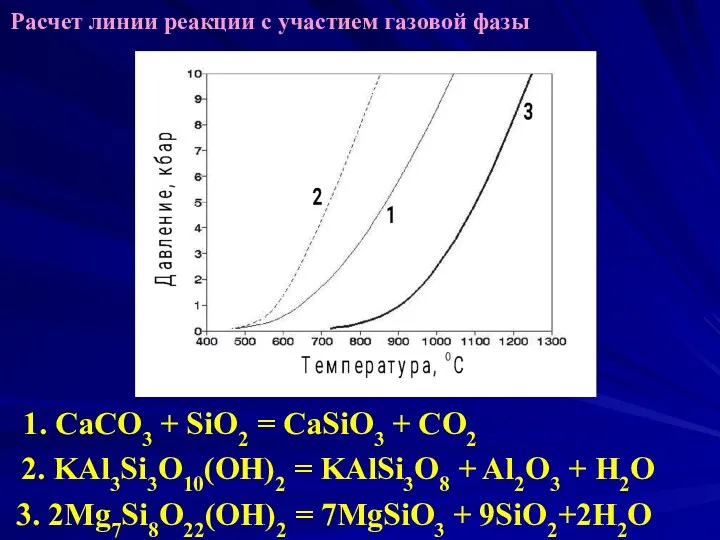
- 25. Расчет линии реакции с участием газовой фазы 1. CaCO3 + SiO2 = CaSiO3 + CO2 2.
- 26. Рассмотрим реакцию (1). Условие равновесия этой реакции запишется следующим образом: где Интеграл по объему можно разбить
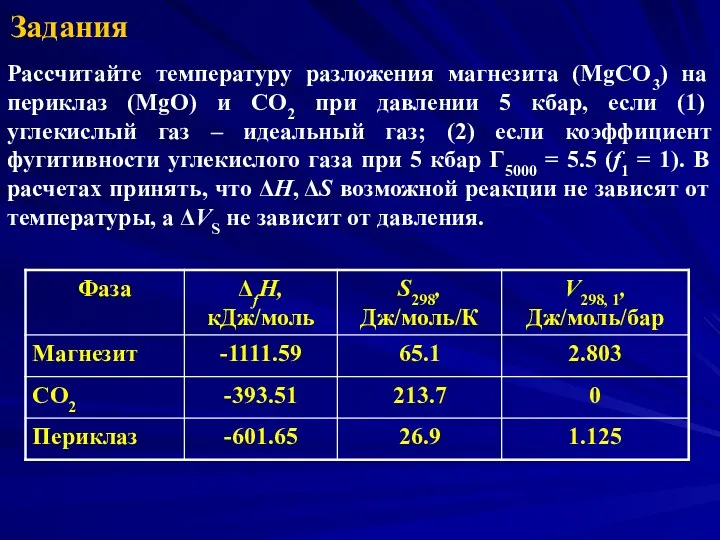
- 27. Задания Рассчитайте температуру разложения магнезита (MgCO3) на периклаз (MgO) и CO2 при давлении 5 кбар, если
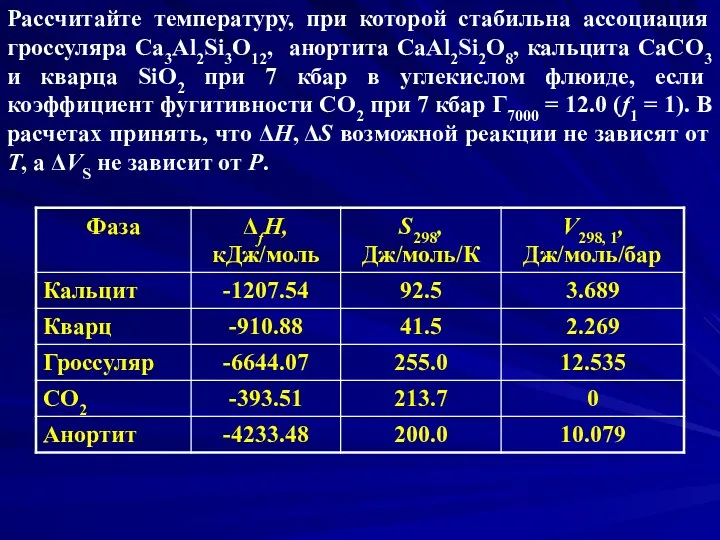
- 28. Рассчитайте температуру, при которой стабильна ассоциация гроссуляра Ca3Al2Si3O12, анортита CaAl2Si2O8, кальцита CaCO3 и кварца SiO2 при
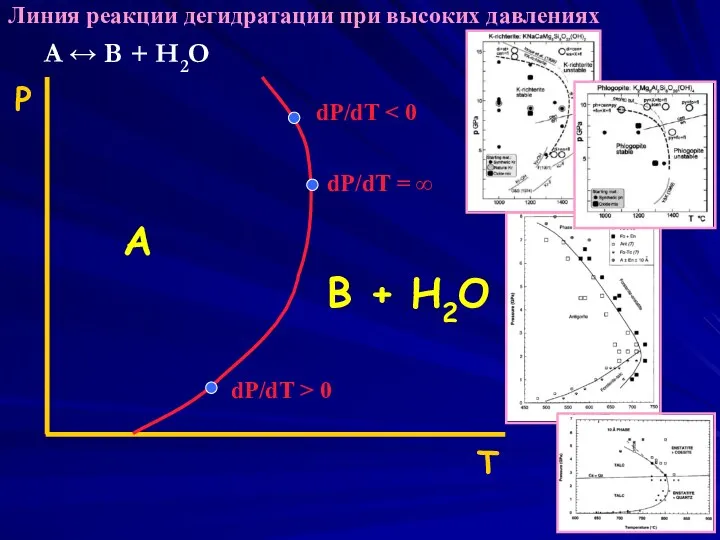
- 30. Р T A ↔ B + H2O A B + H2O dP/dT dP/dT = ∞ dP/dT
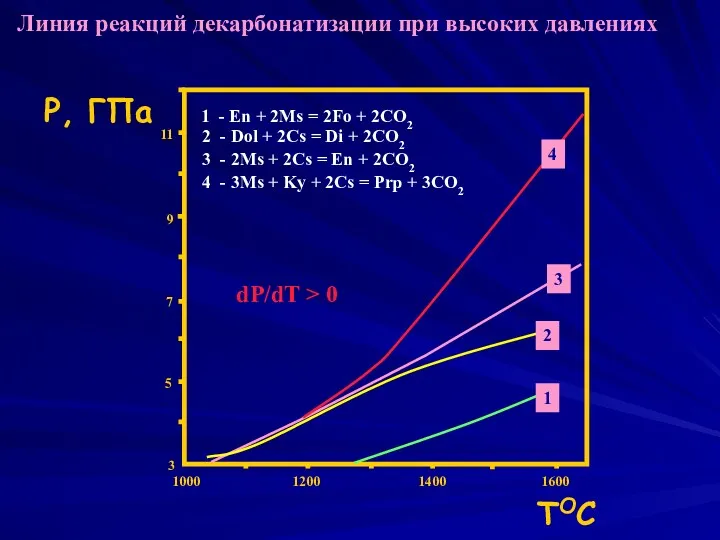
- 31. 1000 1200 1400 1600 3 5 7 9 11 Р, ГПа TОС 1 2 3 4
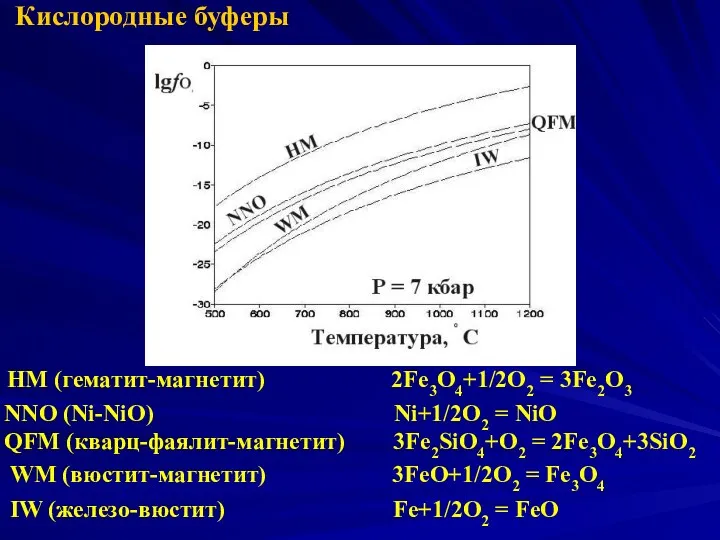
- 32. Кислородные буферы HM (гематит-магнетит) 2Fe3O4+1/2O2 = 3Fe2O3 NNO (Ni-NiO) Ni+1/2O2 = NiO QFM (кварц-фаялит-магнетит) 3Fe2SiO4+O2 =
- 33. Рассмотрим метод расчета fО2 в реакциях окисления металлов (Ме). В качестве примера произведем расчет реакции окисления
- 35. Скачать презентацию









 Механическая работа. Мощность
Механическая работа. Мощность Балка на упругом основании
Балка на упругом основании Измерение удельной теплоёмкости твердого тела
Измерение удельной теплоёмкости твердого тела Рідкі кристали та їх властивості
Рідкі кристали та їх властивості Электроприборы в быту
Электроприборы в быту Техническое обслуживание и текущий ремонт систем электроснабжения автомобиля
Техническое обслуживание и текущий ремонт систем электроснабжения автомобиля Подшипники качения
Подшипники качения Свисты-волны ОНЧ диапазона (1-30 кГц) в магнитосфере
Свисты-волны ОНЧ диапазона (1-30 кГц) в магнитосфере Общие сведения о механических передачах
Общие сведения о механических передачах Биофизика мембранных процессов. Мембранный транспорт
Биофизика мембранных процессов. Мембранный транспорт Основные понятия непотопляемости
Основные понятия непотопляемости Diodo shockley
Diodo shockley Направление тока и направление линий его магнитного поля. Сила Ампера
Направление тока и направление линий его магнитного поля. Сила Ампера Технологии на квантовых эффектах
Технологии на квантовых эффектах Физика - наука о природе
Физика - наука о природе Расчет линейных разветвленных цепей
Расчет линейных разветвленных цепей Определение эдс и внутреннего сопротивления источника тока
Определение эдс и внутреннего сопротивления источника тока Передаточна функція систем автоматики. Стуктурно-динамічні схеми систем автоматики та їх перетворення
Передаточна функція систем автоматики. Стуктурно-динамічні схеми систем автоматики та їх перетворення Диэлектриктегі физикалық процесс. Диэлектрлік шығындар және диэлектриктардың тесілуі
Диэлектриктегі физикалық процесс. Диэлектрлік шығындар және диэлектриктардың тесілуі Теории прочности
Теории прочности Цепные передачи
Цепные передачи Тонкослойная хроматография
Тонкослойная хроматография Урок Лист Успеха Работа и мощность 7 класс
Урок Лист Успеха Работа и мощность 7 класс Акустика. Затухание волн
Акустика. Затухание волн Сферические зеркала.Ход лучей в призме, плоскопараллельной пластине
Сферические зеркала.Ход лучей в призме, плоскопараллельной пластине Радиометрия и спектрометрия ионизирующих излучений. (Лекция 9)
Радиометрия и спектрометрия ионизирующих излучений. (Лекция 9) Понятия отверстие и вал
Понятия отверстие и вал Інерція та інертність. Маса та імпульс тіла. Другий закон Ньютона
Інерція та інертність. Маса та імпульс тіла. Другий закон Ньютона