Содержание
- 2. 1. ПОСТУЛАТ ПЛАНКА Энтропия идеального кристаллического тела при абсолютном нуле равна нулю: (1) Для неидеальных существуют
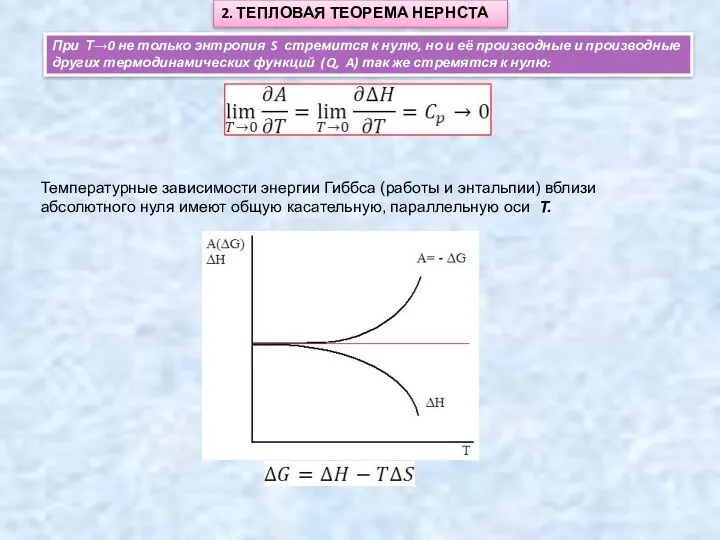
- 3. 2. ТЕПЛОВАЯ ТЕОРЕМА НЕРНСТА При Т→0 не только энтропия S стремится к нулю, но и её
- 4. 3. ПРИНЦИП НЕДОСТИЖИМОСТИ АБСОЛЮТНОГО НУЛЯ Конечным числом операций невозможно отнять всю теплоту от тела, охлаждая его
- 6. Скачать презентацию


 Электрическое поле
Электрическое поле Электронные спектры поглощения различных классов органических соединений
Электронные спектры поглощения различных классов органических соединений Трансформаторы тока и напряжения
Трансформаторы тока и напряжения Атомная физика. Строение атома
Атомная физика. Строение атома Электротехника и электроника
Электротехника и электроника Лекции 3-4 курса Ф -3 2020 — копия
Лекции 3-4 курса Ф -3 2020 — копия Активные методы обучения как эффективное средство реализации ФГОС
Активные методы обучения как эффективное средство реализации ФГОС Теорема об изменении кинетической энергии
Теорема об изменении кинетической энергии Источники света
Источники света Игра К вершинам физики
Игра К вершинам физики Общие сведения о двигателях внутреннего сгорания. Принцип работы четырехтактного дизеля. Урок № 1
Общие сведения о двигателях внутреннего сгорания. Принцип работы четырехтактного дизеля. Урок № 1 Вплив електричного поля на живі організми
Вплив електричного поля на живі організми Итоговый урок по теме Взаимодействие тел
Итоговый урок по теме Взаимодействие тел Водомер Вентури
Водомер Вентури Устройство и принцип действия холодильника
Устройство и принцип действия холодильника Частица в одномерной глубокой потенциальной яме. Прохождение частицы через потенциальный барьер. Туннельный эффект. (Лекция 5)
Частица в одномерной глубокой потенциальной яме. Прохождение частицы через потенциальный барьер. Туннельный эффект. (Лекция 5) Заттың тығыздығы
Заттың тығыздығы Сообщающиеся сосуды
Сообщающиеся сосуды Тепловые двигатели
Тепловые двигатели Двигатели внутреннего сгорания. Эксплуатация и ремонт базовых машин бронетанковой техники
Двигатели внутреннего сгорания. Эксплуатация и ремонт базовых машин бронетанковой техники Магнитное поле
Магнитное поле Электричество и магнитизм. Лабораторная работа №1
Электричество и магнитизм. Лабораторная работа №1 Современный урок физики в аспекте реализации ФГОС
Современный урок физики в аспекте реализации ФГОС Общая физика. Оптика
Общая физика. Оптика Самофокусировка света: физическая картина
Самофокусировка света: физическая картина Акустические методы контроля
Акустические методы контроля Эффект Зеебека
Эффект Зеебека Оптика. Поляризация света (лекция 25)
Оптика. Поляризация света (лекция 25)