Содержание
- 2. Тема 2. ВОДОРОДОПОДОБНЫЕ СИСТЕМЫ В КВАНТОВОЙ МЕХАНИКЕ 2.1. Квантовомеханическая картина строения атома 2.2. Квантовые числа 2.3.
- 3. Дополнение механической планетарной модели Резерфорда квантовыми постулатами Бора-Зоммерфельда -
- 4. приводит к согласию с экспериментальными данными Ангстрема, Бальмера, Зеемана и других исследователей.
- 5. И все же …. Теория Бора-Зоммерфельда использовала два принципиально различных подхода:
- 6. понятие непрерывной траектории механики Ньютона, - представление о дискретных квантовых состояниях.
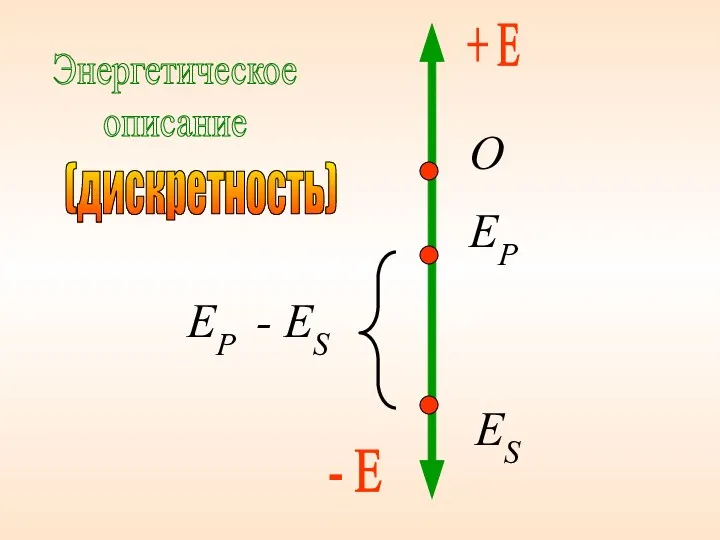
- 7. Геометрическое (пространственное) описание (l=0) (l=1) S-орбита P-орбита (непрерывность)
- 8. (дискретность)
- 9. Аналогия теории Бора - Зоммерфельда как слияния двух описаний микромира (Feline)
- 10. Дальнейшее развитие квантовой механики привело к отказу от механической картины движения электрона в поле ядра.
- 11. Планетарная модель была заменена квантово-волновым описанием строения атома.
- 12. 2.1. Квантовомеханическая картина строения атома х На прошлой лекции мы обсуждали ограниченность боровской теории строения атома.
- 13. Согласно квантовой механике, не существует определенных круговых орбит электронов, как в теории Бора. В силу волновой
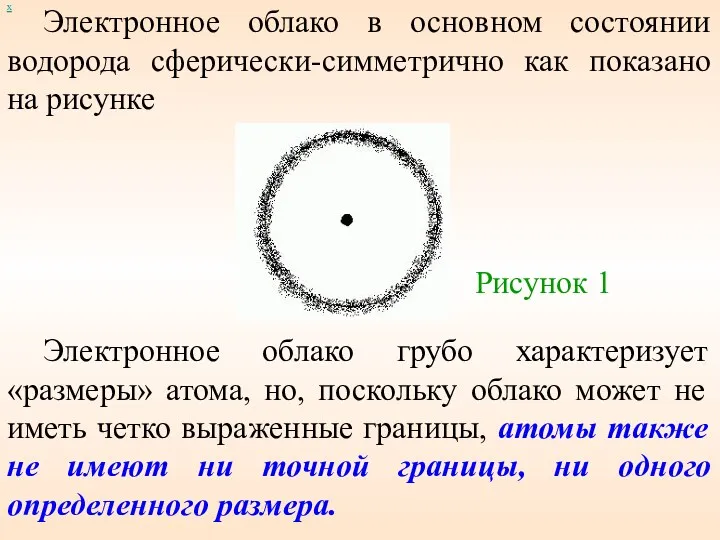
- 14. Электронное облако в основном состоянии водорода сферически-симметрично как показано на рисунке х Электронное облако грубо характеризует
- 15. х Как мы увидим в дальнейшем, не все электронные облака сферически-симметричны. Обратите внимание на то, что
- 16. х Электронное облако можно интерпретировать как с корпускулярной, так и с волновой точки зрения. Напомним, что
- 17. х Если измерить положение электрона 1000 раз, то большинство результатов измерений соответствовало бы точкам, в которых
- 18. х Мы можем лишь вычислить вероятность обнаружить электрон в различных точках. Ясно, что подобная ситуация в
- 19. Потенциальная энергия взаимодействия электрона с ядром, обладающим зарядом Ze (для атома водорода Z = 1) х
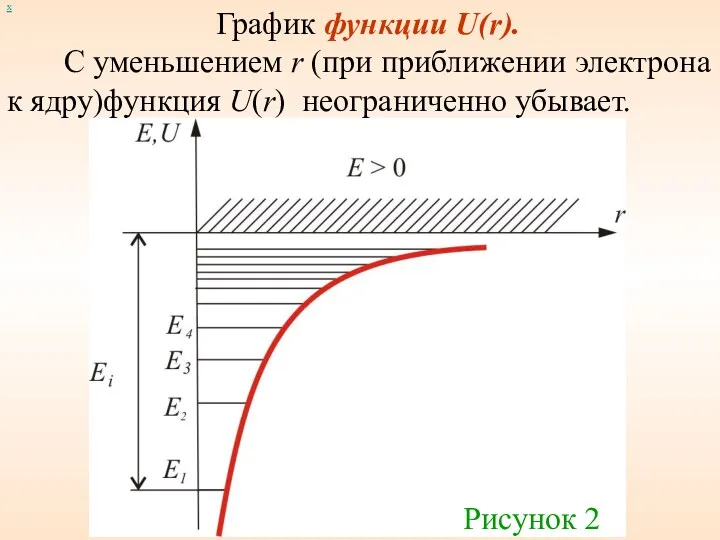
- 20. График функции U(r). С уменьшением r (при приближении электрона к ядру)функция U(r) неограниченно убывает. х Рисунок
- 21. х Шредингер Эрвин (1887 – 1961) – австрийский физик-теоретик, один из создателей квантовой механики. Основные работы
- 22. Состояние электрона в атоме водорода описывается волновой функцией Ψ, удовлетворяющей стационарному уравнению Шредингера: х E –
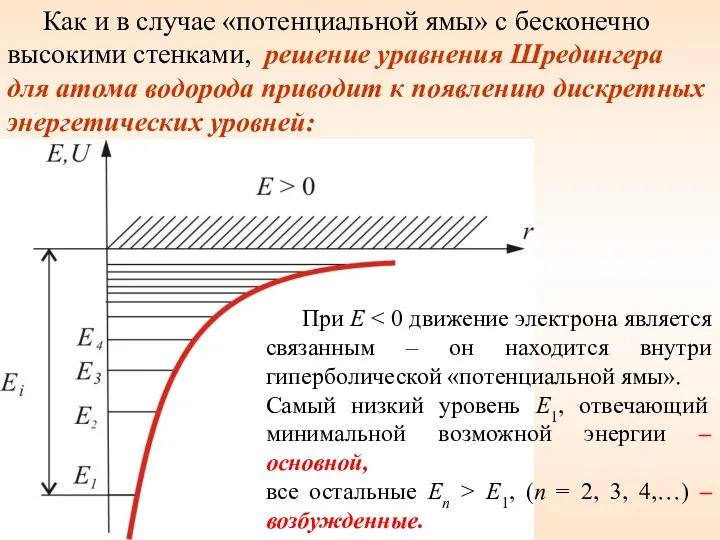
- 23. Как и в случае «потенциальной ямы» с бесконечно высокими стенками, решение уравнения Шредингера для атома водорода
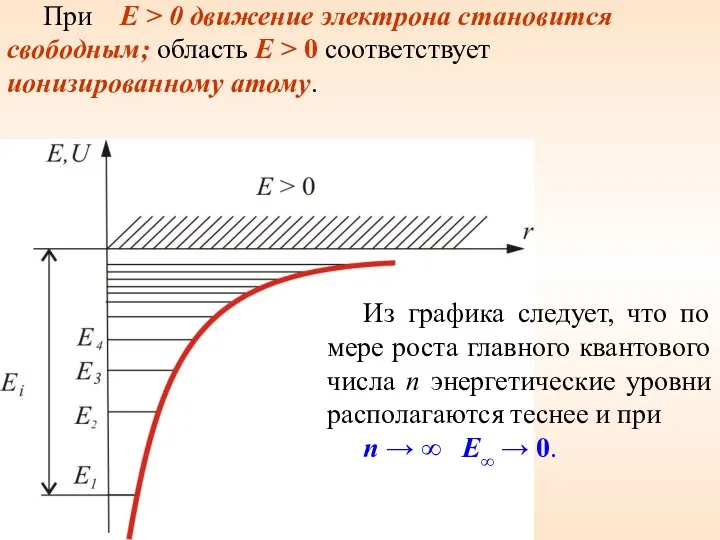
- 24. При E > 0 движение электрона становится свободным; область E > 0 соответствует ионизированному атому. Из
- 25. Итак, если Бору пришлось вводить дополнительные гипотезы (постулаты), то в квантовой механике дискретные значения энергии, являясь
- 26. В квантовой механике доказывается, что уравнению Шредингера удовлетворяют собственные функции , определяемые тремя квантовыми числами: главным
- 27. Главное квантовое число n характеризует расстояние электрона от ядра – радиус орбиты. х В атомной физике
- 28. Состояния, соответствующие орбитальному числу l = 0, 1, 2, 3,…, также обозначаются буквами s, p, d,
- 29. Эллиптические орбиты А. Зоммерфельда 1915 г.
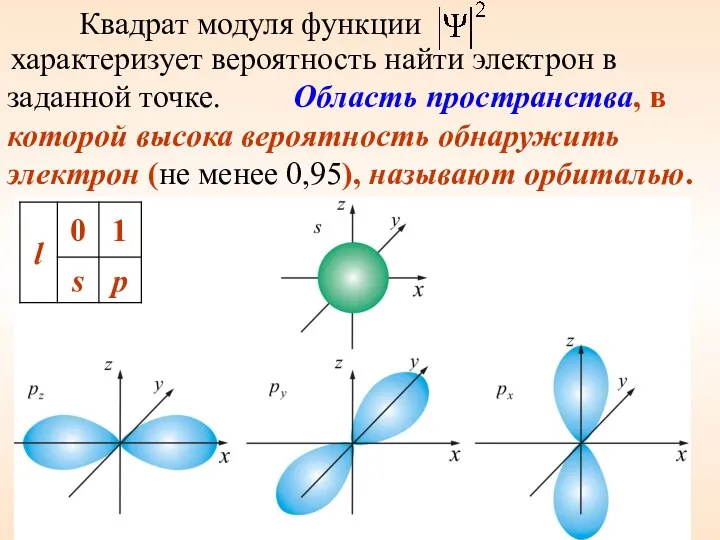
- 30. Квадрат модуля функции характеризует вероятность найти электрон в заданной точке. Область пространства, в которой высока вероятность
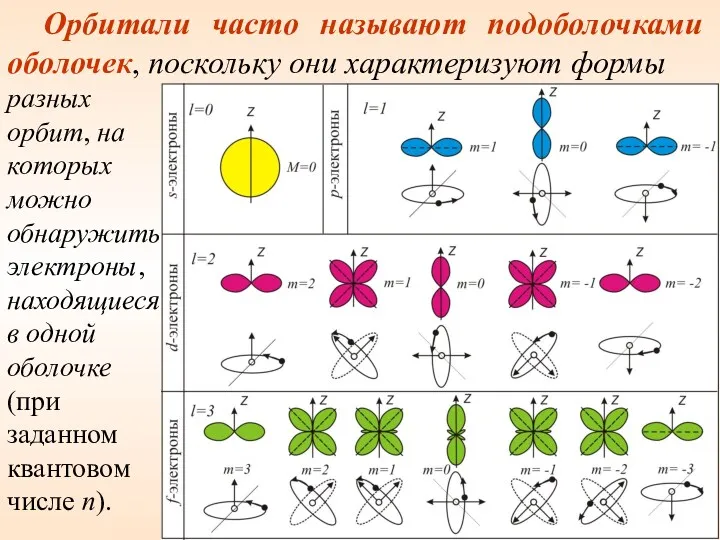
- 31. Орбитали часто называют подоболочками оболочек, поскольку они характеризуют формы разных орбит, на которых можно обнаружить электроны,
- 32. х Решая последовательно задачу об электроне в прямоугольной потенциальной яме мы доказали только то, что энергия
- 33. Рассмотрим (без вывода) движение электрона в потенциальном поле Стационарное уравнение Шредингера х (1) Так как электрическое
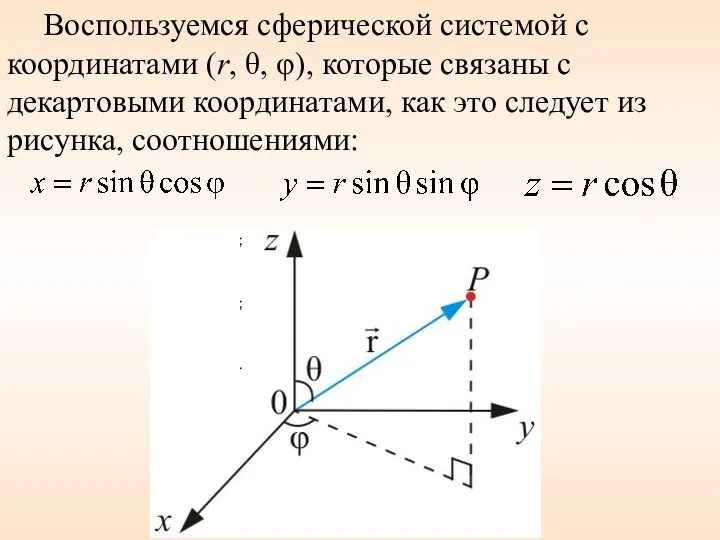
- 34. Воспользуемся сферической системой с координатами (r, θ, φ), которые связаны с декартовыми координатами, как это следует
- 35. Подставим в (1) выражение оператора Лапласа в сферических координатах, получим уравнение Шредингера в виде: х (2)
- 36. В квантовой механике широко используется понятие – оператор. Под оператором понимают правило, посредством которого одной функции
- 37. х С помощью оператора стационарное уравнение Шредингера можно записать в виде (4) Здесь – оператор энергии.
- 38. х Для момента импульса в квантовой механике вводятся четыре оператора: оператор квадрата момента импульса и три
- 39. х Решение этого уравнения является очень трудным Ограничимся только конечным результатом: Собственное значение орбитального момента импульса
- 40. х Если обратиться к привычной нам модели атома, то: n – характеризует среднее расстояние электрона от
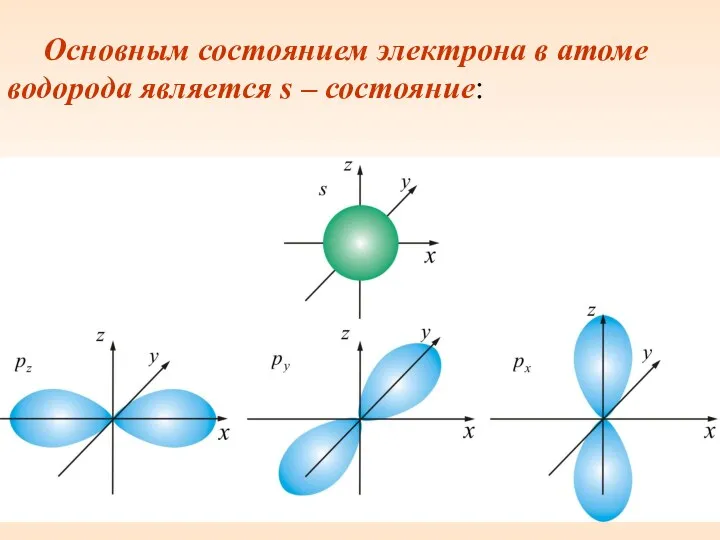
- 41. Основным состоянием электрона в атоме водорода является s – состояние:
- 42. х Если вычислить наиболее вероятное расстояние от ядра для электрона в s –состоянии, получим: – это
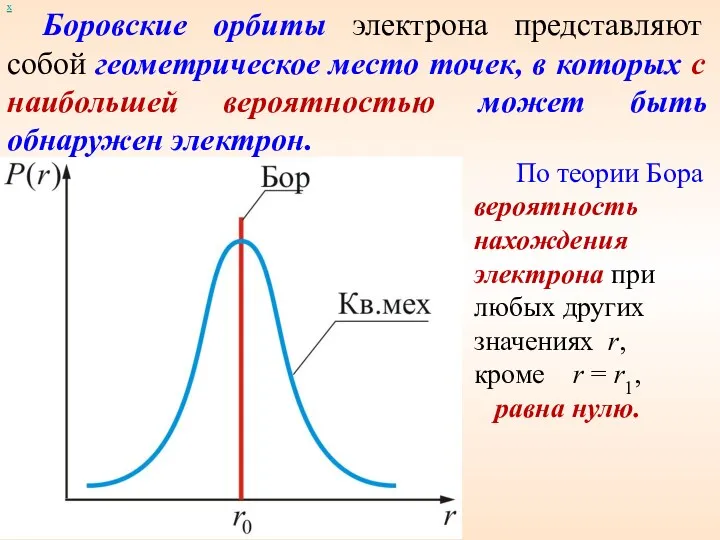
- 43. х Боровские орбиты электрона представляют собой геометрическое место точек, в которых с наибольшей вероятностью может быть
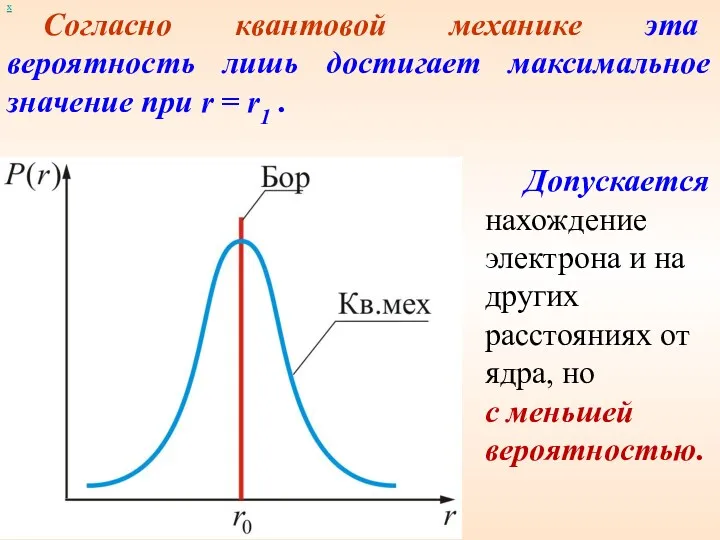
- 44. х Согласно квантовой механике эта вероятность лишь достигает максимальное значение при r = r1 . Допускается
- 45. 1S состояние
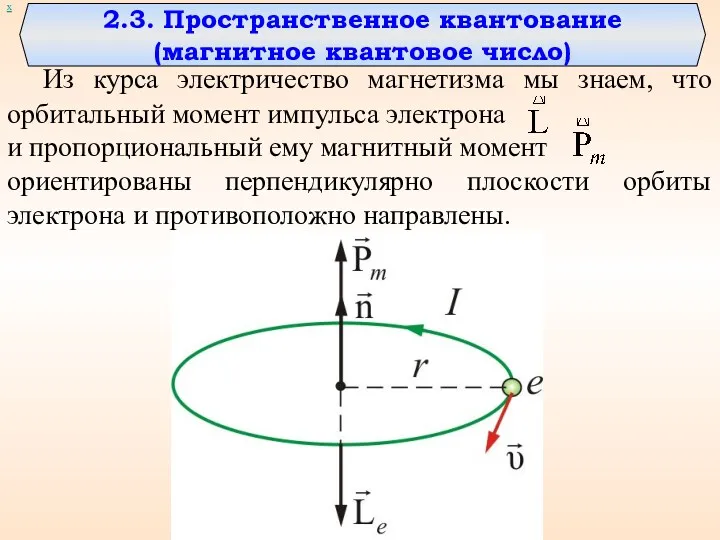
- 46. Из курса электричество магнетизма мы знаем, что орбитальный момент импульса электрона и пропорциональный ему магнитный момент
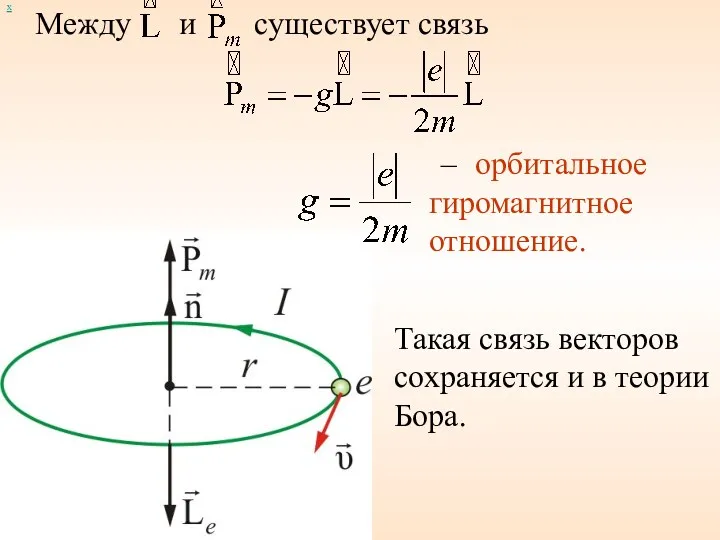
- 47. Между и х существует связь – орбитальное гиромагнитное отношение. Такая связь векторов сохраняется и в теории
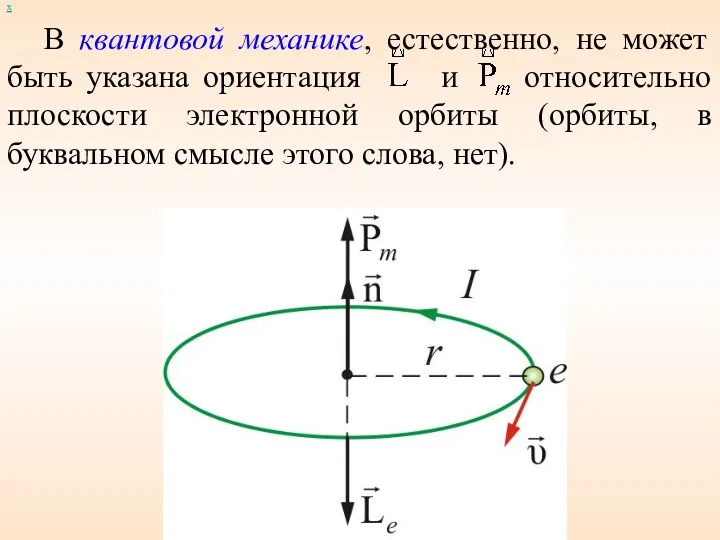
- 48. В квантовой механике, естественно, не может быть указана ориентация и относительно плоскости электронной орбиты (орбиты, в
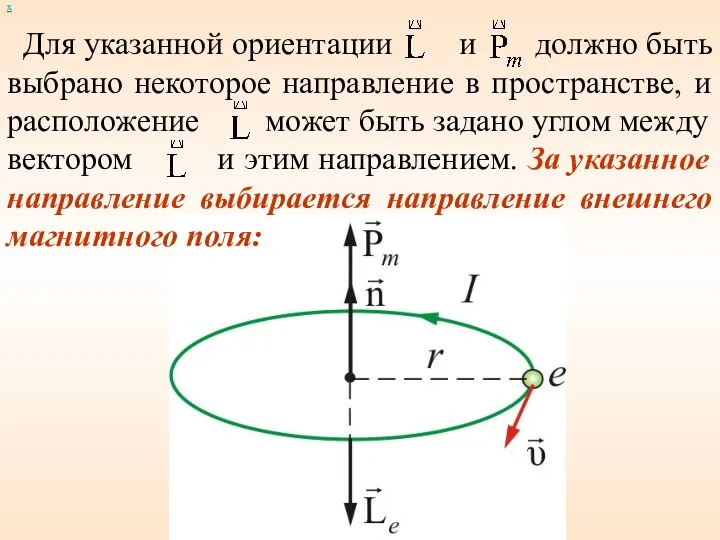
- 49. Для указанной ориентации и должно быть выбрано некоторое направление в пространстве, и расположение может быть задано
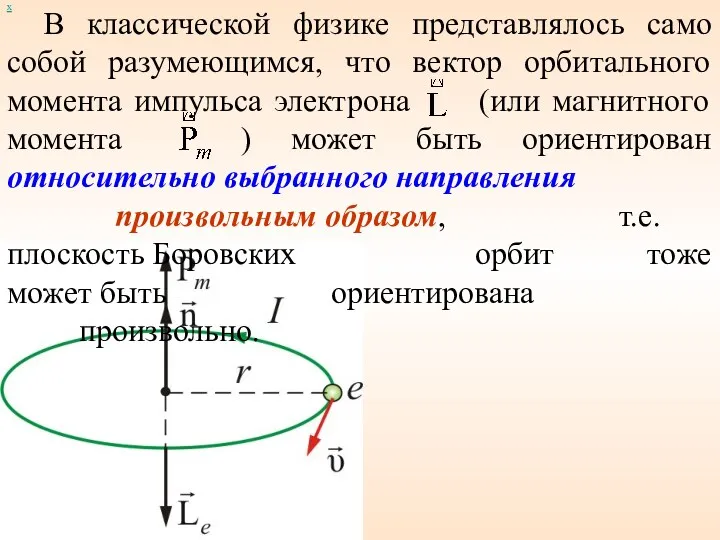
- 50. В классической физике представлялось само собой разумеющимся, что вектор орбитального момента импульса электрона (или магнитного момента
- 51. Однако, такое предположение оказалось ошибочным. В квантовой механике строго доказывается (это следует из решения уравнения Шредингера),
- 52. Определим величину модуля . Т.к. проекция не может быть больше модуля вектора, то, следовательно . Отсюда
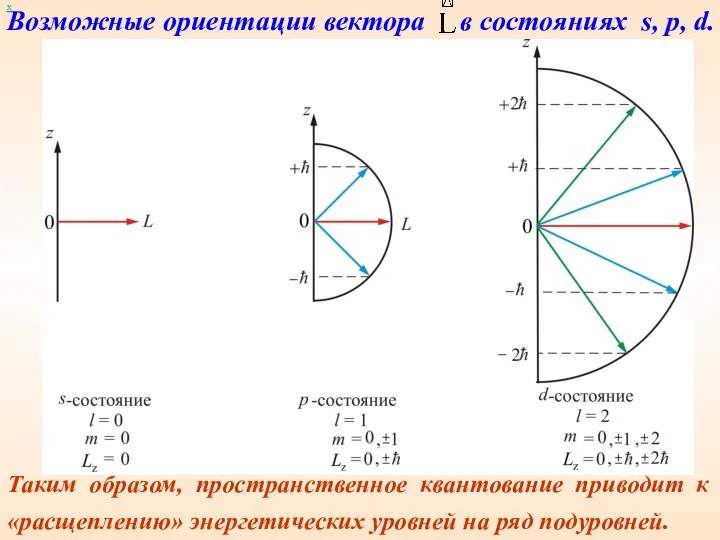
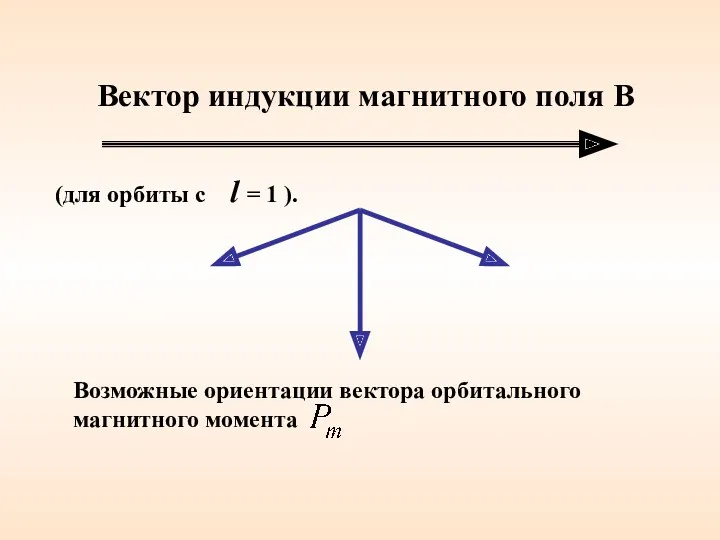
- 53. х Таким образом, пространственное квантование приводит к «расщеплению» энергетических уровней на ряд подуровней. Возможные ориентации вектора
- 54. Расщепление энергетических уровней в магнитном поле было обнаружено в 1896 г. голландским физиком П. Зееманом и
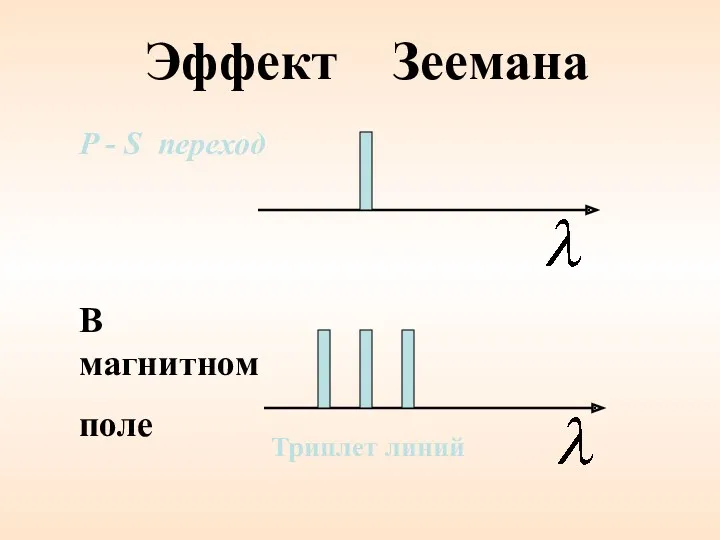
- 55. Эффект Зеемана В магнитном поле P - S переход Триплет линий
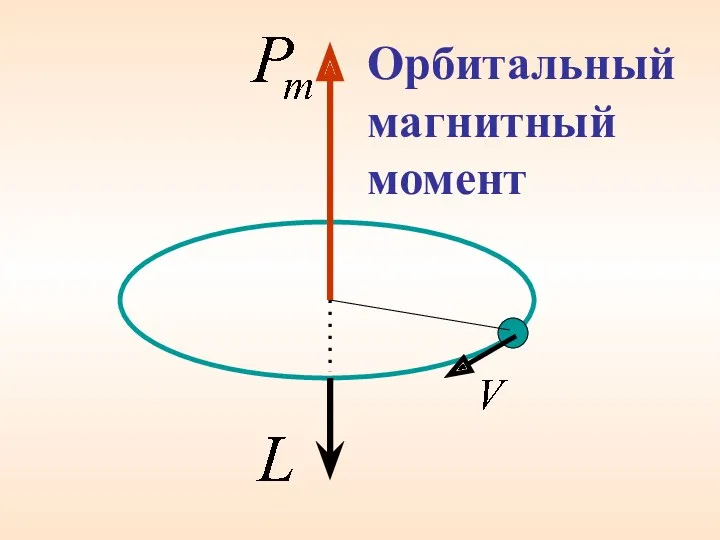
- 56. Орбитальный магнитный момент
- 57. Вектор индукции магнитного поля В Возможные ориентации вектора орбитального магнитного момента (для орбиты с l =
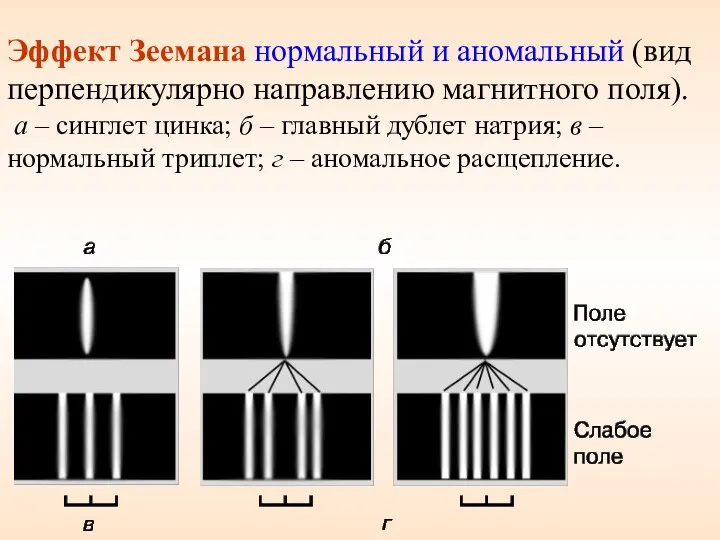
- 58. Эффект Зеемана нормальный и аномальный (вид перпендикулярно направлению магнитного поля). а – синглет цинка; б –
- 59. х 2.4. Опыт Штерна и Герлаха. В 1922 году Штерн и Герлах поставили опыты, целью которых
- 60. х Идея опыта заключалась в измерении силы, действующей на атом в сильно - неоднородном магнитном поле.
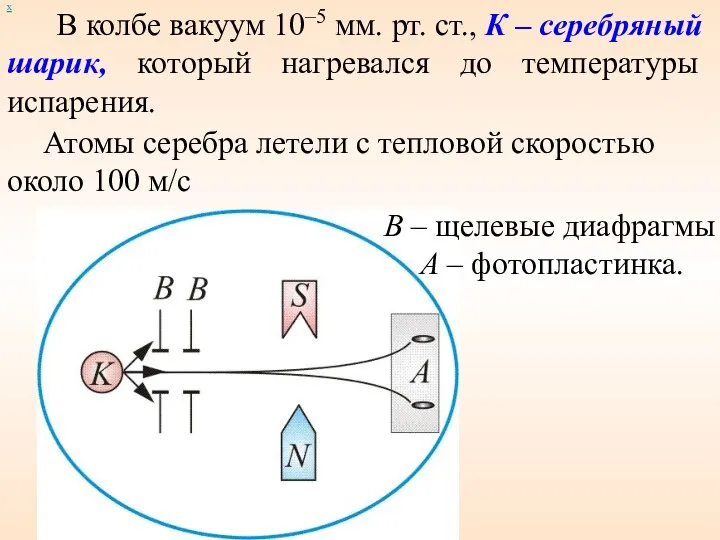
- 61. х В колбе вакуум 10–5 мм. рт. ст., К – серебряный шарик, который нагревался до температуры
- 62. х Если бы момент импульса атома (и его магнитный момент ) мог принимать произвольные ориентации в
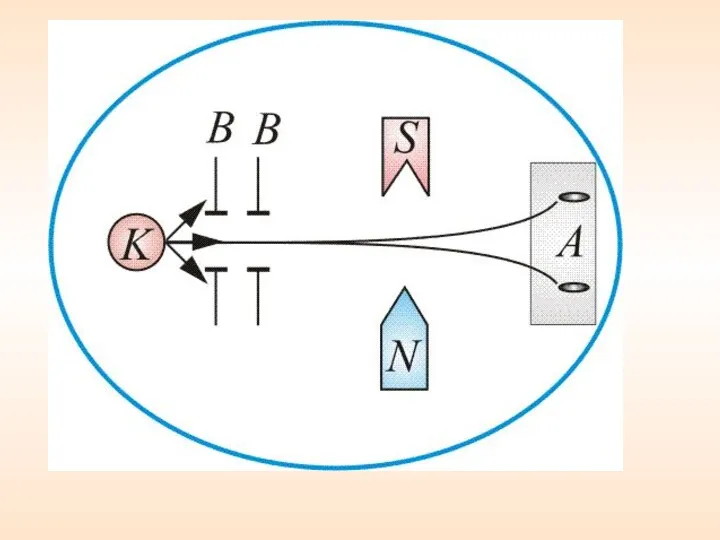
- 64. х Рисунок 6
- 65. Этим доказывался квантовый характер магнитных моментов электронов. Количественный анализ показал, что проекция магнитного момента электрона равна
- 66. х Опыты Штерна и Герлаха не только подтвердили пространственное квантование моментов импульсов в магнитном поле, но
- 67. х Кроме того, в этих опытах было обнаружено новое явление. Валентный электрон в основном состоянии атома
- 68. х В 1925 г. студенты Геттингенского университета Гаудсмит и Уленбек предложили существование собственного механического момента импульса
- 69. Спин электрона S Собственный магнитный момент электрона
- 70. х Спин, как заряд и масса есть свойство электрона П.Дирак впоследствии показал, что существование спина вытекает
- 71. х Аналогично, проекция спина на ось z (LSz) (ось z совпадает с направлением внешнего магнитного поля)
- 72. х Для атомов первой группы, валентный электрон которых находится в s – состоянии (l = 0)
- 73. х Численное значение спина электрона По аналогии с пространственным квантованием орбитального момента (L) проекция LSz =
- 74. И так магнитное спиновое квантовое число может принимать два значения. Спиновое квантовое число S имеет только
- 75. Проекция магнитного момента электрона на направление внешнего поля: (часто говорят о собственном магнитном моменте электрона) Отношение
- 77. Скачать презентацию
































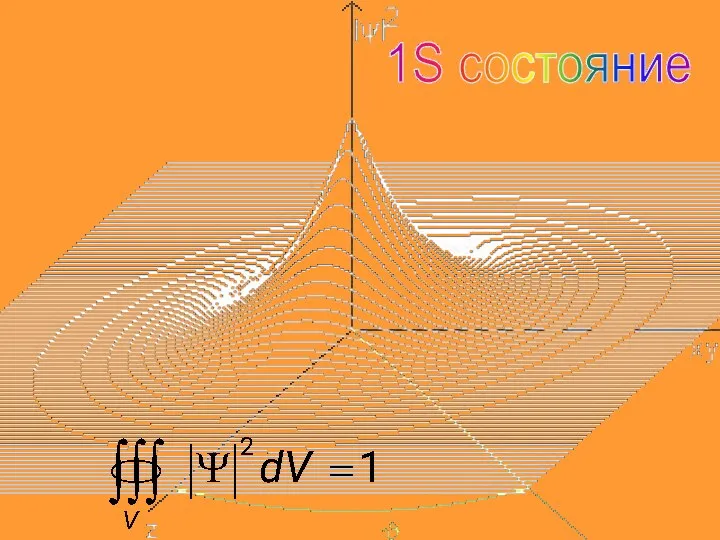


















 Производство, передача и потребление электроэнергии. Типы электростанций
Производство, передача и потребление электроэнергии. Типы электростанций Выбор и обоснование узлов приводов робота - манипулятора для загрузочных операций
Выбор и обоснование узлов приводов робота - манипулятора для загрузочных операций Управление и характеристики машин
Управление и характеристики машин Ремонт и хранение бронетанкового вооружения и техники. Возможные неисправности трансмиссии. (Занятие 6)
Ремонт и хранение бронетанкового вооружения и техники. Возможные неисправности трансмиссии. (Занятие 6) Кривошипно-шатунный механизм
Кривошипно-шатунный механизм Вводный урок физики в 7 классе
Вводный урок физики в 7 классе Механикалық энергия
Механикалық энергия Занятие № 1 Методы повышения эффективности усвоения понятийпри изучении темы:Кинематика
Занятие № 1 Методы повышения эффективности усвоения понятийпри изучении темы:Кинематика Карбюраторный двигатель
Карбюраторный двигатель Двигатель внутреннего сгорания
Двигатель внутреннего сгорания Применение кристаллов в науке и технике
Применение кристаллов в науке и технике Презентация Давление твердых тел
Презентация Давление твердых тел Електричний струм у напівпровідниках
Електричний струм у напівпровідниках Будова атомного ядра
Будова атомного ядра Эффект Зеебека
Эффект Зеебека Да здравствует физика!
Да здравствует физика! Радиоактивные вещества
Радиоактивные вещества Опыт Карла Рикке
Опыт Карла Рикке презентации к урокам
презентации к урокам Мастер класс по использованию сингапурской системы для учителей физики Татарстан
Мастер класс по использованию сингапурской системы для учителей физики Татарстан Теплофикационная установка. Испарители
Теплофикационная установка. Испарители Физическая природа радуги. Создание радуги в домашних условиях
Физическая природа радуги. Создание радуги в домашних условиях Механическая коробка передач
Механическая коробка передач Электрический ток. Источники электрического тока
Электрический ток. Источники электрического тока Аеродинаміка та динаміка польоту літака. Характеристики профілю крила. Поздовжні аеродинамічні сили та момент. (Лекція 3.2.1)
Аеродинаміка та динаміка польоту літака. Характеристики профілю крила. Поздовжні аеродинамічні сили та момент. (Лекція 3.2.1) Взаимное притяжение и отталкивание молекул
Взаимное притяжение и отталкивание молекул Разрушение. Теоретический предел прочности
Разрушение. Теоретический предел прочности 2.1 МЕХАНИКА ЖИДКОСТЕЙ И ГАЗОВ
2.1 МЕХАНИКА ЖИДКОСТЕЙ И ГАЗОВ