Содержание
- 2. необратимый процесс При сжатии При расширении Суммарная работа При весьма малых скоростях l1-2-1
- 3. Циклы и их КПД А Б С Для любого цикла первое начало термодинамики
- 4. Циклы и их КПД КПД обратимого цикла называется термическим ηt Из равенств следует, что lc =
- 5. Формулировки второго начала Р. Клаузиус : Невозможен самопроизвольный переход теплоты от менее нагретого тела к более
- 6. Формулировки второго начала Невозможно создать двигатель, который мог бы бесконечно совершать работу без подвода энергии извне
- 7. Цикл Карно. Теорема Карно ∆T1=Th-T1 ∆T3=T3-Tс
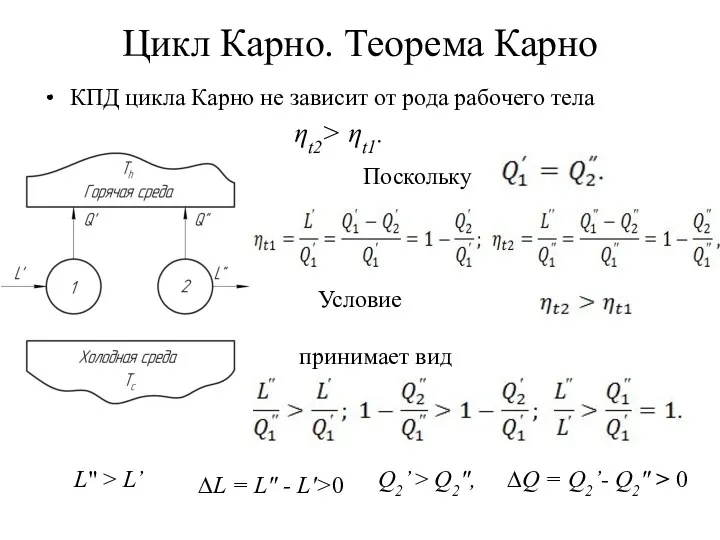
- 8. Цикл Карно. Теорема Карно КПД цикла Карно не зависит от рода рабочего тела Поскольку принимает вид
- 9. Энтропия, ее изменение в обратимых и необратимых процессах Для каждого i-ого цикла Карно Уравнение Р. Клаузиуса
- 10. Энтропия, ее изменение в обратимых и необратимых процессах интеграл Клаузиуса удельная энтропия S=ms – полная энтропия
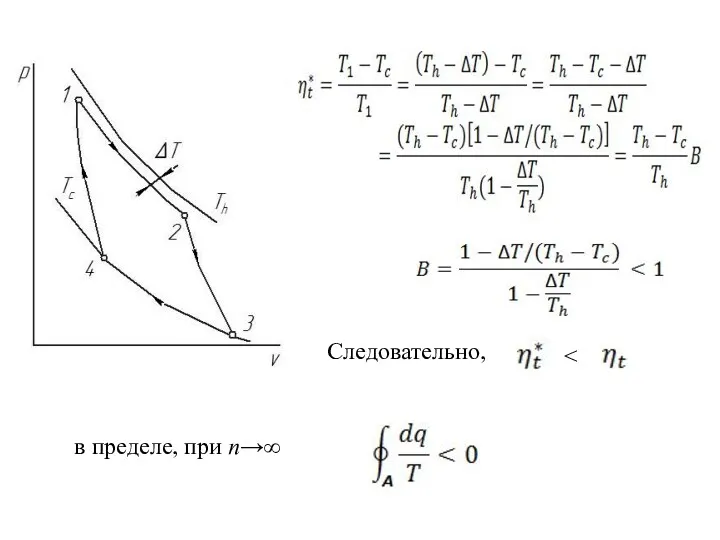
- 11. Следовательно, в пределе, при n→∞
- 12. отсюда следует, что изменение энтропии в необратимом процессе больше, чем интеграл Клаузиуса в этом же процессе.
- 13. при протекании любых процессов энтропия теплоизолированной системы убывать не может энтропия — мера необратимости процессов в
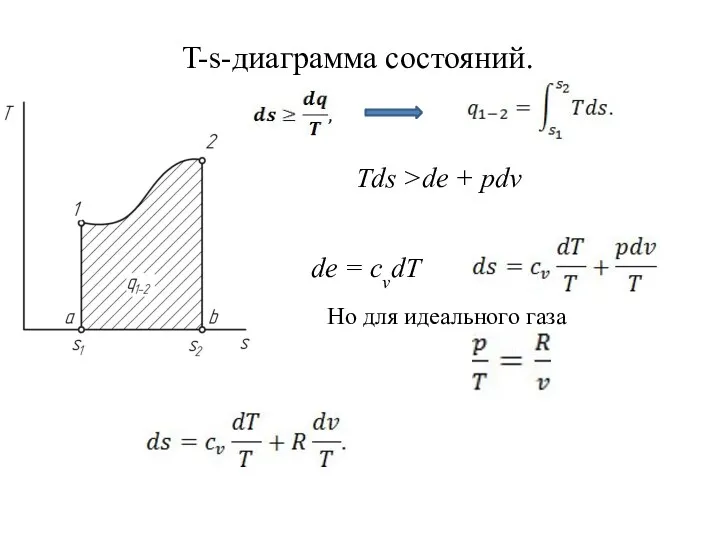
- 14. T-s-диаграмма состояний. Но для идеального газа Tds >de + pdv de = cvdT
- 15. изменение энтропии в произвольном обратимом процессе Уравнения справедливы для любого обратимого процесса идеального газа x=const. b
- 16. частные случаи: T=const, v=const, p = const, q=0 и s=const Изотермический процесс 1-2T изменение энтропии изохорный
- 17. частные случаи: для изобарного процесса 1-2p Адиабата 1-2s вертикальная прямая, совпадающая с линией s=const. q1-2s=0
- 18. В политропном процессе (n=const) из уравнения Tvn-1= const точка, где энтропии приписывают нулевое значение TN =
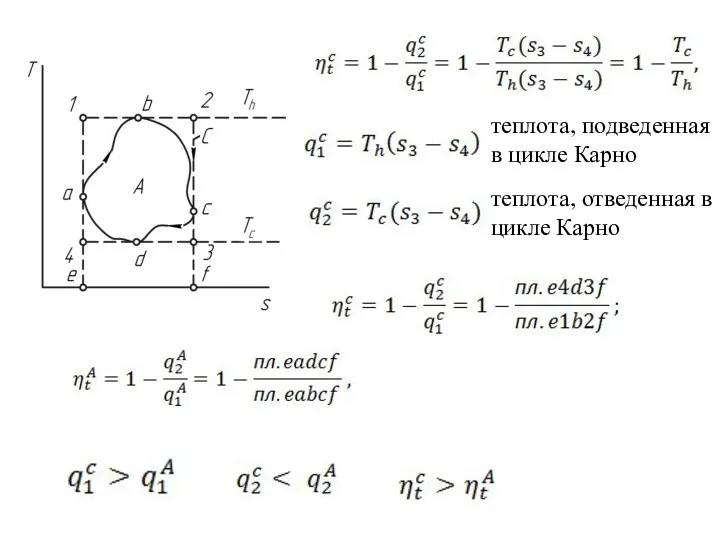
- 19. теплота, подведенная в цикле Карно теплота, отведенная в цикле Карно
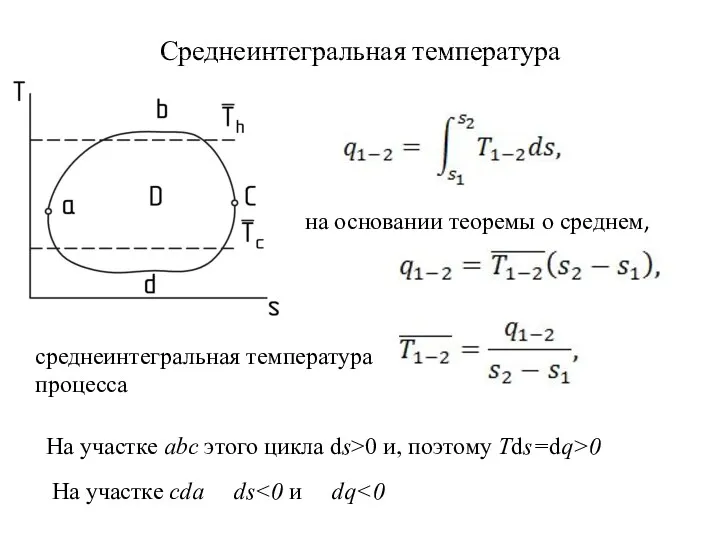
- 20. на основании теоремы о среднем, Среднеинтегральная температура среднеинтегральная температура процесса На участке abc этого цикла ds>0
- 21. Среднеинтегральная температура термический КПД цикла D Подведенная теплота отведенная теплота
- 23. Скачать презентацию















 Механические колебания
Механические колебания Архимедова сила. Подготовка к ГИА
Архимедова сила. Подготовка к ГИА Бытовая швейная машина. Правила техники безопасности при работе на швейной машине. 5 класс
Бытовая швейная машина. Правила техники безопасности при работе на швейной машине. 5 класс Звуковые волны. Ультразвук
Звуковые волны. Ультразвук разработка к уроку на тему Электролизация тел 8 класс
разработка к уроку на тему Электролизация тел 8 класс Система EDS (Elektronische Differentialsperre) для автомобилей
Система EDS (Elektronische Differentialsperre) для автомобилей Преломление света. Закон преломления света. 9 класс
Преломление света. Закон преломления света. 9 класс Определение твёрдости металлов и сплавов
Определение твёрдости металлов и сплавов Высота всасывания насоса. Условия бескавитационной работы насоса. (Лекция 8)
Высота всасывания насоса. Условия бескавитационной работы насоса. (Лекция 8) Моторамы. Назначение моторам
Моторамы. Назначение моторам Архимедова сила
Архимедова сила Теплоизоляция домов
Теплоизоляция домов Отчет по производственной практике по специализации: Слесарь по контрольно-измерительным приборам и автоматике
Отчет по производственной практике по специализации: Слесарь по контрольно-измерительным приборам и автоматике Формирование навыков смыслового чтения и работы с текстом на уроках физики (Часть2)
Формирование навыков смыслового чтения и работы с текстом на уроках физики (Часть2) Интерактивная мозаика-2017. Знатоки физики 8 класс
Интерактивная мозаика-2017. Знатоки физики 8 класс Работа электрического поля при перемещении заряда
Работа электрического поля при перемещении заряда Резьбовые соединения
Резьбовые соединения Ремонт авиационной техники
Ремонт авиационной техники Рентгеноструктурный анализ
Рентгеноструктурный анализ Три состояния вещества
Три состояния вещества Пасивні елементи засобів вимірювань
Пасивні елементи засобів вимірювань Винаходи під час промислового перевороту в Англії
Винаходи під час промислового перевороту в Англії Классификация твердых тел
Классификация твердых тел Давление на дне морей и океанов
Давление на дне морей и океанов Динамика. Законы динамики
Динамика. Законы динамики Зубчатые передачи
Зубчатые передачи Буксовые узлы. Устройство. Наблюдение и уход за буксами в эксплуатации. Основные детали и их неисправности
Буксовые узлы. Устройство. Наблюдение и уход за буксами в эксплуатации. Основные детали и их неисправности Презентация к уроку Исследование капиллярных свойств столовых салфеток. Урок-контрольная закупка.
Презентация к уроку Исследование капиллярных свойств столовых салфеток. Урок-контрольная закупка.