Содержание
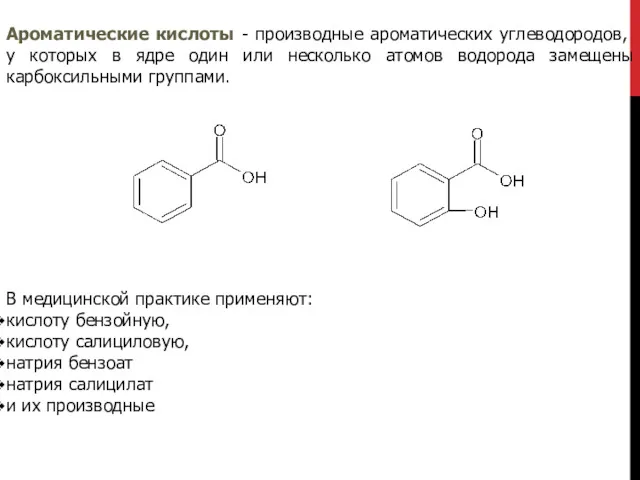
- 2. Ароматические кислоты - производные ароматических углеводородов, у которых в ядре один или несколько атомов водорода замещены
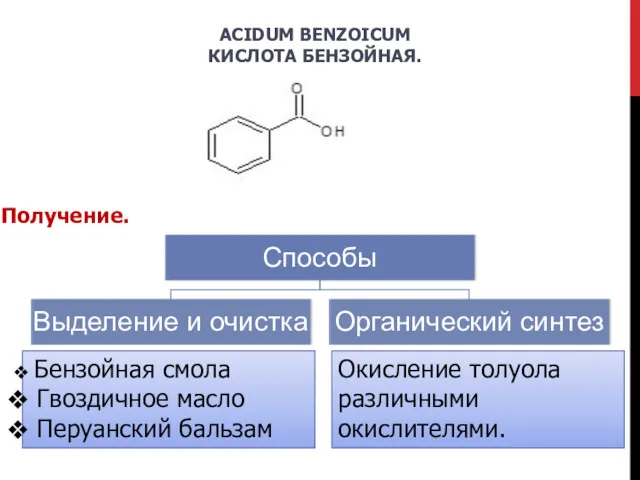
- 3. ACIDUM BENZOICUM КИСЛОТА БЕНЗОЙНАЯ. Получение. Бензойная смола Гвоздичное масло Перуанский бальзам Окисление толуола различными окислителями.
- 4. Описание. Белый мелко кристаллический порошок. Кислота летучая с водяным паром и при осторожном нагревании возгоняются. Температура
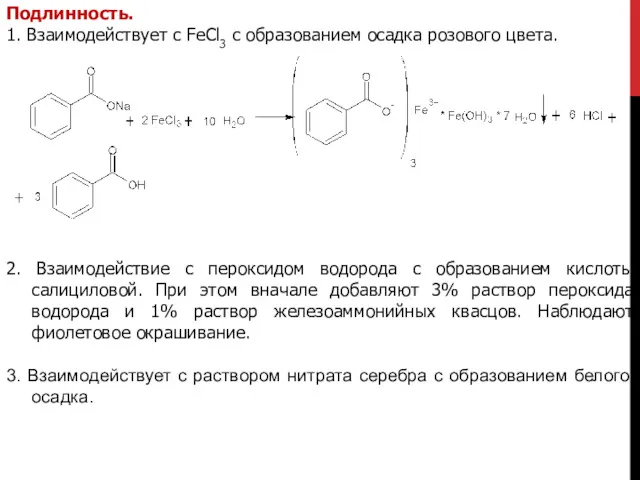
- 5. Подлинность. 1. Взаимодействует с FeCl3 с образованием осадка розового цвета. 2. Взаимодействие с пероксидом водорода с
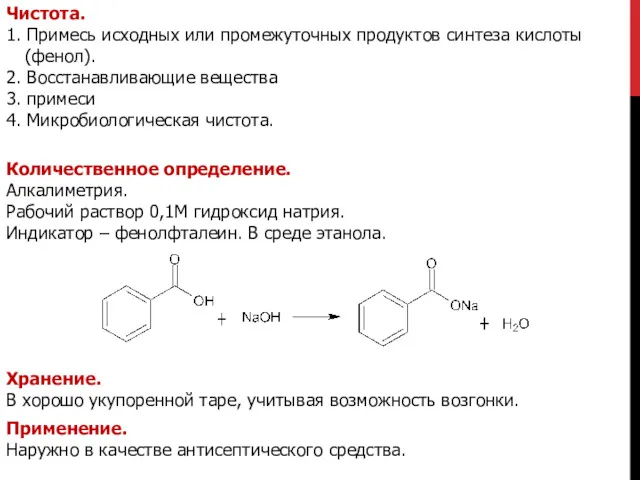
- 6. Чистота. 1. Примесь исходных или промежуточных продуктов синтеза кислоты (фенол). 2. Восстанавливающие вещества 3. примеси 4.
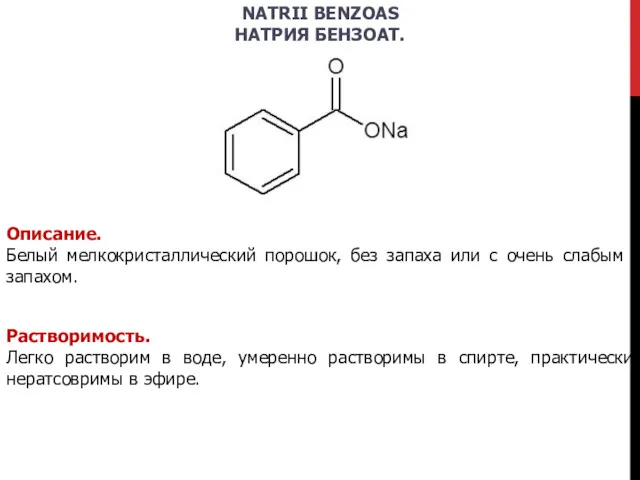
- 7. NATRII BENZOAS НАТРИЯ БЕНЗОАТ. Описание. Белый мелкокристаллический порошок, без запаха или с очень слабым запахом. Растворимость.
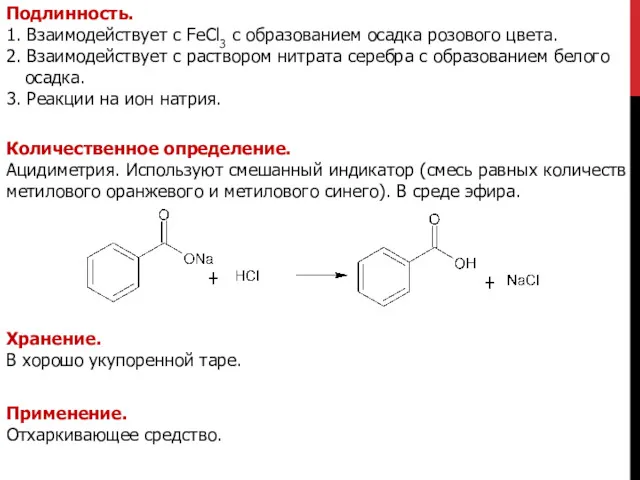
- 8. Подлинность. 1. Взаимодействует с FeCl3 с образованием осадка розового цвета. 2. Взаимодействует с раствором нитрата серебра
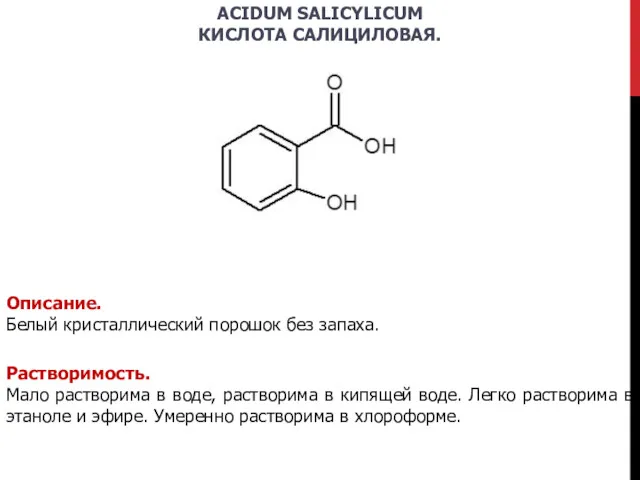
- 9. ACIDUM SALICYLICUM КИСЛОТА САЛИЦИЛОВАЯ. Описание. Белый кристаллический порошок без запаха. Растворимость. Мало растворима в воде, растворима
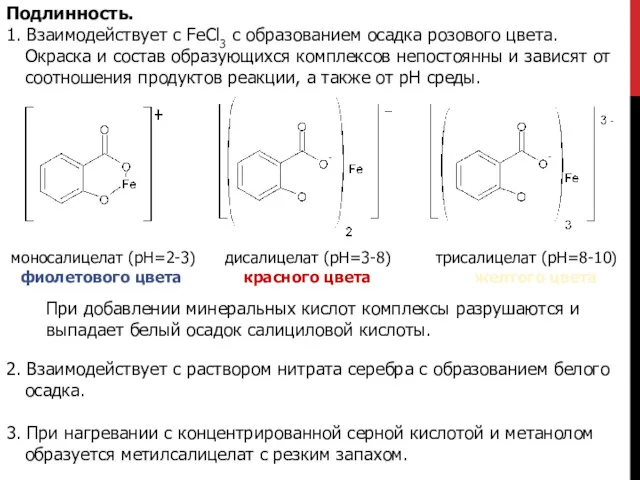
- 10. Подлинность. 1. Взаимодействует с FeCl3 с образованием осадка розового цвета. Окраска и состав образующихся комплексов непостоянны
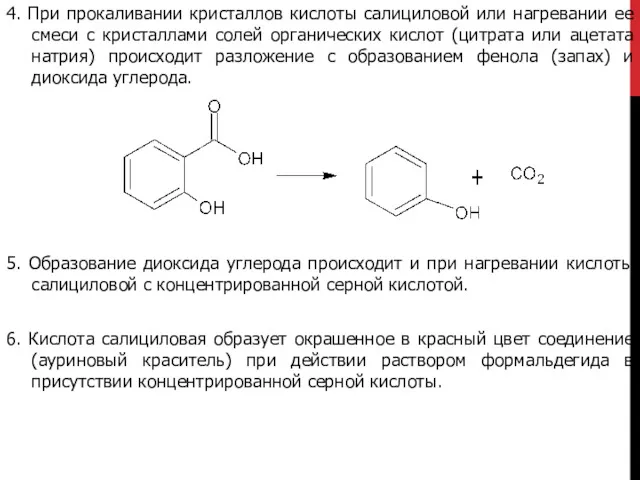
- 11. 4. При прокаливании кристаллов кислоты салициловой или нагревании ее смеси с кристаллами солей органических кислот (цитрата
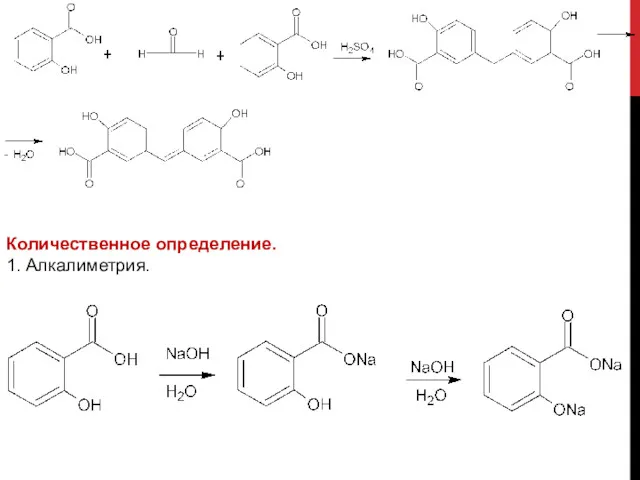
- 12. Количественное определение. 1. Алкалиметрия.
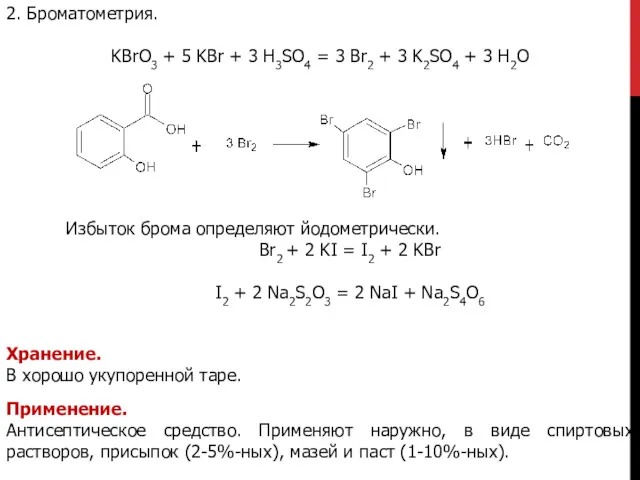
- 13. 2. Броматометрия. KBrO3 + 5 KBr + 3 H3SO4 = 3 Br2 + 3 K2SO4 +
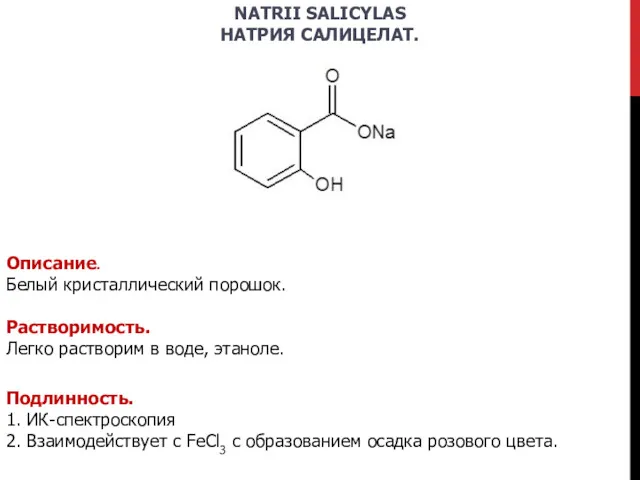
- 14. NATRII SALICYLAS НАТРИЯ САЛИЦЕЛАТ. Описание. Белый кристаллический порошок. Растворимость. Легко растворим в воде, этаноле. Подлинность. 1.
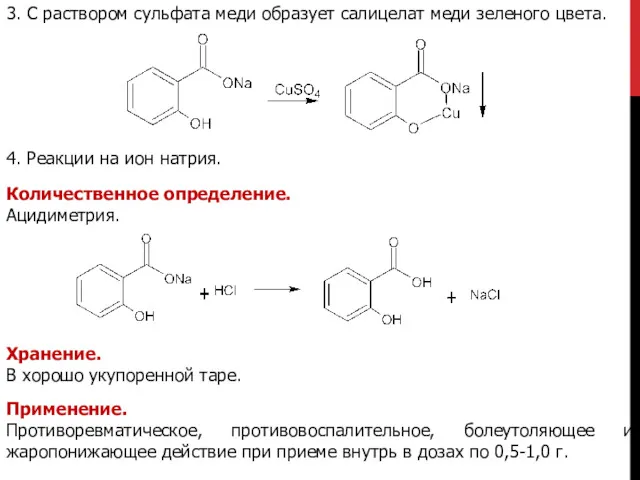
- 15. 3. С раствором сульфата меди образует салицелат меди зеленого цвета. 4. Реакции на ион натрия. Количественное
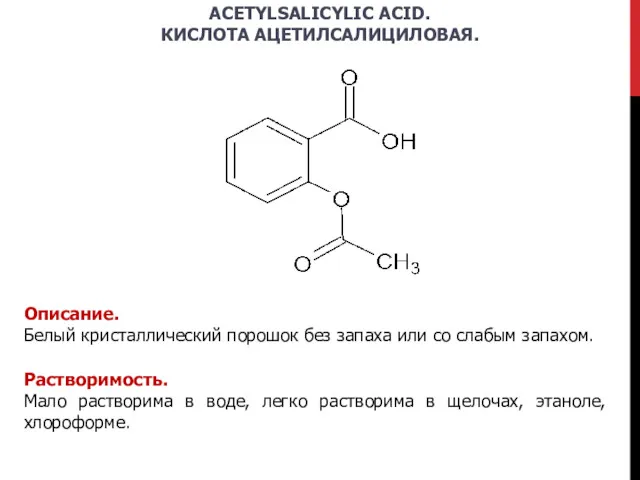
- 16. ACETYLSALICYLIC ACID. КИСЛОТА АЦЕТИЛСАЛИЦИЛОВАЯ. Описание. Белый кристаллический порошок без запаха или со слабым запахом. Растворимость. Мало
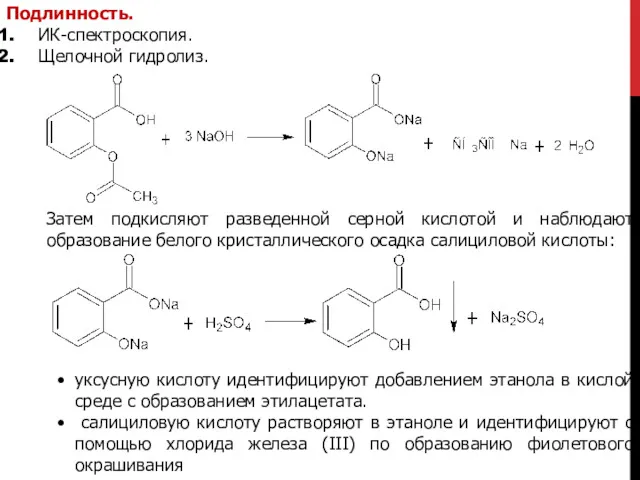
- 17. Подлинность. ИК-спектроскопия. Щелочной гидролиз. Затем подкисляют разведенной серной кислотой и наблюдают образование белого кристаллического осадка салициловой
- 18. 3. Кислотный гидролиз. При добавлении концентрированной серной кислоты и воды ощущается запах уксусной кислоты. При добавлении
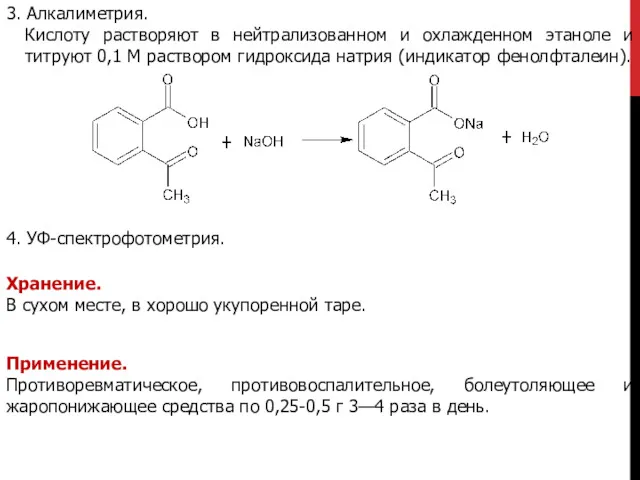
- 19. 3. Алкалиметрия. Кислоту растворяют в нейтрализованном и охлажденном этаноле и титруют 0,1 М раствором гидроксида натрия
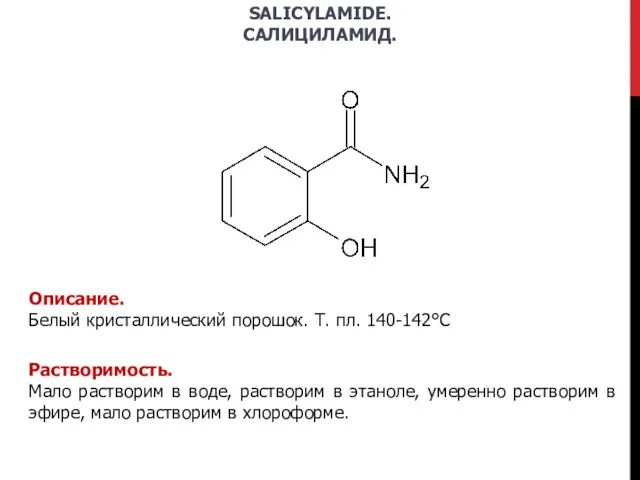
- 20. SALICYLAMIDE. САЛИЦИЛАМИД. Описание. Белый кристаллический порошок. Т. пл. 140-142°С Растворимость. Мало растворим в воде, растворим в
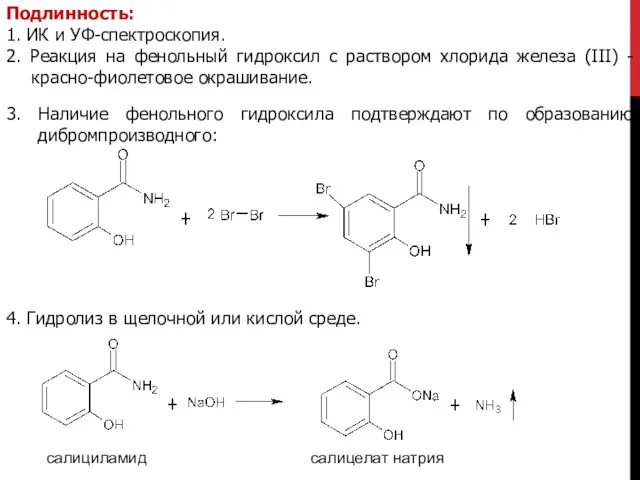
- 21. Подлинность: 1. ИК и УФ-спектроскопия. 2. Реакция на фенольный гидроксил с раствором хлорида железа (III) -
- 22. 5. С азотистой кислотой в присутствии концентрированной серной кислоты образуется розоватое окрашивание. 6. При взаимодействии с
- 23. Количественное определение. 1. Алкалиметрия в неводной среде. Титрант 0,1 М раствором гидроксида натрия в смеси метанола
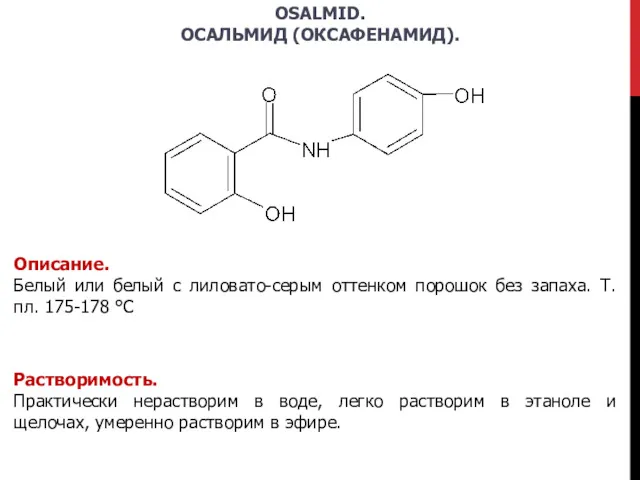
- 24. OSALMID. ОСАЛЬМИД (ОКСАФЕНАМИД). Описание. Белый или белый с лиловато-серым оттенком порошок без запаха. Т. пл. 175-178
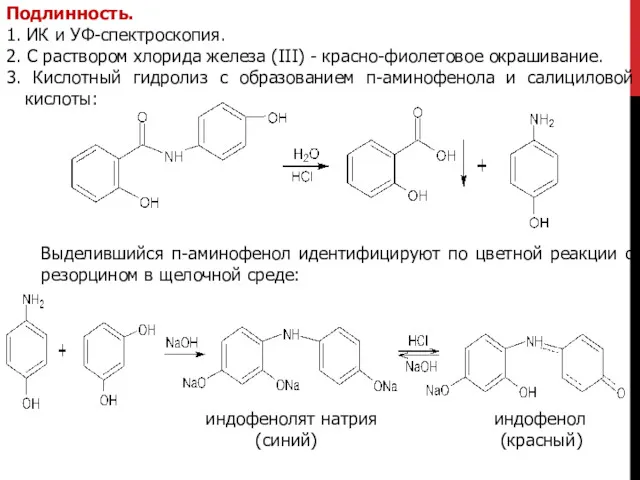
- 25. Подлинность. 1. ИК и УФ-спектроскопия. 2. С раствором хлорида железа (III) - красно-фиолетовое окрашивание. 3. Кислотный
- 26. 4. С азотистой кислотой в присутствии концентрированной серной кислоты образуется грязно-фиолетовое окрашивание. 5. При взаимодействии с
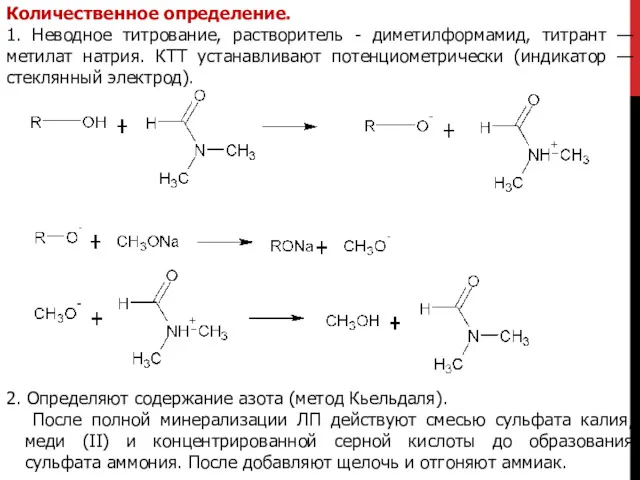
- 27. Количественное определение. 1. Неводное титрование, растворитель - диметилформамид, титрант — метилат натрия. КТТ устанавливают потенциометрически (индикатор
- 28. Хранение. В хорошо укупоренной таре, в сухом, защищенном от света месте. Применение. Желчегонное средство в таблетках
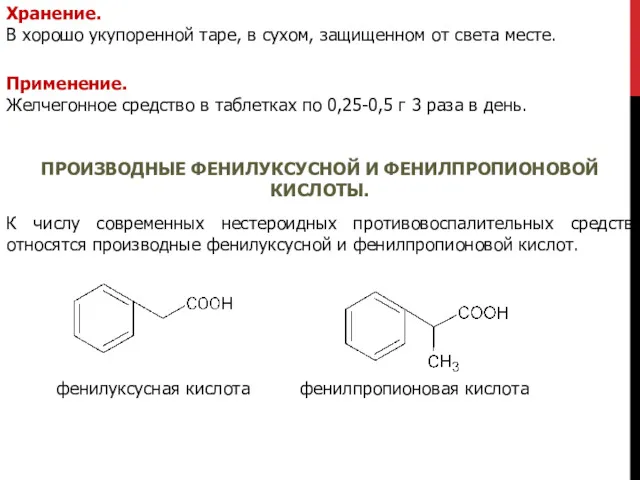
- 29. DICLOFENAC SODIUM. НАТРИЯ ДИКЛОФЕНАК. Натриевая соль2-[(2,6-дихлорфенил)-амино]-фенилуксусной кислоты Описание. Белый с кремоватым оттенком кристаллический порошок.
- 30. Растворимость. Мало растворим в воде, легко — в этаноле и метаноле, практически нерастворим в хлороформе. Подлинность.
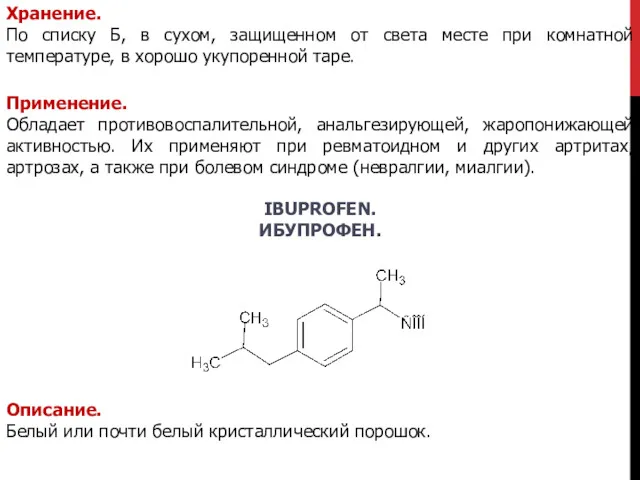
- 31. 6. При добавлении разведенной хлороводородной кислоты выпадает белый осадок. 2-[2,6-(дихлорфенил)-амино] индолинон -фенилуксусной кислоты Чистота. Наличие примесей
- 32. Хранение. По списку Б, в сухом, защищенном от света месте при комнатной температуре, в хорошо укупоренной
- 33. Подлинность. 1. ИК- и УФ-спектроскопия. 2. ВЭЖХ. Чистота. Наличие посторонних примесей методом ГЖХ и методом ТСХ.
- 34. Количественное определение. 1. Алкалиметрия. После растворения в предварительно нейтрализованном этаноле, титруют 0,1 М раствором гидроксида натрия
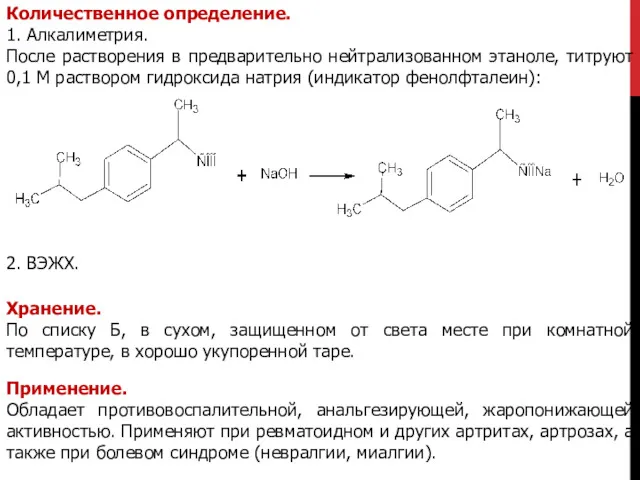
- 35. ПРОИЗВОДНЫЕ БУТИРОФЕНОНА. HALOPERIDOL. ГАЛОПЕРИДОЛ. 4-(п-хлорфенил)-1-[3-(п-фторбензол)-пропил]-пиперидинол-4 Описание. Белый кристаллический порошок. Растворимость. Практически нерастворимое в воде, мало растворимое
- 37. Скачать презентацию





![DICLOFENAC SODIUM. НАТРИЯ ДИКЛОФЕНАК. Натриевая соль2-[(2,6-дихлорфенил)-амино]-фенилуксусной кислоты Описание. Белый с кремоватым оттенком кристаллический порошок.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/154480/slide-28.jpg)

![6. При добавлении разведенной хлороводородной кислоты выпадает белый осадок. 2-[2,6-(дихлорфенил)-амино]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/154480/slide-30.jpg)

![ПРОИЗВОДНЫЕ БУТИРОФЕНОНА. HALOPERIDOL. ГАЛОПЕРИДОЛ. 4-(п-хлорфенил)-1-[3-(п-фторбензол)-пропил]-пиперидинол-4 Описание. Белый кристаллический порошок. Растворимость.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/154480/slide-34.jpg)
 Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Катализаторы. Ферменты
Катализаторы. Ферменты Электролитическая диссоциация веществ
Электролитическая диссоциация веществ Элементный, фракционный и химический состав нефти. Классификация нефтей
Элементный, фракционный и химический состав нефти. Классификация нефтей Галогены. Расположите галогены в порядке их открытия
Галогены. Расположите галогены в порядке их открытия Атомно-кристаллическое строение материалов
Атомно-кристаллическое строение материалов Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота
Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота Реакции при нагревании
Реакции при нагревании Природные источники углеводородов
Природные источники углеводородов Суды тазарту әдістері
Суды тазарту әдістері Алюминий. Сплавы алюминия
Алюминий. Сплавы алюминия Молярный объем. Закон Авогадро
Молярный объем. Закон Авогадро Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды
Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды Вода и здоровье
Вода и здоровье Атмосфера. Химия стратосферы
Атмосфера. Химия стратосферы Углерод. Аллотропные модификации
Углерод. Аллотропные модификации Сплав золота и серебра - электрум
Сплав золота и серебра - электрум Алкени та алкіни
Алкени та алкіни Комплексні сполуки
Комплексні сполуки Марганец и его соединения
Марганец и его соединения Методы определения механических свойств полимерных композиционных материалов
Методы определения механических свойств полимерных композиционных материалов Свойства простых веществ в свете ОВР
Свойства простых веществ в свете ОВР Углеводы (сахариды)
Углеводы (сахариды) Простые и сложные вещества. Химический элемент
Простые и сложные вещества. Химический элемент Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Кислородные соединения азота
Кислородные соединения азота Химические свойста воды
Химические свойста воды Химическое равновесие
Химическое равновесие