Содержание
- 2. Нахождение в природе В земной коре - около 0,1 % марганца по массе. В свободном виде
- 3. Пиролюзит Мангинит Браунит Родохрозит Псиломелан Нахождение в природе
- 4. Марганец содержат марганцевые конкреции, которые находятся на дне Тихого, Атлантического и Индийского океанов. В морской воде
- 5. Mn 55 25 + 25 ) ) ) ) 1s² 2 8 13 2 2s² 2p
- 6. Физические свойства Марганец - твердый хрупкий металл T плавления = 1244°C Т кипения = 2080°C Серебристо-белого
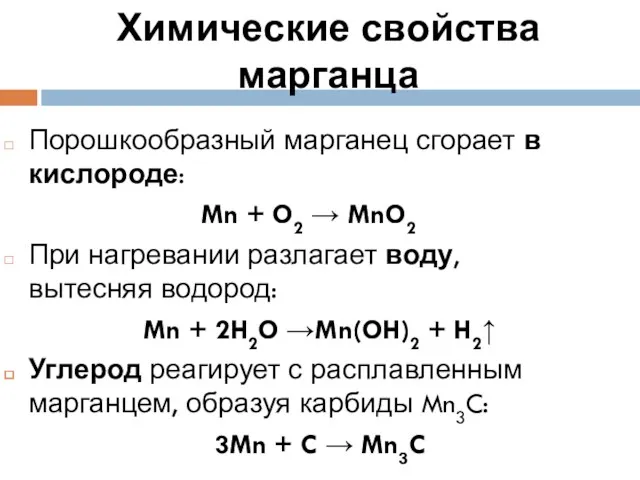
- 7. Химические свойства марганца Порошкообразный марганец сгорает в кислороде: Mn + O2 → MnO2 При нагревании разлагает
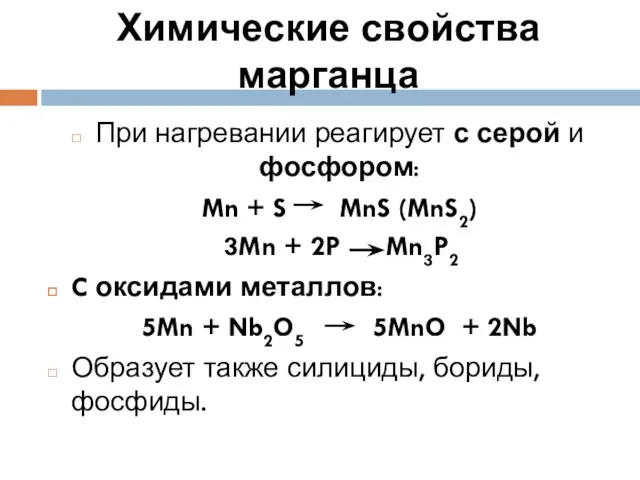
- 8. Химические свойства марганца При нагревании реагирует с серой и фосфором: Mn + S MnS (MnS2) 3Mn
- 9. Химические свойства марганца C соляной и серной кислотами реагирует по уравнению: Mn + 2H+ → Mn2+
- 10. Применение Более 90% производимого марганца идет в черную металлургию: - как добавку к сталям для раскисления;
- 11. Биологическая роль марганца Марганец содержится в организмах всех растений и животных, он оказывает значительное влияние на
- 12. Содержание в живых и растительных организмах Особо богаты марганцем листья свёклы — до 0,03 %. В
- 13. Оксиды и гидроксиды марганца Оксиды: Гидроксиды: Усиление кислотных свойств Усиление окислительных свойств
- 14. Mn+2O (основный оксид) – порошок зелёно-серого цвета, нерастворим в воде. Оксид марганца может быть получен при
- 15. Mn+2(OH)2 (основание) – белый осадок. При растворении в воде (при нагревании)образуется гидроксид Mn(II): Mn+2HOH =Mn(OH)2+H2 Гидроксид
- 16. Соединения Mn(II) на воздухе неустойчивы, и Mn(OH)2 на воздухе быстро буреет, превращаясь в оксид-гидроксид четырёхвалентного марганца.
- 17. Соединения марганца (IV) Mn+4O2 пиролюзит - (амфотерный) - вещество чёрного цвета. Образуется при разложении нитрата марганца(II)
- 18. Соединения марганца (VI) Mn+6O3 проявляют кислотный характер, H2Mn+6O4 в свободном виде не получены. Степень окисления +
- 19. Водой манганаты быстро разлагаются (диспропорционируют на +7 и +4) 2K2MnO4 + 2Н2О = KMnO4 + MnO2
- 20. Mn2+7O7 (кислотный) - жидкое маслянистое вещество тёмно-зелёного цвета, очень неустойчивое; в смеси с концентрированной серной кислотой
- 21. HMn+7O4 – марганцевая кислота - одна из самых сильных кислот. марганцевая кислота устойчива только в разбавленных
- 22. В семивалентном состоянии марганец проявляет только окислительные свойства. Среди применяемых в лабораторной практике и в промышленности
- 23. При нагревании сухого перманганата калия до температуры выше 2000С он разлагается. 2KMnO4 = K2MnO4 + MnO2
- 24. Mn H H2O OH Mn обесцвечивание +2 MnO2 (Mn ) Бурый осадок +4 MnO4 зелёный 2-
- 26. Скачать презентацию





















 Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Кремний и его соединения
Кремний и его соединения Водородная связь
Водородная связь Природные источники углеводородов, их переработка, применение и экологические проблемы
Природные источники углеводородов, их переработка, применение и экологические проблемы Металлы и их свойства. Способы получения
Металлы и их свойства. Способы получения Органическая химия. Вещества
Органическая химия. Вещества Магматизм. (Лекция 6)
Магматизм. (Лекция 6) Кислород
Кислород Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Прочность полимеров
Прочность полимеров Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Буферные растворы
Буферные растворы Місце хімії серед наук про природу
Місце хімії серед наук про природу Химические волокна
Химические волокна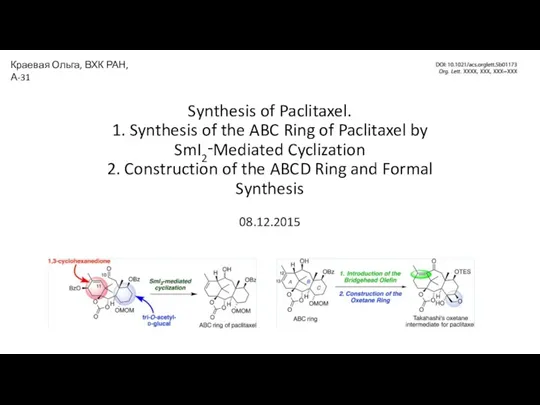 Synthesis of Paclitaxel
Synthesis of Paclitaxel Строение атома. 8 класс
Строение атома. 8 класс Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Витамины. Ашылу тарихы
Витамины. Ашылу тарихы ГИА-9 Химия. А4
ГИА-9 Химия. А4 Массовая и объемная доли компонентов смеси (раствора)
Массовая и объемная доли компонентов смеси (раствора) Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Рідкі кристали
Рідкі кристали Спирты
Спирты Химические уравнения
Химические уравнения Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Применение алюминия и его сплава в машиностроении
Применение алюминия и его сплава в машиностроении Химическая связь. 8 класс
Химическая связь. 8 класс