Содержание
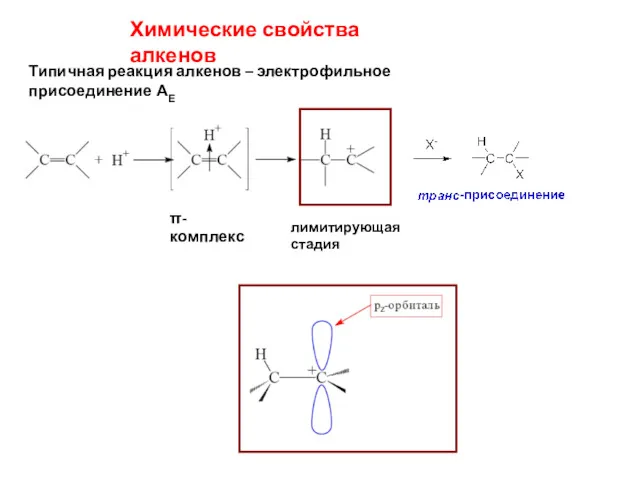
- 2. Химические свойства алкенов Типичная реакция алкенов – электрофильное присоединение АЕ π-комплекс лимитирующая стадия
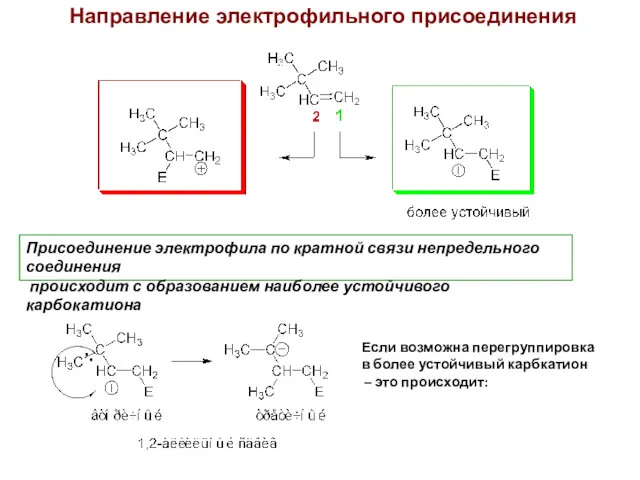
- 3. Направление электрофильного присоединения Присоединение электрофила по кратной связи непредельного соединения происходит с образованием наиболее устойчивого карбокатиона
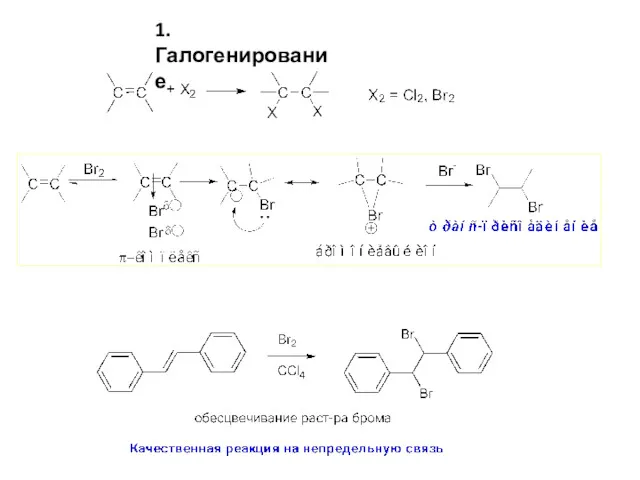
- 4. 1. Галогенирование
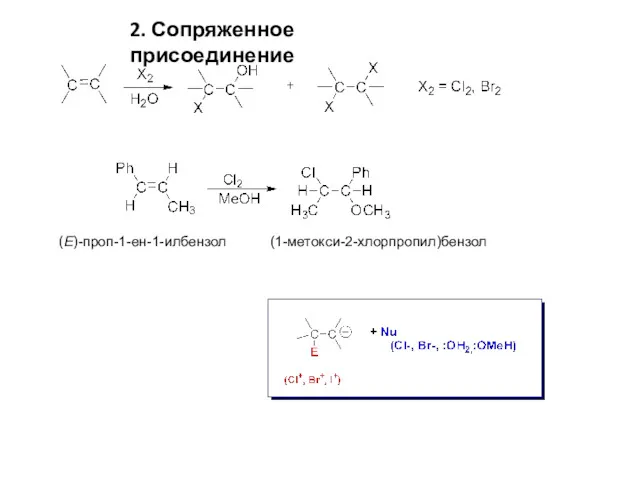
- 5. 2. Сопряженное присоединение (Е)-проп-1-ен-1-илбензол (1-метокси-2-хлорпропил)бензол
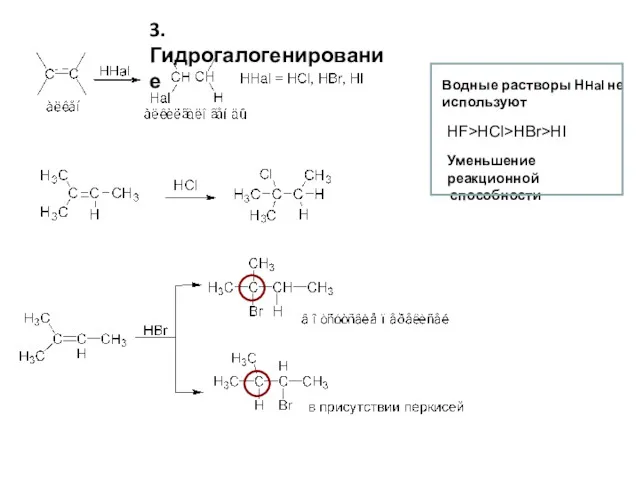
- 6. 3. Гидрогалогенирование Водные растворы НHal не используют HF>HCl>HBr>HI Уменьшение реакционной способности
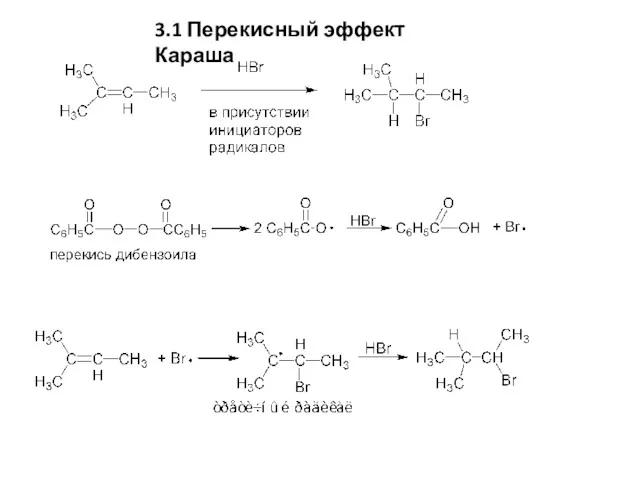
- 7. 3.1 Перекисный эффект Караша
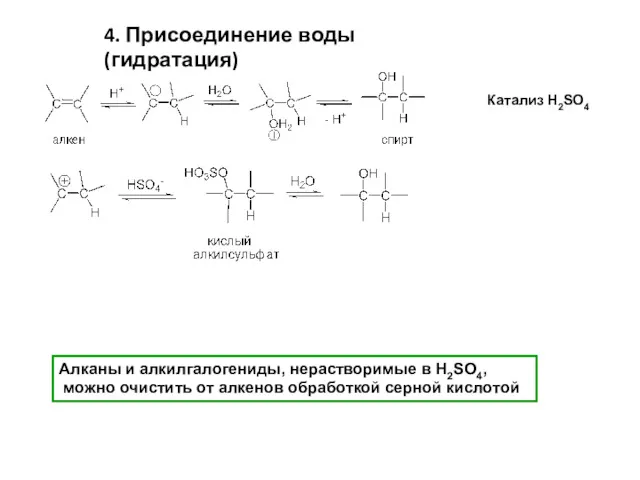
- 8. 4. Присоединение воды (гидратация) Катализ H2SO4 Алканы и алкилгалогениды, нерастворимые в H2SO4, можно очистить от алкенов
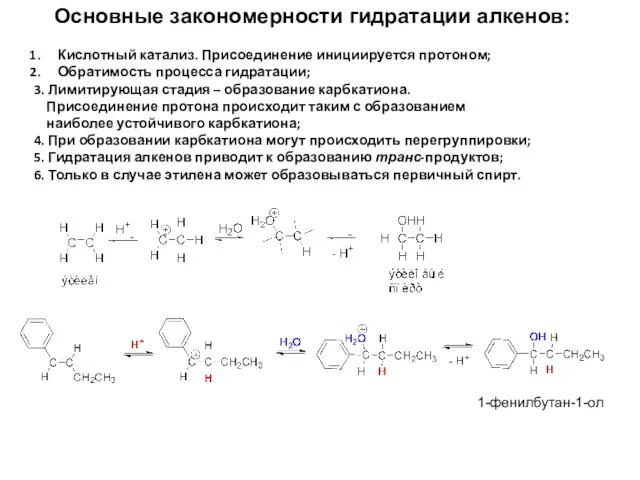
- 9. Основные закономерности гидратации алкенов: Кислотный катализ. Присоединение инициируется протоном; Обратимость процесса гидратации; 3. Лимитирующая стадия –
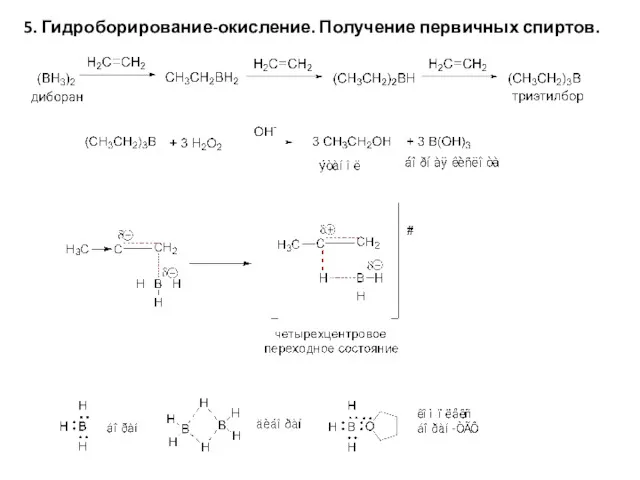
- 10. 5. Гидроборирование-окисление. Получение первичных спиртов.
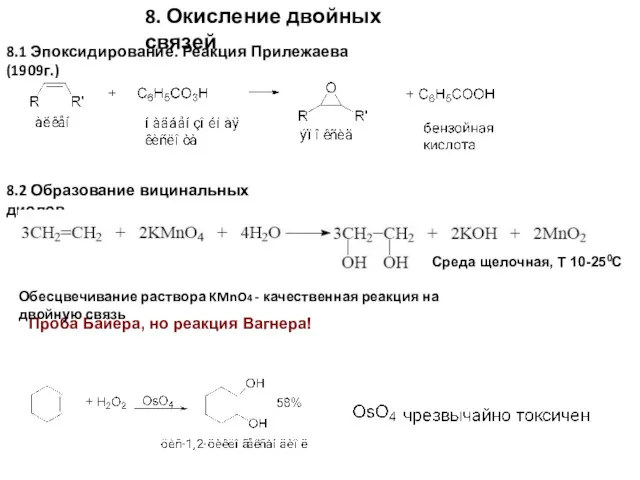
- 11. 8.2 Образование вицинальных диолов 8. Окисление двойных связей 8.1 Эпоксидирование. Реакция Прилежаева (1909г.) Проба Байера, но
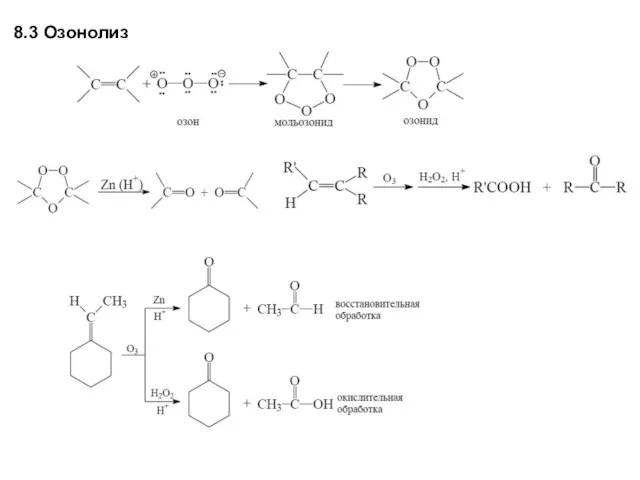
- 12. 8.3 Озонолиз
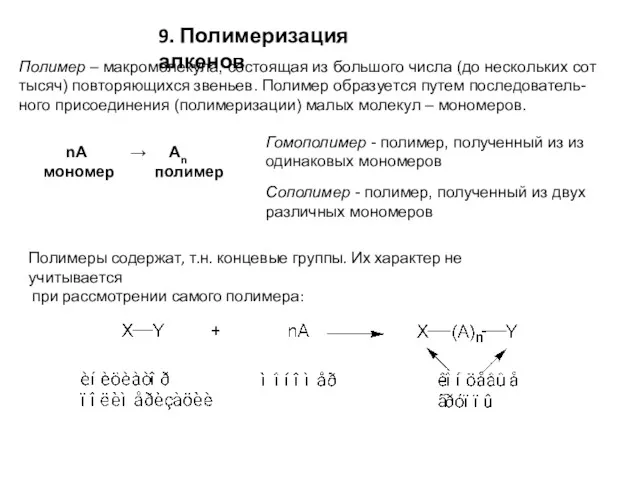
- 13. 9. Полимеризация алкенов Полимер – макромолекула, состоящая из большого числа (до нескольких сот тысяч) повторяющихся звеньев.
- 14. Полимеризация может инициироваться катионамми, анионами, радикалами, металлорганическими соединениями 9.1 Ионная полимеризация Инициаторы катионной полимеризации кислоты Льюиса:
- 16. Скачать презентацию

 Органічні розчинники. Їх застосування
Органічні розчинники. Їх застосування Поверхностные явления. Адсорбция
Поверхностные явления. Адсорбция Обмоточные провода
Обмоточные провода Химический элемент титан
Химический элемент титан Металлы
Металлы Хімія елементів VIIВ групи (Mn, Tc, Re)
Хімія елементів VIIВ групи (Mn, Tc, Re) Электрохимический ряд напряжения металлов
Электрохимический ряд напряжения металлов Строение вещества. Строение атома
Строение вещества. Строение атома Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение
Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение Элементарные частицы вещества
Элементарные частицы вещества Химиялық байланыс және заттардың құрылымдық түрлі сатылары
Химиялық байланыс және заттардың құрылымдық түрлі сатылары Органическая химия. ДО. Глицерин как представитель многоатомных спиртов
Органическая химия. ДО. Глицерин как представитель многоатомных спиртов Волокна. Классификация волокон
Волокна. Классификация волокон Химический состав клетки
Химический состав клетки Химические свойства органических веществ
Химические свойства органических веществ Хлор. Состав. Строение
Хлор. Состав. Строение Багатоядерні ароматичні сполуки
Багатоядерні ароматичні сполуки Металлы. Общие свойства и получение
Металлы. Общие свойства и получение Органика – 4 галогенпроизводные
Органика – 4 галогенпроизводные Минеральные вещества
Минеральные вещества Күйдіргіш натрий
Күйдіргіш натрий Кристаллизация
Кристаллизация Сарқынды сулардан ренийді бөлу әдісі. құмда мысты қайта өңдеу
Сарқынды сулардан ренийді бөлу әдісі. құмда мысты қайта өңдеу Introduction to Biochemistry
Introduction to Biochemistry Stoffe bestehen aus kleinsten teilchen
Stoffe bestehen aus kleinsten teilchen Щелочные металлы
Щелочные металлы Химические свойства спиртов
Химические свойства спиртов Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение
Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение