Содержание
- 2. АТОМ – сложная частица, состоящая из положительно заряженного ядра и электронных оболочек, на которых помещаются отрицательно
- 3. Символы химических элементов представляются обычно в виде: где X – символ элемента; a – массовое число
- 4. Протоны и нейтроны объединяются в компактное ядро за счет ядерных сил, возникновение которых приводит к дефекту
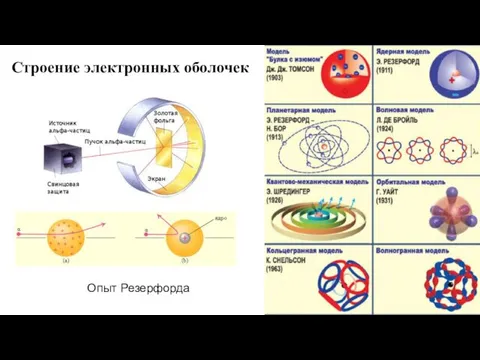
- 5. Строение электронных оболочек Опыт Резерфорда
- 6. Корпускулярно-волновой дуализм электрона (электрон обладает одновременно свойствами частицы и волны). λ – длина волны частицы; m
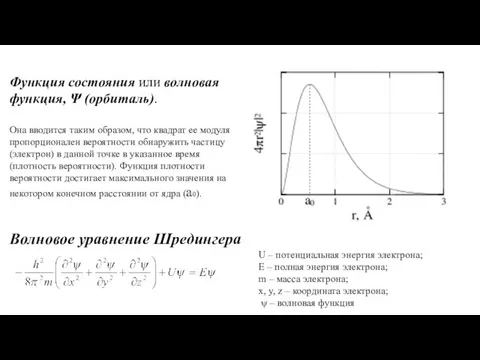
- 7. Функция состояния или волновая функция, Ψ (орбиталь). Она вводится таким образом, что квадрат ее модуля пропорционален
- 8. Решение уравнения Шредингера содержит набор квантовых чисел, характеризующих поведение электрона в атоме. n – главное квантовое
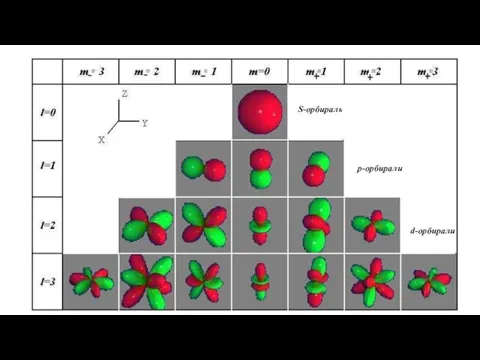
- 9. S-орбираль р-орбирали d-орбирали
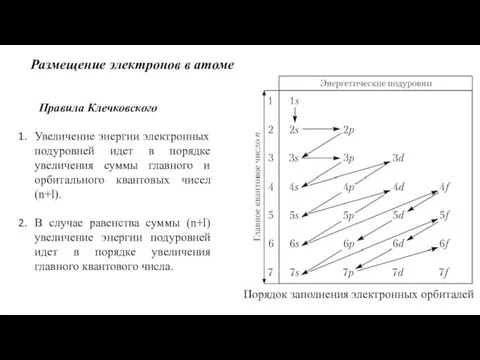
- 10. Размещение электронов в атоме Правила Клечковского Увеличение энергии электронных подуровней идет в порядке увеличения суммы главного
- 11. Принцип Паули В атоме не может существовать двух электронов с одинаковым набором квантовых чисел. Следствием принципа
- 12. Правило Хунда Внутри подуровня электроны заполняют орбитали таким образом, чтобы суммарное спиновое квантовое число было максимальным
- 14. Электронные формулы атомов и ионов: Число электронов в нейтральном атоме равно порядковому номеру элемента в Периодической
- 15. Валентные электроны – это все электроны последнего энергетического уровня и электроны незавершенных подуровней. Число валентных электронов
- 16. Часть 2. СТРОЕНИЕ МОЛЕКУЛ (ХИМИЧЕСКАЯ СВЯЗЬ) Строение вещества
- 17. Химическая связь возникает при взаимодействии атомов, обусловливающем образование химически устойчивой двух- или многоатомной системы (молекулы, кристалла
- 18. Химическая связь между атомами, осуществляемая обобществленными электронами, называется ковалентной связью. Она возникает между одинаковыми атомами, образующими
- 19. Атомы образуют ограниченное число связей, равное их валентности. Это соответствует насыщаемости ковалентной связи. В зависимости от
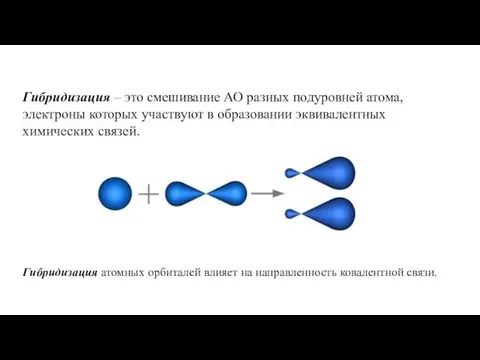
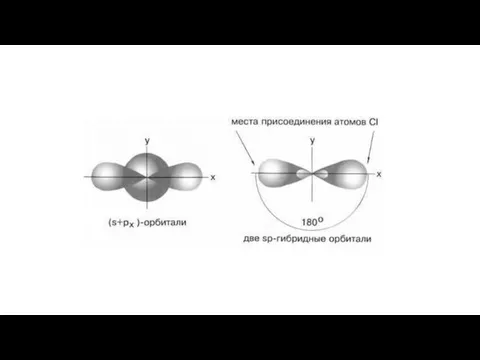
- 20. Гибридизация – это смешивание АО разных подуровней атома, электроны которых участвуют в образовании эквивалентных химических связей.
- 24. Донорно-акцепторный механизм образования ковалентной связи
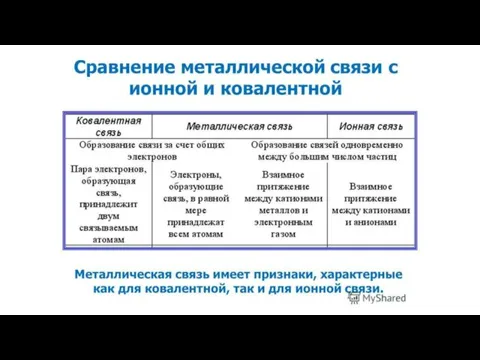
- 25. Ионная связь Ионная связь – это электростатическая связь между ионами противоположных зарядов. Ионная связь может рассматриваться
- 29. Часть 3. Конденсированное состояние (взаимодействие молекул) Строение вещества
- 30. Химическая устойчивость молекул проявляется лишь в системах, где расстояние между молекулами много больше их размеров (r
- 33. Скачать презентацию























 Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Магия кристаллов
Магия кристаллов Пластмаси. Види пластмас. (11 клас)
Пластмаси. Види пластмас. (11 клас) Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ Производство полимеров
Производство полимеров Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте
Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте Геохимия гидротермального процесса
Геохимия гидротермального процесса Защита металлоконструкций от коррозии
Защита металлоконструкций от коррозии Химия металлов: влияние металлов на организм человека
Химия металлов: влияние металлов на организм человека Типы химических реакций
Типы химических реакций Органическая химия
Органическая химия Химия титанорганических соединений
Химия титанорганических соединений Соли и их свойства
Соли и их свойства Соединения серы
Соединения серы Химическая связь
Химическая связь Нанотехнологии в школьном образовании. Семинар учителей химии
Нанотехнологии в школьном образовании. Семинар учителей химии Генетическая связь между классами веществ
Генетическая связь между классами веществ Беломорская соль, проектная работа
Беломорская соль, проектная работа Химические свойства спиртов
Химические свойства спиртов Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока
Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Значение органической химии в жизни человека
Значение органической химии в жизни человека Классификация химических реакций
Классификация химических реакций Полезные геологические химические соединения. Получение меди из малахита
Полезные геологические химические соединения. Получение меди из малахита Механическая смесь и растворы
Механическая смесь и растворы Общая характеристика реакций органических соединений. Кислотные и основные свойства органических соединений
Общая характеристика реакций органических соединений. Кислотные и основные свойства органических соединений Применение солей
Применение солей Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс