Содержание
- 2. это процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и
- 3. По числу и составу реагирующих и образующихся веществ По изменению степени окисления атомов элементов По использованию
- 4. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 1.
- 5. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 2.
- 6. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 3.
- 7. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 4.
- 8. II. По изменению степеней окисления химических элементов: 1. Окислительно-восстановительные реакции – реакции, идущие с изменением степеней
- 9. III. По использованию катализатора: 1. Некаталитические реакции – реакции, идущие без участия катализатора: Классификация химических реакций
- 10. III. По использованию катализатора: 1. Каталитические реакции – реакции, идущие с участием катализатора: Классификация химических реакций
- 11. IV. По тепловому эффекту: 1. Экзотермические реакции протекают с выделением энергии: Классификация химических реакций 4P +
- 12. IV. По тепловому эффекту: 2. Эндотермические реакции протекают с поглощением энергии: Классификация химических реакций N2 +
- 13. V. По направлению протекания реакций: 1.Обратимые реакции - в зависимости от условий могут протекать как в
- 14. V. По направлению протекания реакций: 2.Необратимые реакции - протекают только в прямом направлении, завершаются полным превращением
- 15. VI. По фазовому составу: 1. Гетерогенные реакции – реакции, в которых реагирующие вещества и продукты находятся
- 16. VI. По фазовому составу: 2. Гомогенные реакции – реакции, в которых реагирующие вещества и продукты находятся
- 17. Охарактеризуйте химические реакции по всем признакам: Задание для самостоятельной работы HCl (р-р) +NaOH(р-р) = NaCl +
- 19. Скачать презентацию
 Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты
Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты Геохимия и космохимия: история возникновения и развития, основное содержание и задачи
Геохимия и космохимия: история возникновения и развития, основное содержание и задачи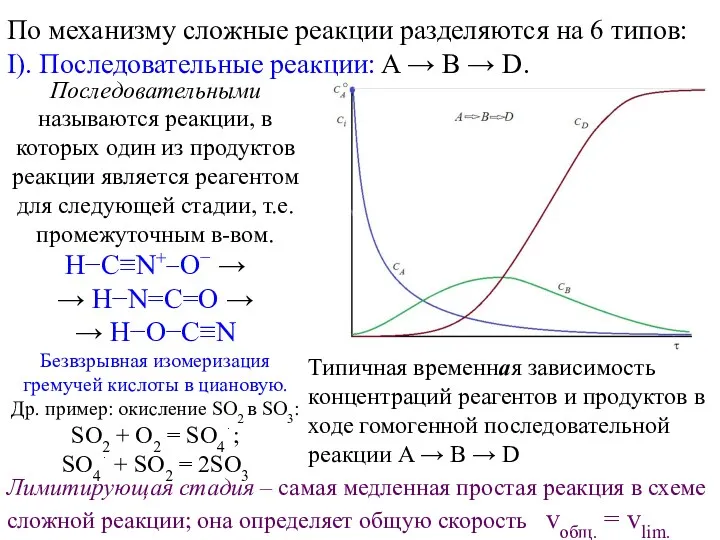 Сложные реакции по механизму
Сложные реакции по механизму Оксиды(1)
Оксиды(1) Галогены. Положение в периодической системе. Химические свойства
Галогены. Положение в периодической системе. Химические свойства Галогены в природе. Хлор, бром, иод
Галогены в природе. Хлор, бром, иод Нанотехнологии в школьном образовании. Семинар учителей химии
Нанотехнологии в школьном образовании. Семинар учителей химии Кристалогідрати. Номенклатура, найважливіші кристалогідрати та їх застосування
Кристалогідрати. Номенклатура, найважливіші кристалогідрати та їх застосування Состояние атмосферного воздуха в Ярославской области
Состояние атмосферного воздуха в Ярославской области Признаки и условия протекания химических реакций
Признаки и условия протекания химических реакций Водневий показник ph
Водневий показник ph Жидкокристаллические композиты ЖКК. Керамические композиционные материалы (ККМ). Углерод-углеродные композиционные (УУКМ)
Жидкокристаллические композиты ЖКК. Керамические композиционные материалы (ККМ). Углерод-углеродные композиционные (УУКМ) Атомы и молекулы
Атомы и молекулы Су қоймасындағы тіршілік үшін темірдің рөлі
Су қоймасындағы тіршілік үшін темірдің рөлі Главная подгруппа IV группы
Главная подгруппа IV группы Химия, как часть естествознания. Предмет химии
Химия, как часть естествознания. Предмет химии Алкадиены
Алкадиены Неметаллы
Неметаллы Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение Медь. Химические свойства. Получение меди. Применение
Медь. Химические свойства. Получение меди. Применение Полимеры (10 класс)
Полимеры (10 класс) Превращения веществ. Роль химии в жизни человека
Превращения веществ. Роль химии в жизни человека Фосфор и его соединения
Фосфор и его соединения 20230816_belki_2
20230816_belki_2 Фосфор
Фосфор Кафедра биохимии УГМУ в прошлом и настоящем. Локализация
Кафедра биохимии УГМУ в прошлом и настоящем. Локализация Электрохимические процессы
Электрохимические процессы Аппаратчик химводоочистки. Билеты для экзамена с ответами (1-16)
Аппаратчик химводоочистки. Билеты для экзамена с ответами (1-16)