Слайд 2

План
1. Що таке водневий показник.
2. Історія винекнення.
3. Методи визначення рн.
Слайд 3
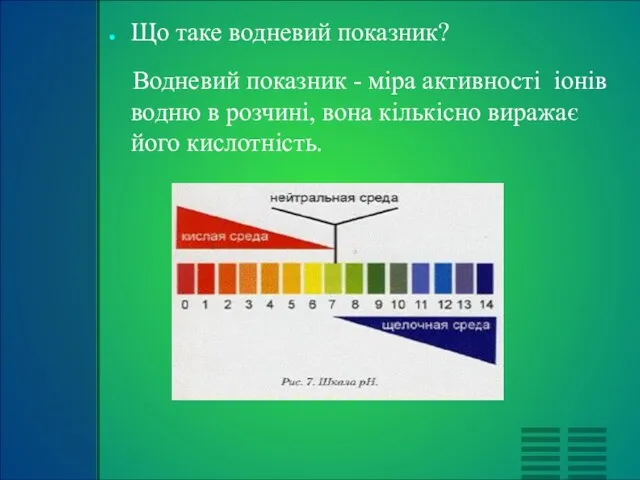
Що таке водневий показник?
Водневий показник - міра активності іонів водню в
розчині, вона кількісно виражає його кислотність.
Слайд 4

Історія винекнення.
Це поняття було введено в 1909 році датським хіміком Серенсеном.
Слайд 5

Показник називається pH, за першими літерами латинських слів potentia hydrogeni -
сила водню, або pondus hydrogenii - вага водню.
Слайд 6

Слайд 7

Для визначення значення pH розчинів широко використовують кілька методик. Водневий показник
можна приблизно оцінювати з допомогою індикаторів або визначати аналітично шляхом, проведенням кислотно-основного титрування.
Слайд 8

1. Кислотно-основні індикатори.
Слайд 9

Для грубої оцінки концентрації водневих іонів широко використовуються кислотно-основні індикатори -
органічні речовини- барвники, колір яких залежить від pH середовища.
Слайд 10

До найбільш відомих індикаторів належать лакмус, фенолфталеїн, метиловий оранжевий (метилоранж)
та інші. Індикатори здатні існувати у двох по-різному пофарбованих формах - або в кислотній, або в основний. Зміна кольору кожного індикатора відбувається в своєму інтервалі кислотності, зазвичай становить 1-2 одиниці.
Слайд 11

2. Універсальний індикатор.
Слайд 12

Для розширення робочого інтервалу вимірювання pH використовують так званий універсальний індикатор,
що представляє собою суміш з кількох індикаторів.
Слайд 13

Універсальний індикатор послідовно змінює колір з червоного через жовтий, зелений, синій
до фіолетового при переході з кислої області в лужну.
Слайд 14

3. Іонометріческій метод.
Слайд 15

Іонометріческій метод визначення pH грунтується на вимірюванні милливольтметром-ионометрии ЕРС гальванічного
ланцюга, що включає спеціальний скляний електрод, потенціал якого залежить від концентрації іонів H + у навколишньому розчині.
Слайд 16

Спосіб відрізняється зручністю і високою точністю, особливо після калібрування індикаторного
електрода в обраному діапазоні рН, дозволяє вимірювати pH непрозорих і кольорових розчинів і тому широко використовується.
Слайд 17

4. Аналітичний об'ємний метод .
Слайд 18

Аналітичний об'ємний метод - кислотно-основне титрування - також дає точні
результати визначення кислотності розчинів. Розчин відомої концентрації (титрант) по краплях додається до досліджуваного розчину. При їх змішуванні протікає хімічна реакції.
Слайд 19

5.Вплив температури на значення pH.
Слайд 20

Вплив температури на значення pH об'яснятеся різної дисоціацією іонів водню
(H +) і не є помилкою експерименту. Температурний ефект неможливо компенсувати за рахунок електроніки pH-метра.
Слайд 21

0.001 моль / Л HCl при 20 C має pH =
3, при 30 C pH = 3
0.001 моль / Л NaOH при 20 C має pH = 11.73, при 30 C pH = 10.83
Слайд 22

Кислотність середовища має важливе значення для безлічі хімічних процесів, і можливість
протікання або результат тієї або іншої реакції часто залежить від pH середовища.





















 Жиры
Жиры Относительная атомная масса. Знаки химических элементов
Относительная атомная масса. Знаки химических элементов Водород. Общая характеристика по плану
Водород. Общая характеристика по плану 20230316_otkrytyy_urok_v_8_kl_geneticheskaya_svyaz.docx
20230316_otkrytyy_urok_v_8_kl_geneticheskaya_svyaz.docx Воспламенение (зажигание) газовых смесей
Воспламенение (зажигание) газовых смесей Периодическая система элементов, предсказание химических свойств элементов на основе таблицы
Периодическая система элементов, предсказание химических свойств элементов на основе таблицы Алкени i Алкіни. Загальна та молекулярні формули, структурна ізомерія, систематична номенклатура
Алкени i Алкіни. Загальна та молекулярні формули, структурна ізомерія, систематична номенклатура Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение Изменение числа электронов на внешнем энергетическом уровне атомов химических элементов. Ионная связь
Изменение числа электронов на внешнем энергетическом уровне атомов химических элементов. Ионная связь Подгруппа азота
Подгруппа азота Непредельные углеводороды: алкены, олефины
Непредельные углеводороды: алкены, олефины Положение металлов в периодической системе химических элементов. Особенности строения их атомов
Положение металлов в периодической системе химических элементов. Особенности строения их атомов Минералы и горные породы
Минералы и горные породы Хімічні явища, їх ознаки
Хімічні явища, їх ознаки Жидкие кристаллы
Жидкие кристаллы Карбоновые кислоты. Нахождение в природе
Карбоновые кислоты. Нахождение в природе Структура легированной стали
Структура легированной стали Строение атома в соответствии с положением в периодической системе химических элементов Д.И. Менделеева
Строение атома в соответствии с положением в периодической системе химических элементов Д.И. Менделеева Химические уравнения
Химические уравнения Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2)
Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2) Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе
Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе Антибиотики как ЛС
Антибиотики как ЛС КСЕ. Концепции химии. (Лекция 6)
КСЕ. Концепции химии. (Лекция 6) Азотсодержащие органические соединения. Амины
Азотсодержащие органические соединения. Амины Относительная атомная масса химических элементов. Знаки химических элементов
Относительная атомная масса химических элементов. Знаки химических элементов Кристаллическое строение и свойства металлов
Кристаллическое строение и свойства металлов Оксид углерода II. Угарный газ
Оксид углерода II. Угарный газ Обобщение и систематизация по теме Соединения химических элементов. 8 класс
Обобщение и систематизация по теме Соединения химических элементов. 8 класс