Периодическая система элементов, предсказание химических свойств элементов на основе таблицы презентация
Содержание
- 2. Немецкий химик Иоганн Вольфганг Дёберейнер родился 15 декабря 1780 г. в баварском городке Хоф в семье
- 3. В 1829 г немецкий химик Иоган Вольфганг Дёберейнер сформулировал закон триад.
- 4. Разбить все известные элементы на триады Дёберейнеру, естественно, не удалось, тем не менее, закон триад явно
- 5. Немецкий химик Леопольд Гмелин родился 2 августа 1788 г. в Гёттингене в семье известного химика и
- 6. В 1843 г Леопольд Гмелин привёл таблицу химически сходных элементов, расставленных по группам в порядке возрастания
- 7. Таблица Леопольда Гмелина
- 8. Джон Александр Рейна Ньюлендс родился в Лондоне 26 ноября 1837 г. Отец, шотландский священник Уильям Ньюлендс,
- 9. Джон Александр Рейна Ньюлендс в1864 г. опубликовал таблицу элементов, отражающую предложенный им закон октав. Ньюлендс показал,
- 10. Таблица Ньюлендса
- 11. Английский химик Уильям Одлинг родился 5 сентября 1829 г. в Саутуорке, близ Лондона. В 1846-1850 гг.
- 12. В 1864 году Уильям Одлинг, пересмотрев предложенную им в 1857 г. систематику элементов, основанную на эквивалентных
- 13. Таблица Одлинга
- 14. Юлиус Лотар Мейер родился 19 августа 1830 года в семье врача в маленьком городке Фареле в
- 15. В 1870 г. Юлиус Лотар Мейер опубликовал свою первую таблицу, в которую включены 42 элемента (из
- 16. Таблица Майера
- 17. Дмитрий Иванович Менделеев родился 8 февраля 1834 г. в г. Тобольске, в семье директора гимназии и
- 18. В марте 1869 г. русский химик Дмитрий Иванович Менделеев представил Русскому химическому обществу периодический закон химических
- 19. Первая таблица Д.И.Менделеева, 1869 г
- 20. В 1871 г. Менделеев в итоговой статье "Периодическая законность химических элементов" дал формулировку Периодического закона: «Свойства
- 21. В конце 1870 г. Менделеев доложил РХО статью "Естественная система элементов и применение её к указанию
- 22. Распространённее других являются 3 формы таблицы Менделеева: «короткая» (короткопериодная) «длинная» (длиннопериодная) «сверхдлинная». В «сверхдлинном» варианте каждый
- 25. Вторая формулировка Периодического закона Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от
- 26. Третья формулировка Периодического закона Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от
- 27. ВОПРОС №2: Типы химической связи.
- 28. Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы
- 29. Ионная связь – это электростатическое притяжение между ионами; Возникает между атомами, имеющими большую разность электроотрицательности (более
- 30. Вещества с ионной связью при н.у. находятся в твердом агрегатном состоянии и образуют кристаллы с ионной
- 31. Ковалентная связь – это связь между атомами, возникающая за счет образования общих электронных пар. По обменному
- 32. Число общих электронных пар равно числу связей между двумя атомами, или кратности связи Простая (одинарная связь)
- 33. Полярность ковалентной связи степень смещенности общих электронных пар к одному из связанных ими атомов электроотрицательность (ЭО)
- 34. Металлы образуют металлические кристаллические решетки, в узлах которых находятся катион-атомы, а между ними «электронный газ», определяющий
- 36. ВОПРОС №3: Типы химических реакций, правила протекания химических реакций; современные представления о скорости химических реакций.
- 37. Химическая реакция - превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому
- 38. Условия которые должны выполняться, чтобы произошла химическая реакция: 1. Необходимо, чтобы реагирующие вещества соприкоснулись и чем
- 39. Типы химических реакций
- 40. Реакции соединения – химические реакции, в которых из двух или нескольких менее сложных по элементному составу
- 41. Реакция разложения - это реакции, в результате которых сложное вещество разлагается на несколько других, более простых
- 42. Реакция, протекающая между простыми и сложными веществами, при которой атомы простого вещества замещают атомы одного из
- 43. Реакция, протекающая между двумя сложными веществами, при которой атомы или группы атомов одного вещества замещают атомы
- 45. По тепловому эффекту химические реакции бывают:
- 46. По присутствию других веществ химические реакции бывают:
- 47. ВОПРОС №4: Химические системы: растворы, дисперсные системы электрохимические системы, катализаторы и каталитические системы, полимеры.
- 49. Растворы - однородные смеси переменного состава. Растворы Жидкие - воды озер, рек, морей, нефть и др.
- 50. Дисперсными называют гетерогенные системы, в которых одно вещество в виде очень мелких частиц равномерно распределено в
- 51. Дисперсные системы классифицируются по агрегатным состояниям дисперсной фазы и дисперсной среды:
- 52. Полимеры - высокомолекулярные соединения, которые характеризуются молекулярной массой от нескольких тысяч до многих миллионов. Молекулы полимеров,
- 53. Электрохимические процессы – это процессы взаимного превращения двух видов энергии. Химической в электрическую – химические источники
- 54. а – равновесная электрохимическая система; б – химический источник тока; в – электрохимическая ванна; 1 –
- 55. Катализ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализаторы -
- 56. ВОПРОС №5: Кислотно-основные и окислительно-восстановительные свойства веществ.
- 57. Любое вещество в определенных условиях может проявлять свойства кислоты и основания по отношению к какому-либо другому
- 61. Окислительно-восстановительные свойства вещества связаны с процессом отдачи и приема электронов атомами, ионами или молекулами. Окислитель -
- 62. Окисление - процесс отдачи электронов атомом, молекулой или ионом. Атом превращается в положительно заряженный ион: Zn0
- 63. Восстановление - процесс присоединения электронов атомом, молекулой или ионом. Атом превращается в отрицательно заряженный ион S0
- 64. Восстановители - атомы, молекулы или ионы, отдающие электроны. Они в процессе ОВР окисляются. Типичные восстановители: ●
- 65. Окислители - атомы, молекулы или ионы, присоединяющие электроны. Они в процессе ОВР восстанавливаются. Типичные окислители: ●
- 66. Значение окислительно-восстановительных реакций (ОВР) ОВР чрезвычайно распространены. С ними связаны процессы обмена веществ в живых организмах,
- 67. ВОПРОС №6: Основные процессы, протекающие в электрохимических системах, процессы коррозии и методы борьбы с коррозией.
- 68. Электрохимические процессы Химические источники тока - аккумуляторы, - топливные элементы Электрические методы получения различных материалов -
- 69. Коррозия металлов (от латинского corrodere - грызть) – процессы, происходящие в результате химического воздействия окружающей среды,
- 70. Химическая Коррозия бывает двух видов: Электрохимическая
- 71. Разрушение металла окислением его в окружающей среде при контакте с газами и электролитами без возникновения электрического
- 72. Разрушение металла в среде электролита с возникновением внутри системы электрического тока Электрохимическая коррозия Пример: Zn2 +
- 73. Всегда требуется наличие контакта двух металлов и электролита, как, например, при ржавлении железа во влажной атмосфере
- 74. Коррозия приводит ежегодно к миллиардным убыткам. Основной ущерб заключается в огромной стоимости изделий, разрушаемых коррозией. Ежегодные
- 76. Скачать презентацию
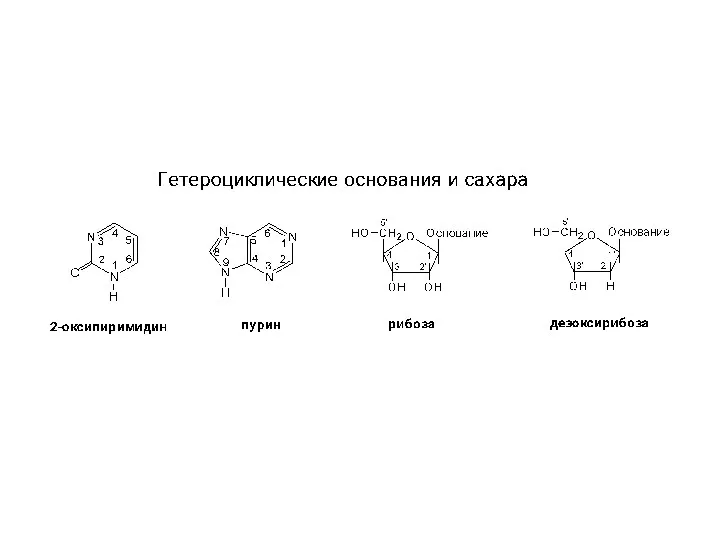 Структура гетероциклов, нуклеозидов и нуклеотидов
Структура гетероциклов, нуклеозидов и нуклеотидов Тепловой эффект химических реакций
Тепловой эффект химических реакций Чистые вещества и смеси
Чистые вещества и смеси Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Применение серной кислоты
Применение серной кислоты Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Технология промышленных газов
Технология промышленных газов Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі
Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі Свойства смесей ПАВ
Свойства смесей ПАВ Гідроліз солей
Гідроліз солей Rhodium
Rhodium Неметаллы. Элементы неметаллы в ПСХЭ
Неметаллы. Элементы неметаллы в ПСХЭ 20230205_metally_pobochnyh_podgrupp
20230205_metally_pobochnyh_podgrupp Основы общей химии. Тема 1
Основы общей химии. Тема 1 Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу
Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу Речовини. Молекули. Атоми
Речовини. Молекули. Атоми Кислоты и их свойства
Кислоты и их свойства Аминокислоты
Аминокислоты Материаловедение. Контрольная работа
Материаловедение. Контрольная работа Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары
Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары Искусственные полимеры
Искусственные полимеры Химическое загрязнение атмосферы
Химическое загрязнение атмосферы Возобновляемое сырье органической химии
Возобновляемое сырье органической химии Промежуточные фазы в металлических сплавах
Промежуточные фазы в металлических сплавах Сорбционные процессы
Сорбционные процессы Современные положения теории А.М. Бутлерова
Современные положения теории А.М. Бутлерова Решение экспериментальных задач по теме Металлы и их соединения. Практическая работа №4
Решение экспериментальных задач по теме Металлы и их соединения. Практическая работа №4 Свойства металлов
Свойства металлов