Содержание
- 2. К основным промышленным газам, получившим самое широкое распространение, относят: · Обычный воздух, представляющий собой смесь азота
- 3. К понижению температуры холодильного агента приводят следующие группы процессов: ♦фазовые превращения – испарение, плавление, возгонка, растворение
- 5. Охлаждение до температуры объекта или вещества, температура Т которого меньше температуры окружающей среды Т0 (Т ♦при
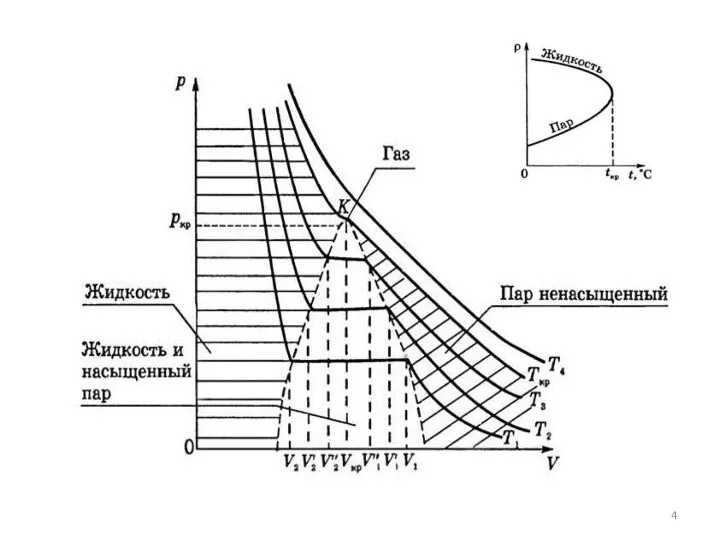
- 6. Работа холодильных установок основана на различии свойств идеальных и реальных газов. Уравнение состояния идеальных газов при
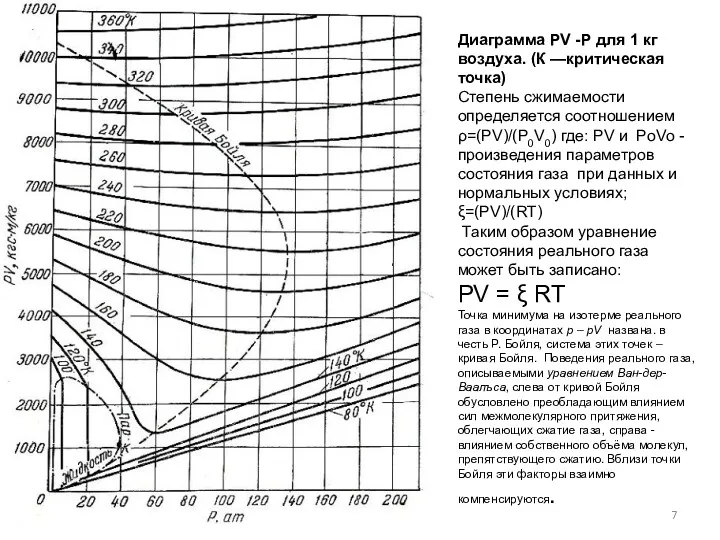
- 7. Диаграмма PV -Р для 1 кг воздуха. (К —критическая точка) Степень сжимаемости определяется соотношением ρ=(PV)/(P0V0) где:
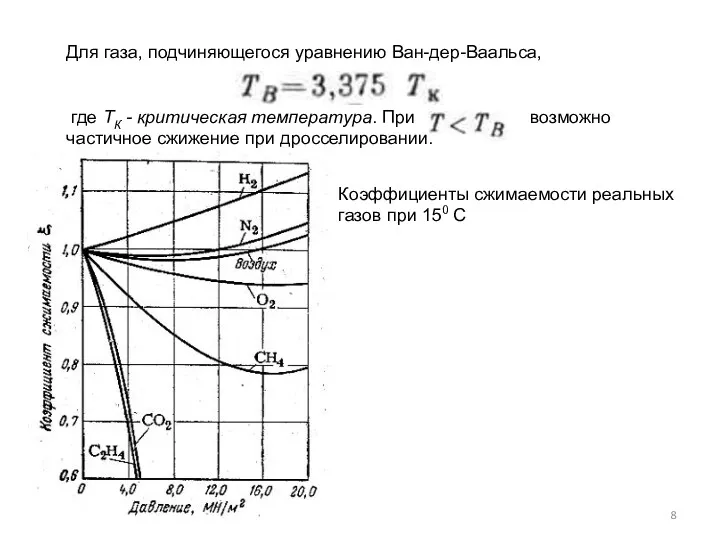
- 8. Для газа, подчиняющегося уравнению Ван-дер-Ваальса, где TК - критическая температура. При возможно частичное сжижение при дросселировании.
- 9. Дросселирование газа. Джоуль и Томсон определили величину изменения температуры реальных газов при их дросселировании. Процесс дросселирования
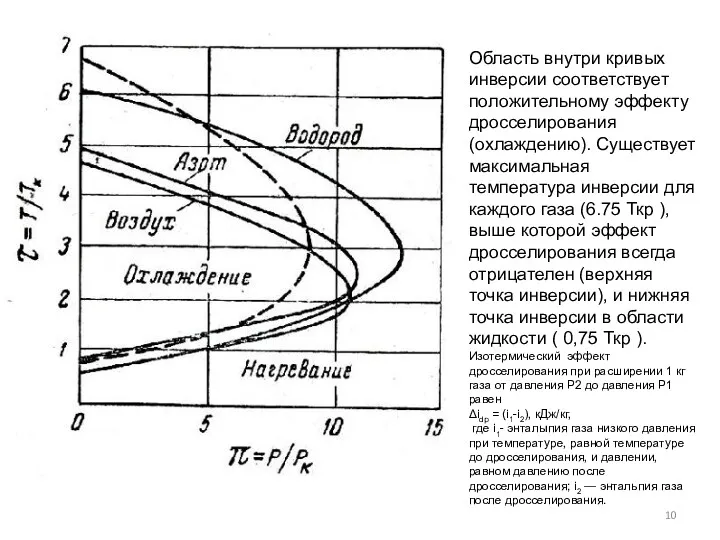
- 10. Область внутри кривых инверсии соответствует положительному эффекту дросселирования (охлаждению). Существует максимальная температура инверсии для каждого газа
- 11. Изоэнтропийное расширение газов. Процесс расширения газа с отдачей внешней работы протекает адиабатически при постоянной энтропии. Дифференциальный
- 12. По назначению циклы охлаждения можно подразделить на рефрижераторные, ожижительные и газоразделительные. Рефрижераторные циклы предназначены для охлаждения
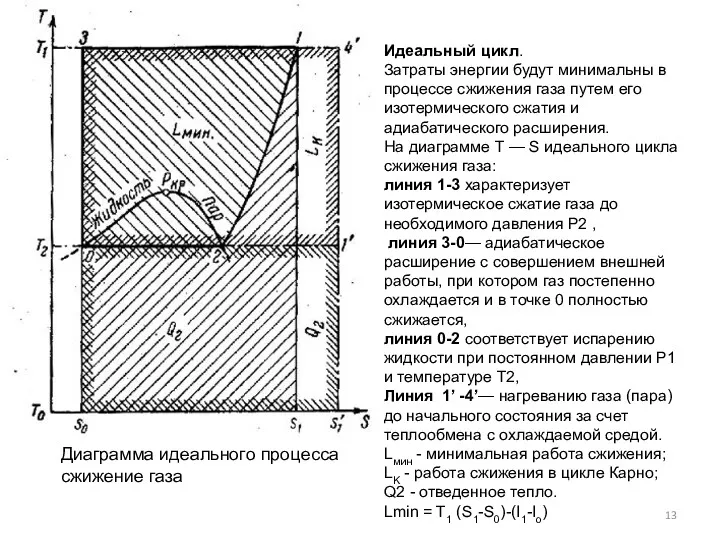
- 13. Идеальный цикл. Затраты энергии будут минимальны в процессе сжижения газа путем его изотермического сжатия и адиабатического
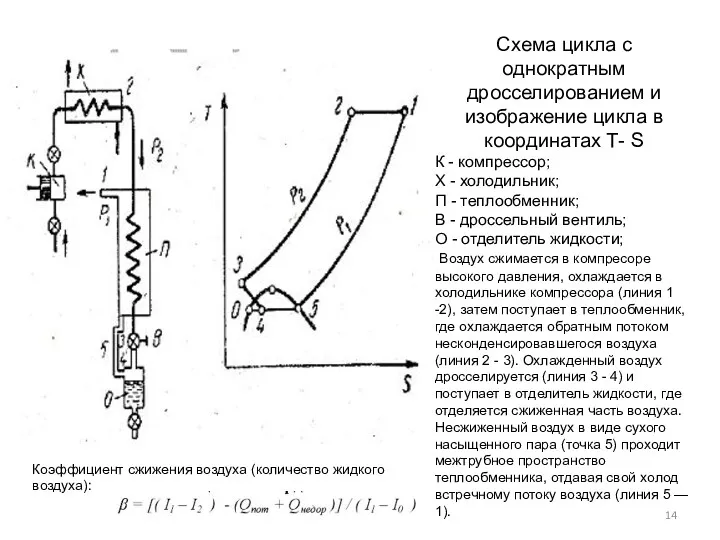
- 14. Схема цикла с однократным дросселированием и изображение цикла в координатах Т- S К - компрессор; X
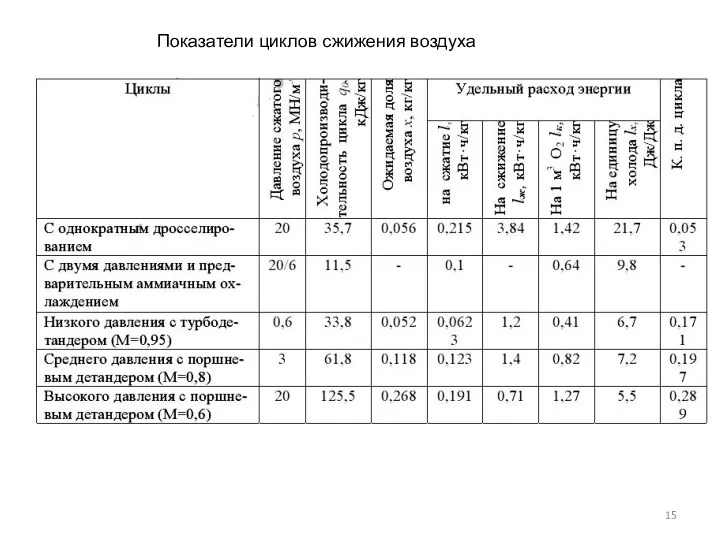
- 15. Показатели циклов сжижения воздуха
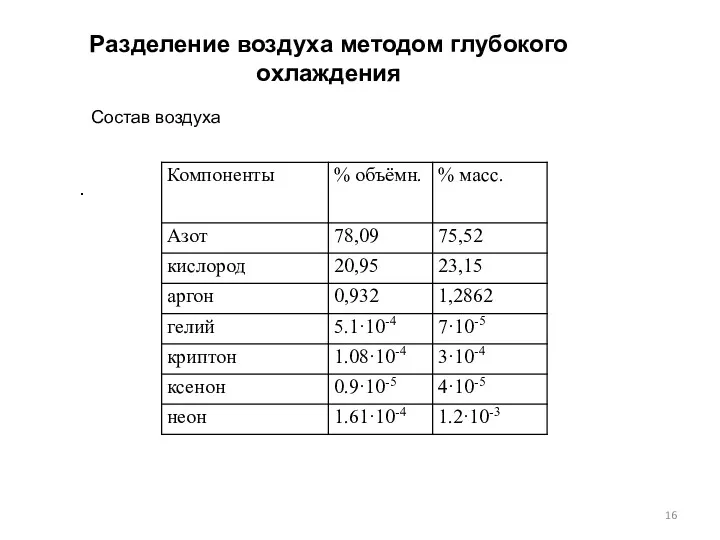
- 16. . Разделение воздуха методом глубокого охлаждения Состав воздуха
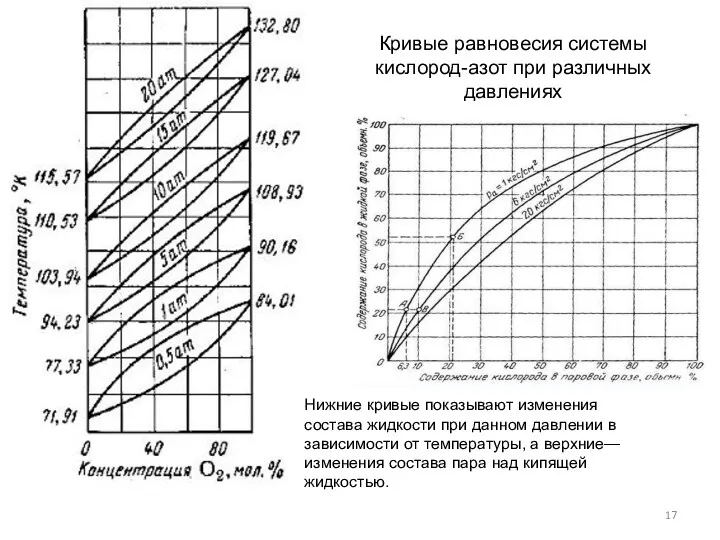
- 17. Кривые равновесия системы кислород-азот при различных давлениях Нижние кривые показывают изменения состава жидкости при данном давлении
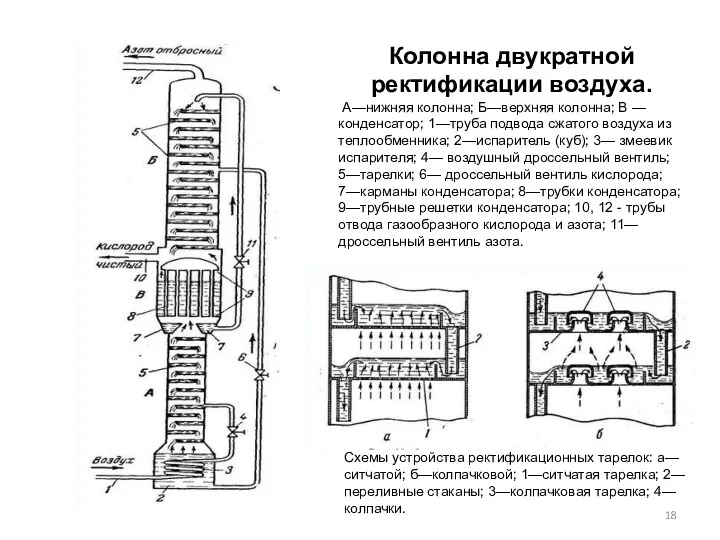
- 18. Колонна двукратной ректификации воздуха. А—нижняя колонна; Б—верхняя колонна; В — конденсатор; 1—труба подвода сжатого воздуха из
- 19. Осушка воздуха производится следующими способами: 1. Путем адсорбции на силикагеле, содержание воды после него должно быть
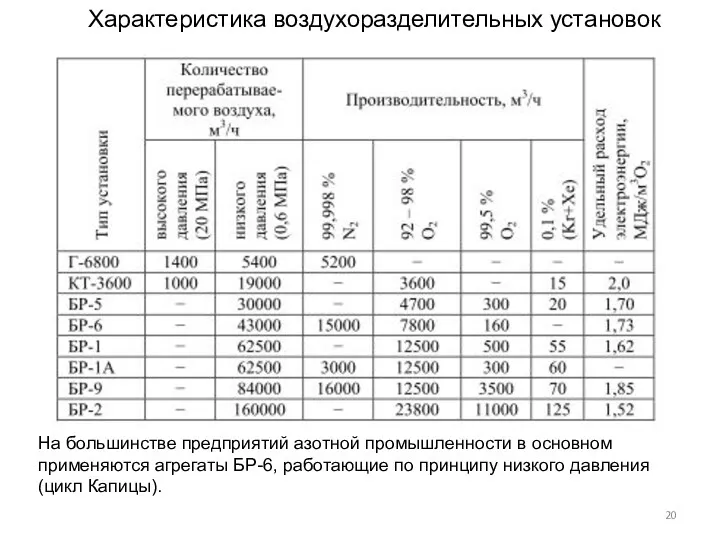
- 20. Характеристика воздухоразделительных установок На большинстве предприятий азотной промышленности в основном применяются агрегаты БР-6, работающие по принципу
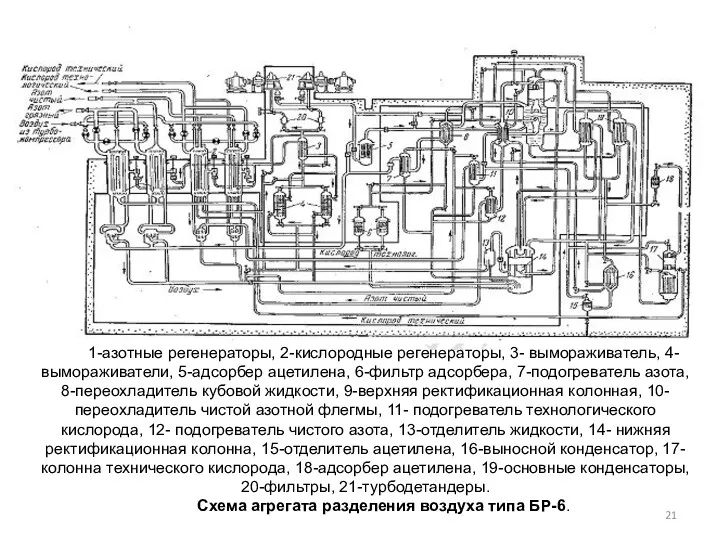
- 21. 1-азотные регенераторы, 2-кислородные регенераторы, 3- вымораживатель, 4-вымораживатели, 5-адсорбер ацетилена, 6-фильтр адсорбера, 7-подогреватель азота, 8-переохладитель кубовой жидкости,
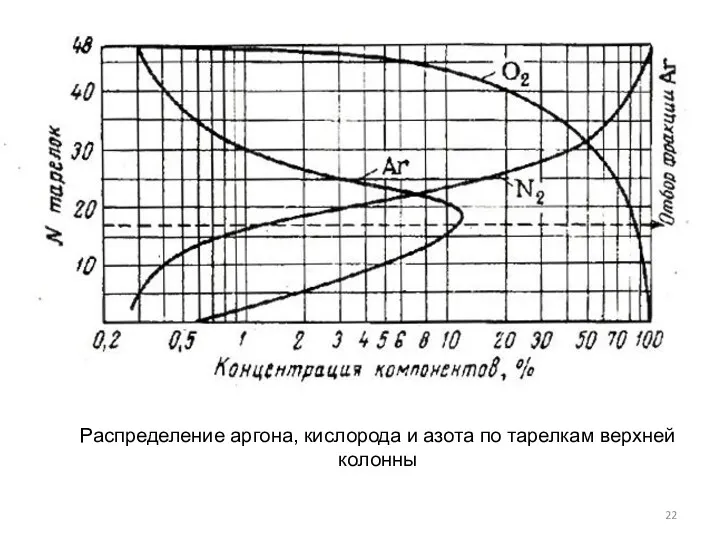
- 22. Распределение аргона, кислорода и азота по тарелкам верхней колонны
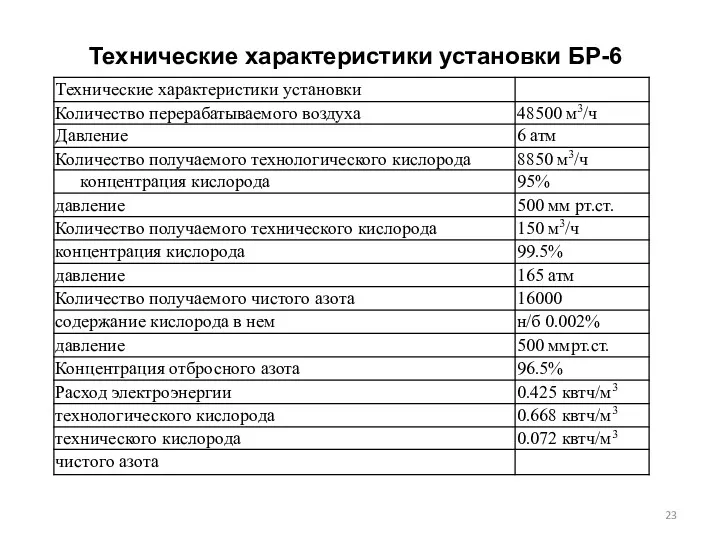
- 23. Технические характеристики установки БР-6
- 25. Способы получения водорода В настоящее время можно выделить 10 методов получения водорода: 1. Парофазная конверсия метана
- 26. Получение азото-водородной смеси методом глубокого охлаждения коксового газа Состав коксового газа
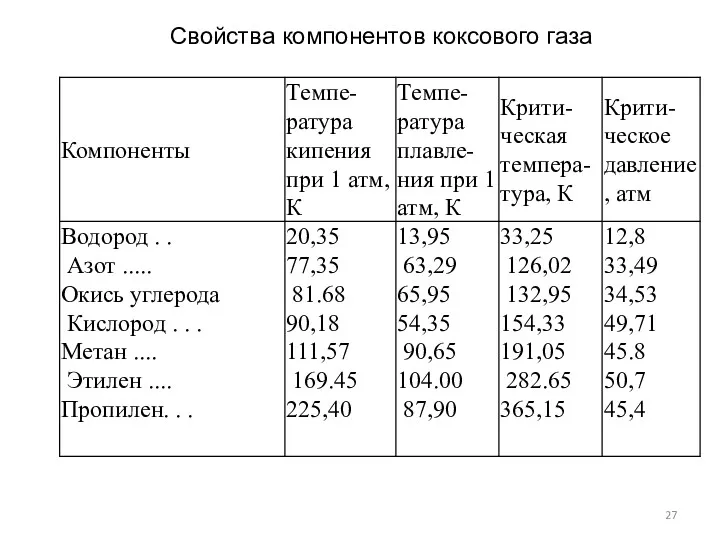
- 27. Свойства компонентов коксового газа
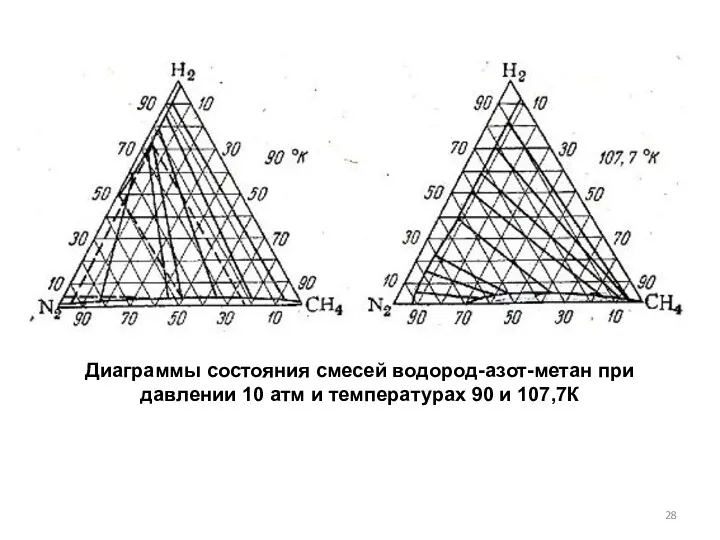
- 28. Диаграммы состояния смесей водород-азот-метан при давлении 10 атм и температурах 90 и 107,7К
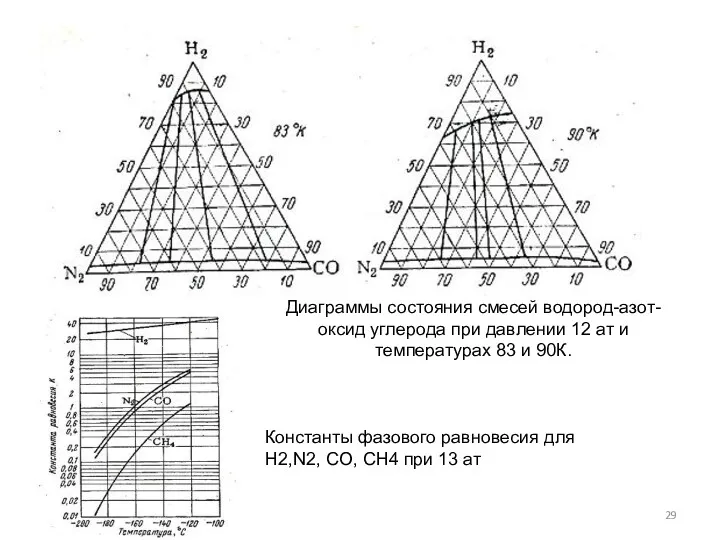
- 29. Диаграммы состояния смесей водород-азот-оксид углерода при давлении 12 ат и температурах 83 и 90К. Константы фазового
- 30. Состав фракций коксового газа
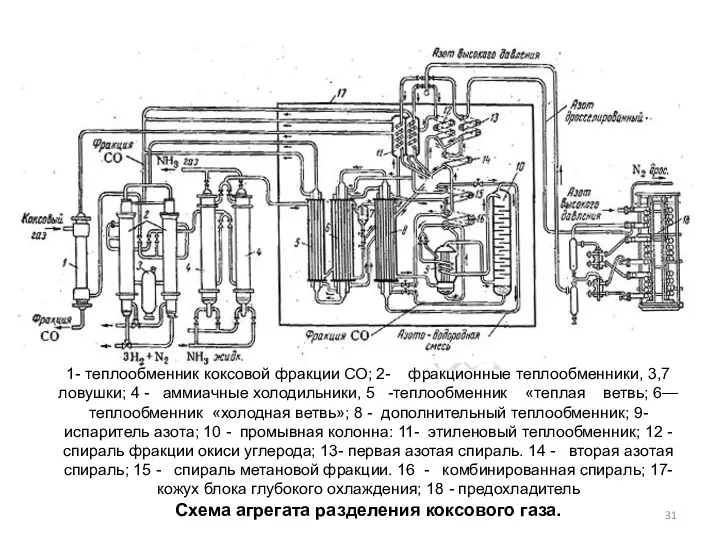
- 31. 1- теплообменник коксовой фракции СО; 2- фракционные теплообменники, 3,7 ловушки; 4 - аммиачные холодильники, 5 -теплообменник
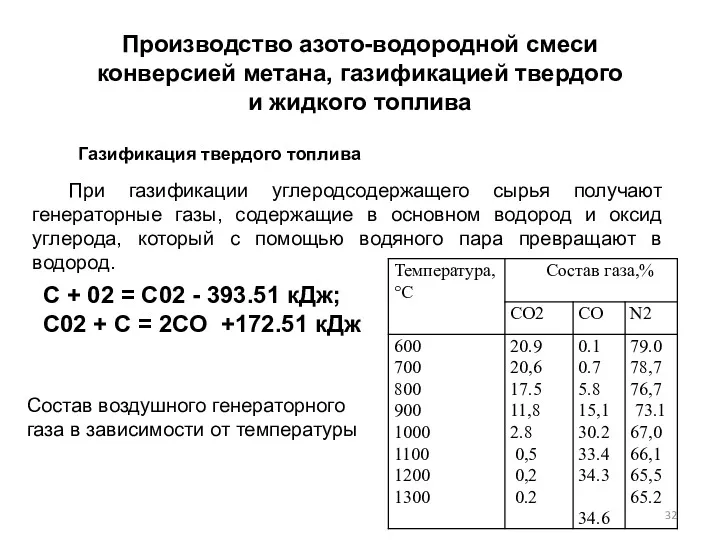
- 32. Производство азото-водородной смеси конверсией метана, газификацией твердого и жидкого топлива Газификация твердого топлива При газификации углеродсодержащего
- 33. С+H20 =СО + Н2 - 131.4 кДж Поскольку эта реакция эндотермична, температура слоя топлива в генераторе
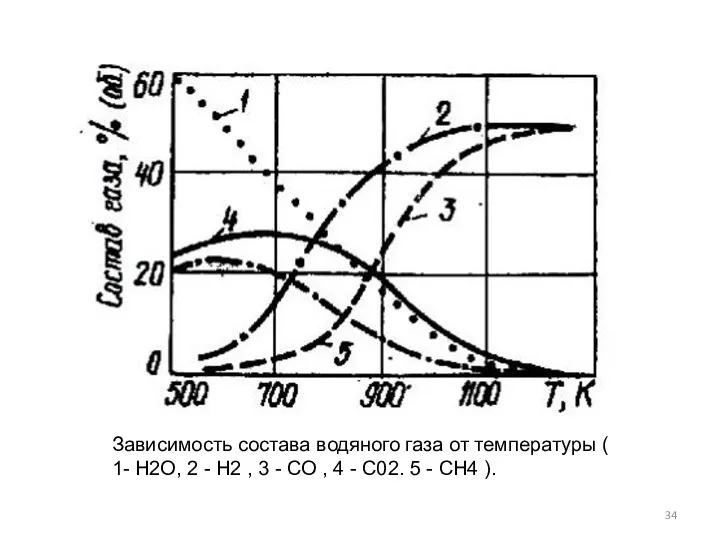
- 34. Зависимость состава водяного газа от температуры ( 1- Н2О, 2 - Н2 , 3 - СО
- 35. Конверсия метана Большинство заводов синтеза аммиака использует для получения азотоводородной смеси природный газ, основной компонент которого
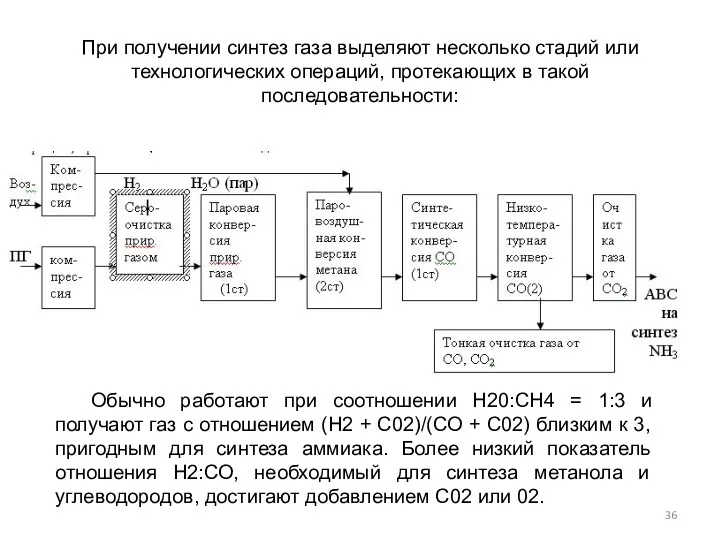
- 36. При получении синтез газа выделяют несколько стадий или технологических операций, протекающих в такой последовательности: Обычно работают
- 37. Основные недостатки паровой конверсии: высокая стоимость перегретого водяного пара; образование значительных избыточных количеств С02; 3) получаемый
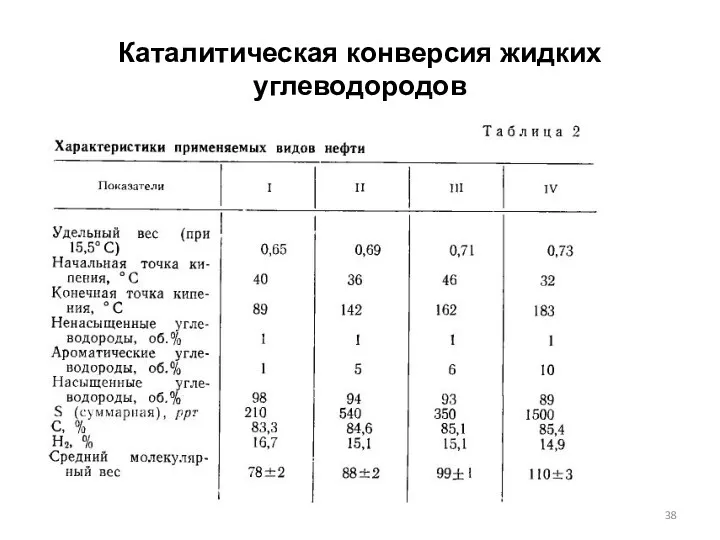
- 38. Каталитическая конверсия жидких углеводородов
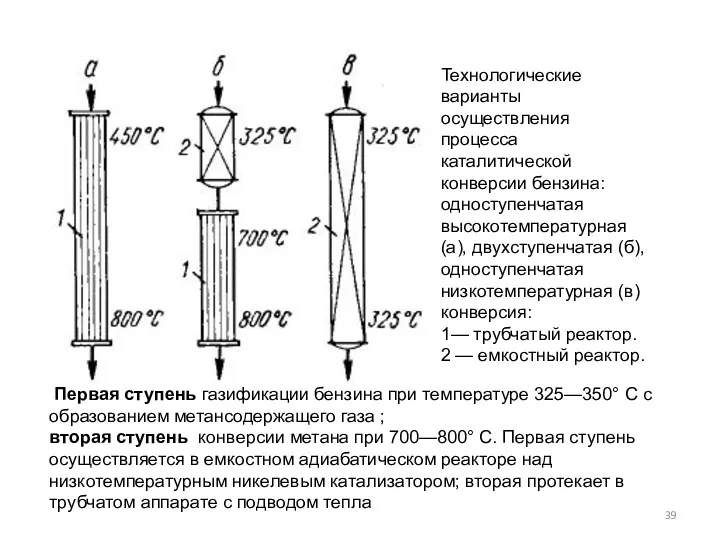
- 39. Технологические варианты осуществления процесса каталитической конверсии бензина: одноступенчатая высокотемпературная (а), двухступенчатая (б), одноступенчатая низкотемпературная (в) конверсия:
- 40. Первоначально углеводороды адсорбируются на никелевой поверхности, где происходит их разрыв на отдельные фрагменты, состоящие из одного
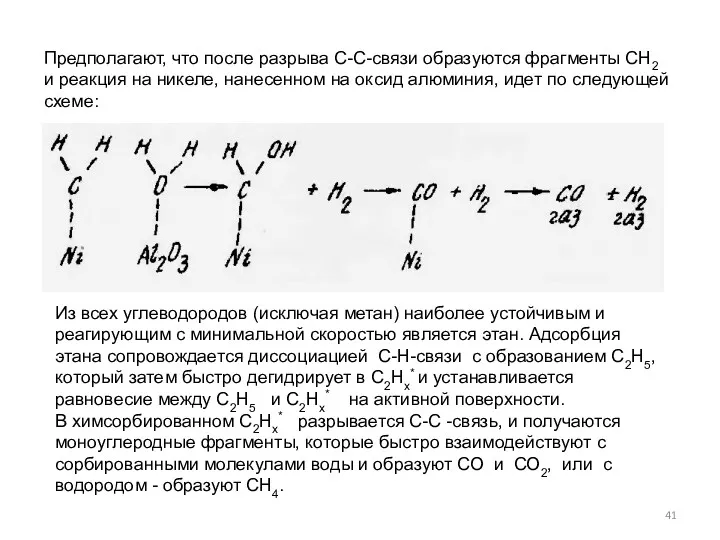
- 41. Предполагают, что после разрыва С-С-связи образуются фрагменты CН2 и реакция на никеле, нанесенном на оксид алюминия,
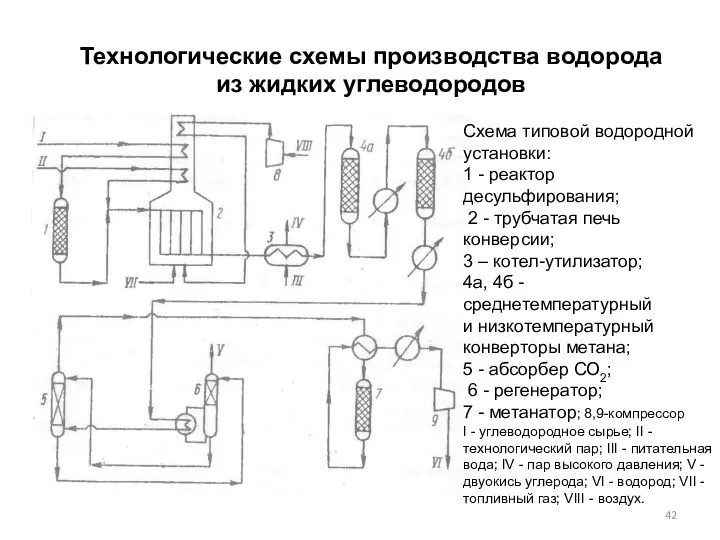
- 42. Технологические схемы производства водорода из жидких углеводородов Схема типовой водородной установки: 1 - реактор десульфирования; 2
- 44. Очистка газа от катализаторных ядов. Общий технологический подход к процессам очистки можно разделить на три метода:
- 45. 2. Адсорбционный метод основан на селективном извлечении примесей твердыми поглотителями - адсорбентами. Поглотительная способность твердого вещества
- 46. Степень очистки газов обусловливается технологическими требованиями и в каждом конкретном случае квалифицируется на грубую, среднюю и
- 47. Очистка от соединений серы. Углеводордные газы различных месторождений, кроме сероводорода H2S, могут содержать сероуглерод CS2, серооксид
- 48. Щелочная очистка от серы. Достаточно эффективным и экономичным способом удаления сернистых соединений является щелочная очистка. Она
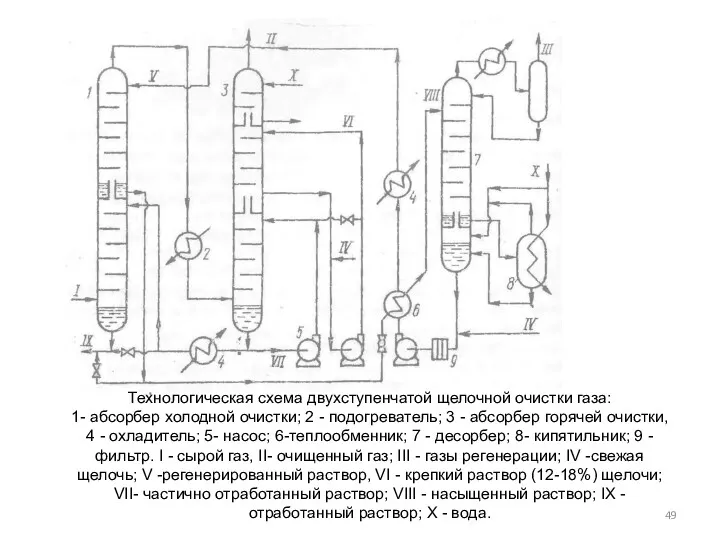
- 49. Технологическая схема двухступенчатой щелочной очистки газа: 1- абсорбер холодной очистки; 2 - подогреватель; 3 - абсорбер
- 50. Сухие методы очистки газа от серы. В качестве твердых поглотителей используются оксиды цинка, меди, марганца, синтетические
- 51. Очистка газа гидроксидом железа основана на реакции: 2Fe(OH)3 + 3H2S = Fe2S3 + 6Н20 Очистку газа
- 52. Очистка углеводородов от серы на активированном угле. Очистка заключается в каталитическом окислении сероводорода кислородом до элементарной
- 53. Регенерацию углей производят раствором сернистого аммония, включающего 110-120 кг/м3 аммиака и 75-80 кг/м3 сульфидной серы. В
- 54. Жидкостные методы очистки газа от серы При содержании в газе 20-40 г/м3 сернистых соединений применяют мышьяково-содовый
- 55. Очистка технологических газов от кислородсодержащих соединений. Кислородсодержащие соединения являются ядами для катализаторов синтеза аммиака и метанола.
- 56. Очистка газа промывкой водой под давлением С02 и H2S достаточно хорошо растворяются в воде по сравнению
- 57. Химические методы очистки. Большинство химических методов основано на абсорбции этих примесей растворами химических реагентов, а в
- 58. В современной технологии переработки природного газа очистка от оксида углерода (4) с использованием аминоспиртов занимает первое
- 59. Практически для извлечения двуокиси углерода из конвертированного газа применяются 12 -35%-ные растворы моноэтаноламина. В зависимости от
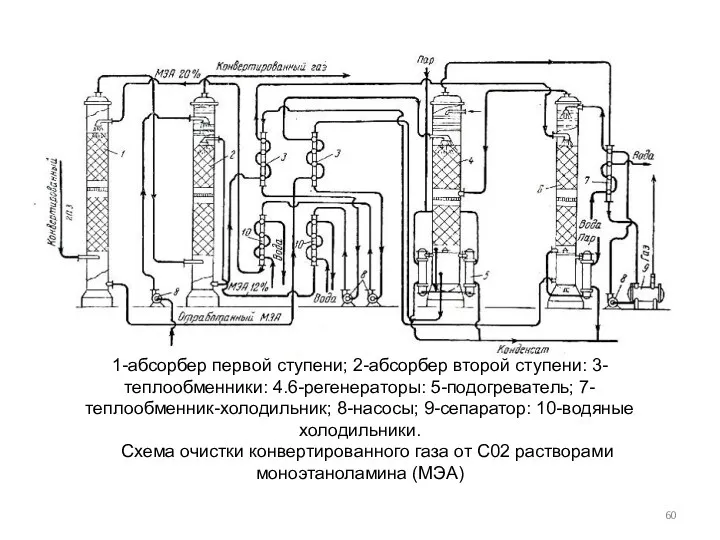
- 60. 1-абсорбер первой ступени; 2-абсорбер второй ступени: 3-теплообменники: 4.6-регенераторы: 5-подогреватель; 7-теплообменник-холодильник; 8-насосы; 9-сепаратор: 10-водяные холодильники. Схема очистки
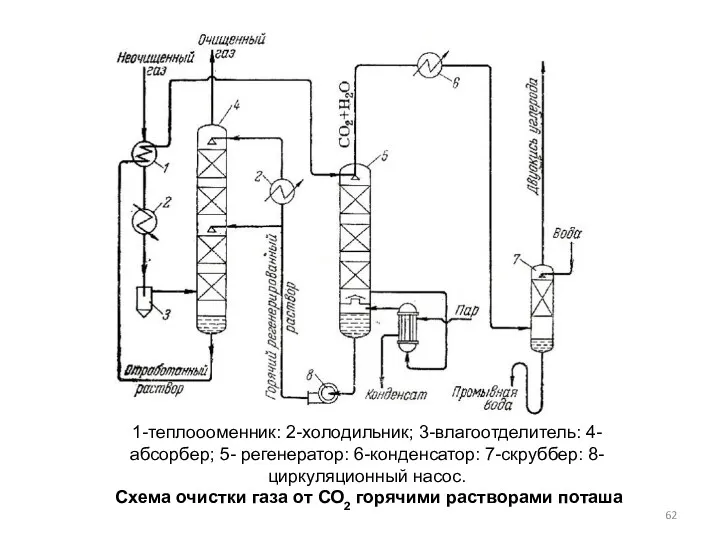
- 61. Очистка газа от С02 горячими растворами поташа При поглощении двуокиси углерода карбонатами натрия или калия происходит
- 62. 1-теплоооменник: 2-холодильник; 3-влагоотделитель: 4-абсорбер; 5- регенератор: 6-конденсатор: 7-скруббер: 8-циркуляционный насос. Схема очистки газа от СО2 горячими
- 63. Наибольшее применение получил метод очистки горячим раствором поташа при давлении 2.56-2.96 МПа и концентрации К2СО3 25-30%
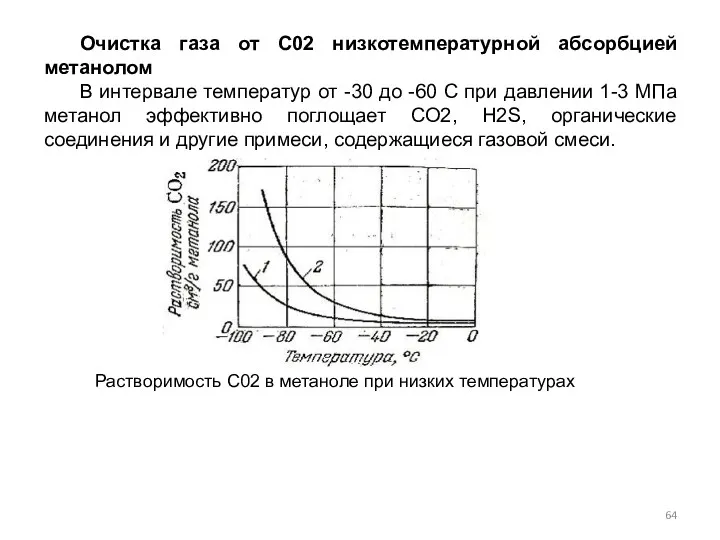
- 64. Очистка газа от С02 низкотемпературной абсорбцией метанолом В интервале температур от -30 до -60 С при
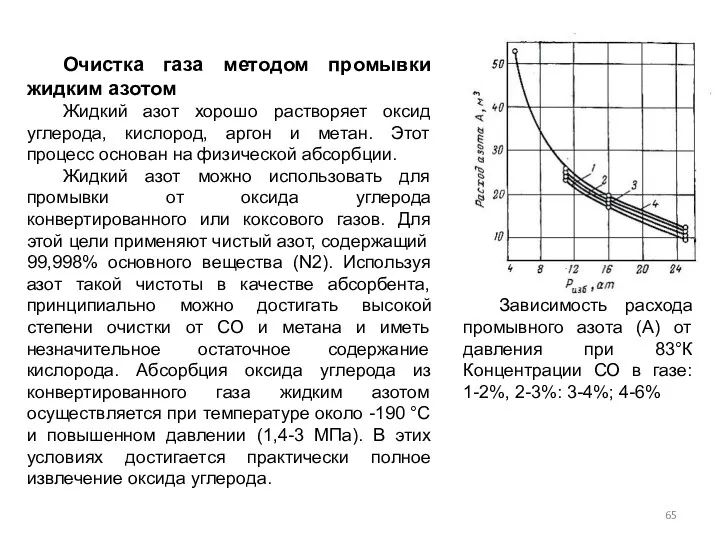
- 65. Очистка газа методом промывки жидким азотом Жидкий азот хорошо растворяет оксид углерода, кислород, аргон и метан.
- 66. Каталитическая очистка N2/H2 смеси от оксидов углерода. Процесс каталитической очистки - гидрирование оксида и диоксида углерода
- 67. Катализаторы гидрирования. Наибольшее распространение в промышленной очистке получили никелевые катализаторы на термостойкой основе (оксиды алюминия, магния,
- 68. Получение ацетилена Ацетилен С2Н2 получают либо из карбида кальция и воды, либо плазмохимическим способом из природного
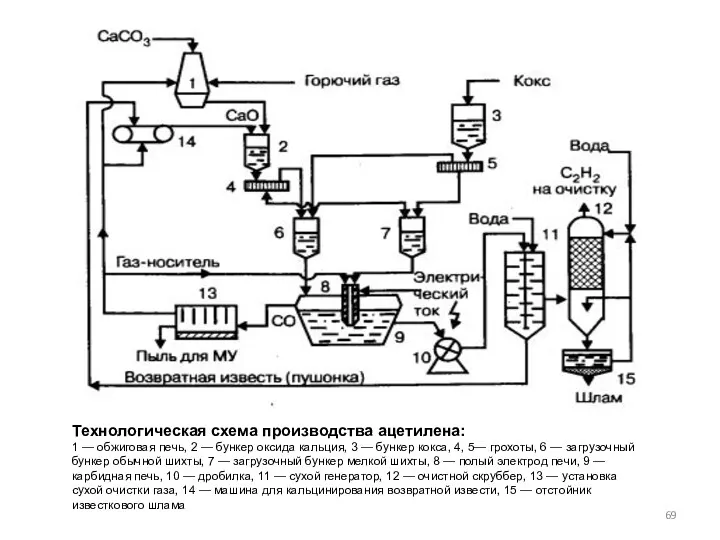
- 69. Технологическая схема производства ацетилена: 1 — обжиговая печь, 2 — бункер оксида кальция, 3 — бункер
- 70. Производство ацетилена из углеводородного сырья Высокотемпературный пиролиз алканов, используемый в производстве ацетилена из углеводородного сырья, представляет
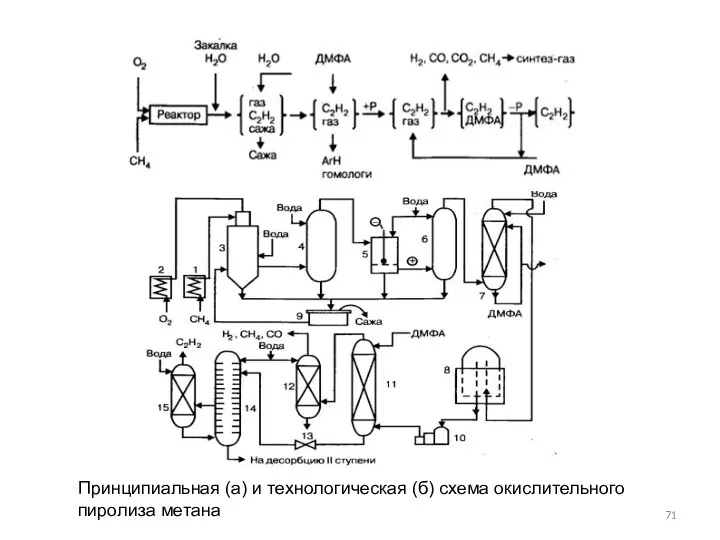
- 71. Принципиальная (а) и технологическая (б) схема окислительного пиролиза метана
- 73. Скачать презентацию





































 Властивості та застосування полімерів
Властивості та застосування полімерів Техника безопасности в химической лаборатории и на уроках химии
Техника безопасности в химической лаборатории и на уроках химии Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер
Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер Применение центрифугирования
Применение центрифугирования Химические формулы. 8 класс
Химические формулы. 8 класс Оксиды. Химические свойства и получение оксидов
Оксиды. Химические свойства и получение оксидов Сплав золота и серебра - электрум
Сплав золота и серебра - электрум Углеводы. Моносахариды. Дисахариды. Полисахариды
Углеводы. Моносахариды. Дисахариды. Полисахариды Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды)
Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды) Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури
Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури Фосфор и его соединения
Фосфор и его соединения Дисперсные системы (продолжение)
Дисперсные системы (продолжение) Классификация и свойства природных энергоносителей
Классификация и свойства природных энергоносителей Оксиды и их классификация
Оксиды и их классификация Органическая химия
Органическая химия Органічні речовини в живій природі. Рівні структурної органшзації
Органічні речовини в живій природі. Рівні структурної органшзації Арены. Бензол и его гомологи
Арены. Бензол и его гомологи Экспертные системы распознавания химических веществ. Тест
Экспертные системы распознавания химических веществ. Тест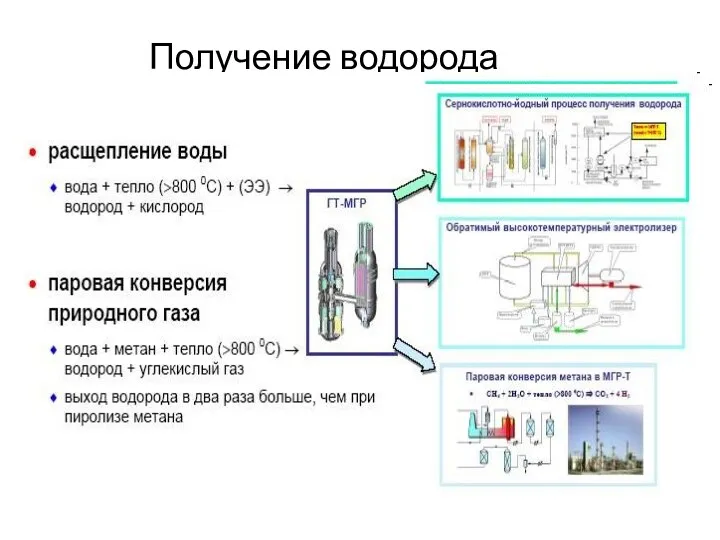 Получение водорода
Получение водорода Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Карбон қышқылдары
Карбон қышқылдары Решение задач на нахождение молекулярной формулы органических веществ
Решение задач на нахождение молекулярной формулы органических веществ Сутектік көрсеткіш ph. Тұздар гидролизі
Сутектік көрсеткіш ph. Тұздар гидролизі Пиролиз. Современная мировая структура сырья
Пиролиз. Современная мировая структура сырья Нахождение металлов в природе. Общие способы получения металлов. 9 класс
Нахождение металлов в природе. Общие способы получения металлов. 9 класс Методы в химии
Методы в химии Бережём планету вместе. Нефть
Бережём планету вместе. Нефть Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии
Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии