Содержание
- 2. Органическая химия – это химия соединений углерода Органическая химия – это химия углеводородов и их производных
- 3. Производные углеводородов Содержат кроме С и Н O N Hal и др.
- 4. Галогенпроизводные углеводородов производные углеводовородов, в которых один или несколько атомов водорода замещены на атомы галогенов
- 5. Этапы изучения Классификация Строение Номенклатура Изомерия Физические свойства Химические свойства Получение Применение
- 6. Классификация 1 По характеру галогена Фтор- Хлор- Бром- Иодпроизводные
- 7. Классификация 2 По числу атомов галогенов Моно- Ди- Тризамещенные и т.д.
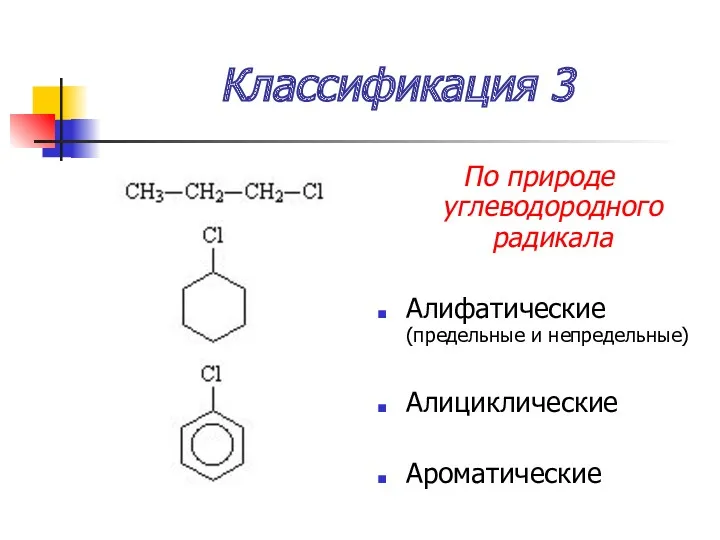
- 8. Классификация 3 По природе углеводородного радикала Алифатические (предельные и непредельные) Алициклические Ароматические
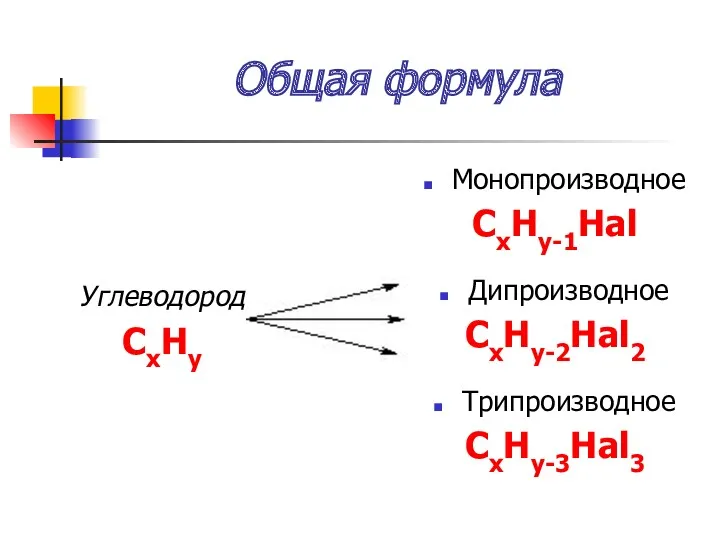
- 9. Общая формула Углеводород СxHy Монопроизводное СxHy-1Hal Дипроизводное СxHy-2Hal2 Трипроизводное СxHy-3Hal3
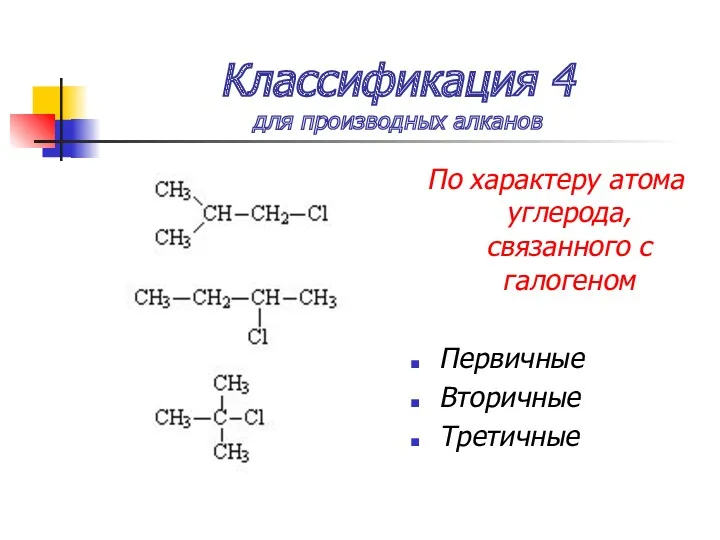
- 10. Классификация 4 для производных алканов По характеру атома углерода, связанного с галогеном Первичные Вторичные Третичные
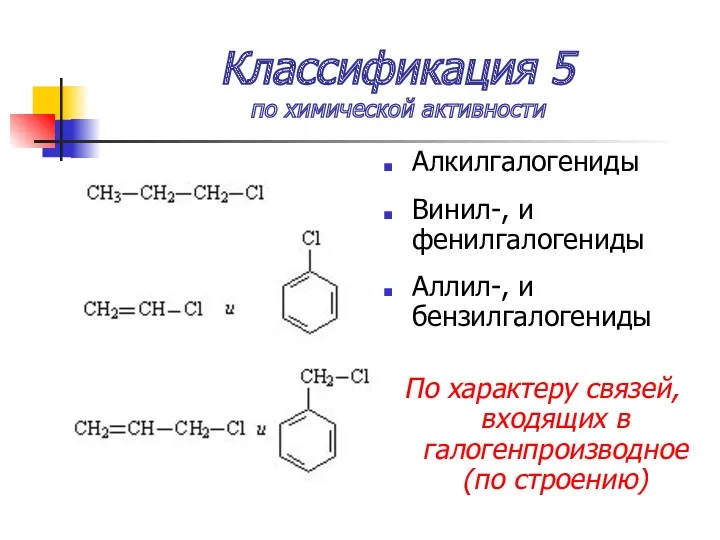
- 11. Классификация 5 по химической активности Алкилгалогениды Винил-, и фенилгалогениды Аллил-, и бензилгалогениды По характеру связей, входящих
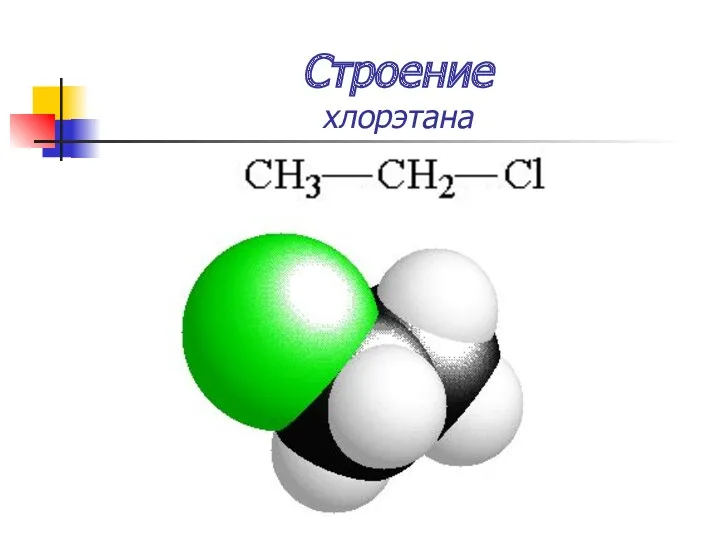
- 12. Строение хлорэтана
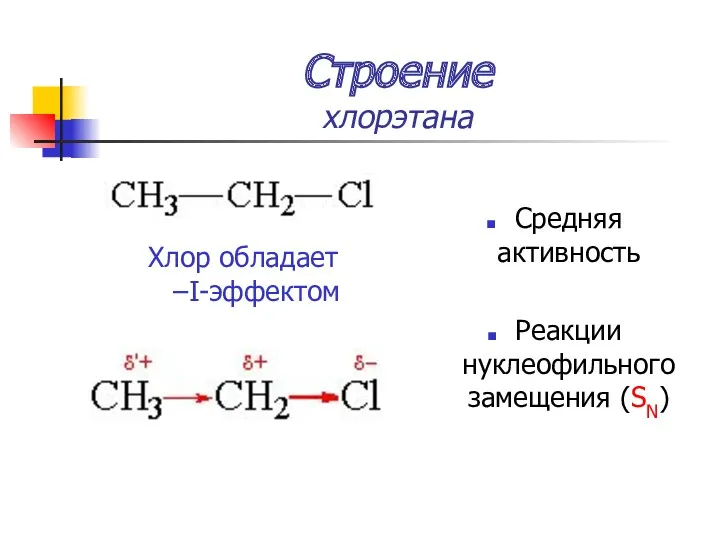
- 13. Строение хлорэтана Хлор обладает –I-эффектом Средняя активность Реакции нуклеофильного замещения (SN)
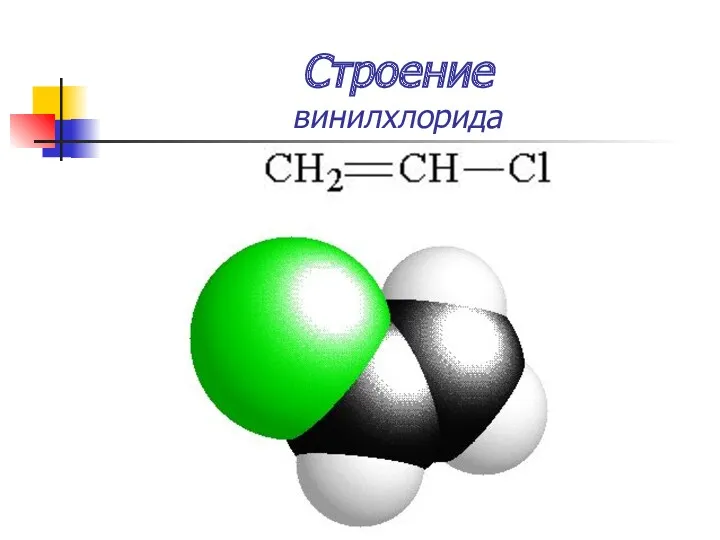
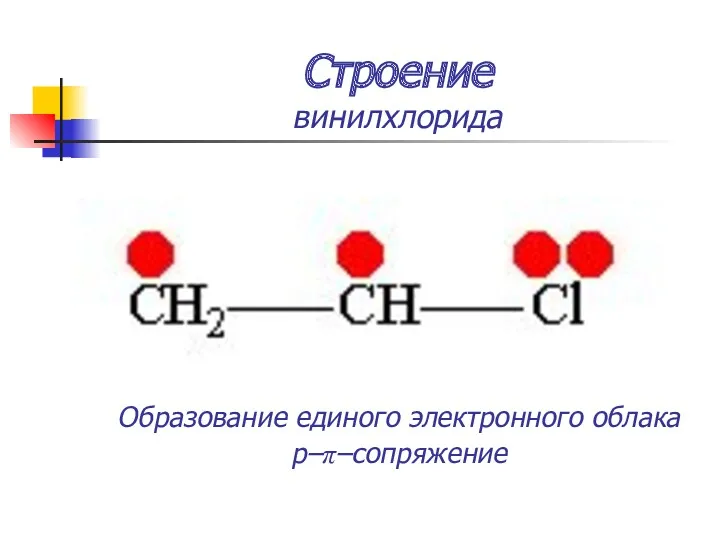
- 14. Строение винилхлорида
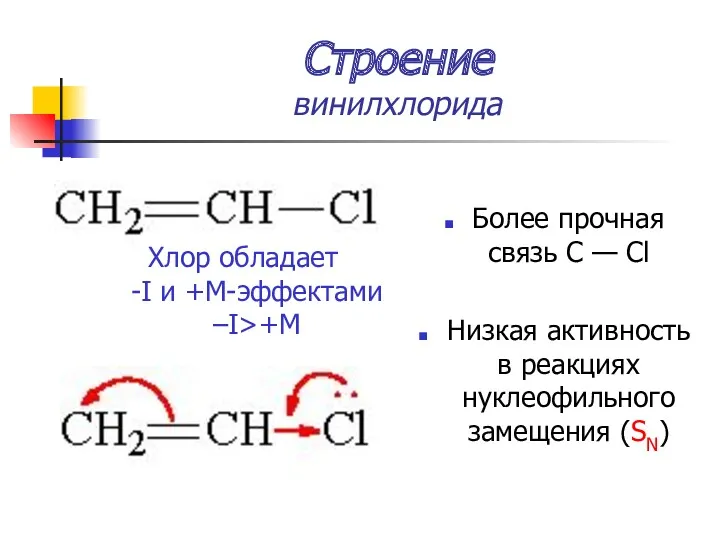
- 15. Строение винилхлорида Более прочная связь С — Cl Низкая активность в реакциях нуклеофильного замещения (SN) Хлор
- 16. Строение винилхлорида Образование единого электронного облака p–π–сопряжение
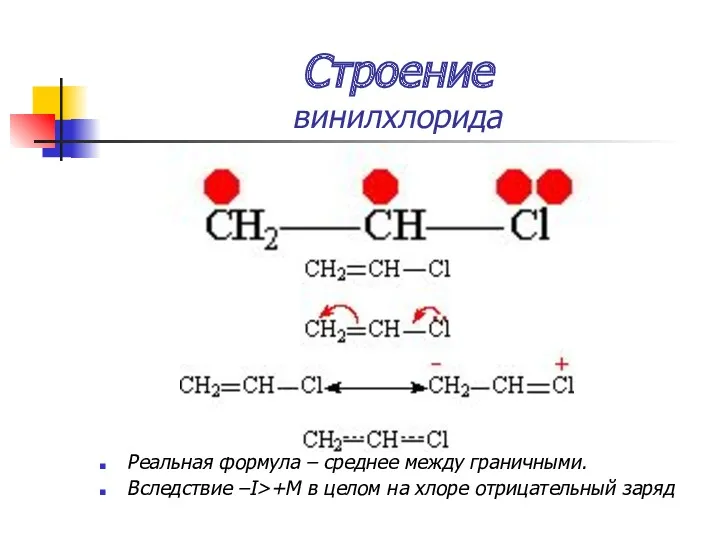
- 17. Строение винилхлорида Реальная формула – среднее между граничными. Вследствие –I>+M в целом на хлоре отрицательный заряд
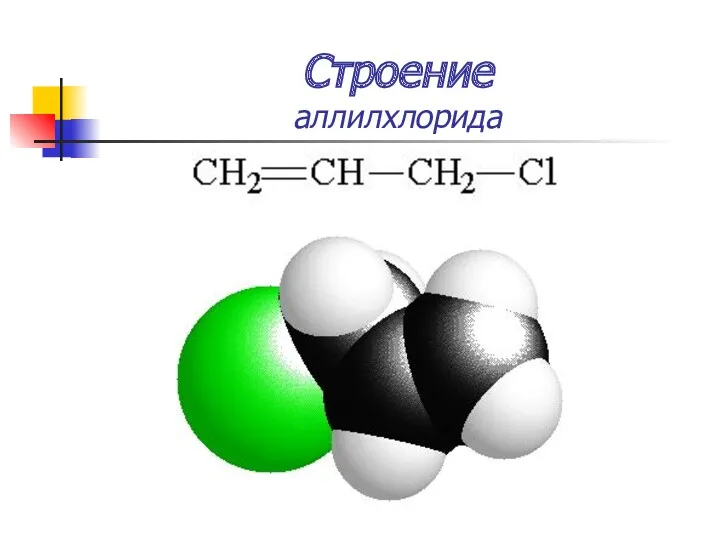
- 18. Строение аллилхлорида
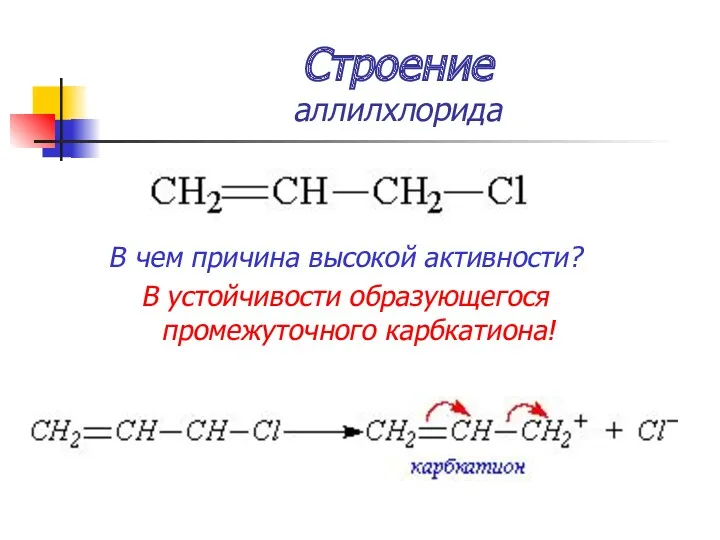
- 19. Строение аллилхлорида В чем причина высокой активности? В устойчивости образующегося промежуточного карбкатиона!
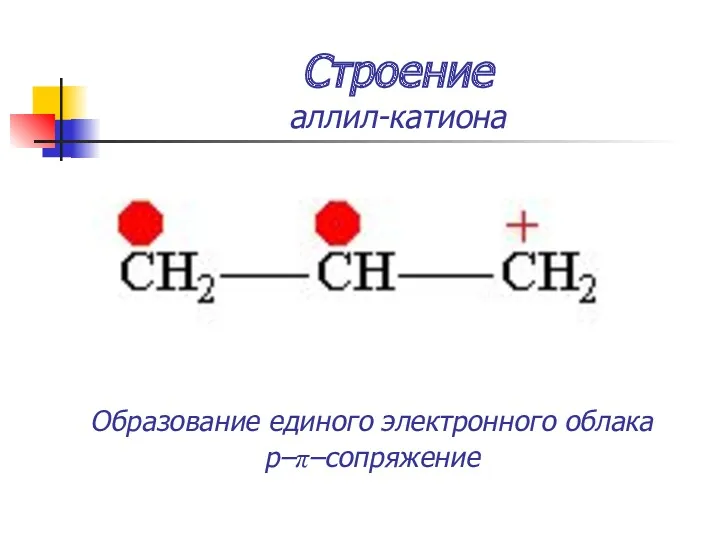
- 20. Строение аллил-катиона Образование единого электронного облака p–π–сопряжение Образование единого электронного облака p–π–сопряжение
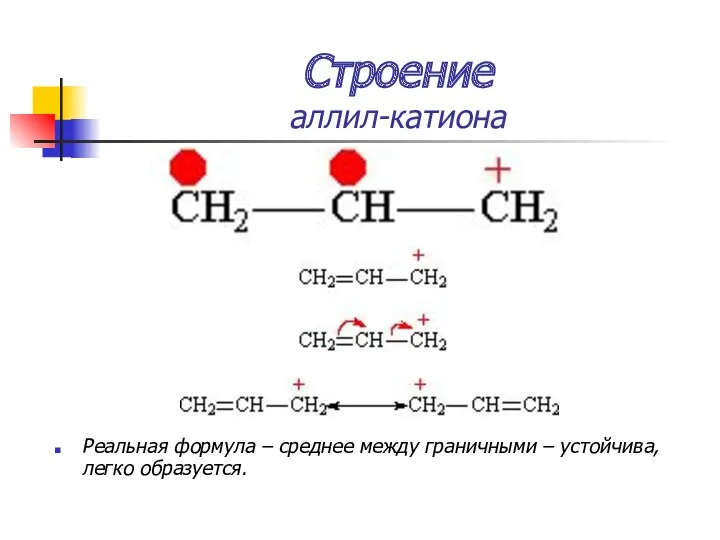
- 21. Строение аллил-катиона Реальная формула – среднее между граничными – устойчива, легко образуется.
- 22. Номенклатура Систематическая (заместительная) Локант (№) + галоген + углеводород Рациональная радикал + галогенид Тривиальная (исторически сложившаяся)
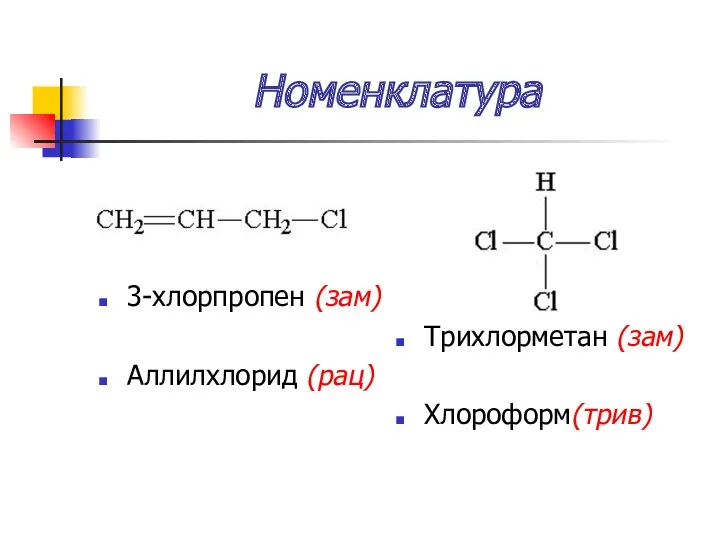
- 23. Номенклатура 3-хлорпропен (зам) Аллилхлорид (рац) Трихлорметан (зам) Хлороформ(трив)
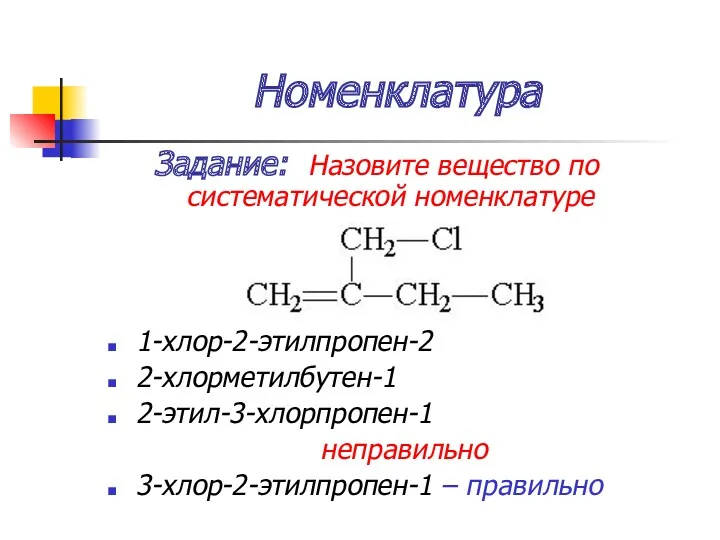
- 24. Номенклатура Задание: Назовите вещество по систематической номенклатуре 1-хлор-2-этилпропен-2 2-хлорметилбутен-1 2-этил-3-хлорпропен-1 неправильно 3-хлор-2-этилпропен-1 – правильно
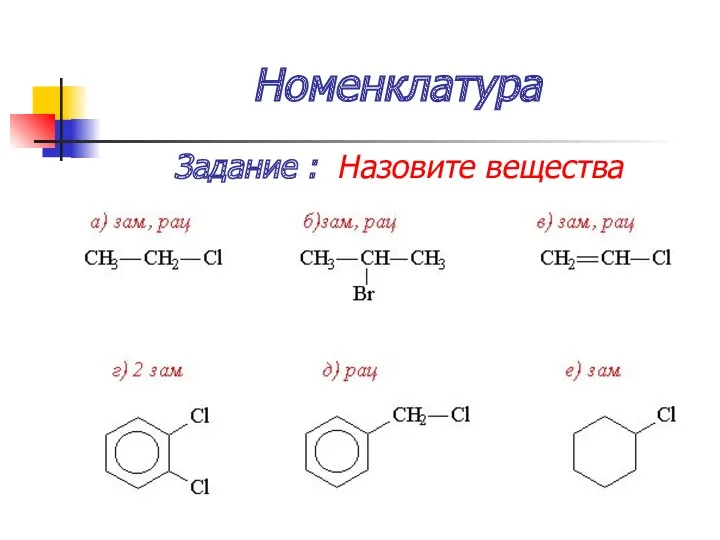
- 25. Номенклатура Задание : Назовите вещества
- 26. Изомерия Структурная А) характерная для углеводородов + Б) положения заместителя Пространственная Если характерна для углеводородов, от
- 27. Изомерия Задание Составьте формулы всех возможных изомеров состава С4Н9Вr. Укажите виды изомерии, характерные для этих соединений.
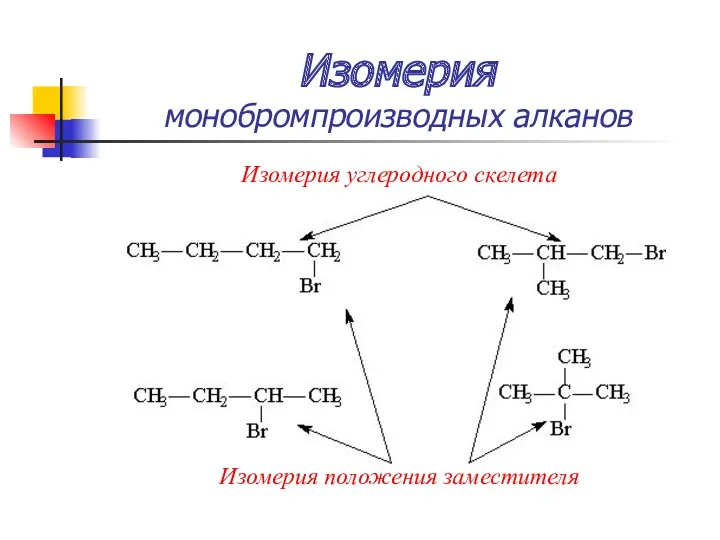
- 28. Изомерия монобромпроизводных алканов Изомерия углеродного скелета Изомерия положения заместителя
- 29. Изомерия пространственная Какие классы галогенпроизводных могут существовать в виде цис-транс-изомеров? Существует ли винилхлорид в виде цис-транс-изомеров?
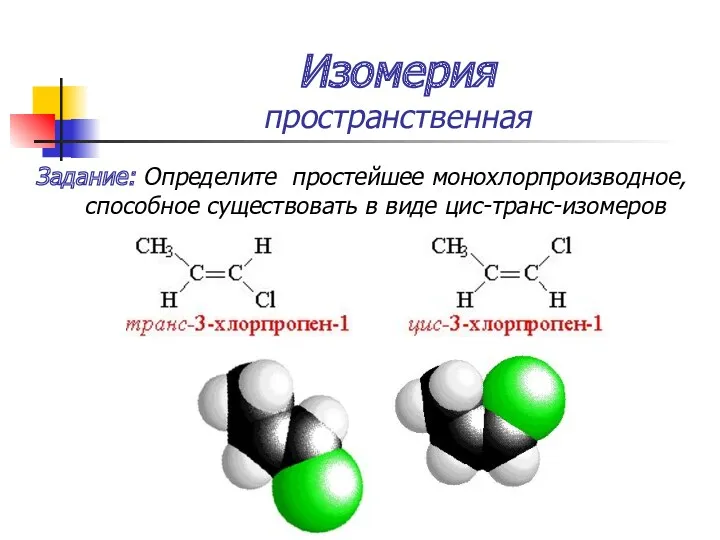
- 30. Изомерия пространственная Задание: Определите простейшее монохлорпроизводное, способное существовать в виде цис-транс-изомеров
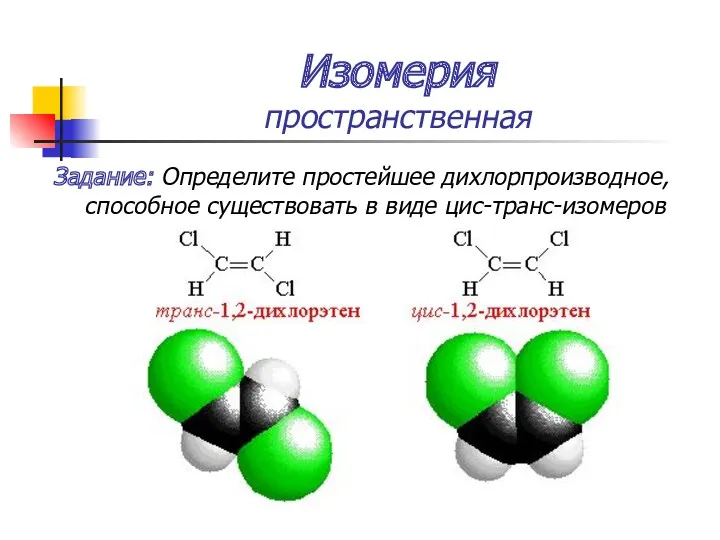
- 31. Изомерия пространственная Задание: Определите простейшее дихлорпроизводное, способное существовать в виде цис-транс-изомеров
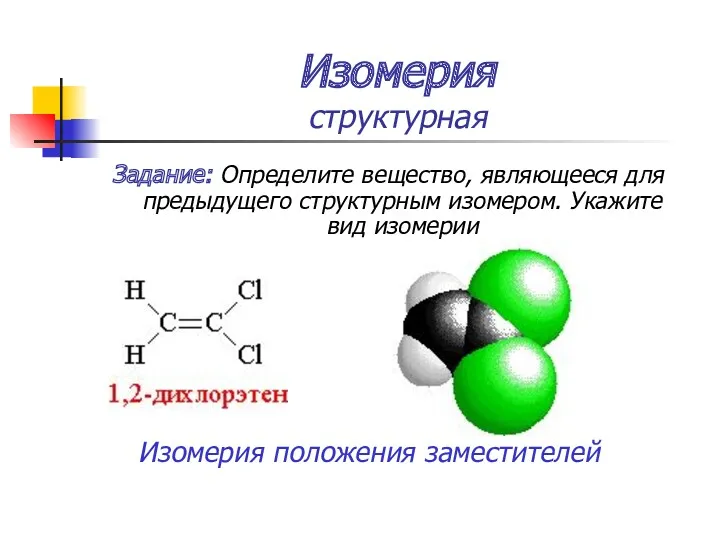
- 32. Изомерия структурная Задание: Определите вещество, являющееся для предыдущего структурным изомером. Укажите вид изомерии Изомерия положения заместителей
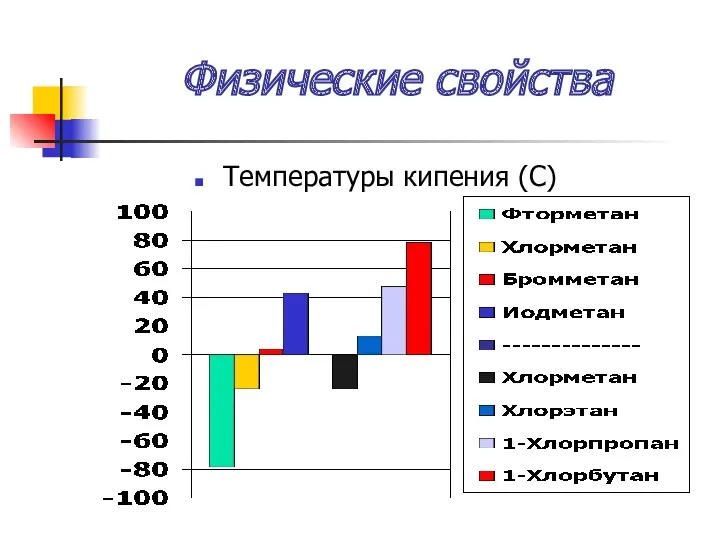
- 33. Физические свойства Температуры кипения (С)
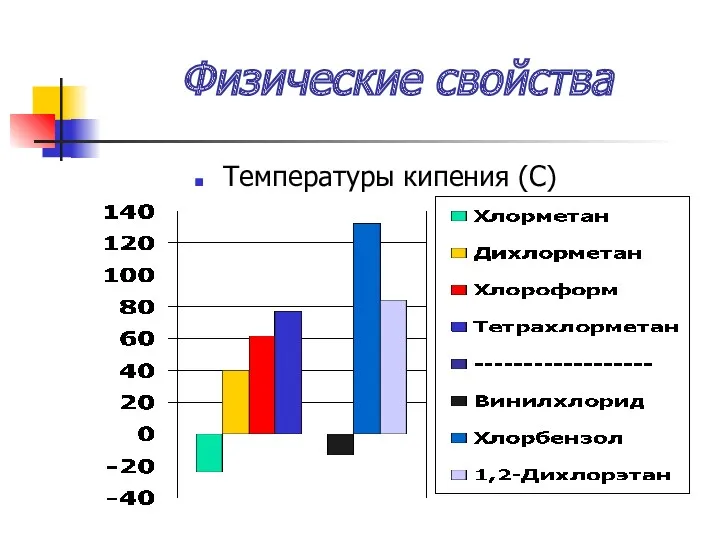
- 34. Физические свойства Температуры кипения (С)
- 35. Физические свойства Температуры кипения увеличиваются: А) с увеличением порядкового номера галогена Б) с увеличением углеводородного радикала
- 36. Физиологическое действие Почти все токсичны (гексахлоран, ДДТ - ядохимикаты), кроме фторпроизводных (тефлон, фреоны) Многие обладают наркотическим
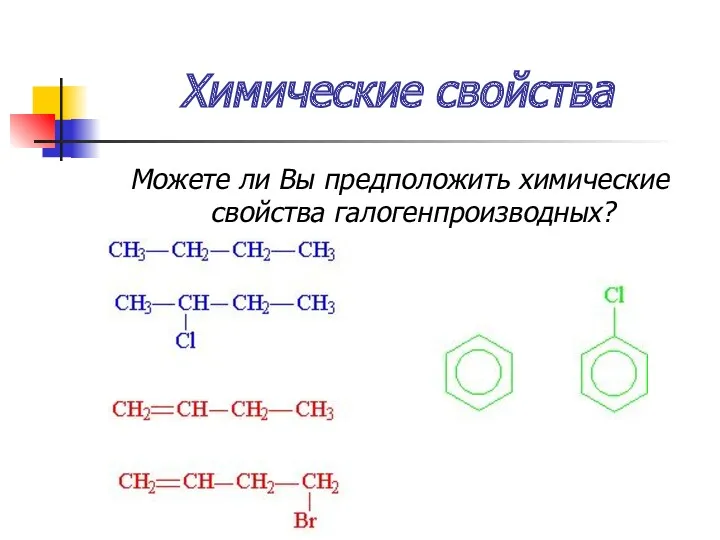
- 37. Химические свойства Можете ли Вы предположить химические свойства галогенпроизводных?
- 38. Химические свойства А) реакции углеводородных радикалов Те же что и у соответствующих у/в предельные – замещение
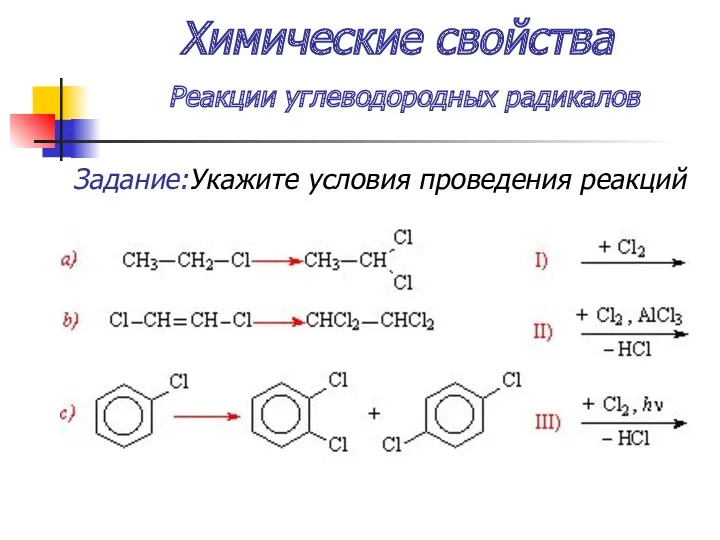
- 39. Химические свойства Реакции углеводородных радикалов Задание:Укажите условия проведения реакций
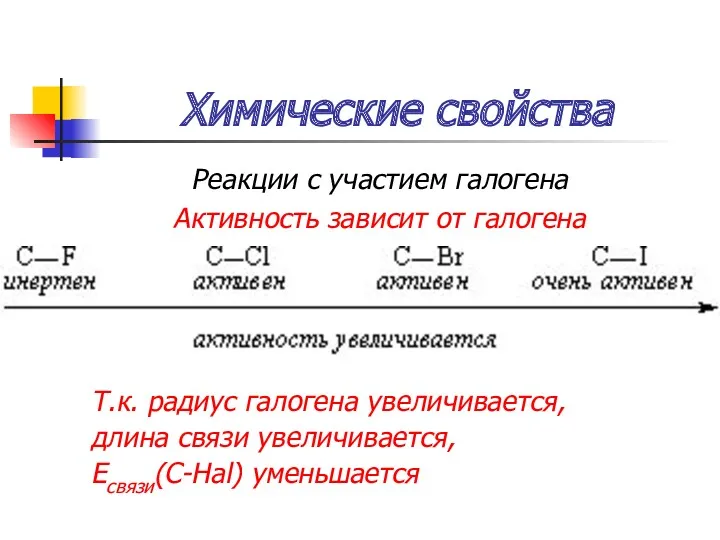
- 40. Химические свойства Реакции с участием галогена Активность зависит от галогена Т.к. радиус галогена увеличивается, длина связи
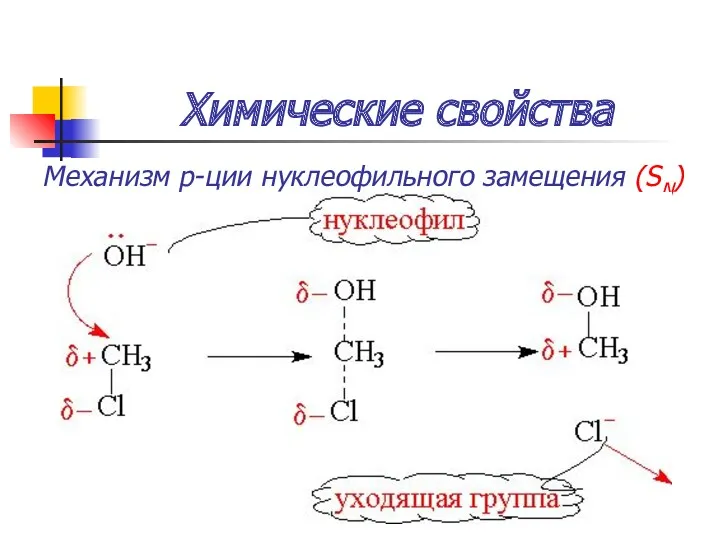
- 41. Химические свойства Механизм р-ции нуклеофильного замещения (SN)
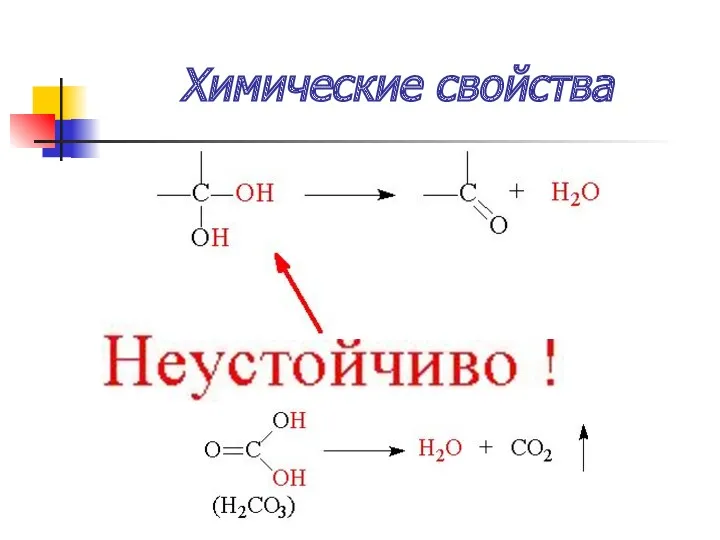
- 42. Химические свойства
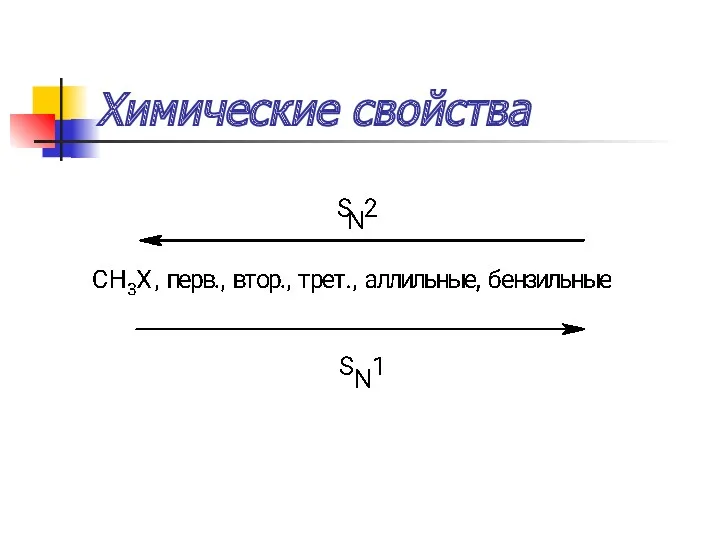
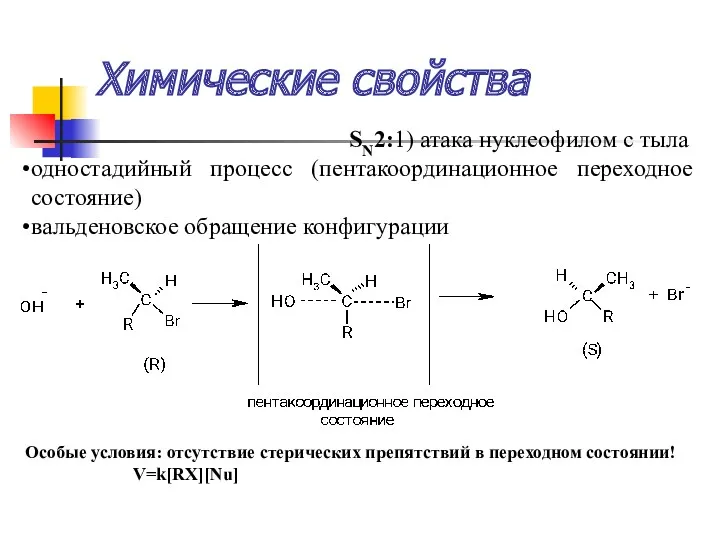
- 43. Химические свойства SN2:1) атака нуклеофилом с тыла одностадийный процесс (пентакоординационное переходное состояние) вальденовское обращение конфигурации Особые
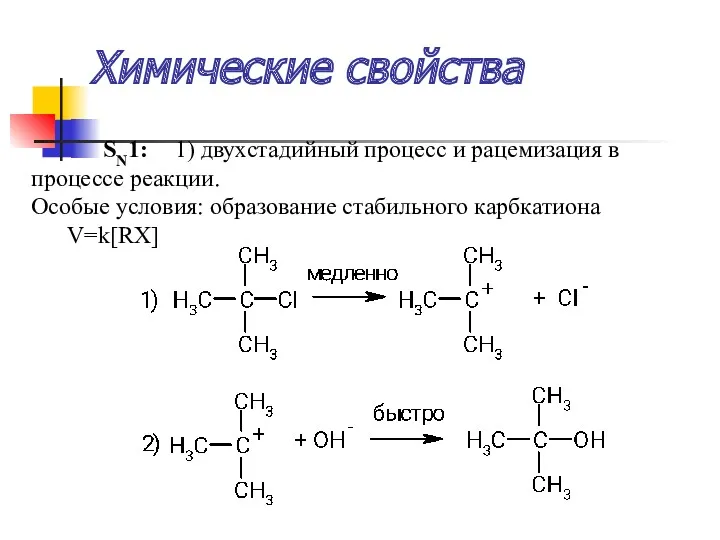
- 44. Химические свойства SN1: 1) двухстадийный процесс и рацемизация в процессе реакции. Особые условия: образование стабильного карбкатиона
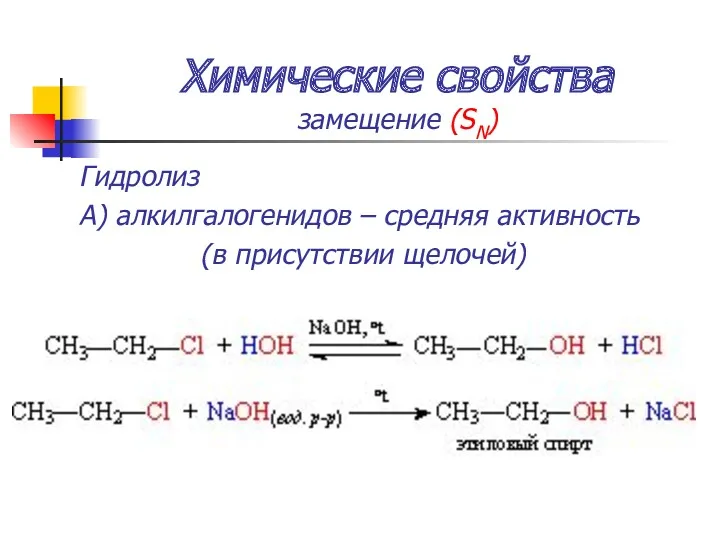
- 45. Химические свойства замещение (SN) Гидролиз А) алкилгалогенидов – средняя активность (в присутствии щелочей)
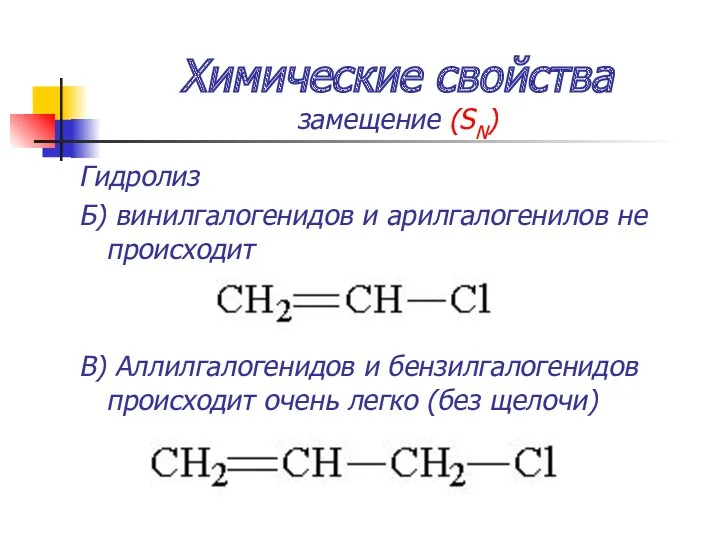
- 46. Химические свойства замещение (SN) Гидролиз Б) винилгалогенидов и арилгалогенилов не происходит В) Аллилгалогенидов и бензилгалогенидов происходит
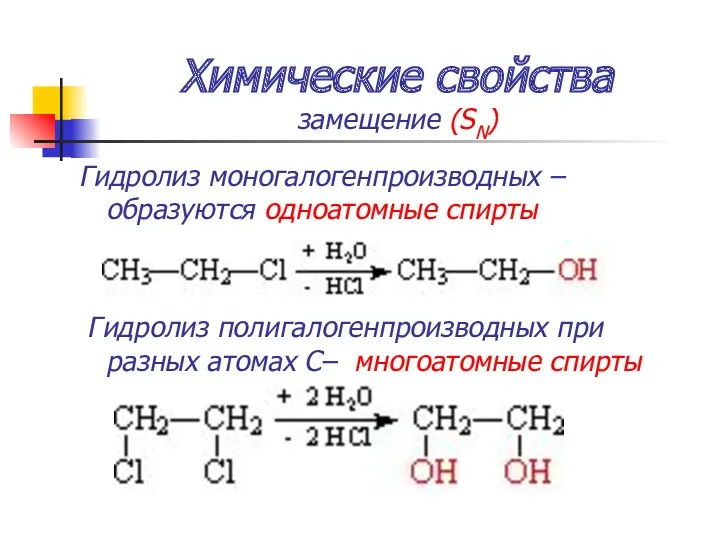
- 47. Химические свойства замещение (SN) Гидролиз моногалогенпроизводных – образуются одноатомные спирты Гидролиз полигалогенпроизводных при разных атомах С–
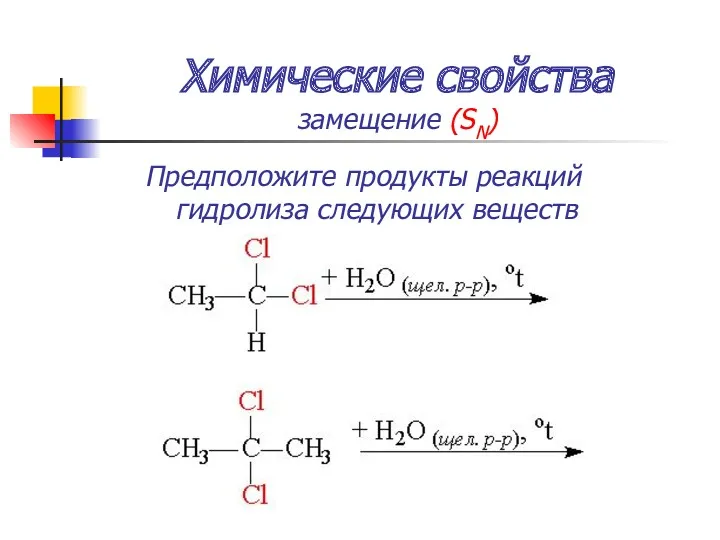
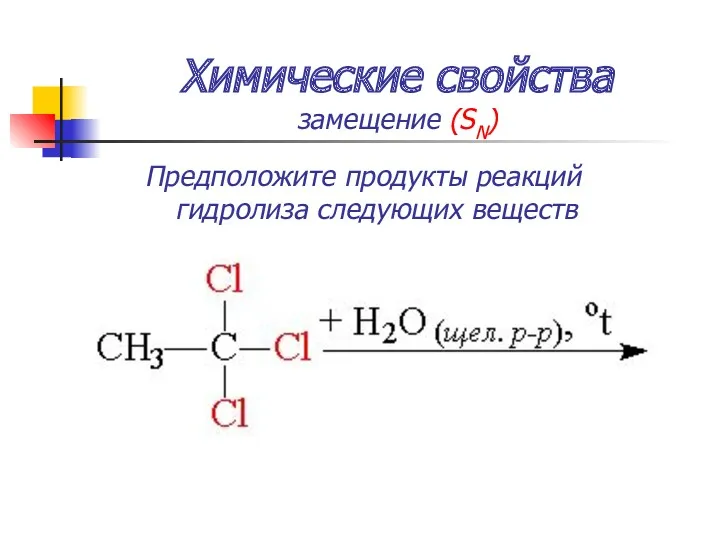
- 48. Химические свойства замещение (SN) Предположите продукты реакций гидролиза следующих веществ
- 49. Химические свойства
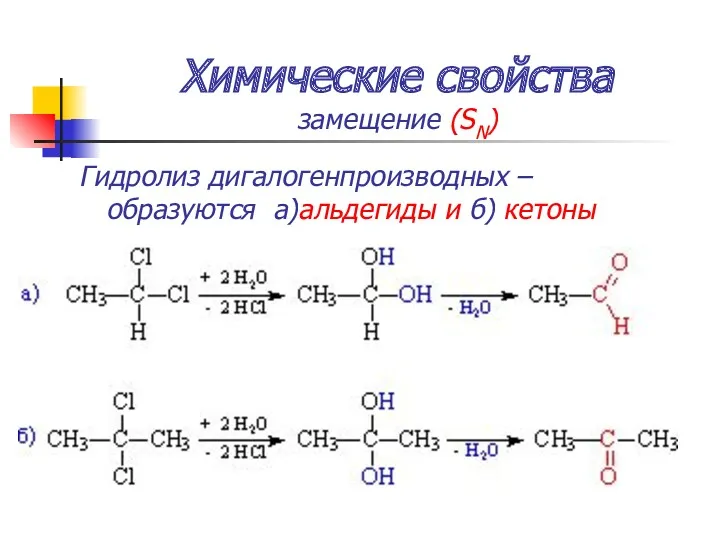
- 50. Химические свойства замещение (SN) Гидролиз дигалогенпроизводных – образуются а)альдегиды и б) кетоны
- 51. Химические свойства замещение (SN) Предположите продукты реакций гидролиза следующих веществ
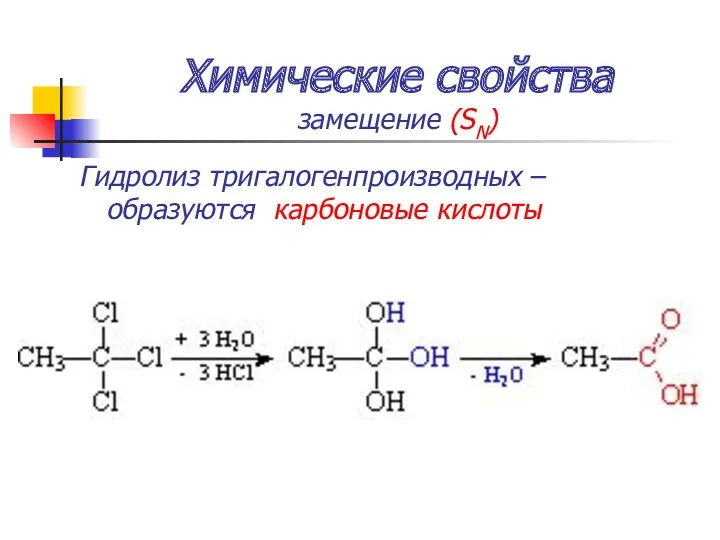
- 52. Химические свойства замещение (SN) Гидролиз тригалогенпроизводных – образуются карбоновые кислоты
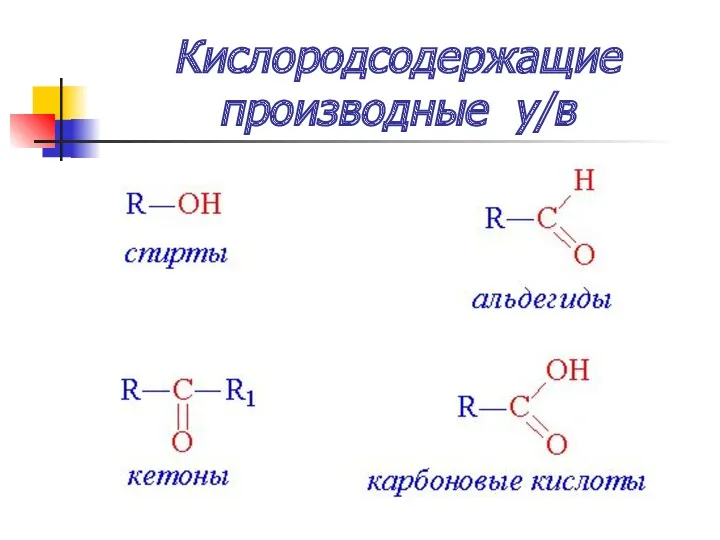
- 53. Кислородсодержащие производные у/в
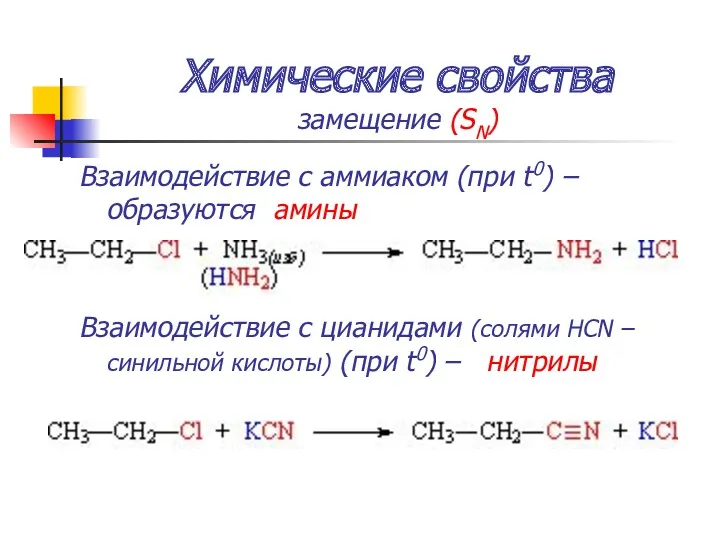
- 54. Химические свойства замещение (SN) Взаимодействие с аммиаком (при t0) – образуются амины Взаимодействие с цианидами (солями
- 55. Химические свойства отщепление (ЕN) Задание: Составьте уравнения реакций отщепления хлороводорода при нагревании со спиртовым раствором щелочи
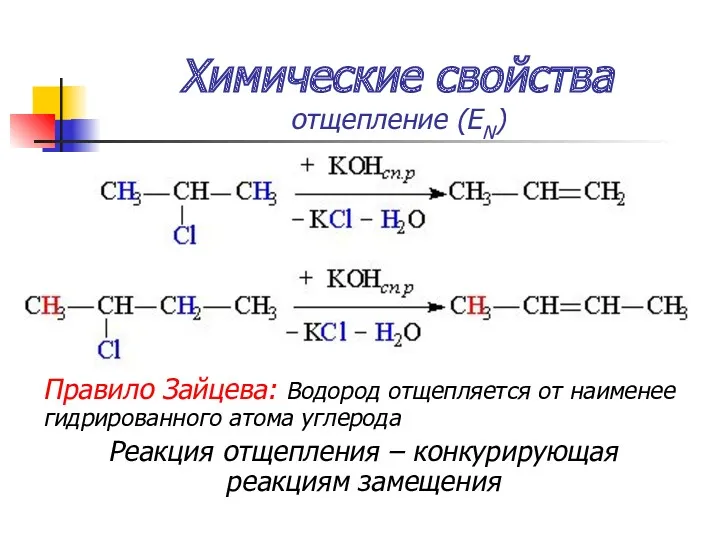
- 56. Химические свойства отщепление (ЕN) Правило Зайцева: Водород отщепляется от наименее гидрированного атома углерода Реакция отщепления –
- 57. Химические свойства окисление Горят плохо, выделяя ядовитые соединения (!!!) (например хлороводород HCl), или не горят вовсе.
- 58. Получение Из алканов и циклоалканов Из алкенов и алкинов Из аренов Из спиртов Из альдегидов и
- 59. Применение Анестезия С2H5Cl и наркоз CF3CHClBr (ранее СНCl3) и др. Растворители CCl4 , CH2ClCH2C и др.
- 61. Скачать презентацию













 Летучие яды. Токсичные газы
Летучие яды. Токсичные газы Тотығу-тотықсыздану реакциялары. Тотығу және тотықсыздану
Тотығу-тотықсыздану реакциялары. Тотығу және тотықсыздану Алюминий
Алюминий Кислоты. Яблочная кислота
Кислоты. Яблочная кислота Алюминий. Характеристика алюминия по положению в ПСХЭ. Строение атома
Алюминий. Характеристика алюминия по положению в ПСХЭ. Строение атома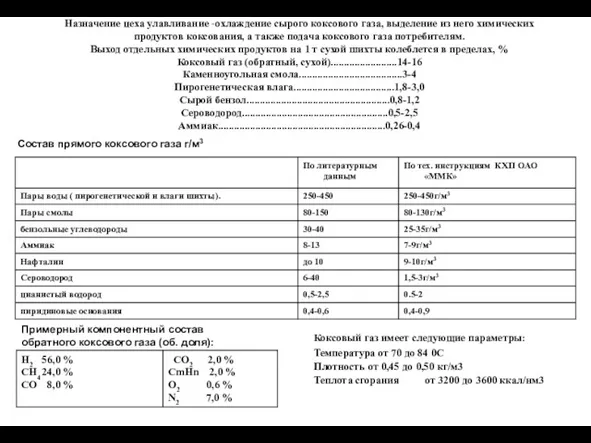 Охлаждение сырого коксового газа, выделение из него химических продуктов коксования
Охлаждение сырого коксового газа, выделение из него химических продуктов коксования Биохимия
Биохимия Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Тест Кто хочет стать отличником по химии
Тест Кто хочет стать отличником по химии Камни и Телец
Камни и Телец Фосфор. Гипофосфатемия и гиперфосфатемия
Фосфор. Гипофосфатемия и гиперфосфатемия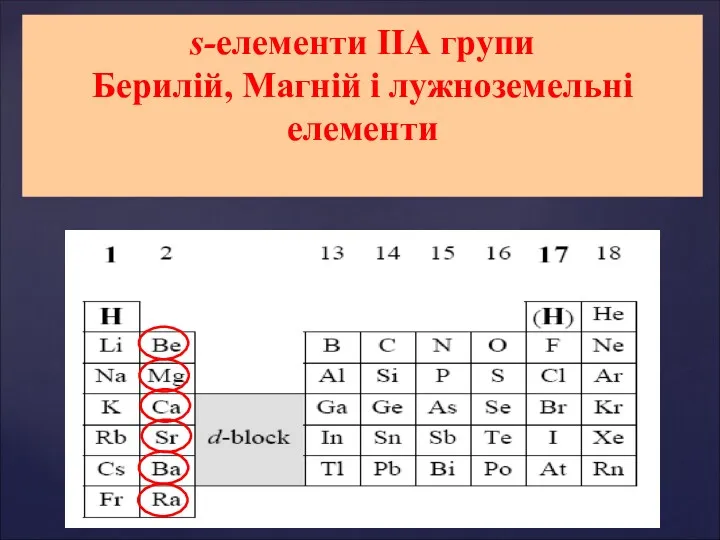 s-елементи ІІ А групи: Берилій, Магній і лужноземельні елементи. Властивості елементів ІІ А групи
s-елементи ІІ А групи: Берилій, Магній і лужноземельні елементи. Властивості елементів ІІ А групи Вода - розчинник. Урок 41
Вода - розчинник. Урок 41 Chemistry of life
Chemistry of life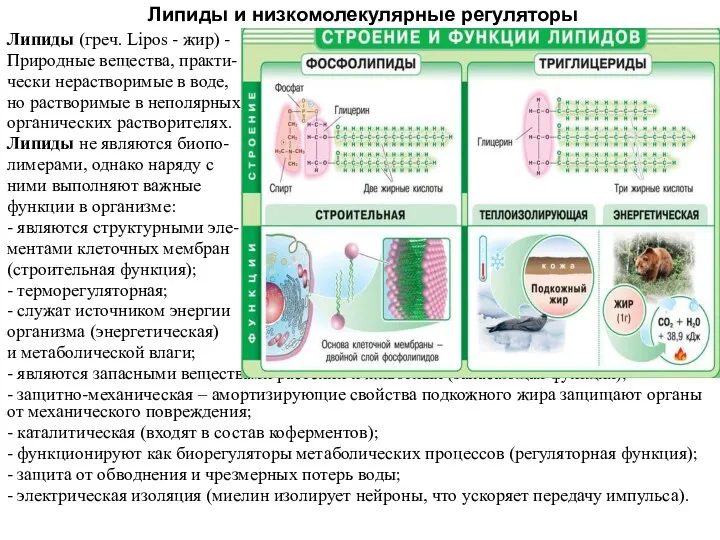 Липиды и низкомолекулярные регуляторы
Липиды и низкомолекулярные регуляторы Химический элемент кремний
Химический элемент кремний Алкины
Алкины Химический факультет
Химический факультет Неметаллы. Особенности строения атомов неметаллов
Неметаллы. Особенности строения атомов неметаллов Взаимодействие ускоренных ионов с веществом (часть 1)
Взаимодействие ускоренных ионов с веществом (часть 1) Энергетика химических процессов. (Лекция 2)
Энергетика химических процессов. (Лекция 2) Теория электролитической диссоциации (ТЭД)
Теория электролитической диссоциации (ТЭД) Эквиваленты веществ. Жидкое состояние, растворы
Эквиваленты веществ. Жидкое состояние, растворы Классификация и номенклатура неорганических соединений (Малый химический тренажёр)
Классификация и номенклатура неорганических соединений (Малый химический тренажёр) Углерод. Аллотропные модификации
Углерод. Аллотропные модификации Галогены. Строение атома
Галогены. Строение атома Окислительно – восстановительные реакции
Окислительно – восстановительные реакции Агрегатные состояния вещества
Агрегатные состояния вещества