Содержание
- 2. Окислительно –восстановительные Реакции
- 3. Цель урока: 1.Сформировать понятие об окислительно-восстановительных реакциях. 2.Научиться уравнивать записи ОВР методом электронного баланса.
- 4. Пример: 2Cu0 + O2 =2 Cu2+O2- 2H+CL- + Zn0 = Zn2+CL2- + H20 Реакции, в резултате
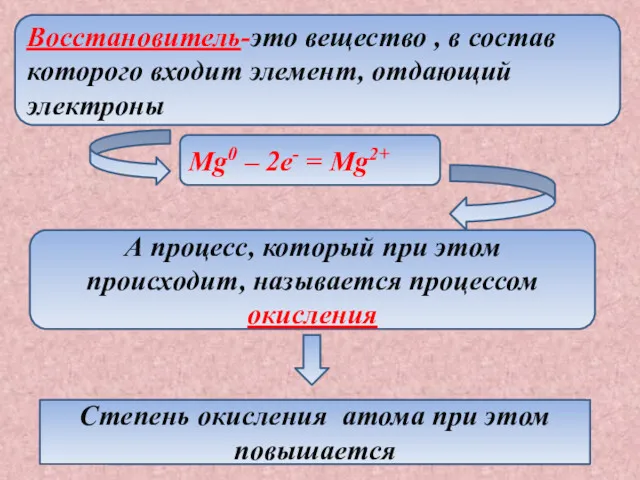
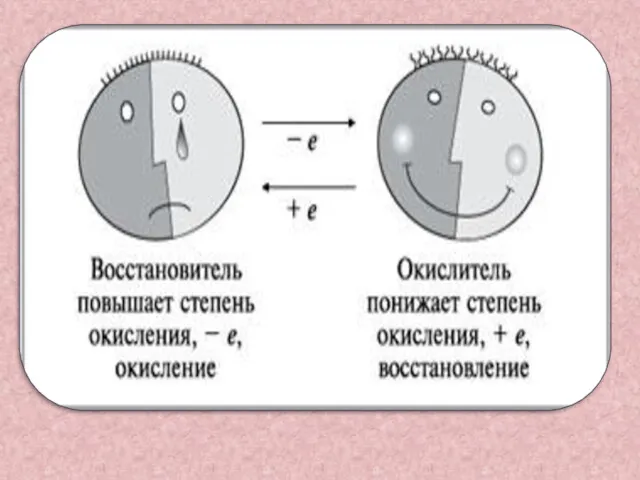
- 5. Восстановитель-это вещество , в состав которого входит элемент, отдающий электроны Mg0 – 2e- = Mg2+ А
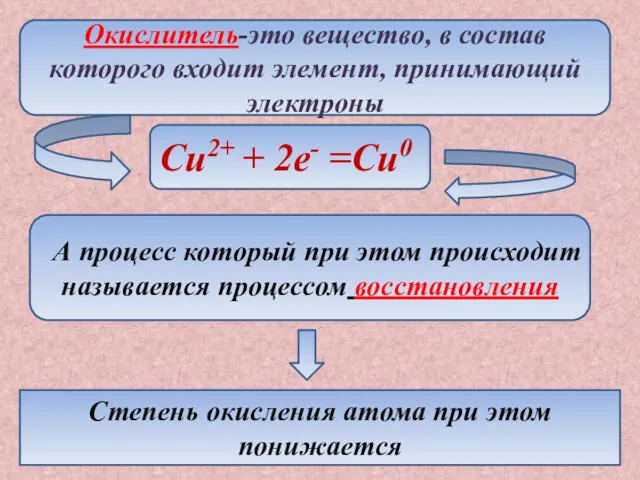
- 6. Окислитель-это вещество, в состав которого входит элемент, принимающий электроны Cu2+ + 2e- =Cu0 А процесс который
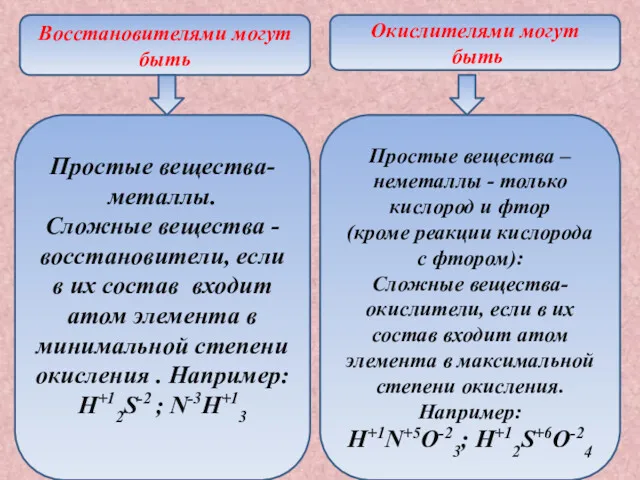
- 8. Восстановителями могут быть Окислителями могут быть Простые вещества-металлы. Сложные вещества - восстановители, если в их состав
- 9. Различают: минимальную (низшую) степень окисления S-2 2e- 8e- 8e- промежуточную степень окисления S0 2e- 8e- 6e-
- 11. Скачать презентацию




 Алкадиены
Алкадиены Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Пластмассы в автомобилестроении
Пластмассы в автомобилестроении Валентность и степень окисления химического элемента
Валентность и степень окисления химического элемента 530f2c0b0bb94f3085ed9ef5fc682ddb
530f2c0b0bb94f3085ed9ef5fc682ddb Технологии получения полимерных нанокомпозитов
Технологии получения полимерных нанокомпозитов Аналитические химические реакции. Классификация аналитических химических реакций
Аналитические химические реакции. Классификация аналитических химических реакций Химиялық кинетика және электрохимия
Химиялық кинетика және электрохимия Поверхностно-активные вещества
Поверхностно-активные вещества Гигиена питания школьников
Гигиена питания школьников Кристаллические решетки
Кристаллические решетки Обчислення за хімічними рівняннями відносного виходу продукту реакції. Урок №19. 11 клас
Обчислення за хімічними рівняннями відносного виходу продукту реакції. Урок №19. 11 клас Азот и его соединения
Азот и его соединения Гідроліз солей
Гідроліз солей Пируватдегидрогеназный комплекс
Пируватдегидрогеназный комплекс Анри Ле Шателье. 1850-1963. Принцип Ле Шателье в химии
Анри Ле Шателье. 1850-1963. Принцип Ле Шателье в химии Квантово-механический подход к описанию строения атомов
Квантово-механический подход к описанию строения атомов Общие правила техники безопасности при работе в кабинете химии. Урок №2. Практическая работа №1
Общие правила техники безопасности при работе в кабинете химии. Урок №2. Практическая работа №1 Аккумуляторные батареи
Аккумуляторные батареи Карбон
Карбон Электрохимические процессы. Лекция 7
Электрохимические процессы. Лекция 7 Признаки химических реакций
Признаки химических реакций Скорость химических реакций
Скорость химических реакций Азотная кислота и ее соли. Физические свойства
Азотная кислота и ее соли. Физические свойства Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ
Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ Общая и медицинская химия
Общая и медицинская химия Химическая связь. (Лекция 4, 5)
Химическая связь. (Лекция 4, 5) Железо и его соединения
Железо и его соединения