Содержание
- 2. Рекомендуемая литература В нашей библиотеке: Хомченко И.Г. Общая химия, 1987 Глинка Н.Л. Общая химия, 1987 Глинка
- 3. Рекомендуемая литература Есть в мире: Общая и неорганическая химия для медиков и фармацевтов. Учебник и практикум
- 4. Периодический закон и периодическая система Основные понятия и закономерности
- 5. Периодическая система Графическое изображение Периодического закона на плоскости - периодическая система Наиболее распространенные формы периодической системы
- 6. Сверхдлинный вариант ПС
- 7. Длинный вариант ПС
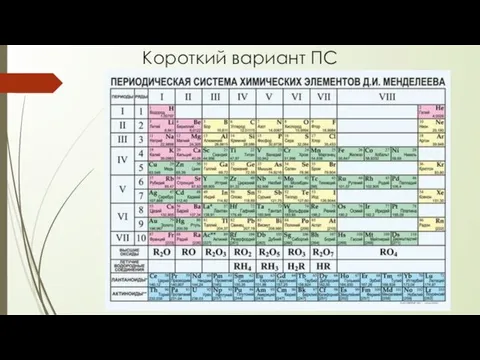
- 8. Короткий вариант ПС
- 9. Развитие представлений о строении атома МОДЕЛИ АТОМОВ Кусочки материи –Демокрит полагал, что свойства того или иного
- 10. QUANTUM NUMBERS Quantum numbers: There are a set of four quantum numbers which specify the energy,
- 11. Principal quantum number (n) It determines the size and to a large extent the energy of
- 12. Azimuthal quantum number (l) It identified the sushell and the three dimensional shape of the orbital.
- 13. Magnetic quantum number or Magnetic orbital quantum number (ml) For any sub-shell (defined by ‘l’ value)
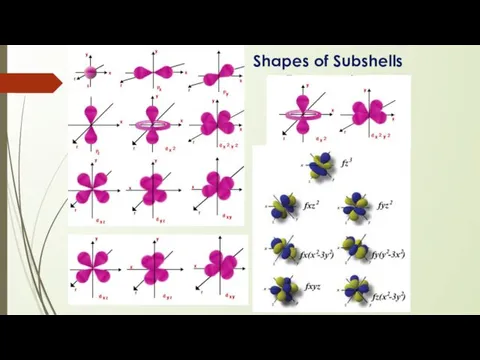
- 14. Shapes of Subshells
- 15. Filling of Electrons The filling of electrons into the orbitals of different atoms takes place according
- 16. Aufbau Principle: In the ground state of the atoms, the orbitals are filled in order of
- 17. Electronic configuration of atoms The electronic configuration of different atoms can be represented in two ways.
- 18. Electron spin quantum number (ms) It refers to orientation of the spin of the electron. It
- 19. Принципы и правила заполнения орбиталей Принцип Паули. В атоме не может быть двух электронов, у которых
- 20. Электронная конфигурация атома - запись, отражающая распределение электронов в атоме химического элемента по энергетическим уровням и
- 21. Правила написания электронных формул атомов Число энергетических уровней или значение главного квантового числа n равно номеру
- 22. Условная классификация простых веществ Металлы на внешнем уровне 1-3 электрона (искл.: Н, В, Не). характерна положительная
- 23. Основные характеристики химических элементов радиус атомов и ионов, энергия ионизации, энергия сродства к электрону, относительная электроотрицательность
- 24. Радиусы атомов и ионов Атомы и ионы не имеют точного размера (волновой характер), поэтому определяют условные
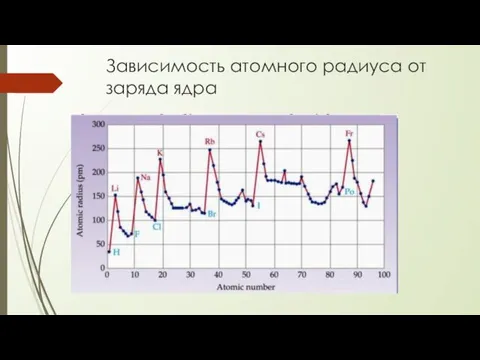
- 25. Зависимость атомного радиуса от заряда ядра
- 26. Зависимость атомного радиуса от заряда ядра По периоду. r уменьшается, т.к. при одинаковом значении n эффективный
- 27. Зависимость атомного радиуса от заряда ядра По подгруппам. В главной подгруппе r увеличивается сверху вниз, т.к.
- 28. Энергия ионизации атомов Энергия ионизации (I) - энергия, требуемая для отрыва и удаления на бесконечное расстояние
- 29. Периодичность энергии ионизации По периоду. Энергия ионизации растет, т.к. уменьшается радиус и растет эффективный заряд ядра.
- 30. Периодичность энергии ионизации По подгруппам наблюдается сложная зависимость, определяемая электронным строением и радиусом атомов. Радиус растет,
- 31. Энергия сродства к электрону Сродство к электрону определяется более всего энергией самой низкой незаполненной (или частично
- 32. Периодичность энергии сродства к электрону По периоду как правило энергия сродства к электрону увеличивается (кроме случая
- 33. Относительная электроотрицательность атомов Чем выше ЭО атома, тем в меньшей степени у него выражены восстановительные способности,
- 34. Относительная электроотрицательность атомов по Полингу По периоду Электроотрицательность увеличивается. По группам Электроотрицательность уменьшается Значения ЭО по
- 35. Практическая шкала электроотрицательности атомов В основу практической шкалы электроотрицательностей атомов взята концепция Луо-Бенсона, использующая понятие ковалентного
- 36. Относительная электроотрицательность атомов Элементу нельзя приписать постоянную электроотрицательность. На электроотрицательность оказывают влияние: Валентное состояния атома, Степень
- 37. Степени окисления Максимальная степень окисления в большинстве случаев равна номеру группы в короткопериодном варианте таблицы Менделеева.
- 38. Основы химической термодинамики Закономерности протекания химических реакций
- 39. Основные понятия химической термодинамики Задачи химической термодинамики: определение термодинамической вероятности протекания процесса определение термодинамических параметров процесса,
- 40. Основные понятия химической термодинамики Параметры – величины, характеризующие термодинамическую систему: интенсивные (величина которых не зависит от
- 41. Начала термодинамики Нулевое начало термодинамики: две системы, находящиеся в термическом равновесии с третьей системой, состоят в
- 42. Первое начало термодинамики внутренняя энергия системы U – определяется суммарным запасом энергии составляющих систему молекул, атомов,
- 43. Ни работа, ни теплота не являются функциями состояния и зависят от пути процесса (функции пути процесса).
- 44. Изохорный процесс V = const m = const Изотермический процесс T = const m = const
- 45. Первый закон термодинамики для изопроцессов
- 46. Термохимия Энтальпия – функция, характеризующая состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных
- 47. ЭНТРОПИЯ Энтропия - свойство системы, изменение которого при обратимом процессе равно отношению теплоты к температуре протекания
- 48. энтропия всегда увеличивается при переходе из конденсированного состояния в газообразное; она возрастает при растворении твердого или
- 49. Второе начало термодинамики в изолированных системах самопроизвольно идут процессы, при которых происходит увеличение энтропии.
- 50. Энергия Гиббса Любая система стремится к минимуму энтальпии и максимуму энтропии. В термодинамике имеется функция состояния,
- 51. Кинетика химических реакций Закономерности протекания химических реакций
- 52. Химическая кинетика изучает закономерности протекания химических реакций во времени, с ее помощью можно оптимизировать процессы и
- 53. Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями. Под элементарной реакцией обычно понимают единичный
- 54. Молекулярность реакции Мономолекулярные реакции – элементарные реакции распада и изомеризации, в которых участвует только одна молекула
- 55. Скорость химической реакции Скорость химической реакции в газовой фазе или растворе определяется как изменениием числа молекул
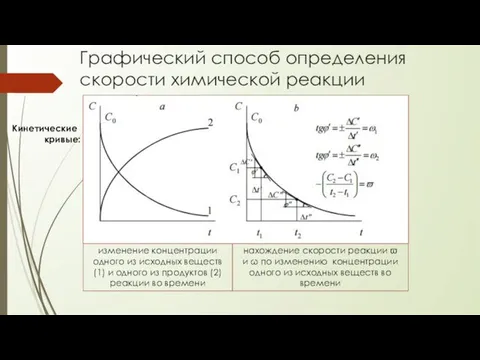
- 56. Графический способ определения скорости химической реакции изменение концентрации одного из исходных веществ (1) и одного из
- 57. Факторы, влияющие на скорость химической реакции природа реагирующих веществ; концентрация реагирующих веществ; температура; наличие катализатора; величина
- 58. Формальная кинетика Для элементарных реакций константа скорости зависит только от температуры, а порядок по веществу совпадает
- 59. Кинетика реакций целого порядка Реакции 0-го порядка: скорость реакции не зависит от концентрации данного компонента при
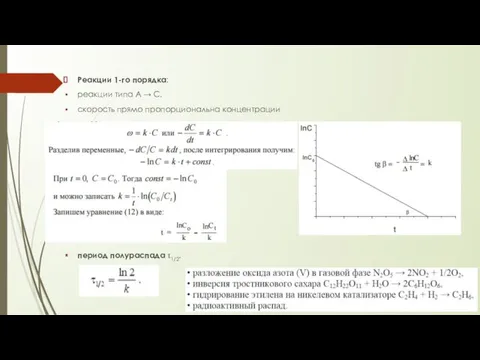
- 60. Реакции 1-го порядка: реакции типа A → С. скорость прямо пропорциональна концентрации период полураспада τ1/2.
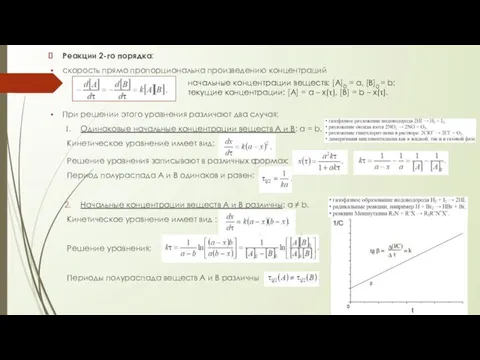
- 61. Реакции 2-го порядка: скорость прямо пропорциональна произведению концентраций При решении этого уравнения различают два случая: Одинаковые
- 62. Реакции 3-го порядка А+В+С → продукты или 2А+В → продукты, 3А → продукты и т.д.
- 63. Реакции n-го порядка А+В+С......→ продукты реакции
- 64. Метод определения порядка реакции интегральные дифференциальные используют интегральные кинетические уравнения для обработки экспериментальных данных о зависимости
- 65. Метод подстановки (метод проб и ошибок) Экспериментальные данные последовательно подставляют в интегральные кинетические уравнения для реакций
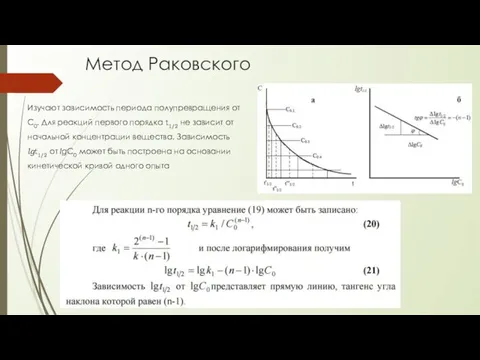
- 66. Метод Раковского Изучают зависимость периода полупревращения от С0. Для реакций первого порядка t1/2 не зависит от
- 67. Метод Вант-Гоффа Аналитический Графический Cтроят зависимость lnυ от ln[A]. Из тангенса угла наклона полученной прямой определяют
- 68. Метод изолирования Оствальда зависимость скорости реакции от начальной концентрации одного из реагентов (например, A) изучают при
- 69. Зависимость скорости реакции от температуры правило ВантГоффа: при увеличении температуры на каждые 10 градусов скорость возрастает
- 70. Химическая связь. Гибридизация.
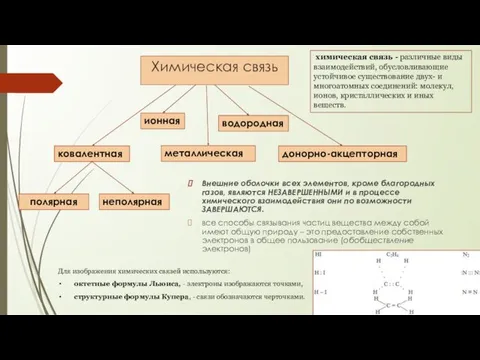
- 71. Химическая связь Внешние оболочки всех элементов, кроме благородных газов, являются НЕЗАВЕРШЕННЫМИ и в процессе химического взаимодействия
- 72. Ковалентная связь Образование может происходить двумя путями: Коллигация 2. Координация (донорно-акцепторная связь) Химическая связь, образованная путем
- 73. Ковалентная неполярная связь атомы образуют химические связи в результате обобществ-ления такого количества электронов, чтобы приобрести электронную
- 74. Ковалентная полярная связь Мерой полярности связи является ее дипольный момент μ : μ = е l,
- 75. Ионная связь Ионная химическая связь представляет собой электростатическое взаимодействие положительных и отрицательных заряженных ионов в химическом
- 76. Полярность связи Для чисто ковалентной связи Δ X = 0. Если величина Δ X меньше, чем
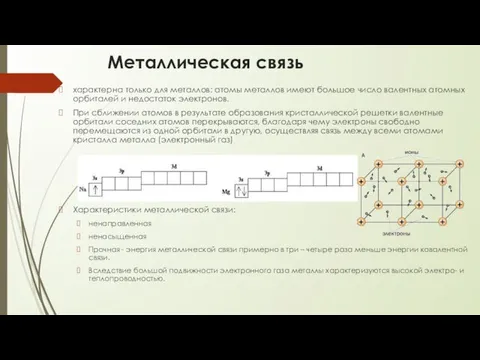
- 77. Металлическая связь характерна только для металлов: атомы металлов имеют большое число валентных атомных орбиталей и недостаток
- 78. Водородная связь Водородная связь по природе относится к электростатическим и образуется в том случае, когда атом
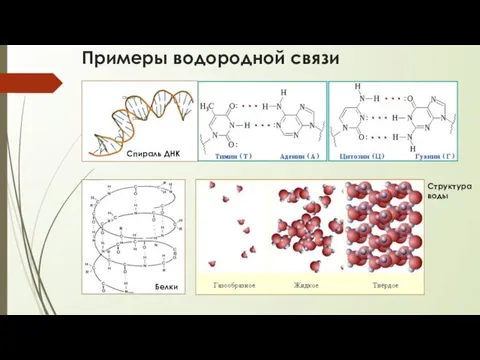
- 79. Примеры водородной связи Спираль ДНК Белки Структура воды
- 80. Характеристики химической связи Полярность связи - степень смещения электронной плотности, приводящего к возникновению разнополярных полюсов. Молекула
- 81. Метод валентных связей (МВС) Ковалентную химическую связь образуют два электрона с противоположными спинами, принадлежащие двум атомам.
- 82. Метод молекулярных орбиталей (ММО) состояние электронов в молекуле может быть описано как совокупность молекулярных электронных орбиталей,
- 83. Кратные связи делокализованная π-связь метод наложения валентных схем на примере азидоводорода HN3 в молекуле остаются два
- 85. Скачать презентацию

























































![Метод Вант-Гоффа Аналитический Графический Cтроят зависимость lnυ от ln[A]. Из](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/108066/slide-66.jpg)













 Композиционные материалы для изоляции электрических машин
Композиционные материалы для изоляции электрических машин Кислоты НСL, H2 O, H2 CO3
Кислоты НСL, H2 O, H2 CO3 Физические явления – основа разделения смесей в химии (урок химии в 8 классе)
Физические явления – основа разделения смесей в химии (урок химии в 8 классе) Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл
Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл Цинк и его применение
Цинк и его применение Полимеры. Каучук
Полимеры. Каучук Полисахариды. Крахмал
Полисахариды. Крахмал Третья группа, главная подгруппа. 9 класс
Третья группа, главная подгруппа. 9 класс Сложные эфиры
Сложные эфиры Закон сохранения массы веществ. Уравнения химических реакций
Закон сохранения массы веществ. Уравнения химических реакций Значення хімічних процесів у природі
Значення хімічних процесів у природі Курс лекций: Методы диагностики и анализа микро- и наносистем
Курс лекций: Методы диагностики и анализа микро- и наносистем Твердое состояние вещества. Кристаллические и аморфные тела
Твердое состояние вещества. Кристаллические и аморфные тела Гидроксиды. Основания: способы получения
Гидроксиды. Основания: способы получения Жер қыртысының заттық және химиялық құрамы
Жер қыртысының заттық және химиялық құрамы Реакции деструкции макромолекул
Реакции деструкции макромолекул Неметаллы
Неметаллы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Классификация веществ по характеру связи
Классификация веществ по характеру связи Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс Chemistry of Coordination Compounds
Chemistry of Coordination Compounds Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов Субстраты и продукты биохимических реакций
Субстраты и продукты биохимических реакций Пурины. Строение пурина
Пурины. Строение пурина Высокомолекулярные соединения полимеры
Высокомолекулярные соединения полимеры Химическая связь
Химическая связь Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Получение и применение алканов
Получение и применение алканов