Содержание
- 2. План лекции 1. Сущность окислительно-восстановительных реакций и условие их протекания. Степени окисления атомов и порядок их
- 3. П.1. Сущность окислительно-восстановительных реакций и условие их протекания. Степени окисления атомов и порядок их определения. Составление
- 4. Степень окисления формальный (условный) заряд атома в соединении, вычисленный, исходя из предположения, что соединение состоит из
- 5. Степень окисления не совпадает с истинным зарядом атома в соединении H+0,17Cl–0,17 не совпадает с валентностью (числом
- 6. Типичные окислители и восстановители Окислители: Простые вещества – cодержащие элементы с высокой электроотрицатель-ностью (F2, O2, Cl2
- 7. Изменение степени окисления = перераспределение электронной плотности ("передача электронов") (НСlO - хлорноватистая кислота – соли гипохлориты)
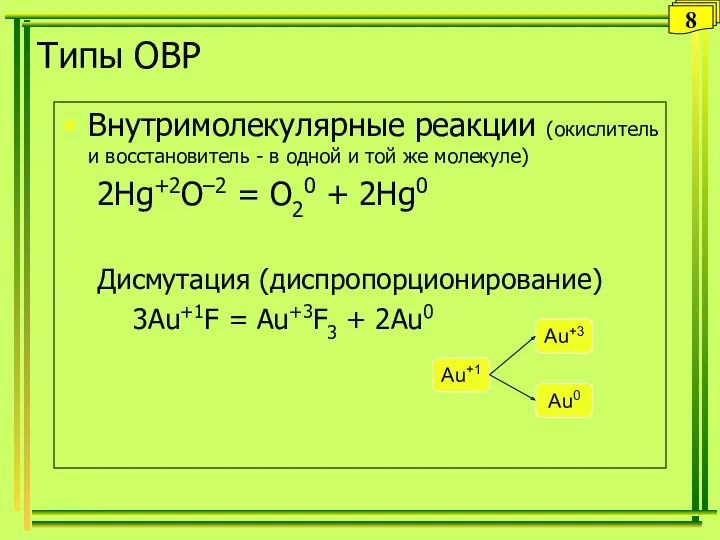
- 8. Типы ОВР Внутримолекулярные реакции (окислитель и восстановитель - в одной и той же молекуле) 2Hg+2O–2 =
- 9. Типы ОВР Межмолекулярные реакции (окислитель и восстановитель - в разных молекулах) 2Mg0 + O20 = 2Mg+2O–2
- 10. Подбор коэффициентов в уравнениях ОВР. Метод электронного баланса 1. Записывают формулы реагентов и продуктов, находят элементы,
- 11. Подбор коэффициентов в уравнениях ОВР. Метод электронного баланса FeСl3 + KJ → FeСl2 + KCl +
- 12. Подбор коэффициентов в уравнениях ОВР. Метод электронного баланса Na2SO3 + KMnO4 + Н2SO4 → Na2SO4 +
- 13. Подбор коэффициентов в уравнениях ОВР. Метод электронного баланса Na2SO3 + KMnO4 + Н2O → Na2SO4 +
- 14. Подбор коэффициентов в уравнениях ОВР. Метод электронного баланса Na2SO3 + KMnO4 + NaOН → Na2SO4 +
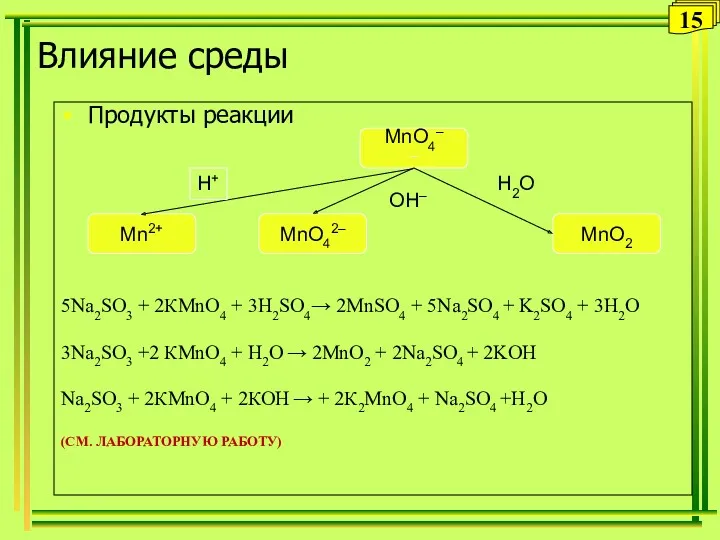
- 15. Влияние среды Продукты реакции 5Na2SO3 + 2КMnO4 + 3H2SO4→ 2MnSO4 + 5Na2SO4 + K2SO4 + 3H2O
- 16. Подбор коэффициентов в уравнениях ОВР. Метод электронного баланса FeS + O2 → Fe2O3 + SO2 Fe+2
- 17. Подбор коэффициентов в уравнениях ОВР. Метод электронно-ионных полуреакций 1. Записывают формулы реагентов и продуктов, находят окислитель,
- 18. Подбор числа атомов водорода и кислорода Кислотная среда [HI] = H+ [OII] + 2H+ = H2O
- 19. Направление ОВР Br– + PbO2 + H+ → Br2 + Pb2+ + H2O Br– + Fe3+
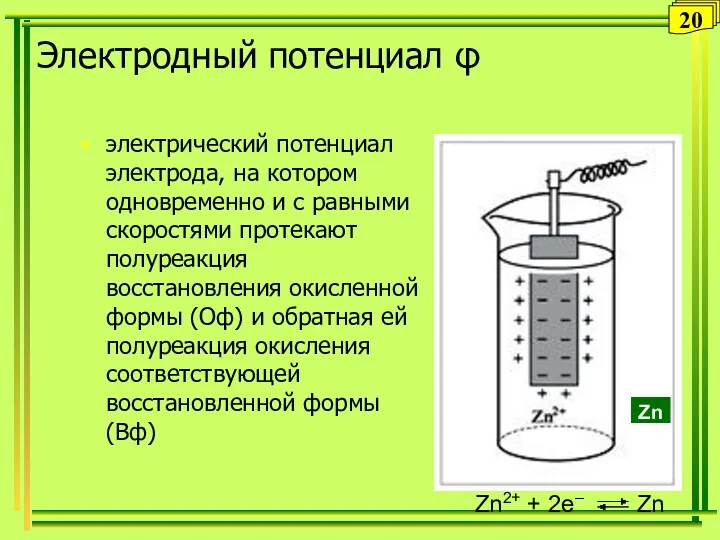
- 20. Электродный потенциал φ электрический потенциал электрода, на котором одновременно и с равными скоростями протекают полуреакция восстановления
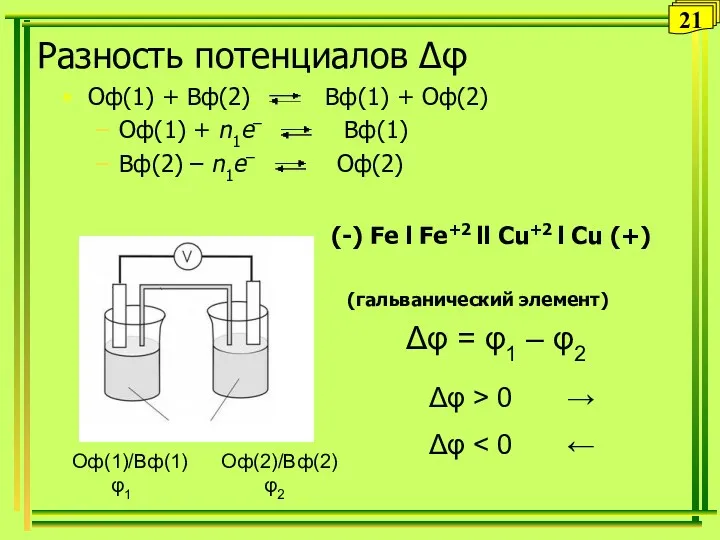
- 21. Разность потенциалов Δφ Оф(1) + Вф(2) Вф(1) + Оф(2) Оф(1) + n1e– Вф(1) Вф(2) – n1e–
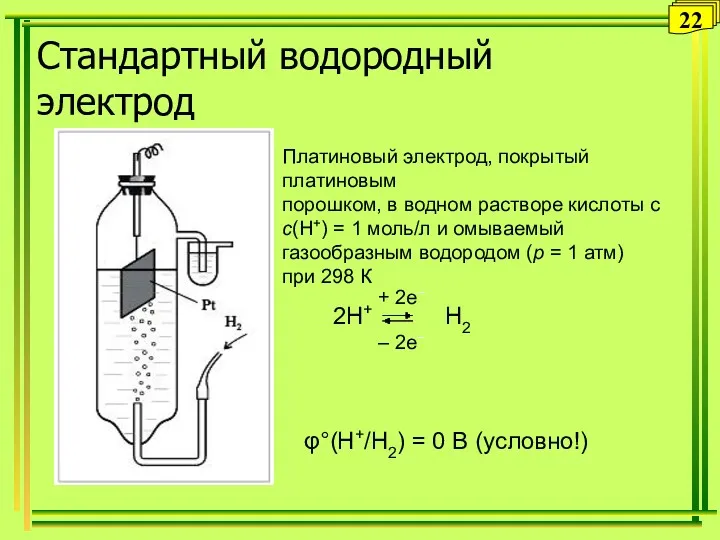
- 22. Стандартный водородный электрод Платиновый электрод, покрытый платиновым порошком, в водном растворе кислоты с с(Н+) = 1
- 23. Стандартный потенциал полуреакции восстановления φ° Оф + Н2 Вф + 2Н+ Δφ° = φ°(Оф/Вф) – φ°(Н+/Н2)
- 24. Сравнение φ° Сила Ок и Вс Сила Вс Сила Ок 24 ЭХРН Электрохимический ряд напряжений
- 25. Критерий протекания ОВР в стандартных условиях ОВР протекает в прямом направлении в стандартных условиях, если Δφ°
- 26. Уравнение Нернста На практике стандартные условия не используются Оф + ne– = Вф MnO4– + 8H+
- 27. Критерий полноты протекания ОВР (В РЕАЛЬНЫХ УСЛОВИЯХ) ОВР протекает в прямом направлении до конца при любых
- 28. Пример Какие галогениды могут быть окислены катионом Fe3+ в стандартных условиях? 2Г– + 2Fe3+ = Г2
- 29. П2. Комплексные соединения металлов, их состав и поведение (устойчивость) в растворах. Константа нестойкости комплексных ионов. Комплексные
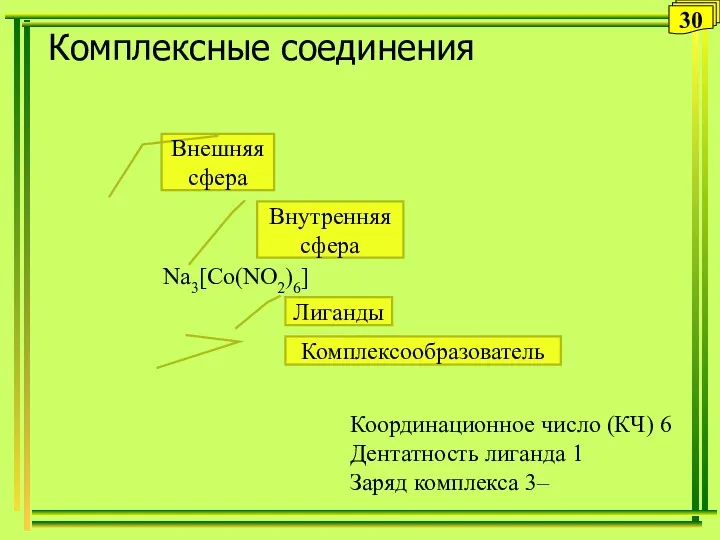
- 30. Комплексные соединения Координационное число (КЧ) 6 Дентатность лиганда 1 Заряд комплекса 3– Внешняя сфера Внутренняя сфера
- 31. Номенклатура комплексных соединений Число лигандов моно, ди, три, тетра, пента и т.д. Названия лигандов Анионные Cl–
- 32. Примеры Гексанитрокобальтат(III) натрия Na3[Co(NO2)6] Гидроксид диамминсеребра(I) [Ag(NH3)2]OH Тетраиодомеркурат(II) калия K2[HgI4] , Тетрароданомеркурат(II) аммония (NH4)2[Hg(SCN)4] 32
- 33. Примеры [Cu(H2O)4]2+ катион тетрааквамеди(II) [Zn(OH)4]2– тетрагидроксоцинкат-ион [Cr(H2O)5OH]2+ катион гидроксопентааквахрома(III) K[BF4] тетрафтороборат калия 33
- 34. Комплексные соединения в растворах Первичная диссоциация комплексных соединений K3[Fe(CN)6] = 3K+ + [Fe(CN)6]3- [Cu(NH3)4]SO4 = [Cu(NH3)4]2+
- 35. Вторичная диссоциация комплексов [Ag(NH3)2]+ [Ag(NH3)]+ + NH3 [Ag(NH3)]+ Ag+ + NH3 [Ag+] [NH3]2 KH = =
- 36. Константы нестойкости некоторых комплексов 36
- 37. Что же такое комплексы? Комплексные соединения – вещества, существующие как в кристаллическом состоянии, так и в
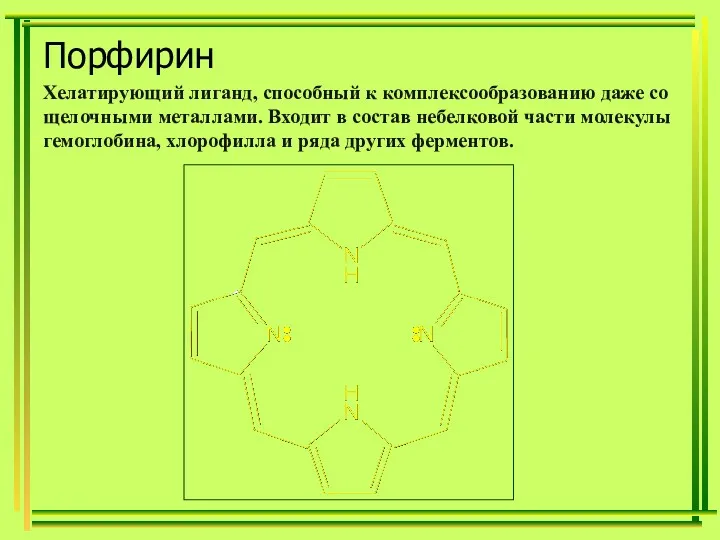
- 38. Порфирин Хелатирующий лиганд, способный к комплексообразованию даже со щелочными металлами. Входит в состав небелковой части молекулы
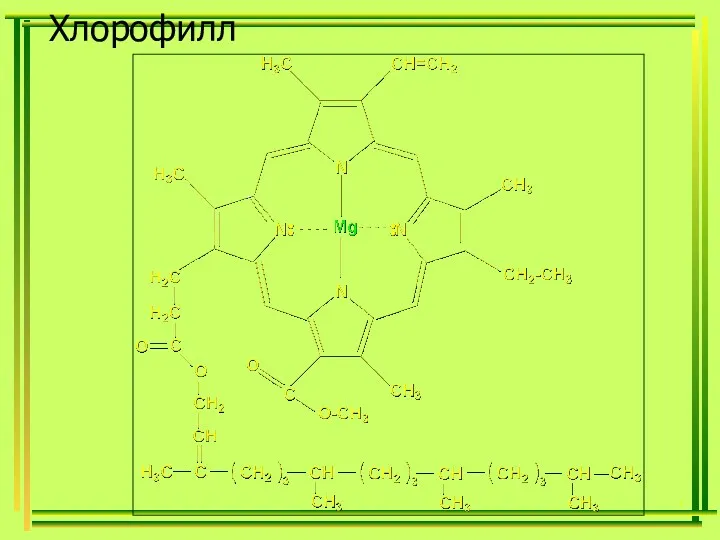
- 39. , Хлорофилл
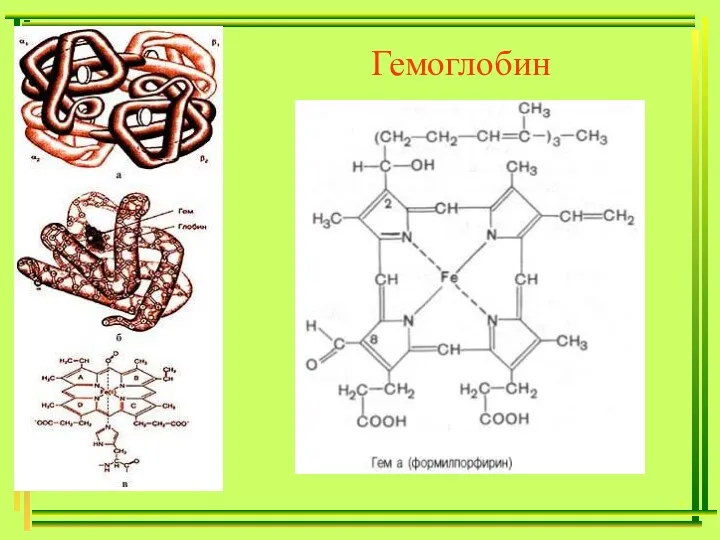
- 40. , Гемоглобин
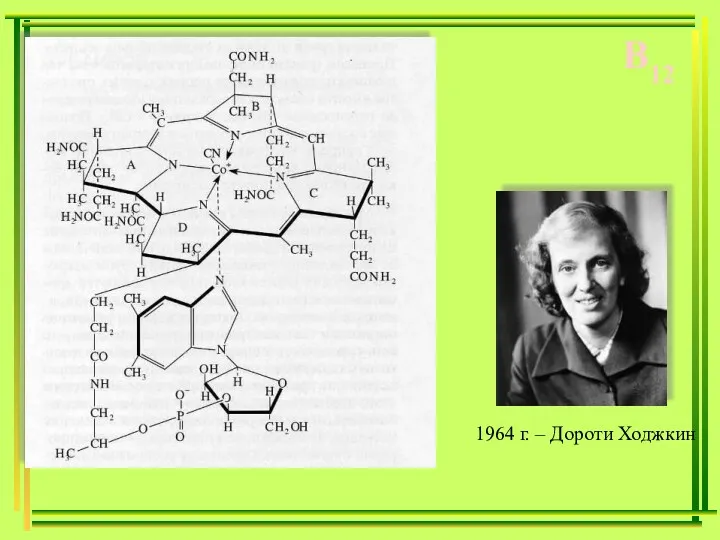
- 41. B12 1964 г. – Дороти Ходжкин
- 42. Дополнительный слайд: Основные соотношения Эквивалент – условная (реально не существующая) частица, в z раз меньшая, чем
- 43. Вопросы к экзамену по общей и неорганической химии 1. Понятия: материя, вещество. Предмет науки химия 2.
- 44. Вопросы к экзамену (продолжение) 10. Основные законы химии: закон сохранения массы вещества, закон постоянства состава вещества,
- 46. Скачать презентацию













![Подбор числа атомов водорода и кислорода Кислотная среда [HI] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/305655/slide-17.jpg)









![Примеры Гексанитрокобальтат(III) натрия Na3[Co(NO2)6] Гидроксид диамминсеребра(I) [Ag(NH3)2]OH Тетраиодомеркурат(II) калия K2[HgI4] , Тетрароданомеркурат(II) аммония (NH4)2[Hg(SCN)4] 32](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/305655/slide-31.jpg)
![Примеры [Cu(H2O)4]2+ катион тетрааквамеди(II) [Zn(OH)4]2– тетрагидроксоцинкат-ион [Cr(H2O)5OH]2+ катион гидроксопентааквахрома(III) K[BF4] тетрафтороборат калия 33](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/305655/slide-32.jpg)
![Комплексные соединения в растворах Первичная диссоциация комплексных соединений K3[Fe(CN)6] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/305655/slide-33.jpg)
![Вторичная диссоциация комплексов [Ag(NH3)2]+ [Ag(NH3)]+ + NH3 [Ag(NH3)]+ Ag+ +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/305655/slide-34.jpg)





 Основы химмотологии моторных топлив. Тема 3
Основы химмотологии моторных топлив. Тема 3 Тему Соли. Нитрат серебра(I) AgNO3
Тему Соли. Нитрат серебра(I) AgNO3 Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов
Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов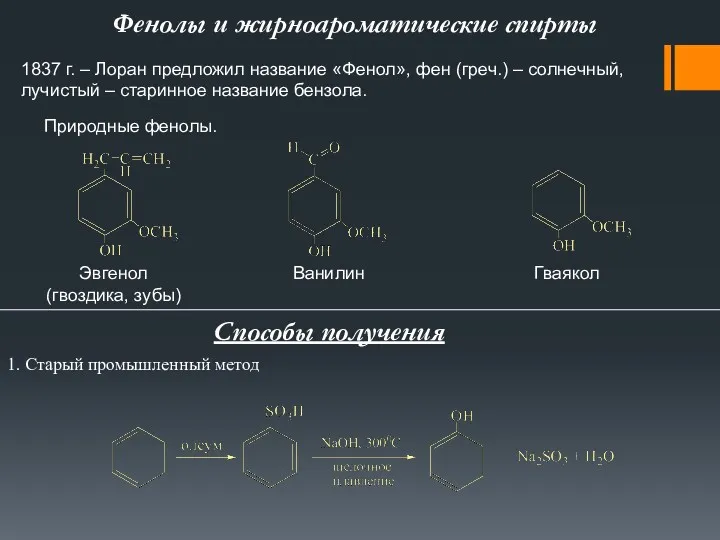 Фенолы и жирноароматические спирты
Фенолы и жирноароматические спирты Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас
Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас бензол
бензол Синтетические моющие средства
Синтетические моющие средства Титриметрический анализ. Кривые титрования
Титриметрический анализ. Кривые титрования III А – топтың элементтері
III А – топтың элементтері Аминокислоты. АТФ
Аминокислоты. АТФ Алканы. Углеводороды. Предельные (насыщенные, алканы)
Алканы. Углеводороды. Предельные (насыщенные, алканы) Амінокислоти
Амінокислоти Типы химических реакций
Типы химических реакций НЮ 2.1.1. Металлы - общая характеристика
НЮ 2.1.1. Металлы - общая характеристика Электрохимические процессы
Электрохимические процессы Марганец. Железо
Марганец. Железо Металлы
Металлы Углерод и его свойства
Углерод и его свойства Лекция № 7. Конкурентные реакции у насыщенного атома
Лекция № 7. Конкурентные реакции у насыщенного атома Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі Кислород
Кислород Химическая кинетика
Химическая кинетика Пластмаси. Пластичні маси
Пластмаси. Пластичні маси Теория твердения минеральных вяжущих веществ
Теория твердения минеральных вяжущих веществ Предмет химии. Вещества
Предмет химии. Вещества Композиты как материалы конструкционного назначения
Композиты как материалы конструкционного назначения Кислородные соединения азота
Кислородные соединения азота Основы химической термодинамики
Основы химической термодинамики