Содержание
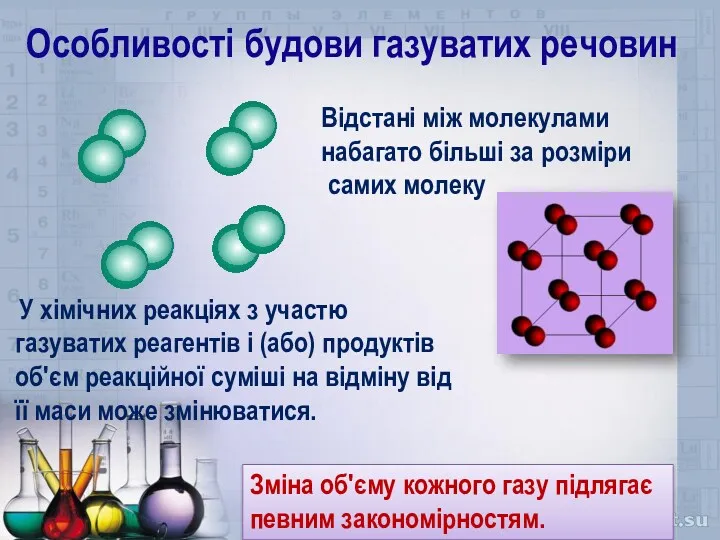
- 2. Особливості будови газуватих речовин Відстані між молекулами набагато більші за розміри самих молеку У хімічних реакціях
- 3. Коротко з історії вивчення відношення об’ємів газів у хімічних реакціях 1783 рік - А.Л. Лавуазьє робить
- 4. Закон об’ємних відношень газів Жозе Луї Гей – Люсак 1808 р. При постійних температурі і тиску
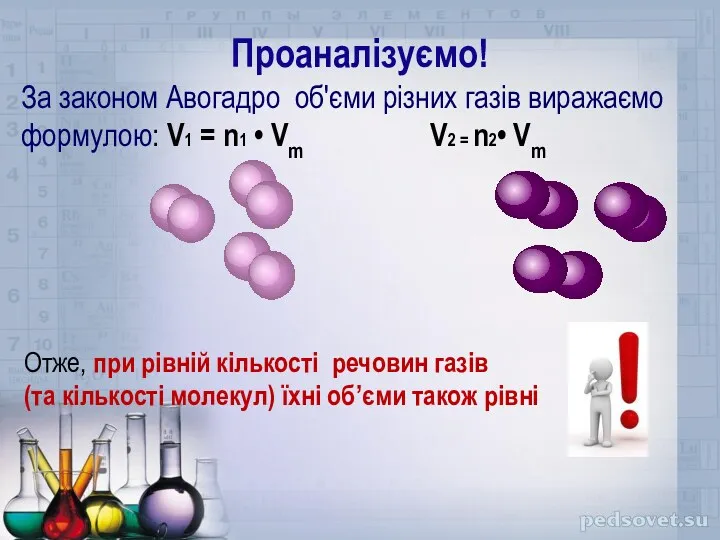
- 5. Проаналізуємо! За законом Авогадро об'єми різних газів виражаємо формулою: V1 = n1 • Vm V2 =
- 6. Об'єми газів відносяться один до одного як їхні кількості Проаналізуймо з огляду на відношення об'ємів газів
- 7. Алгоритм розв’язання найпростіших задач За допомогою відповідних позначень запишемо умову завдання 2. Запишемо рівняння реакції, розставимо
- 8. Дано: V(С2Н2)=50л V(О2)-? Розв’язання: 2С2Н2 + 502 = 4С02 + 2Н2О 50л х л 2 С2Н2
- 9. Задача 1. На опалювання будинку об'ємом 100 м3 за місяць витрачають метану об'ємом 350 м3. Обчисліть
- 11. Задача 3.Обчисліть об’єм повітря ( ᵠ( О2) = 21%), що витратиться для повного спалювання 40 л
- 13. Скачать презентацию








 Аллотропия
Аллотропия Основные классы неорганических соединений
Основные классы неорганических соединений Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Тяжелые металлы. Опасность токсичных металлов для организма
Тяжелые металлы. Опасность токсичных металлов для организма Основные синтетические полимеры
Основные синтетические полимеры Кислотные дожди
Кислотные дожди Механизмы трансформации энергии в фотосинтезе
Механизмы трансформации энергии в фотосинтезе 20230330_zakony_termodinamiki_i_kinetika
20230330_zakony_termodinamiki_i_kinetika S-элементтердің жалпы сипаттамасы
S-элементтердің жалпы сипаттамасы 20230219_prezentatsiya_k_uroku_neft
20230219_prezentatsiya_k_uroku_neft Общая характеристика элементов главной подгруппы второй группы
Общая характеристика элементов главной подгруппы второй группы Розв’язування задач на приготування розчинів із кристалогідратів
Розв’язування задач на приготування розчинів із кристалогідратів Термодинамика растворов неэлектролитов
Термодинамика растворов неэлектролитов Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Технология монокристаллов и особо чистых веществ
Технология монокристаллов и особо чистых веществ Оксиды и гидроксиды металлов. 11 класс
Оксиды и гидроксиды металлов. 11 класс Химические реакции или химические явления
Химические реакции или химические явления Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Факторы и процессы формирования химического состава подземных вод
Факторы и процессы формирования химического состава подземных вод Комплексиметрическое титрование
Комплексиметрическое титрование Электролиз. Классификация
Электролиз. Классификация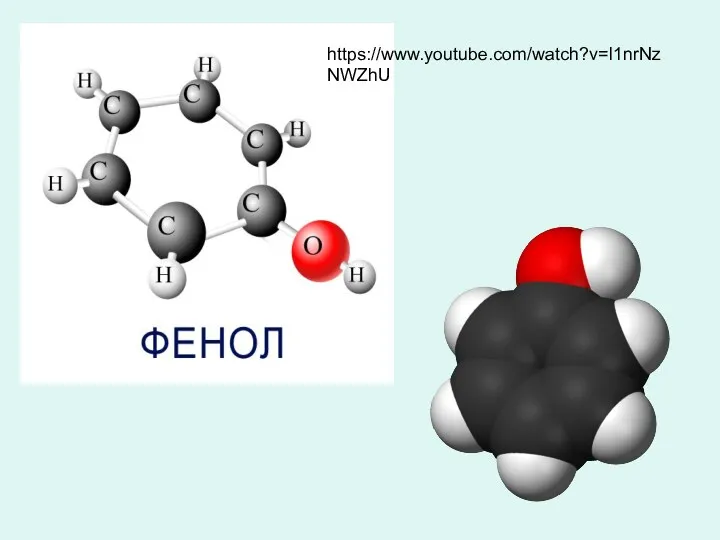 Фенол. Феноловая катастрофа
Фенол. Феноловая катастрофа Составление формул молекулярных простых веществ
Составление формул молекулярных простых веществ Щавелевая кислота
Щавелевая кислота Нанотехнологии и Наноматериалы
Нанотехнологии и Наноматериалы Кислоты. Определение и классификация
Кислоты. Определение и классификация Исследование Е. Е. Вагнера в области терпенов и камфоры
Исследование Е. Е. Вагнера в области терпенов и камфоры