Содержание
- 2. Егор Егорович Вагнер (1849—1903) Родился в Казани. В 1874 г. окончил Казанский университет, ученик А. М.
- 3. Используя эту реакцию, осуществил (1874—18Й) синтез ряда спиртов. Уточнил (1885) правило окисления кетонов, сформулированное Л. Н.
- 4. Терпены Группа преимущественно ненасыщенных углеводородов состава (C5H8)n, где n>=2; широко распространены в природе. Все терпены обычно
- 5. Терпены Каждый ряд терпенов разделяется на группы: 1.Алифатические или ациклические -соед. с открытой цепью углеродных атомов;
- 6. Терпены Сопутствующие обычно терпенам их производные часто называют терпеноидами, по характеру функцнальной групп они разделяются на
- 7. Исследование в области терпенов Результаты исследований в области терпенов Е. Е. Вагнер обобщил в статьях: "К
- 8. Исследование в области терпенов Установив структуру пинола, Е. Е. Вагнер исправил ряд формул для многих родственных
- 9. Исследование в области терпенов Выяснение строения пинена представляло исключительно трудную задачу, так как он легко подвергается
- 10. Исследование в области терпенов Вагнеровская формула пинена была подтверждена Байером в 1896 г. В числе продуктов
- 11. Исследование в области камфары Е. Е. Вагнер провел много исследований в области камфары, ее производных и
- 13. Скачать презентацию
Егор Егорович Вагнер (1849—1903)
Родился в Казани. В 1874 г. окончил
Егор Егорович Вагнер (1849—1903)
Родился в Казани. В 1874 г. окончил
Используя эту реакцию, осуществил (1874—18Й) синтез ряда спиртов. Уточнил (1885) правило
Используя эту реакцию, осуществил (1874—18Й) синтез ряда спиртов. Уточнил (1885) правило
Терпены
Группа преимущественно ненасыщенных углеводородов состава (C5H8)n, где n>=2; широко распространены в
Терпены
Группа преимущественно ненасыщенных углеводородов состава (C5H8)n, где n>=2; широко распространены в
Терпены
Каждый ряд терпенов разделяется на группы:
1.Алифатические или ациклические -соед. с открытой
Терпены
Каждый ряд терпенов разделяется на группы: 1.Алифатические или ациклические -соед. с открытой
Терпены
Сопутствующие обычно терпенам их производные часто называют терпеноидами, по характеру функцнальной
Терпены
Сопутствующие обычно терпенам их производные часто называют терпеноидами, по характеру функцнальной
Исследование в области терпенов
Результаты исследований в области терпенов Е. Е. Вагнер
Исследование в области терпенов
Результаты исследований в области терпенов Е. Е. Вагнер
Сопоставляя строение терпениловой кислоты как нормального продукта окисления с формулой пинола, Е. Е. Вагнер установил, что пинол имеет строение.
Исследование в области терпенов
Установив структуру пинола, Е. Е. Вагнер исправил ряд
Исследование в области терпенов
Установив структуру пинола, Е. Е. Вагнер исправил ряд
Для названных соединений Е. Е. Вагнер предложил следующие формулы.
Исследование в области терпенов
Выяснение строения пинена представляло исключительно трудную задачу, так
Исследование в области терпенов
Выяснение строения пинена представляло исключительно трудную задачу, так
Превращение пинена в собрерол, которое происходит при присоединении к нему двух водных остатков с сохранением этиленовой связи, привело автора к определению строения кольца его молекулы. Иначе говоря, здесь разрывается та же связь, что и при гидратации пинена в терпинеол. Сравнивая эти две формулы, Е. Е. Вагнер выводит формулу пинена
Исследование в области терпенов
Вагнеровская формула пинена была подтверждена Байером в 1896
Исследование в области терпенов
Вагнеровская формула пинена была подтверждена Байером в 1896
Для точного установления наличия в пинене тетраметиленового кольца Е. Е. Вагнер исследовал реакции присоединения к пинену четырех одновалентных атомов или групп, при которых можно было точно найти местонахождение связей; за счет последних и происходит присоединение. Ученый доказал, что при воздействии хлорноватистой кислоты на пинен образуется тридихлоргидрин при прямом присоединении к пинену двух частиц хлорноватистой кислоты по этиленовой и по легко размыкаемой пицеанной связям. Это только подтверждает правильность формулы пинена, установленной Е. Е. Вагнером.
Исследование в области камфары
Е. Е. Вагнер провел много исследований в области
Исследование в области камфары
Е. Е. Вагнер провел много исследований в области
Для камфары в 1894 г. была принята формула строения Бредта.










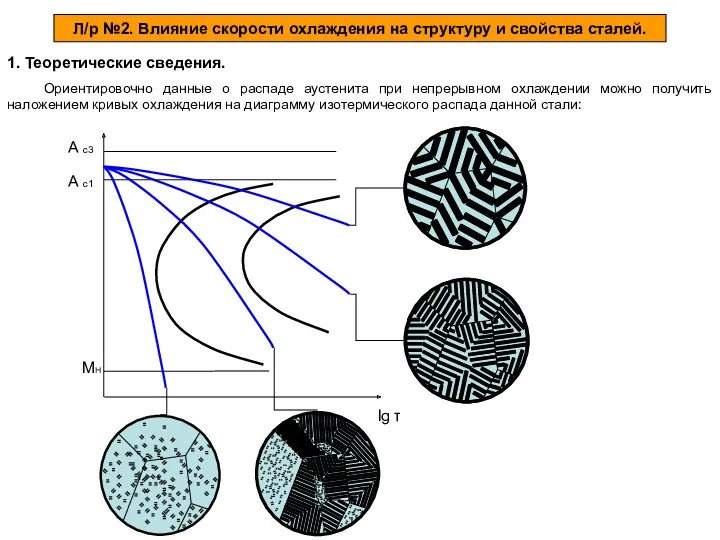 Влияние скорости охлаждения на структуру и свойства сталей
Влияние скорости охлаждения на структуру и свойства сталей Тема 7-Карбоновые кислоты
Тема 7-Карбоновые кислоты Ионное произведение воды. Водородный показатель воды
Ионное произведение воды. Водородный показатель воды Поліметилметакрилат
Поліметилметакрилат Растворение как физико-химический процесс
Растворение как физико-химический процесс 20231011_8_klass_binarnye_soedineniya
20231011_8_klass_binarnye_soedineniya Порівняльний аналіз методів відновлення свинцево-кислотних акумуляторів
Порівняльний аналіз методів відновлення свинцево-кислотних акумуляторів Коррозия металлов. Причины коррозии металлов
Коррозия металлов. Причины коррозии металлов Классификация органических соединений. Теория химического строения вещества. 10 класс
Классификация органических соединений. Теория химического строения вещества. 10 класс Кислоты и щелочи. Индикаторы. 6 класс
Кислоты и щелочи. Индикаторы. 6 класс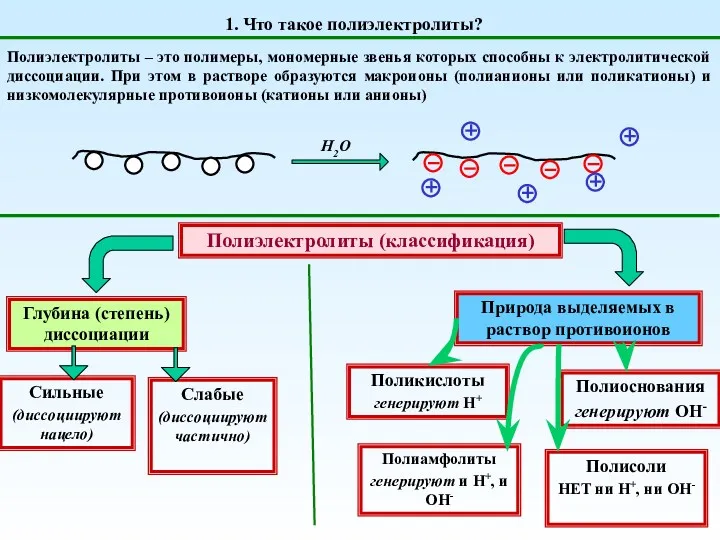 Полиэлектролиты. (Тема 3)
Полиэлектролиты. (Тема 3) Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Кислоты. Классификация. Химические свойства. 8 класс
Кислоты. Классификация. Химические свойства. 8 класс Осадочные и метаморфические горные породы
Осадочные и метаморфические горные породы Реакции ионного обмена
Реакции ионного обмена Щелочные металлы
Щелочные металлы 20230419_kontsentratsiya
20230419_kontsentratsiya Морские льды. Их классификация и закономерности движения
Морские льды. Их классификация и закономерности движения Одноатомные спирты. Простые эфиры
Одноатомные спирты. Простые эфиры Основные законы и понятия химии
Основные законы и понятия химии Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток
Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток Техника безопасности и правила работы в лаборатории. 10 класс
Техника безопасности и правила работы в лаборатории. 10 класс Органическая химия. Подготовка к контрольной работе № 2
Органическая химия. Подготовка к контрольной работе № 2 Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Analytical methods in modern research. Chromatography
Analytical methods in modern research. Chromatography Аммиак. Строение молекулы аммиака, его физические и химические свойства
Аммиак. Строение молекулы аммиака, его физические и химические свойства Разбираем задания
Разбираем задания Механическая смесь и растворы
Механическая смесь и растворы