Содержание
- 2. Реакции между ионами называют ионными реакциями, а уравнения таких реакций – ионными уравнениями. Большинство химических реакций
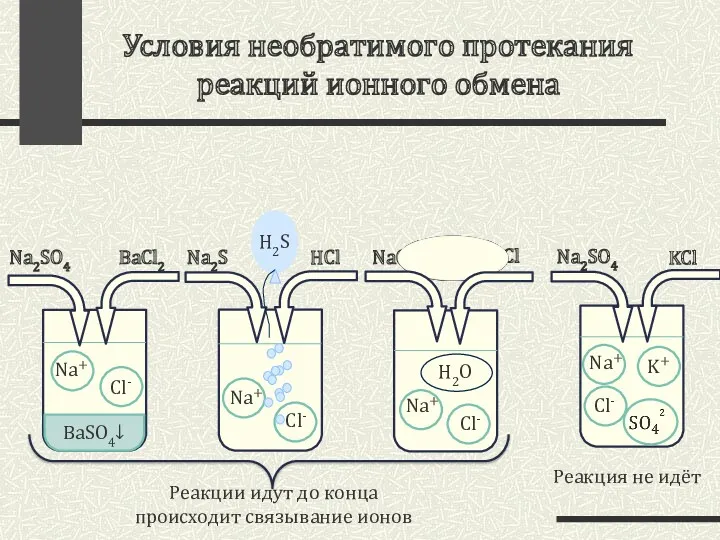
- 3. Условия необратимого протекания реакций ионного обмена Na2SO4 KCl Na2SO4 BaCl2 Реакция не идёт Na2S HCl NaOH
- 4. Правила составления ионных уравнений При составлении ионных уравнений следует руководствоваться тем, что вещества малодиссоциирующие, нерастворимые и
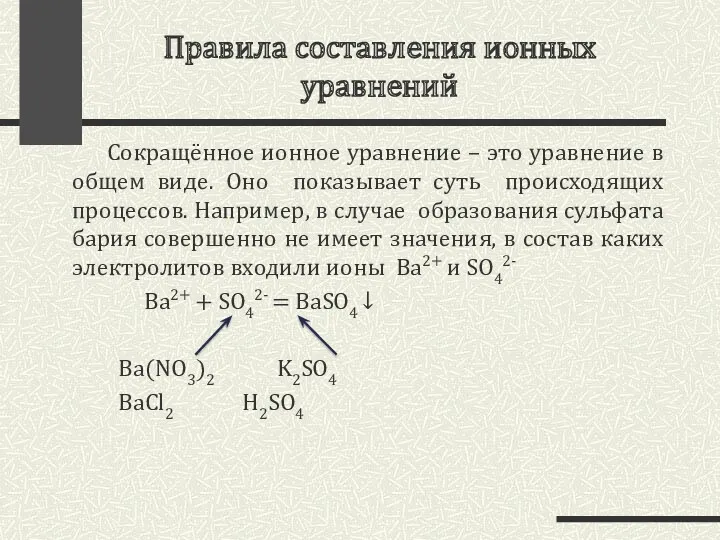
- 5. Правила составления ионных уравнений Сокращённое ионное уравнение – это уравнение в общем виде. Оно показывает суть
- 6. Правила составления ионных уравнений
- 7. Правила составления ионных уравнений Пример: Взаимодействие сульфата натрия с хлоридом бария. 1. Запишем уравнение в молекулярном
- 8. Правила составления ионных уравнений Пример: Взаимодействие серной кислоты с хлоридом бария. 1. Запишем уравнение в молекулярном
- 9. Примеры реакций ионного обмена Молекулярное уравнение реакции щелочи с кислотой: КOH + HCl = KCl +
- 10. Примеры реакций ионного обмена Молекулярное уравнение реакции основного оксида с кислотой: CaO + 2HNO3 = Ca(NO3)2
- 11. Примеры реакций ионного обмена Молекулярное уравнение реакции растворимой соли со щелочью: CuCl2 + 2KOH = 2KCl
- 12. Примеры реакций ионного обмена
- 13. Примеры реакций ионного обмена Молекулярное уравнение реакции растворимой соли (сульфида) с кислотой: K2S + 2HCl =
- 14. Примеры реакций ионного обмена
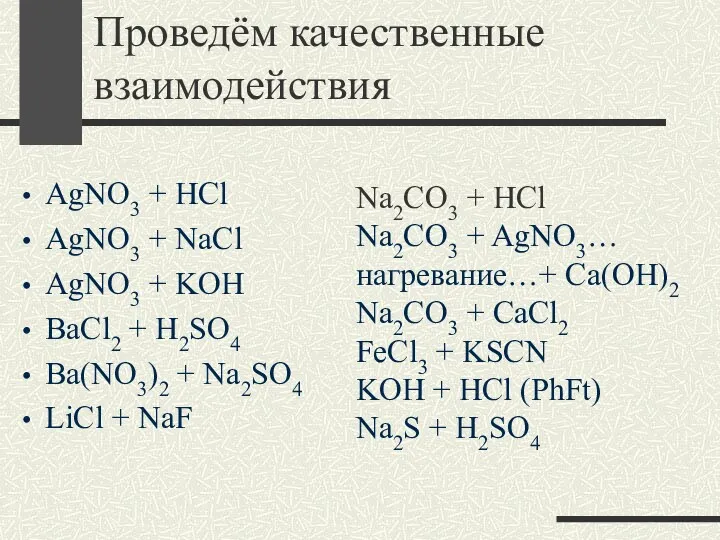
- 15. Проведём качественные взаимодействия AgNO3 + HCl AgNO3 + NaCl AgNO3 + KOH BaCl2 + H2SO4 Ba(NO3)2
- 17. Скачать презентацию











 Углерод. Элемент IV группы
Углерод. Элемент IV группы Электронный помощник по химии 8 класс
Электронный помощник по химии 8 класс Химия переходных элементов IV – V группы
Химия переходных элементов IV – V группы Общая характеристика неметаллов
Общая характеристика неметаллов Ископаемые углеводороды
Ископаемые углеводороды Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Гидролиз солей
Гидролиз солей Неорганическая химия
Неорганическая химия Химический анализ веществ
Химический анализ веществ Альдегиды и кетоны
Альдегиды и кетоны Углеводы. 10 класс
Углеводы. 10 класс Углеводороды. Применение природных источников углеводородов и продуктов их переработки
Углеводороды. Применение природных источников углеводородов и продуктов их переработки Состав, строение и свойства натурального каучука
Состав, строение и свойства натурального каучука Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары
Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары Химическая технология природных энергоносителей и углеродных материалов
Химическая технология природных энергоносителей и углеродных материалов Кислые породы умеренно-щелочного ряда
Кислые породы умеренно-щелочного ряда Классификация химических реакций
Классификация химических реакций Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды Первые шаги в минералогию: от новичка до знатока
Первые шаги в минералогию: от новичка до знатока Инертные газы
Инертные газы Металлогеническая периодизация истории Земли. Геолого-металлогенические ранги
Металлогеническая периодизация истории Земли. Геолого-металлогенические ранги Диссоциация кислот, оснований, солей
Диссоциация кислот, оснований, солей 20231110_zakon_avogadro
20231110_zakon_avogadro Спирттер мен фенолдар
Спирттер мен фенолдар Аминокислоты и белки
Аминокислоты и белки Карбон
Карбон Класифікація дисперсних систем харчових продуктів. Характеристика колоїдних систем
Класифікація дисперсних систем харчових продуктів. Характеристика колоїдних систем Азотная кислота
Азотная кислота