Содержание
- 2. Происхождения названий Ti – титаны, персонажи древнегреч. мифологии, дети Геи; название дал Мартин Клапрот. Zr –
- 3. IV группа
- 4. Природа сходства Zr и Hf (лантанидное сжатие) Устойчивость высших степеней окисления Ti Zr Hf TiO, Ti2O3,
- 6. Природные формы, получение Ti (0.6 %), 10-й элемент по распространенности (7-ой среди металлов) FeTiO3 – ильменит
- 7. Природные формы, получение Zr (0.02%), 21-й элемент по распространенности ZrSiO4 – циркон ZrO2 – бадделит
- 8. Природные формы, получение Hf (4·10-4 %, сопутствует Zr), 52-й элемент по распространенности Th (2·10-3 %), 232Th
- 9. TiO2 + 2C + 2Cl2→ TiCl4 + 2CO Дистилляция TiCl4 (283ºC) – FeCl3 (317 ºC) TiCl4
- 10. Ti открыт в рутиле 200 лет назад Клапротом Zr открыт более 150 лет назад в цирконе
- 11. Ti легкий конструкционный материал ( в 3-5 раз прочнее Al и Mg) ферротитан ( 0,1% Ti
- 12. Материалы с эффектом памяти формы
- 13. Химические свойства Восстановители, пассивация С водородом МНх (обратимость, аккумуляторы, 1 г Ti → 2 л Н2)
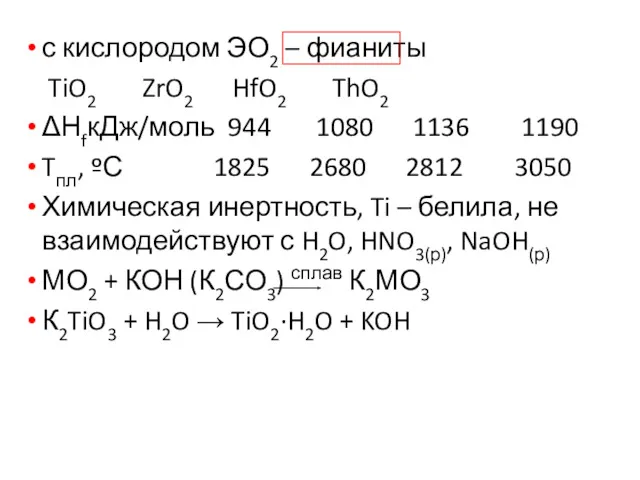
- 14. с кислородом ЭО2 – фианиты TiO2 ZrO2 HfO2 ThO2 ΔΗfкДж/моль 944 1080 1136 1190 Tпл, ºС
- 15. M + N2→ MN “TiN” ~ Au (коронки) — MO2 + 6HF → H2[ЭF6] + 2H2O
- 16. M + 2Г2→ МГ4 МО2 + 2Г2 = МГ4 + О2 (ΔG>0) 2C + О2 =
- 17. Фотокатализ (нанопроволока TiO2) Гидротермальная обработка геля TiO2·nH2O (T = 110 – 250 ºC; t = 20
- 18. Фотонный кристалл TiO2
- 19. МГ4 – бесцветные, твердые вещества (исключение TiCl4) Молекулярные решетки TiCl4 ZrCl4 HfCl4 ThCl4 tплºC -23 437
- 20. 3 TiCl4 +4H2O → 2H2TiCl6 + Ti(OH)4 [TiCl6]2-+H2O→[TiCl5(H2O)]1- H2O [TiCl4(H2O)2] 2H2O [TiCl2(H2O)4]2+ → [Ti(OH)Cl2(H2O)3]1+ → →
- 21. H2O OH OH OH OH H2O Ti H2O H2O OH OH OH OH Ti -2H2O H2O
- 22. Оловые мостики + 2H+ 2- Ti Ti OH OH OH OH O O OH OH HO
- 23. Э4+ + H2O = ЭО2+ + 2H+ Солеобразующий характер МОГ2, МО(NO3)2 Соли титанила, цирконила TiOCl2, ZrOBr2
- 24. Соединения М (+3) 2TiOSO4 + Zn + 2H2SO4 = Ti2(SO4)3 + ZnSO4 +2H2O [Ti(H2O)6]3+ [Ti(H2O)6]3+ Δ
- 26. Место в п.с.э. V –“ванадис” – богиня радости, красоты Nb – “ниобея” – полубогиня, дочь Тантала
- 27. Флеров, Дубна
- 28. Сходство V5+ (0.40 Å) и P5+ (0.37 Å) Оксоанионы ЭО3- (NaVO3, NaPO3) В высших степенях окисления
- 31. Степени окисления и стереохимия
- 32. Степени окисления и стереохимия
- 33. V – 0.02% (22 место), сопутствует Fe (Fe3+ - 0.67 Å, V3+ - 0.65 Å) Mn
- 34. Ta~ 10-5 % (65 место) танталит(Fe, Mn)(TaO3)2 Лопарит (Хибины) (Ca, Sr, Ce, Na, K)[(Nb, Ta, Ti)O3]
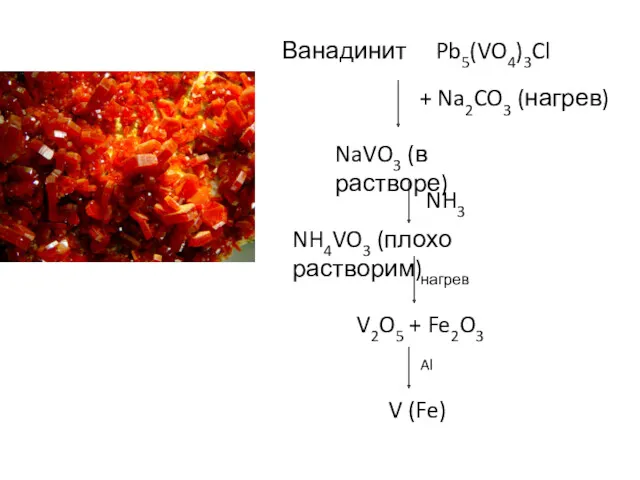
- 35. Ванадинит Pb5(VO4)3Cl + Na2CO3 (нагрев) NaVO3 (в растворе) NH3 NH4VO3 (плохо растворим) нагрев V2O5 + Fe2O3
- 36. При выплавке стали V переходит в шлаки в форме FeV2O4 (структура шпинели) Далее обжигают смесь 2
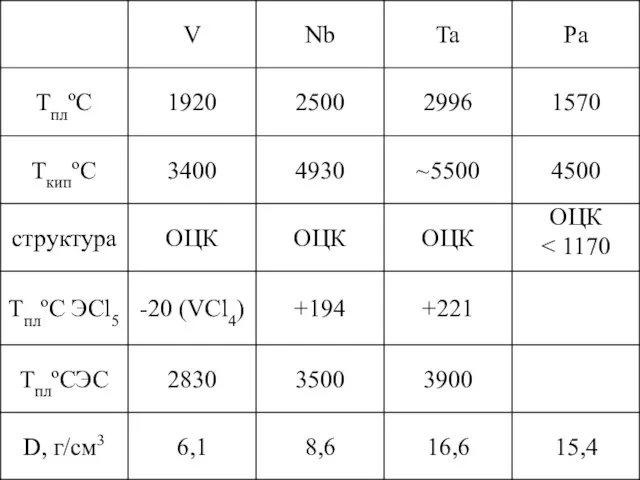
- 38. Высокая химическая инертность V, особенно Nb и Ta V – растворяется только в концентрированных HNO3, H2SO4,
- 39. V(5) → V(4) VnO2n+1, Катализ: SO2 → SO3, нафталин → фталевый ангидрид
- 40. Оксиды ванадия V2O5 – структура из тригональных бипирамид ∙ ∙ ∙VnO2n+1 (V3O7, V4O9, V6O13) ∙ ∙
- 41. V + HF → H[VF6] + H2↑ V + HNO3 → VO2NO3 + NO2 ↑ +
- 42. Э + HF → H[ЭF6] + H2↑, Э = Nb, Ta Э + HNO3 + HF→H2[ЭF7]
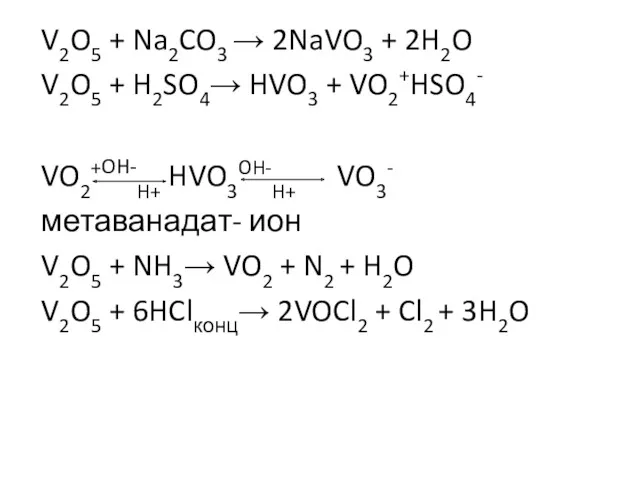
- 43. V2O5 + Na2CO3 → 2NaVO3 + 2H2O V2O5 + H2SO4→ HVO3 + VO2+HSO4- VO2+OH-H+ HVO3OH-H+ VO3-
- 44. Ванадиевые бронзы LixV2O5 Э2O5 + 10 NaOH спл. 2Na5ЭO5 + 5H2O↑ Э2O5 + 3Na2CO3спл. 2Na3ЭO5 +
- 45. Катионные и анионные формы V5+в водном растворе В сильнощелочной среде VO43- Аналогия VO43- и РO43-, тетраэдр
- 46. Изополисоединения 3HVO42- (б/цв)+ 3H+ = V3O93-(ж)+ 3H2O Дальнейшее подкисление дает V4O124-, V10O286-, V2O5
- 47. Изополиванадаты
- 48. Закономерности (по мере уменьшения pH) Повышение КЧ от 4 до 6 Усиление окраски Усиление способности к
- 49. Пероксидные соединения V2O5 + 4H2O2 + 6NaOH = 2Na3VO6 + 3H2O пероксоанион фиолетовый (pH > 12),
- 50. желтый синий зеленый фиолетовый VSO4·7H2O – ванадиевый купорос
- 52. Nb (Ta) + O2tº Nb2(Ta2)O5 Э2O5 – химически инертны, не реагируют с H2O, водными растворами кислот
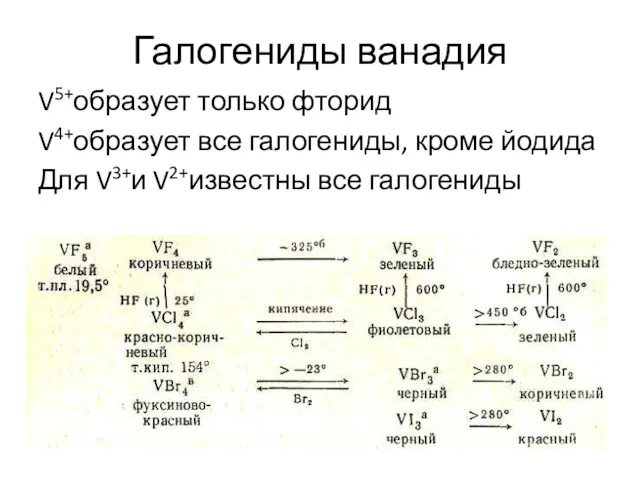
- 53. Галогениды ванадия V5+образует только фторид V4+образует все галогениды, кроме йодида Для V3+и V2+известны все галогениды
- 54. Ванадий (V) в растворах
- 55. Нитевидные кристаллы BaV8O21-δ + 5.1 Li+ + 5.1 e- ↔ Li5.1BaV8O21-δ(в пределах 4 – 2,1 В)
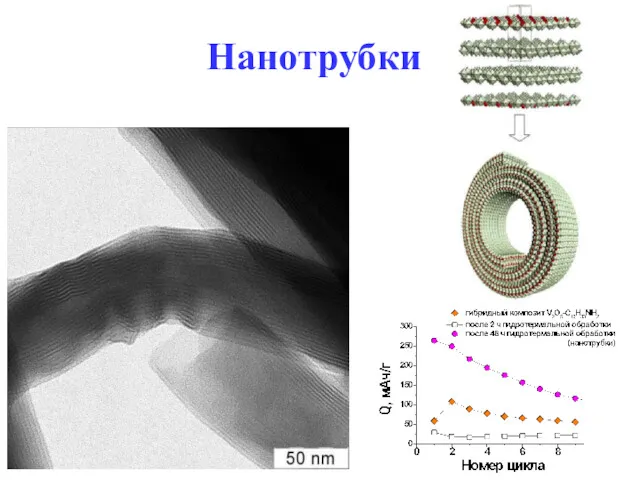
- 56. Нанотрубки
- 57. Аккумулятор Системы с высоким потенциалом полуреакции Высокая емкость Высокая площадь поверхности для быстрой перезарядки Сохранение свойств
- 59. Скачать презентацию












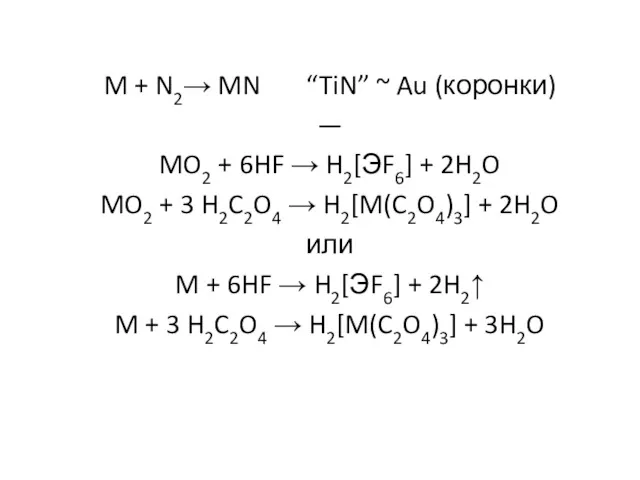




![3 TiCl4 +4H2O → 2H2TiCl6 + Ti(OH)4 [TiCl6]2-+H2O→[TiCl5(H2O)]1- H2O [TiCl4(H2O)2]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/157760/slide-19.jpg)


















![V + HF → H[VF6] + H2↑ V + HNO3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/157760/slide-40.jpg)
![Э + HF → H[ЭF6] + H2↑, Э = Nb,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/157760/slide-41.jpg)












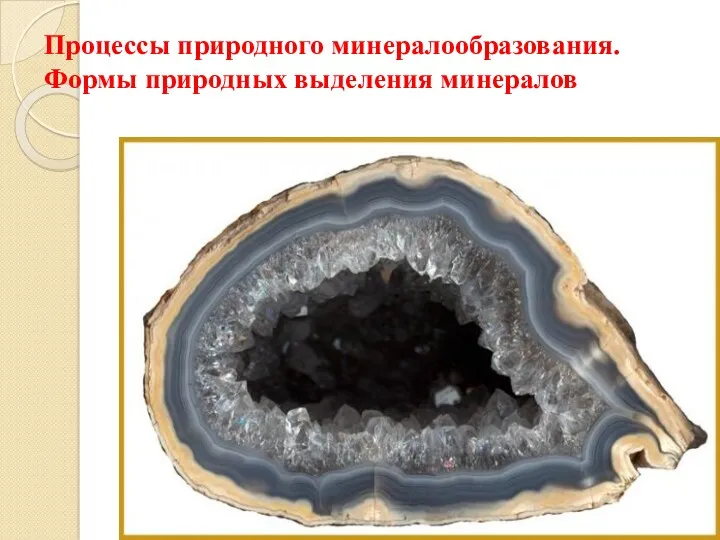 Процессы природного минералообразования. Формы природных выделений минералов
Процессы природного минералообразования. Формы природных выделений минералов 20191107_binarnye_oksidy_1
20191107_binarnye_oksidy_1 Основания
Основания Характер химического элемента по кислотно- основным свойствам. (Амфотерные соединения)
Характер химического элемента по кислотно- основным свойствам. (Амфотерные соединения) Химические свойства спиртов. Химические свойства предельных одноатомных спиртов
Химические свойства спиртов. Химические свойства предельных одноатомных спиртов Жаңа дәрілерді жасау
Жаңа дәрілерді жасау Реакции ионного обмена в растворах электролитов. рH раствора как показатель кислотности среды
Реакции ионного обмена в растворах электролитов. рH раствора как показатель кислотности среды Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах
Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах Спирты одноатомные и многоатомные
Спирты одноатомные и многоатомные Углерод
Углерод 20230306_oksidy
20230306_oksidy Химические свойства металлов. Электрохимический ряд напряжения металлов
Химические свойства металлов. Электрохимический ряд напряжения металлов Индикаторы на кухне
Индикаторы на кухне Развитие теории восстановления металлов
Развитие теории восстановления металлов Химическая связь
Химическая связь Экспериментальное решение задач по теме: Классы неорганических соединений
Экспериментальное решение задач по теме: Классы неорганических соединений Алкадиены
Алкадиены Правила работы в лаборатории и приёмы обращения с лабораторным оборудованием (8 класс)
Правила работы в лаборатории и приёмы обращения с лабораторным оборудованием (8 класс) Термопластичные полимеры
Термопластичные полимеры Сутектік көрсеткіш ph. Тұздар гидролизі
Сутектік көрсеткіш ph. Тұздар гидролизі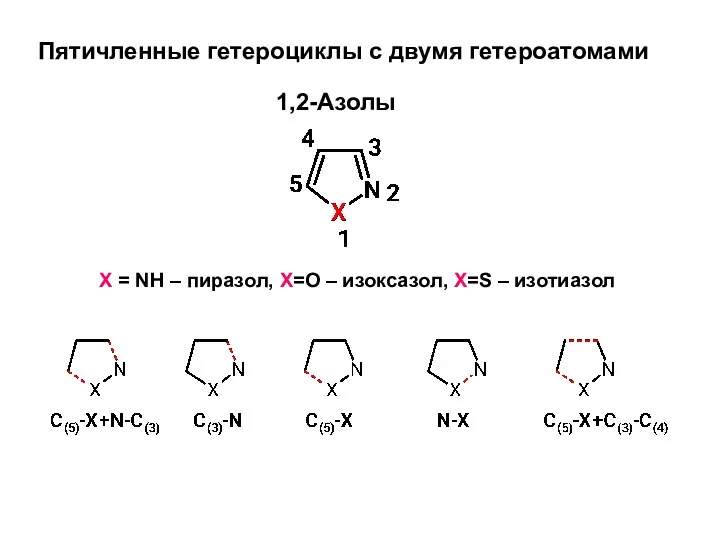 Пятичленные гетероциклы с двумя гетероатомами
Пятичленные гетероциклы с двумя гетероатомами Знакомство с образцами химических средств санитарии и гигиены
Знакомство с образцами химических средств санитарии и гигиены Периодический закон Д. И. Менделеева
Периодический закон Д. И. Менделеева Твердотільний ямр
Твердотільний ямр Оксид меди
Оксид меди Возникновение и развитие научной химии
Возникновение и развитие научной химии Технология получения многослойного и малослойного графена
Технология получения многослойного и малослойного графена Коррозия металлов
Коррозия металлов