Слайд 2

История:
Латинское название меди Cuprum произошло от названия острова Кипр, где уже
в III в. до н. э. существовали медные рудники и производилась выплавка меди. Слова медь и медный встречаются в древнейших русских литературных памятниках. Русское слово "медь" производят от греческого слова, означающего рудник, копь.
Слайд 3

Физические свойства:
Медь — тяжелый розово-красный металл, мягкий и ковкий, плавится при
температуре 1083°С, очень хорошо проводит элект рический ток и теплоту: электрическая проводимость меди в 1,7 раза выше, чем алюминия, в 6 раз выше железа и лишь немного уступает электрической проводимости серебра.
Слайд 4

Химические свойства:
Оксид меди (II) разлагается при нагревании до 1100оС:2CuO=2Cu+O2.
- Окись меди
реагирует с кислотами:
CuO+2HNO3=Cu(NO3)2+H2O;
CuO+H2SO4=CuSO4+H2O - получение медного купороса.
- При реакции с гидроксидами образуются купраты:
CuO+2NaOH=Na2CuO2+H2O.
- Реакции оксида меди (II) с углем, монооксидом углерода, аммиаком и водородом являются реакциями восстановления:
2CuO+C=2Cu+CO2.CuO+H2=Cu+H2O
Слайд 5

Получение:
Получение оксида меди CuO возможно при нагревании соединений:
меди (II) нитрата
2Cu(NO3)2 → 4 NO2+ O2 + 2CuO;
меди (II) гидроксида Cu(OH)2 → H2O + CuO;
меди (II) карбоната CuCO3 → CO2 + CuO.
Cuprum (II) оксид является основным, поэтому он растворяется в минеральных кислотах (соляной, серной и азотной) с получением соответствующей соли двухвалентной Cu:
2HCl + CuO → CuCl2 + H2O; H2SO4 + CuO → CuSO4 + H2O; 2HNO3 + CuO → Cu(NO3)2 + H2O.
Реагирует оксид меди (II) с концентрированной щелочью с образованием соли:
2 KOH + CuO + H2O → K2[Cu (OH)4].
Окисел также может быть восстановлен до металлической Cu при взаимодействии с водородом или окисью углерода: H2 + CuO → Cu + H2O;
CO + CuO → Cu + CO2.
Слайд 6

Применение:
CuO используют при производстве стекла и эмалей для придания им зелёной
и синей окраски. Кроме того, оксид меди применяют в производстве медно-рубинового стекла.
В лабораториях применяют для обнаружения восстановительных свойств веществ. Вещество восстанавливает оксид до металлической меди, при этом чёрный цвет оксида меди переходит в розовую окраску меди.





 Основы химмотологии моторных топлив. Тема 3
Основы химмотологии моторных топлив. Тема 3 Тему Соли. Нитрат серебра(I) AgNO3
Тему Соли. Нитрат серебра(I) AgNO3 Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов
Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов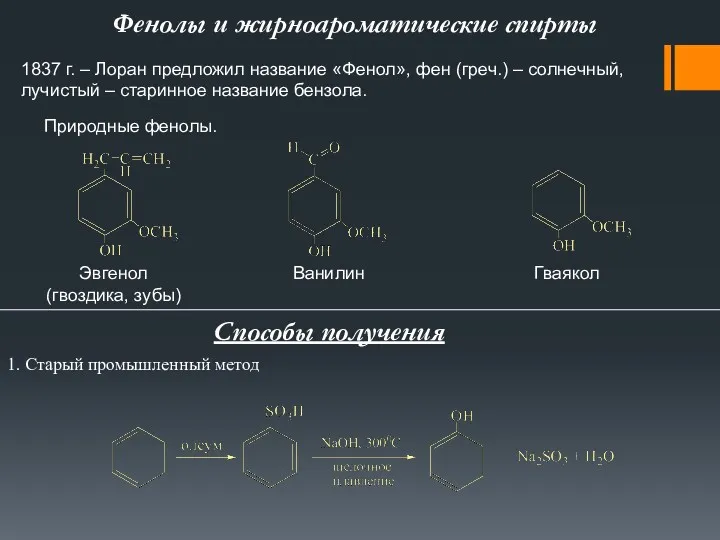 Фенолы и жирноароматические спирты
Фенолы и жирноароматические спирты Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас
Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас бензол
бензол Синтетические моющие средства
Синтетические моющие средства Титриметрический анализ. Кривые титрования
Титриметрический анализ. Кривые титрования III А – топтың элементтері
III А – топтың элементтері Аминокислоты. АТФ
Аминокислоты. АТФ Алканы. Углеводороды. Предельные (насыщенные, алканы)
Алканы. Углеводороды. Предельные (насыщенные, алканы) Амінокислоти
Амінокислоти Типы химических реакций
Типы химических реакций НЮ 2.1.1. Металлы - общая характеристика
НЮ 2.1.1. Металлы - общая характеристика Электрохимические процессы
Электрохимические процессы Марганец. Железо
Марганец. Железо Металлы
Металлы Углерод и его свойства
Углерод и его свойства Лекция № 7. Конкурентные реакции у насыщенного атома
Лекция № 7. Конкурентные реакции у насыщенного атома Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі Кислород
Кислород Химическая кинетика
Химическая кинетика Пластмаси. Пластичні маси
Пластмаси. Пластичні маси Теория твердения минеральных вяжущих веществ
Теория твердения минеральных вяжущих веществ Предмет химии. Вещества
Предмет химии. Вещества Композиты как материалы конструкционного назначения
Композиты как материалы конструкционного назначения Кислородные соединения азота
Кислородные соединения азота Основы химической термодинамики
Основы химической термодинамики