Содержание
- 2. План 7.1.Реакции нуклеофиль-ного замещения (SN) 7.2.Реакции элиминиро-вания (Е)
- 3. К конкурентным реакциям у насыщенного атома углерода относятся реакции нуклеофильного замещения и элиминирования 7.1.Реакции нуклеофильного замещения
- 4. Нуклеофильное замещение у насыщенного атома углерода представляет собой одну из наиболее важных в синтетическом плане органических
- 5. По типу реакций SN и Е протекают многие биологические реакции (алкилирование, дегидратация)
- 6. Конкурентные реакции SN и Е протекают в одной молекуле, но на разных реакционных центрах
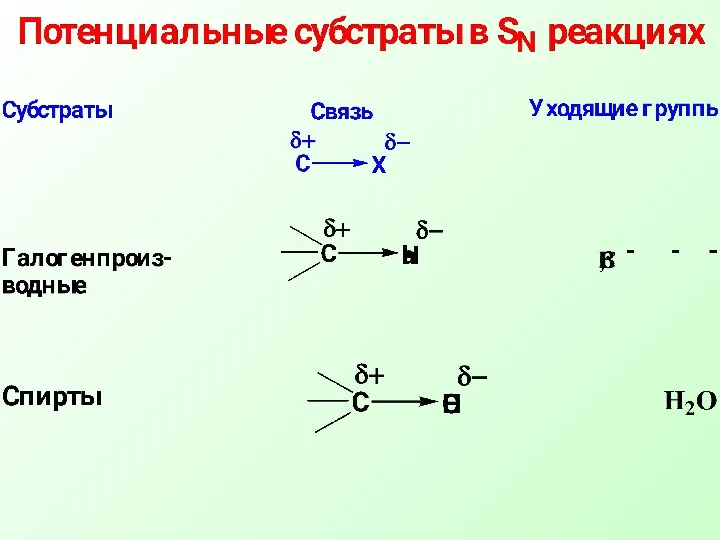
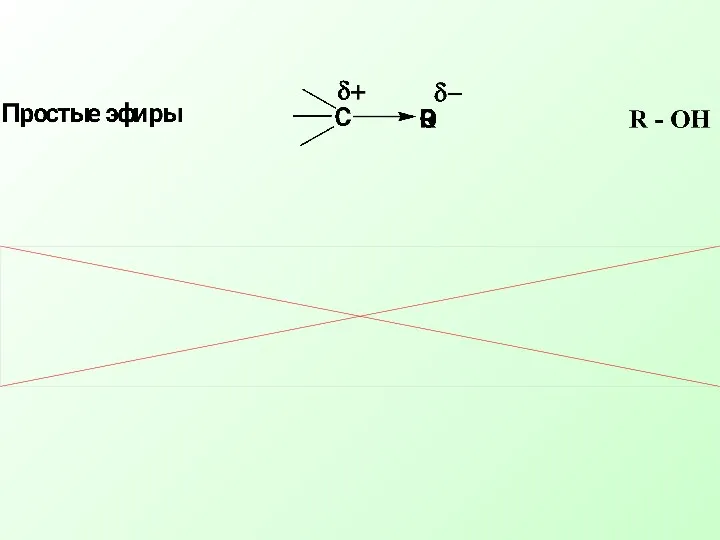
- 7. Нуклеофильное замещение при насыщенном атоме углерода характерно для алкилгалогенидов, спиртов, тиолов, аминов
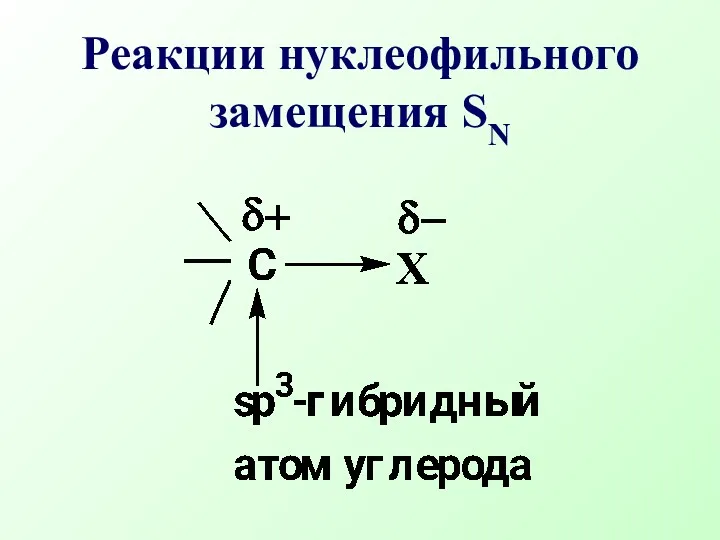
- 8. Реакции нуклеофильного замещения SN
- 9. Введение в насыщенный углеводородный скелет молекулы электроноакцепторной группировки Х приводит к перераспределению электронной плотности в молекуле
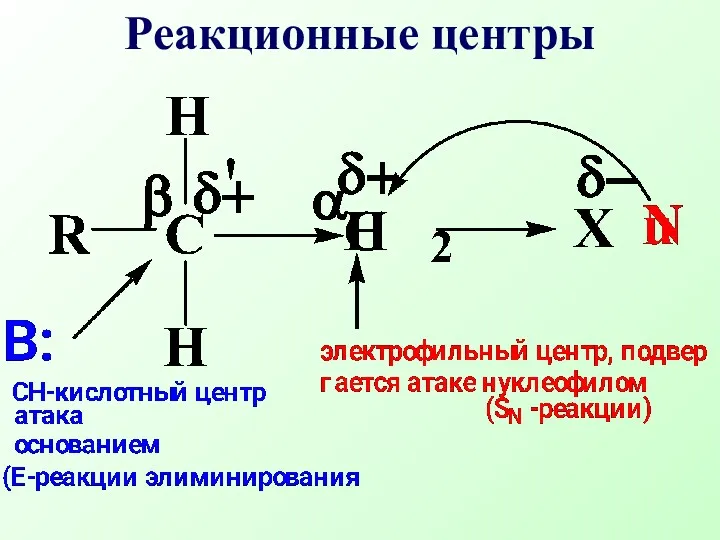
- 10. Реакционные центры
- 11. В таких соединениях атом углерода связан σ-связью с электроакцепторным атомом (Нal, О, N, S) и вследствие
- 12. Схема реакции SN
- 13. Реакция возможна, т.е. протекает вправо, когда уходящая группа (Х-) более стабильна, чем нуклеофил, т.е. имеет меньшую
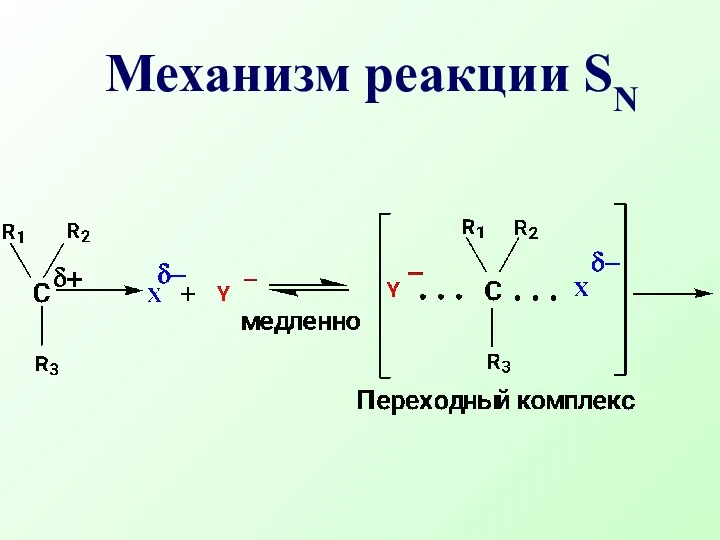
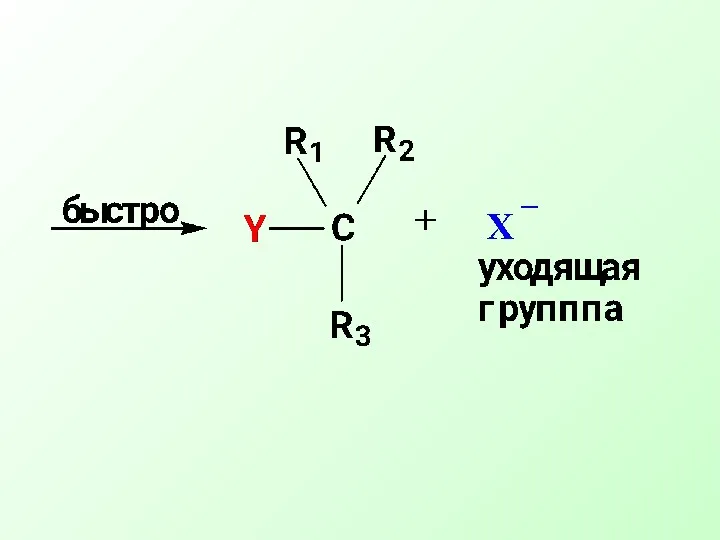
- 14. Механизм реакции SN
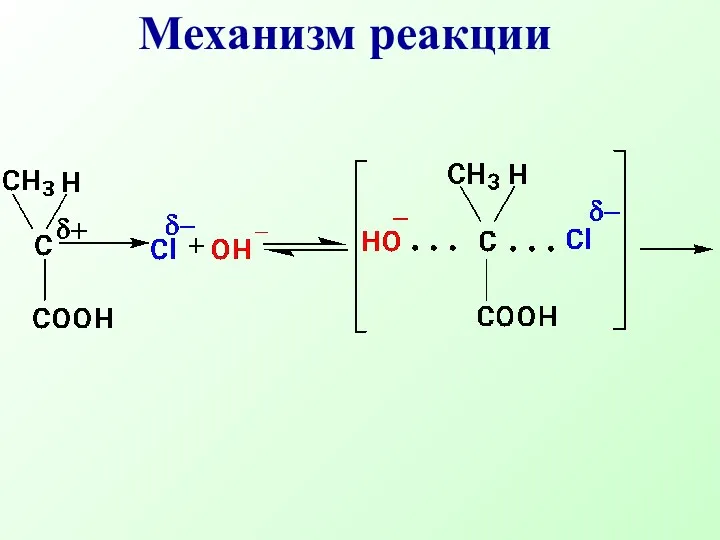
- 16. Нуклеофильная частица Y- атакует атом углерода с наиболее выгодной стороны (противоположной уходящей группе «атака с тыла»).
- 17. Реакция бимолекулярная, скорость реакции зависит от концентрации обоих реагентов. Переходное состояние соответствует максимуму на энергетической кривой
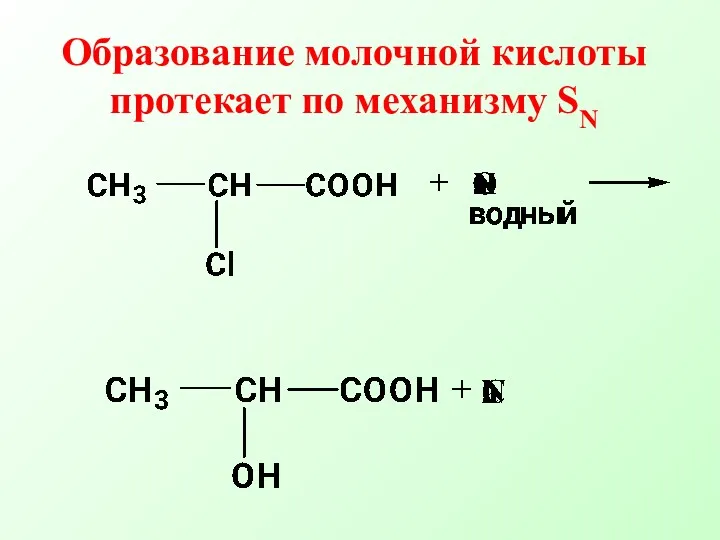
- 18. Образование молочной кислоты протекает по механизму SN
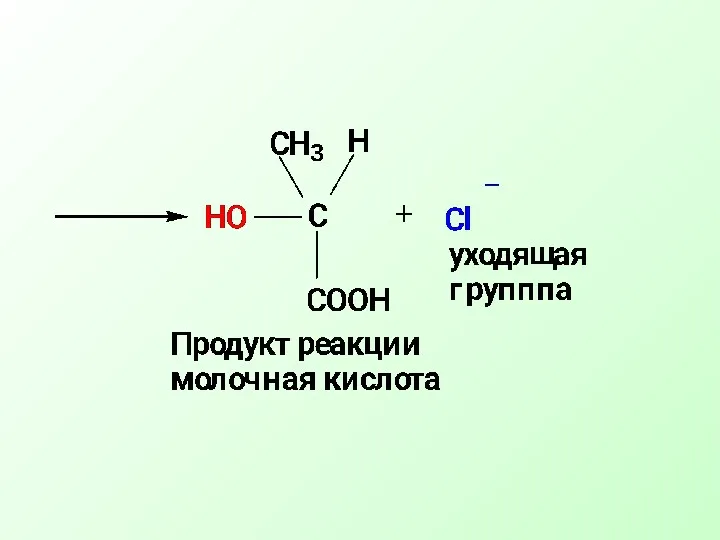
- 19. Механизм реакции
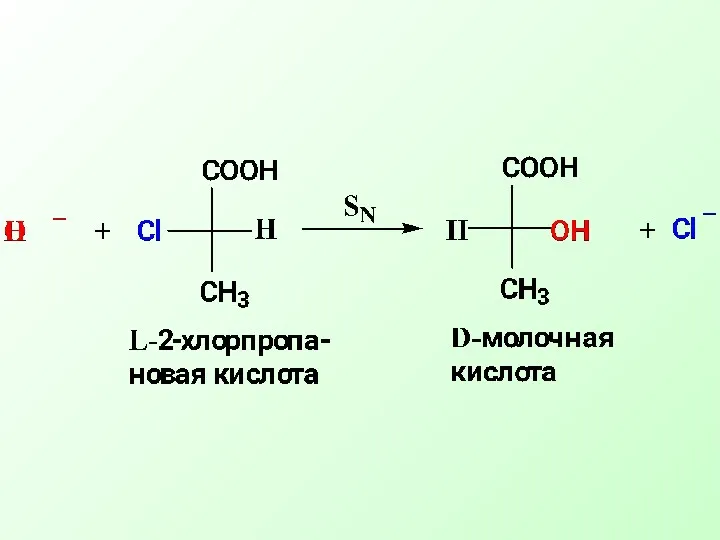
- 21. Протекание реакции нуклеофильного замещения приводит к «обращению» конфигурации атома углерода (т.е. происходит изменение положения заместителей в
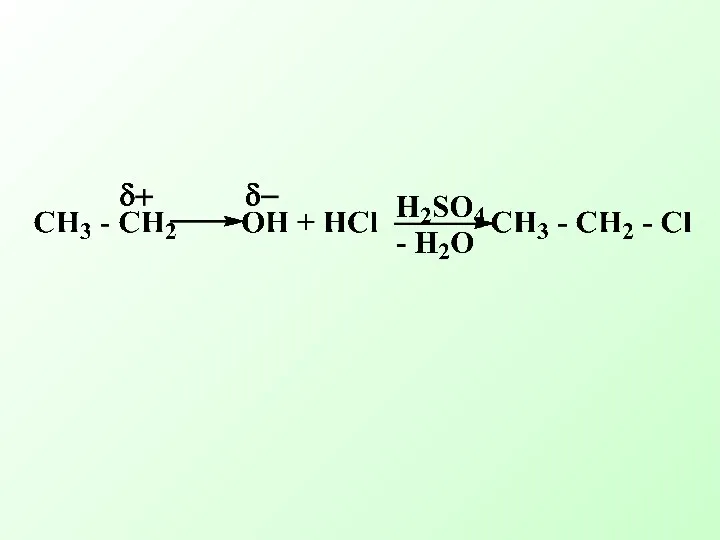
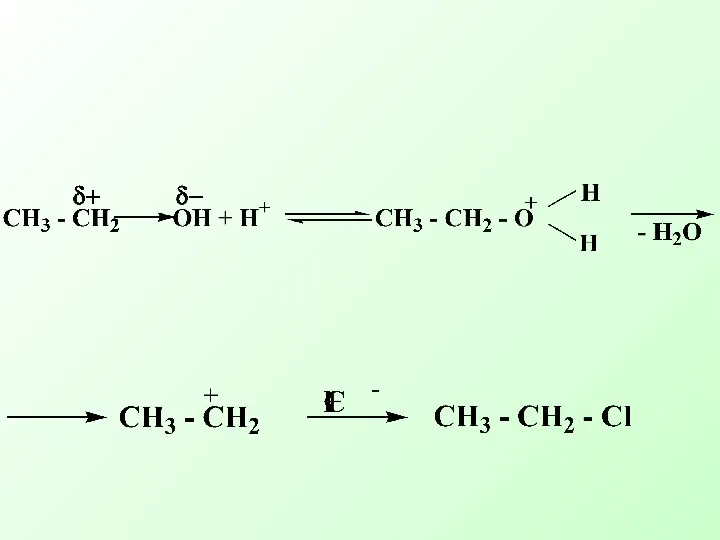
- 23. Нуклеофильное замещение в спиртах, тиолах и аминах протекает аналогично, но эти соединения содержат довольно трудноуходящие группы
- 29. В живых организмах хорошо уходящие группы – стабильные фосфат, дифосфат и трифосфат ионы, в которых отрицательный
- 30. В сложной структуре биологически активных молекул всегда возникает вопрос, какой атом углерода субстрата будет атакован нуклеофилом.
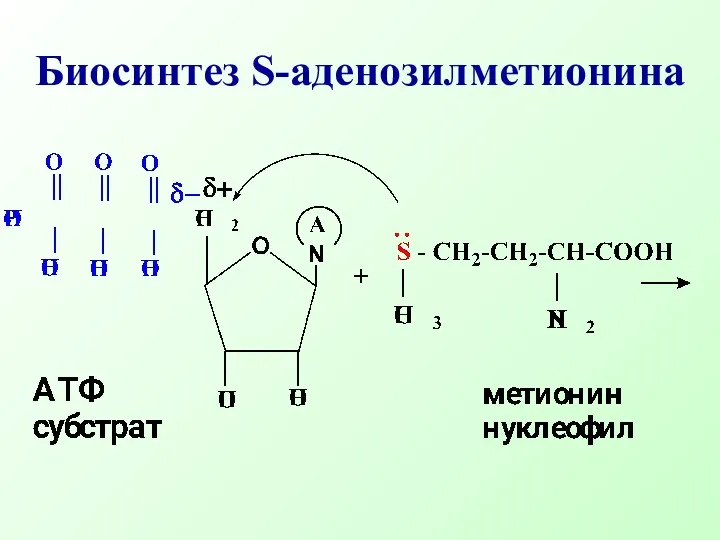
- 31. Многие реакции, происходящие в клетках растений и животных осуществляются по типу нуклеофильного замещения. Например, биосинтез S-аденозилметионина
- 32. Биосинтез S-аденозилметионина
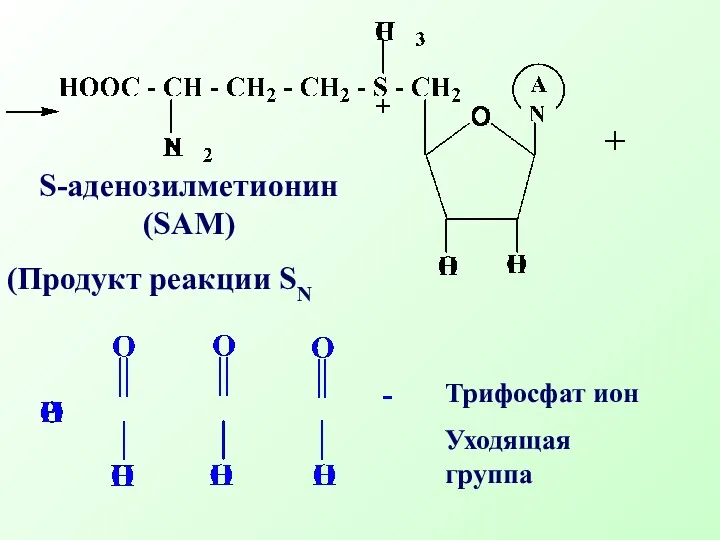
- 33. S-аденозилметионин (SAM) (Продукт реакции SN Трифосфат ион Уходящая группа
- 34. SAM является донором метильной группы и отвечает за биологические реакции метилирования (метилирует природные азотистые нуклеофилы: коламин,
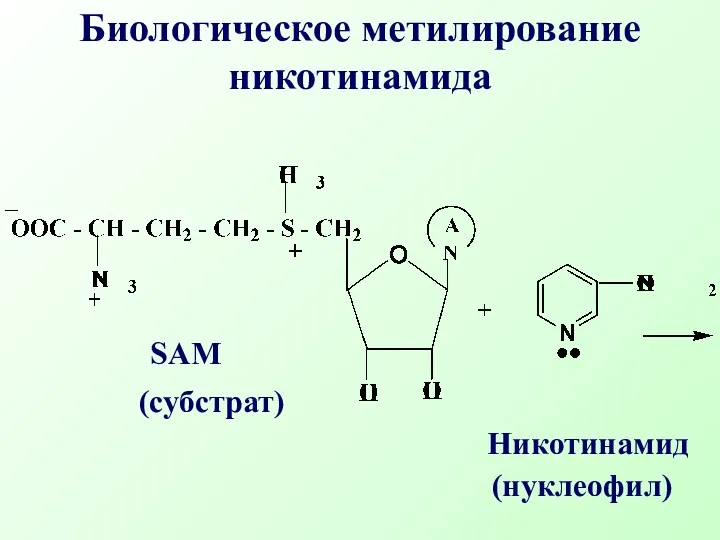
- 35. SAM Никотинамид Биологическое метилирование никотинамида (субстрат) (нуклеофил)
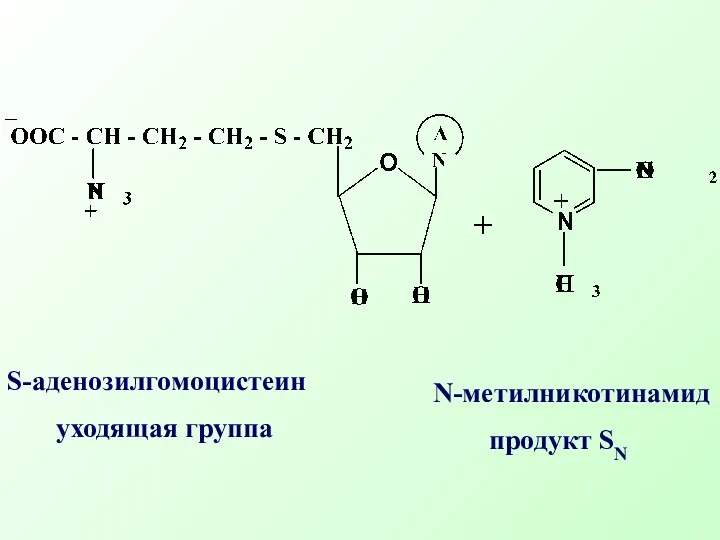
- 36. S-аденозилгомоцистеин уходящая группа N-метилникотинамид продукт SN
- 37. Биологическое ацилирование – пример SN реакции Ацилат ион нуклеофил Замещенный АТФ
- 38. Замещенный ацилфосфат Дифосфат ион уходящая группа Ацилфосфаты играют важную роль in vivo в качестве переносчиков ацильных
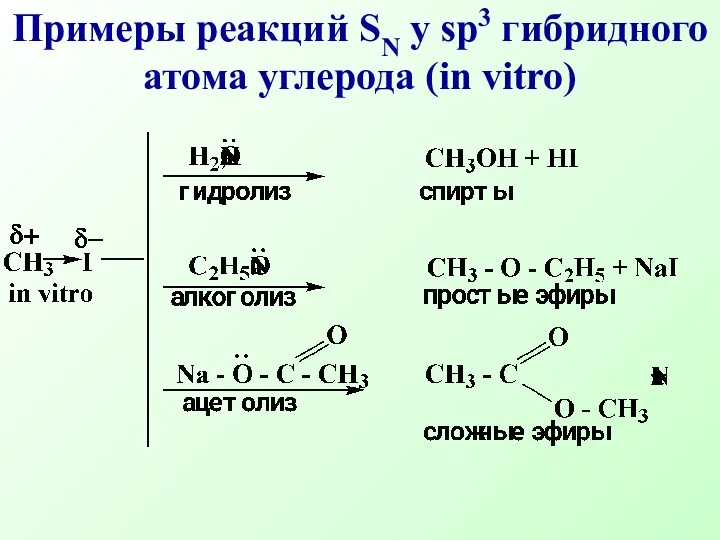
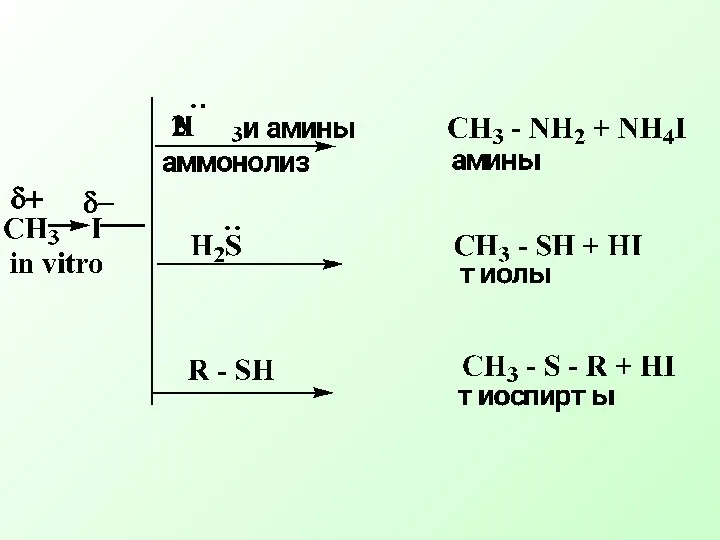
- 39. Примеры реакций SN у sр3 гибридного атома углерода (in vitro)
- 41. 7.2. Реакции элиминирования (Е) Реакция элиминирования заключается в отщеплении двух атомов или групп, входящих в состав
- 42. α-элиминирование – отщепление двух атомов или групп атомов происходит от одного и того же атома углерода
- 43. β-элиминирование – отщепление двух атомов или групп атомов происходит от соседних атомов углерода. β-элиминирование наиболее распространенный
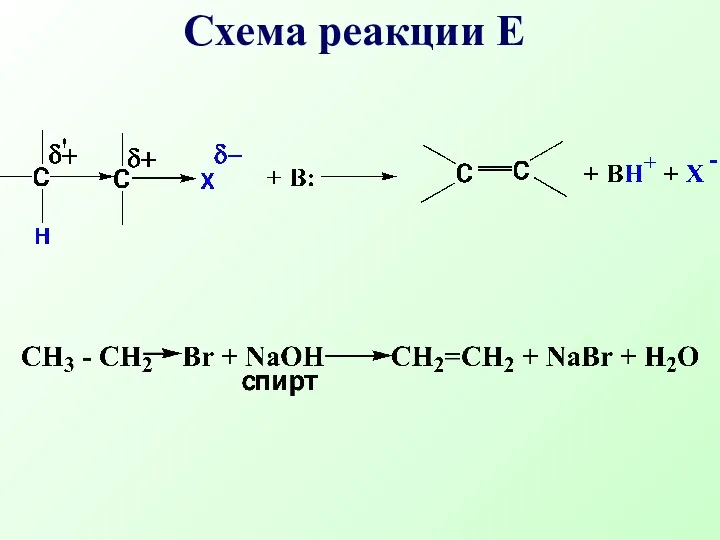
- 44. Схема реакции Е
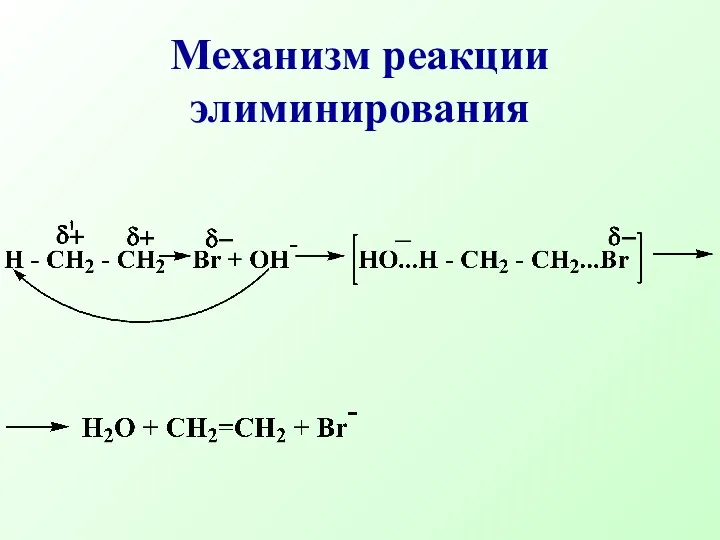
- 45. Механизм реакции элиминирования
- 46. Одной из реакций элиминирования, имеющих биологическое значение – является реакция дегидратации (отщепление воды)
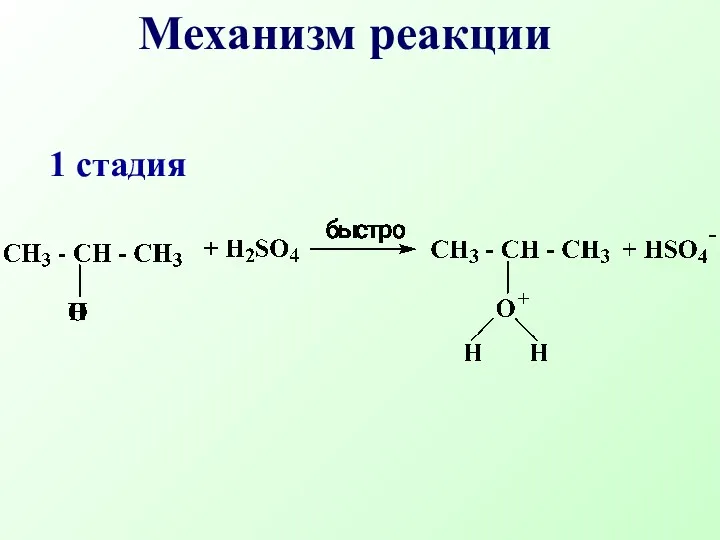
- 47. Механизм реакции 1 стадия
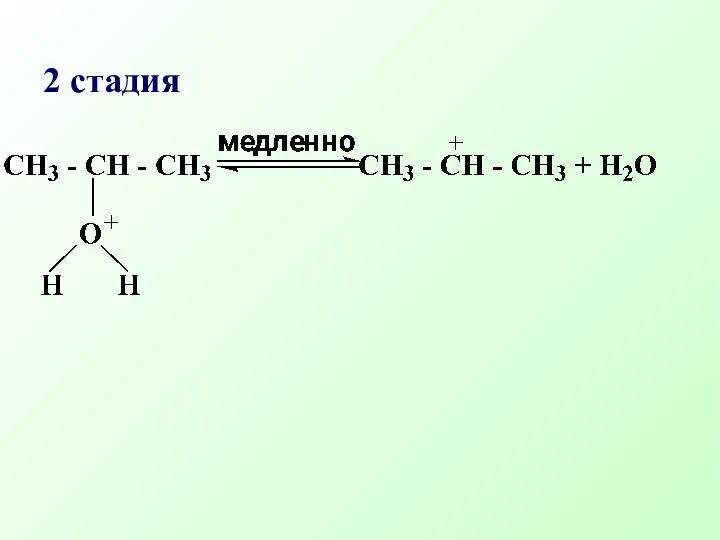
- 48. 2 стадия
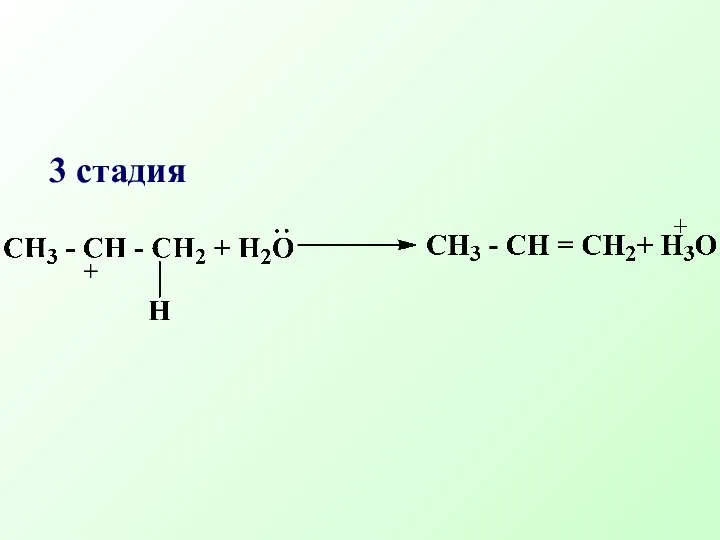
- 49. 3 стадия
- 50. Правило Зайцева: в реакциях дегидратации и дегидрогалогенирования водород отщепляется от наименее гидрогенизированного атома углерода
- 52. Дегидратация характерна для соединений живой природы, содержащих гидроксильную группу и СН-кислотный центр
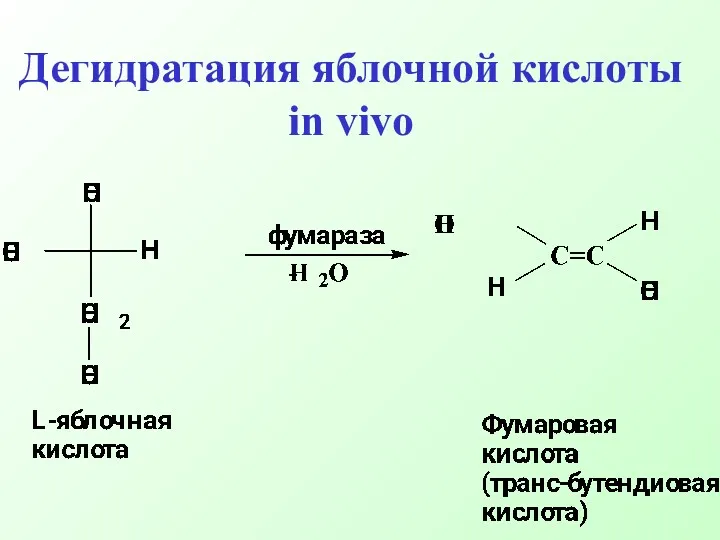
- 53. Классический пример – дегидратация яблочной кислоты. Реакция специфична. Фермент фумараза способен катализировать реакцию дегидратации только одного
- 54. Дегидратация яблочной кислоты in vivo
- 56. Скачать презентацию





























 Положение в ПСХЭ водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в ПСХЭ водорода, лантаноидов, актиноидов и искусственно полученных элементов Методы окислительно-восстановительного и комплексонометри-ческого титрования
Методы окислительно-восстановительного и комплексонометри-ческого титрования Sources of alkanes and cycloalkanes. Crude oil
Sources of alkanes and cycloalkanes. Crude oil Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Механическая смесь и растворы
Механическая смесь и растворы Аминокислоты. Физические свойства
Аминокислоты. Физические свойства Химия. D-элементтер
Химия. D-элементтер Обмен нуклеотидов
Обмен нуклеотидов Амінокислоти. Склад і будова молекул, загальні та структурні формули, систематична номенклатура
Амінокислоти. Склад і будова молекул, загальні та структурні формули, систематична номенклатура Соли. Определение солей
Соли. Определение солей Свинец — простое вещество, металл, химический элемент IV группы таблицы Менделеева
Свинец — простое вещество, металл, химический элемент IV группы таблицы Менделеева Открытие новых химических элементов с атомными номерами 113, 115, 117 и 118
Открытие новых химических элементов с атомными номерами 113, 115, 117 и 118 Лабораторные исследования состава и физико-химических свойств нефти
Лабораторные исследования состава и физико-химических свойств нефти Предмет и объекты исследования коллоидной химии. Лекция 01
Предмет и объекты исследования коллоидной химии. Лекция 01 Азотсодержащие органические соединения. Аминокислоты (часть 2)
Азотсодержащие органические соединения. Аминокислоты (часть 2) Хімічна рівновага. Принцип зміщення хімічної рівноваги
Хімічна рівновага. Принцип зміщення хімічної рівноваги Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Классы неорганических веществ
Классы неорганических веществ Гетерофункциональные соединения
Гетерофункциональные соединения Генетическая связь органических и неорганических соединений
Генетическая связь органических и неорганических соединений Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Маңызды мұнай өнімдері
Маңызды мұнай өнімдері Chemistry th 11 grade The end of second Term
Chemistry th 11 grade The end of second Term Галогены
Галогены Органолептические и визуальные методы идентификация полимера
Органолептические и визуальные методы идентификация полимера Ізомери у природі
Ізомери у природі Жидкое и растворимое стекло
Жидкое и растворимое стекло Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки
Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки