Содержание
- 3. Принцип зміщення хімічної рівноваги На зовнішню дію - протидія
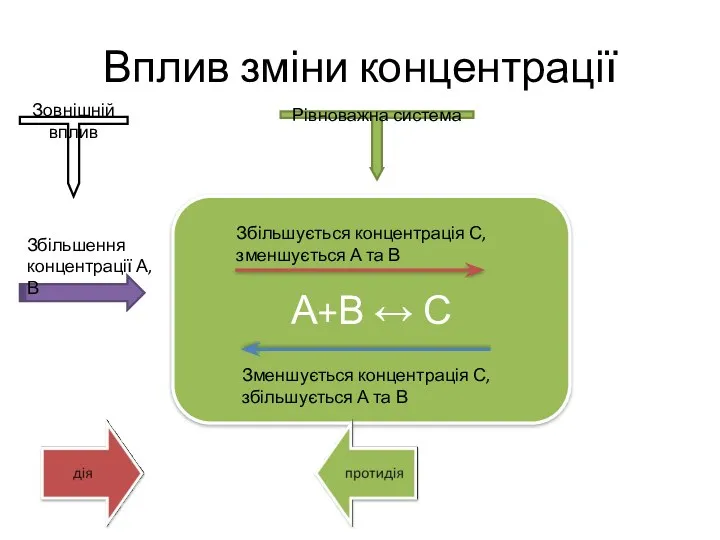
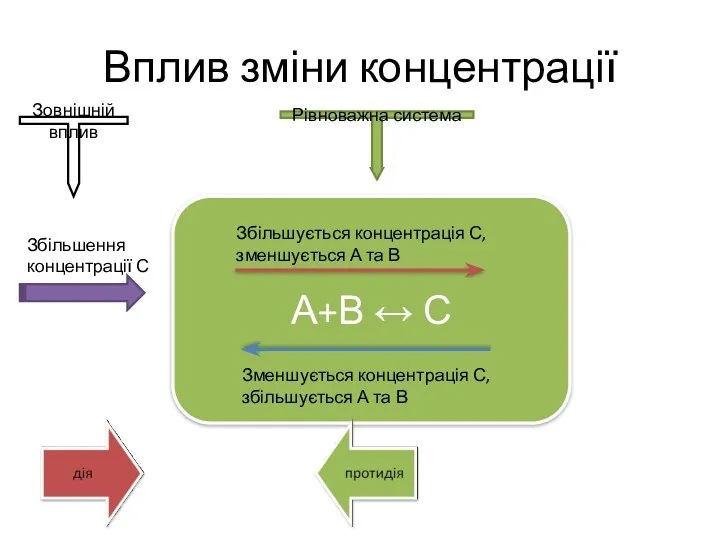
- 5. Вплив зміни концентрації А+В ↔ С Збільшується концентрація С, зменшується А та В Зменшується концентрація С,
- 6. Вплив зміни концентрації А+В ↔ С Збільшується концентрація С, зменшується А та В Зменшується концентрація С,
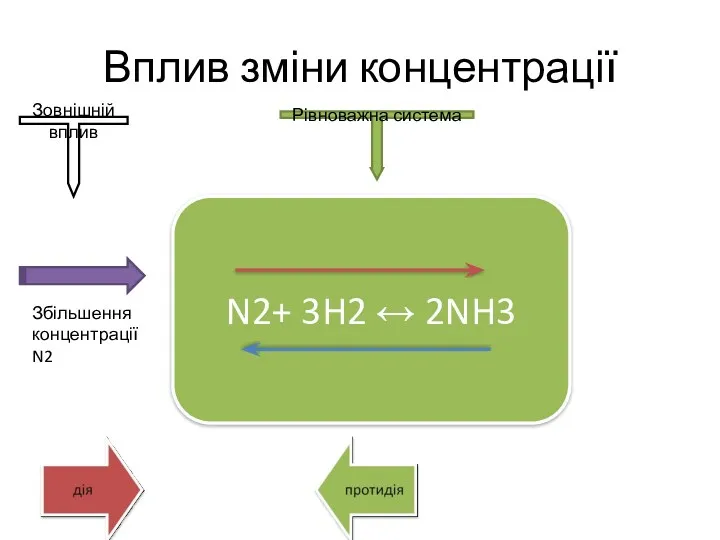
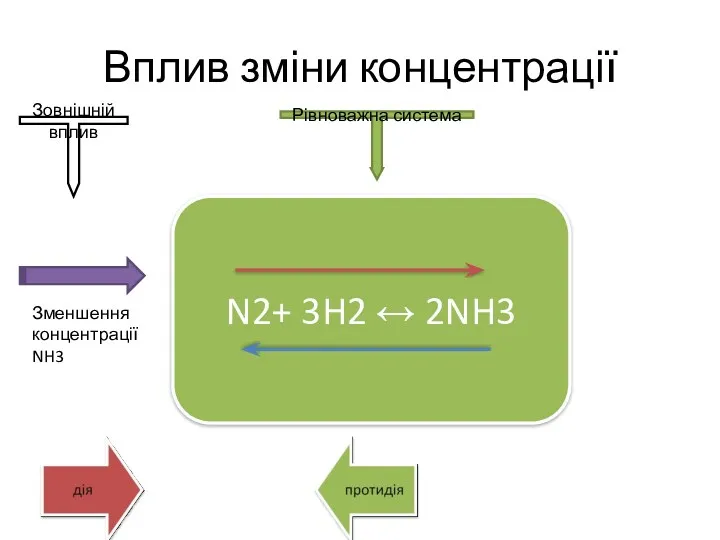
- 7. Вплив зміни концентрації N2+ 3H2 ↔ 2NH3 Збільшення концентрації N2 Зовнішній вплив Рівноважна система
- 8. Вплив зміни концентрації N2+ 3H2 ↔ 2NH3 Зменшення концентрації NH3 Зовнішній вплив Рівноважна система
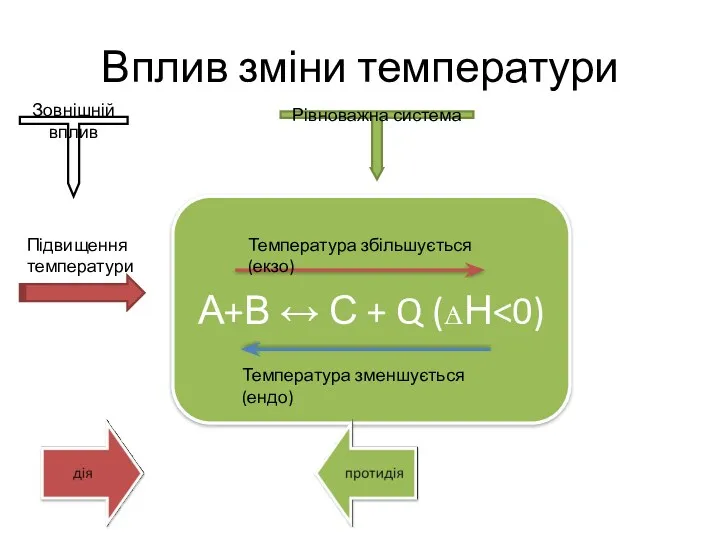
- 9. Вплив зміни температури А+В ↔ С + Q (ꙙН Температура збільшується (екзо) Температура зменшується (ендо) Підвищення
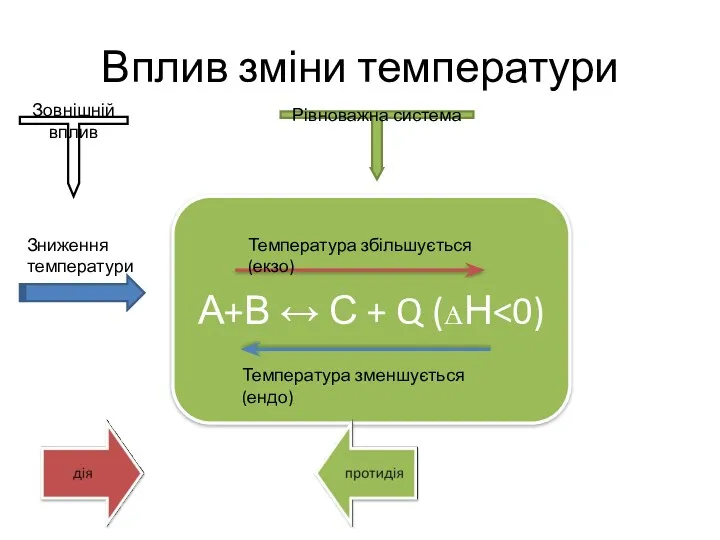
- 10. Вплив зміни температури А+В ↔ С + Q (ꙙН Температура збільшується (екзо) Температура зменшується (ендо) Зниження
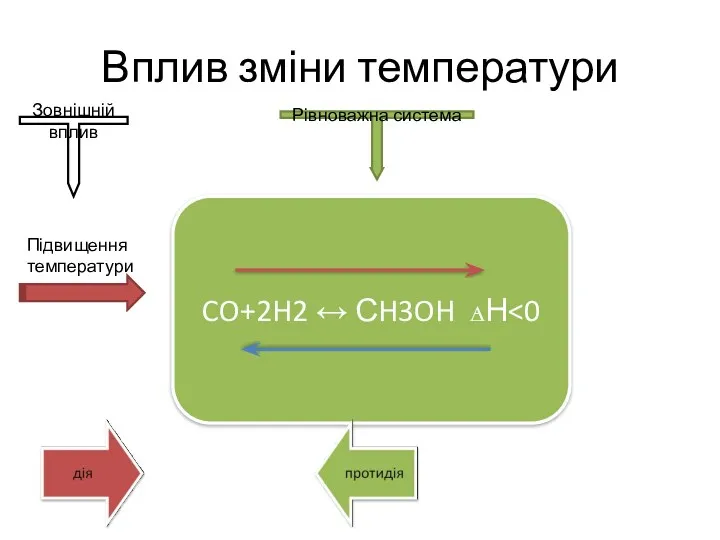
- 11. Вплив зміни температури CO+2H2 ↔ СH3OH ꙙН Підвищення температури Зовнішній вплив Рівноважна система
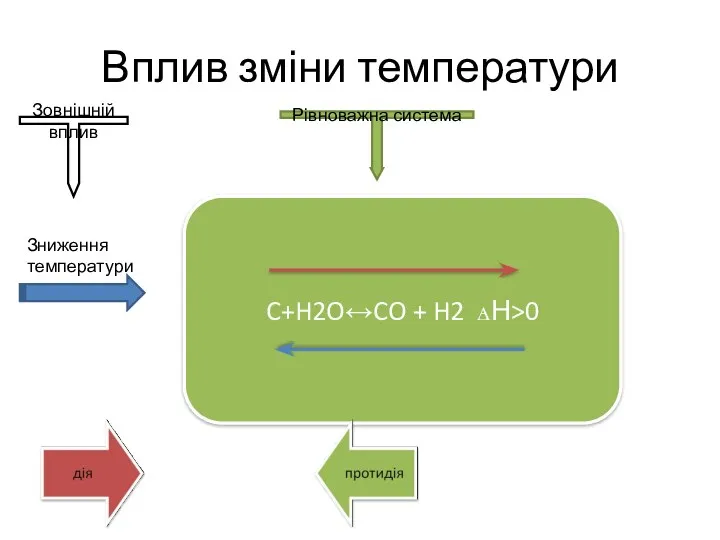
- 12. Вплив зміни температури C+H2O↔CO + H2 ꙙН>0 Зниження температури Зовнішній вплив Рівноважна система
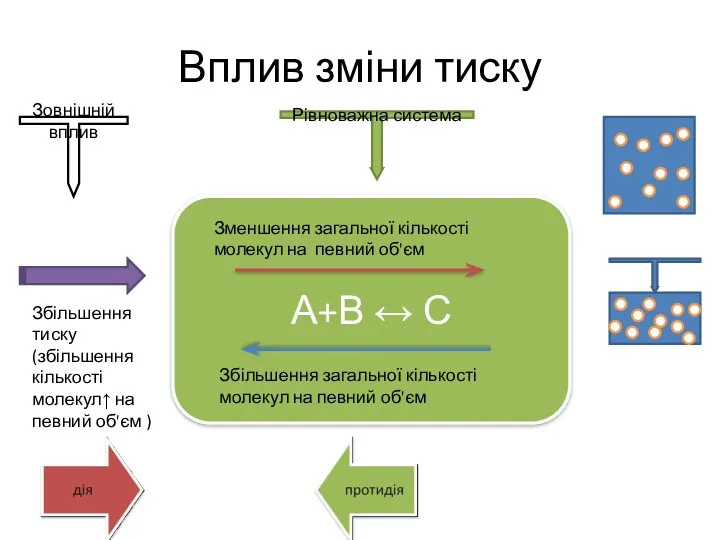
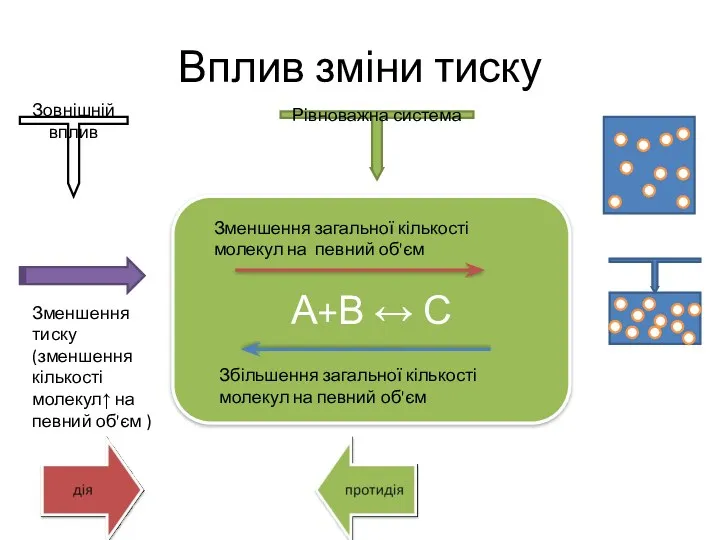
- 13. Вплив зміни тиску А+В ↔ С Зменшення загальної кількості молекул на певний об'єм Збільшення загальної кількості
- 14. Вплив зміни тиску А+В ↔ С Зменшення загальної кількості молекул на певний об'єм Збільшення загальної кількості
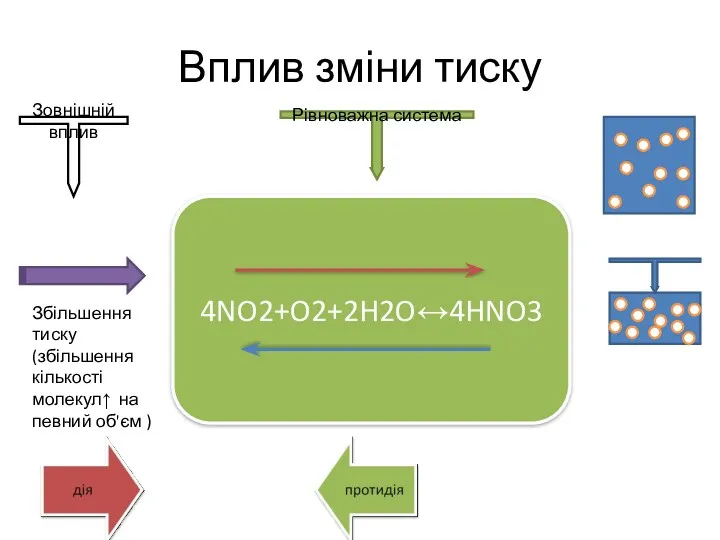
- 15. Вплив зміни тиску 4NO2+O2+2H2O↔4HNO3 Збільшення тиску (збільшення кількості молекул↑ на певний об'єм ) Зовнішній вплив Рівноважна
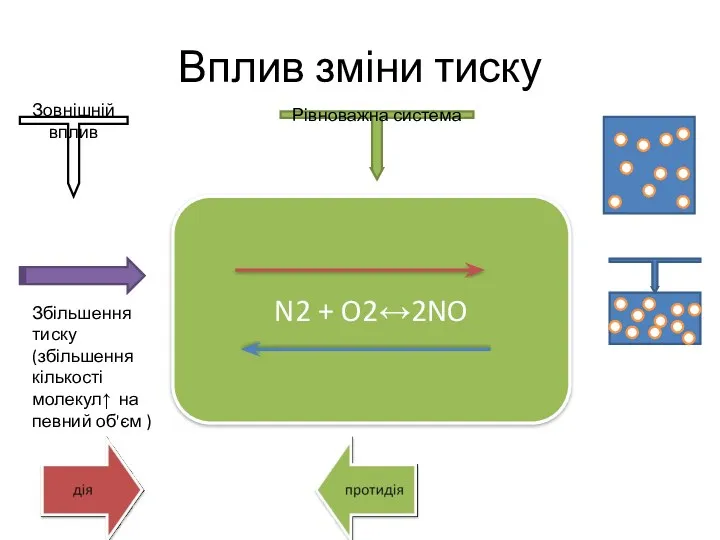
- 16. Вплив зміни тиску N2 + O2↔2NO Збільшення тиску (збільшення кількості молекул↑ на певний об'єм ) Зовнішній
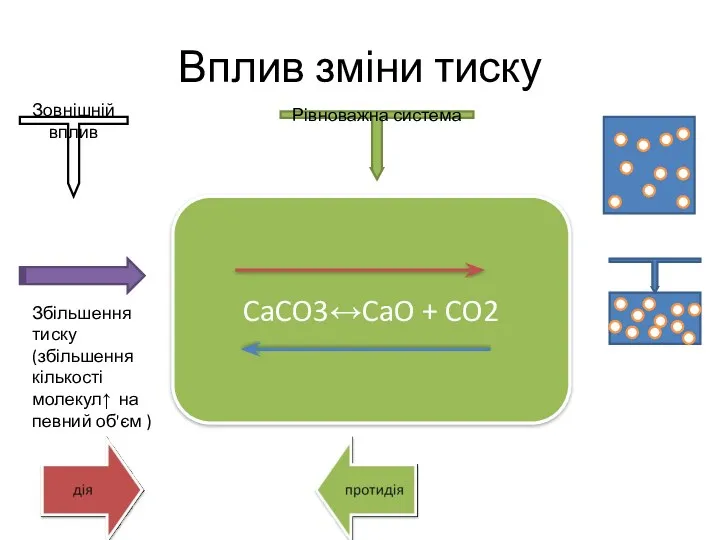
- 17. Вплив зміни тиску CaCO3↔CaO + CO2 Збільшення тиску (збільшення кількості молекул↑ на певний об'єм ) Зовнішній
- 20. Укажіть рівняння оборотних реакцій, рівновагу яких можна зміщувати у бік утворення продуктів реакції за допомогою збільшення
- 22. Скачать презентацию





 Азот и его соединения
Азот и его соединения Будова електронних оболонок атомів
Будова електронних оболонок атомів Будова атома. Ядро й електронні оболонки. Склад атомних ядер
Будова атома. Ядро й електронні оболонки. Склад атомних ядер Алканы
Алканы Игра Химические элементы (формулы и названия)
Игра Химические элементы (формулы и названия) Строение атома. Периодический закон Менделеева
Строение атома. Периодический закон Менделеева Углеводы. Глюкоза
Углеводы. Глюкоза Газовые гидраты
Газовые гидраты Ионный обмен. Хроматография
Ионный обмен. Хроматография Валентність хімічних елементів
Валентність хімічних елементів Методы обучения химии
Методы обучения химии Electronică aplicată. (Curs 2)
Electronică aplicată. (Curs 2) Значение органической химии в жизни человека
Значение органической химии в жизни человека Самоспалахування. Фактори, що впливають на температуру самоспалахування. Лекція 5
Самоспалахування. Фактори, що впливають на температуру самоспалахування. Лекція 5 Радиофармацевтическая химия
Радиофармацевтическая химия Классификация химических реакций
Классификация химических реакций Метанол
Метанол Основы коррозии и защиты металлов
Основы коррозии и защиты металлов Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями
Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями Наглядное пособие Динамические модели. Кристаллы. Немолекулярные вещества. Простые вещества
Наглядное пособие Динамические модели. Кристаллы. Немолекулярные вещества. Простые вещества Роль химии в создании новых материалов
Роль химии в создании новых материалов Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5) Озон. Применение
Озон. Применение Железо. Соединения железа
Железо. Соединения железа Резина и её свойства . Полимеры и их использование
Резина и её свойства . Полимеры и их использование Открытие периодического закона
Открытие периодического закона Растворы
Растворы Нефть. Свойства нефти
Нефть. Свойства нефти