Содержание
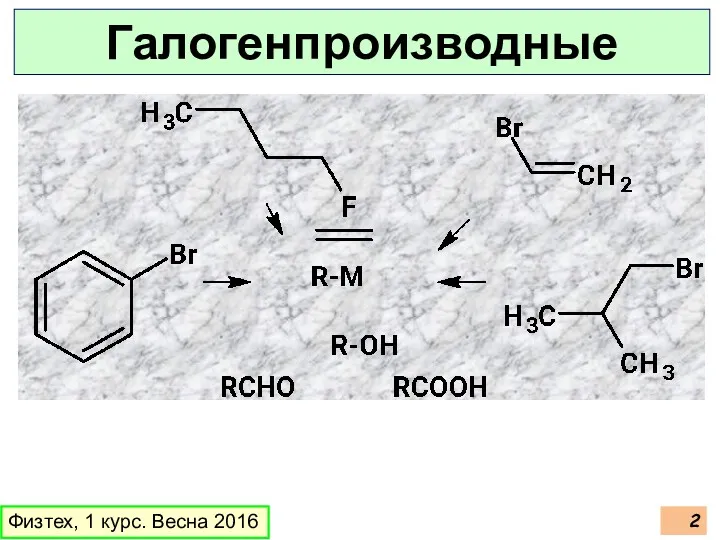
- 2. Физтех, 1 курс. Весна 2016 Галогенпроизводные
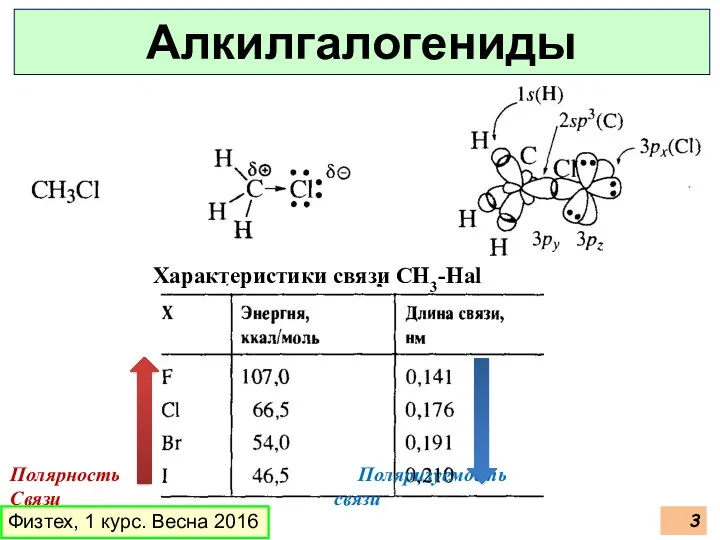
- 3. Полярность Поляризуемость Связи связи Физтех, 1 курс. Весна 2016 Алкилгалогениды Характеристики связи CH3-Hal
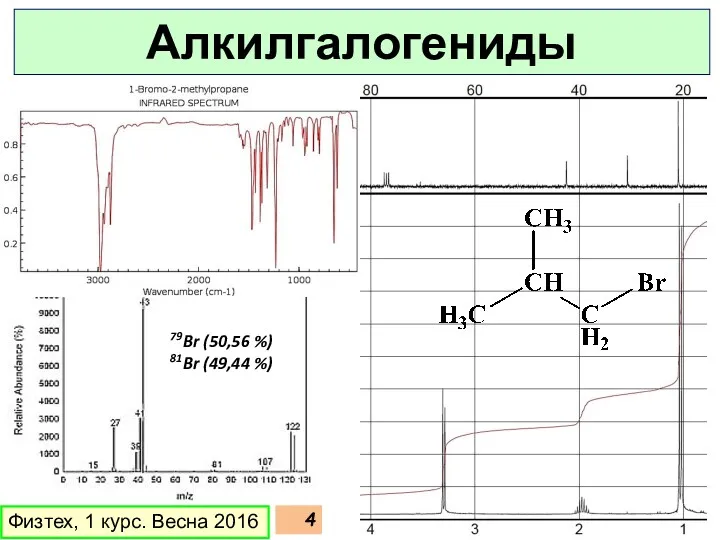
- 4. Физтех, 1 курс. Весна 2016 79Br (50,56 %) 81Br (49,44 %) Алкилгалогениды
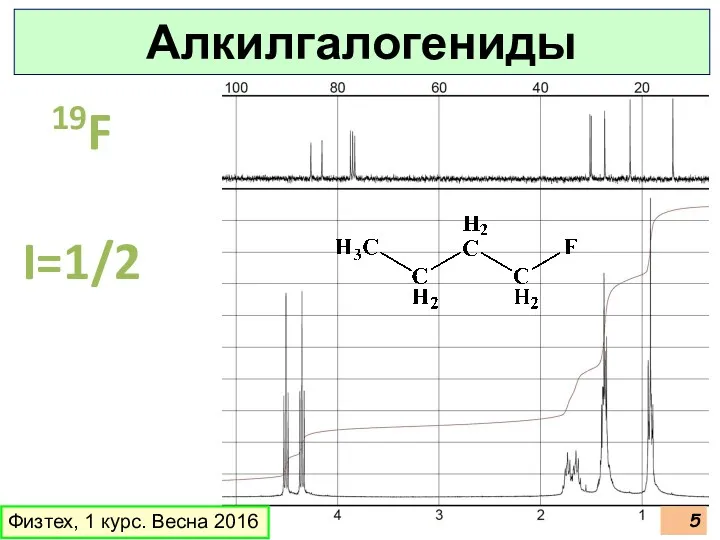
- 5. Физтех, 1 курс. Весна 2016 19F I=1/2 Алкилгалогениды
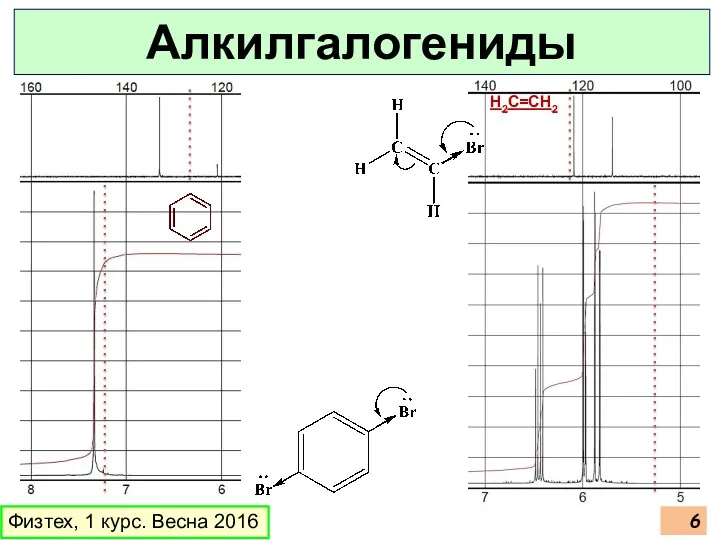
- 6. H2C=CH2 Физтех, 1 курс. Весна 2016 Алкилгалогениды
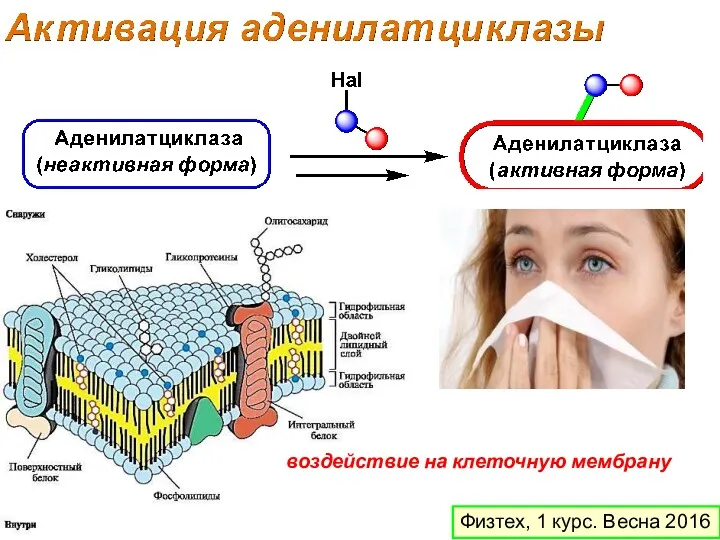
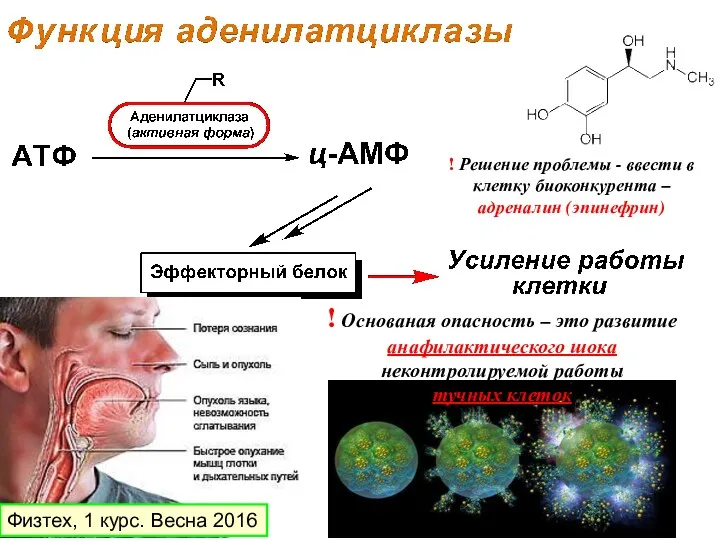
- 7. воздействие на клеточную мембрану Физтех, 1 курс. Весна 2016
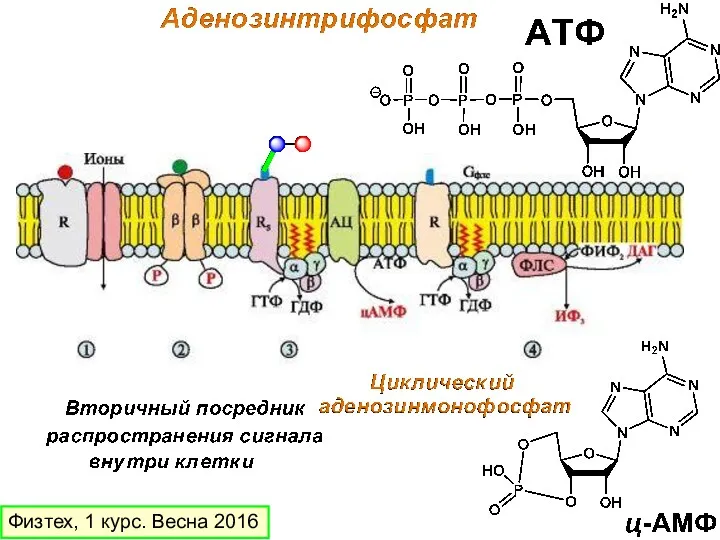
- 8. Физтех, 1 курс. Весна 2016
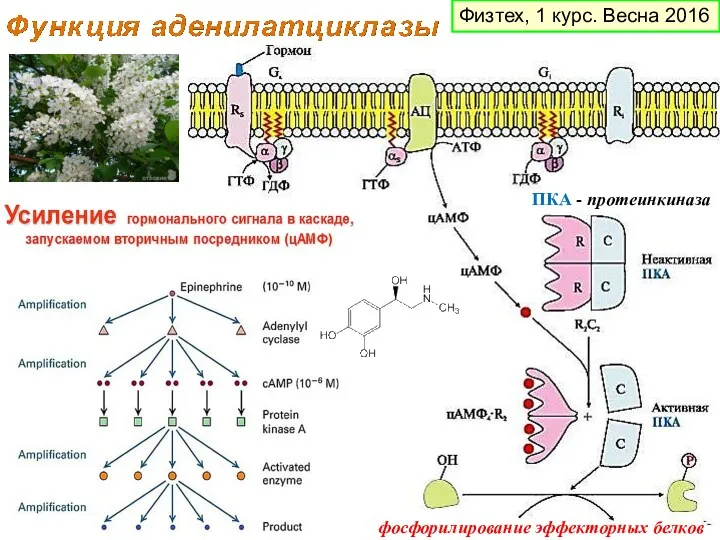
- 9. ПКА - протеинкиназа фосфорилирование эффекторных белков Физтех, 1 курс. Весна 2016
- 10. ! Основаная опасность – это развитие анафилактического шока неконтролируемой работы тучных клеток ! Решение проблемы -
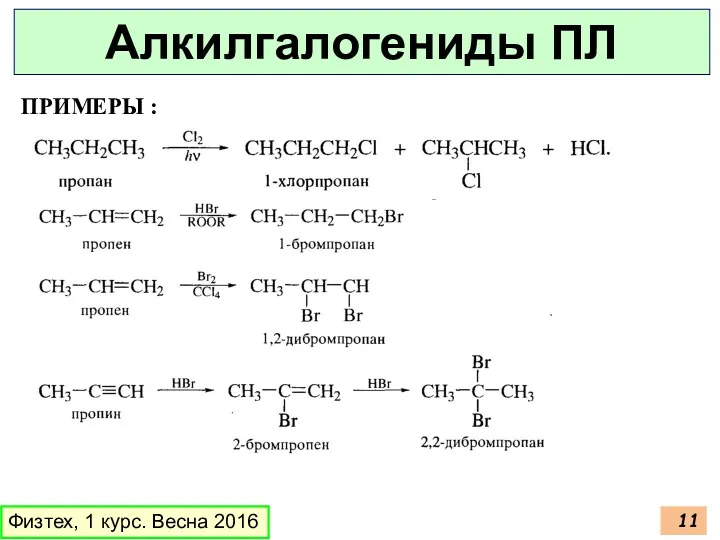
- 11. ПРИМЕРЫ : Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
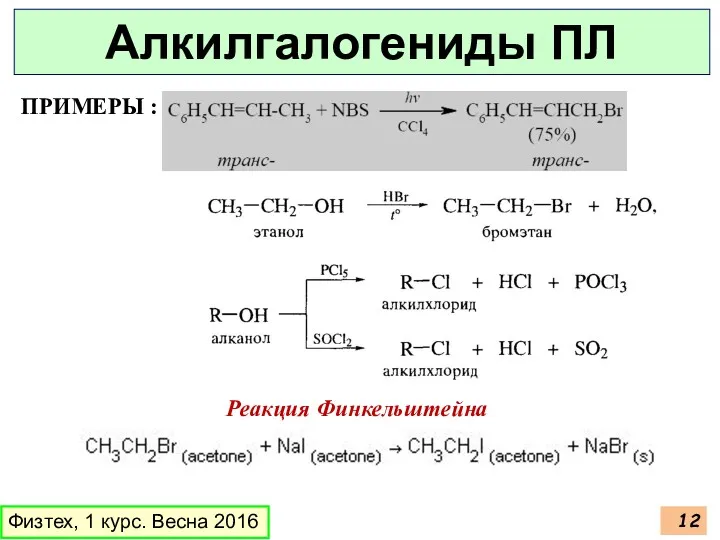
- 12. ПРИМЕРЫ : Реакция Финкельштейна Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
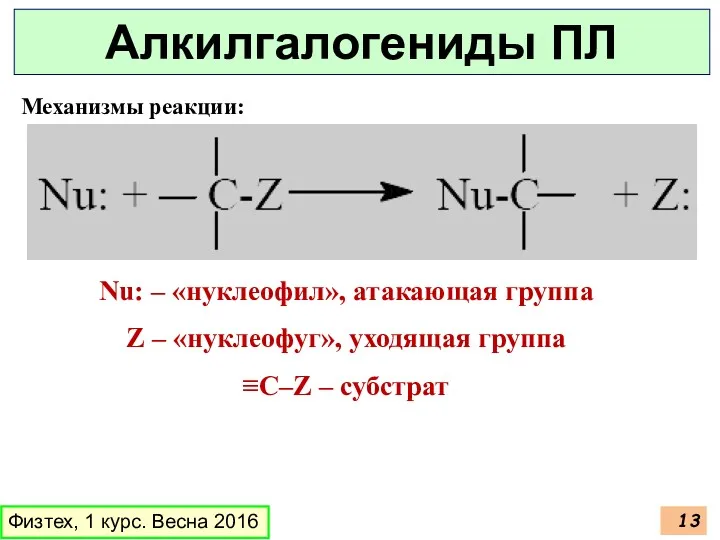
- 13. Механизмы реакции: Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Nu: – «нуклеофил», атакающая группа Z –
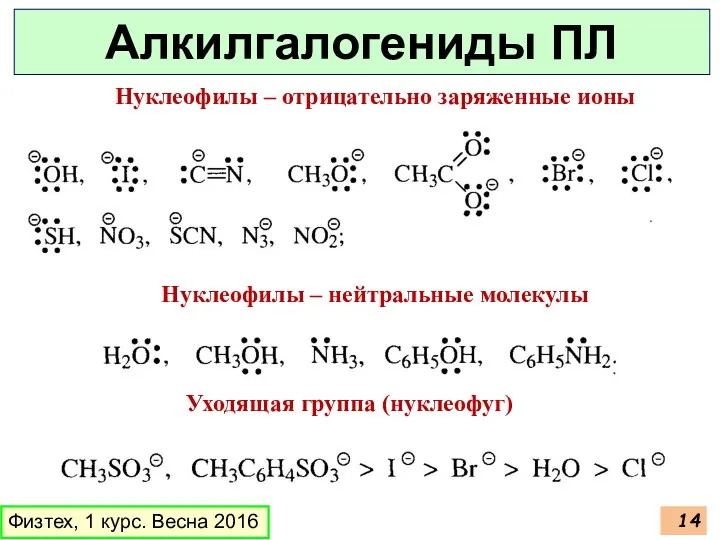
- 14. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Нуклеофилы – отрицательно заряженные ионы Нуклеофилы – нейтральные молекулы
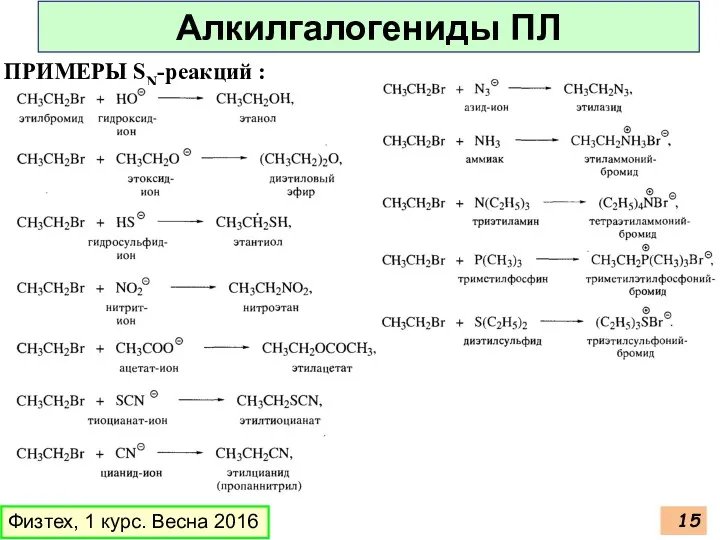
- 15. ПРИМЕРЫ SN-реакций : Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
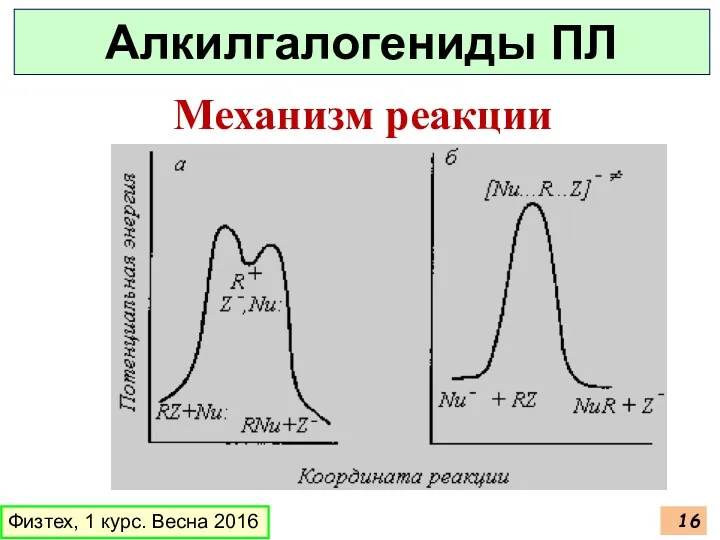
- 16. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Механизм реакции
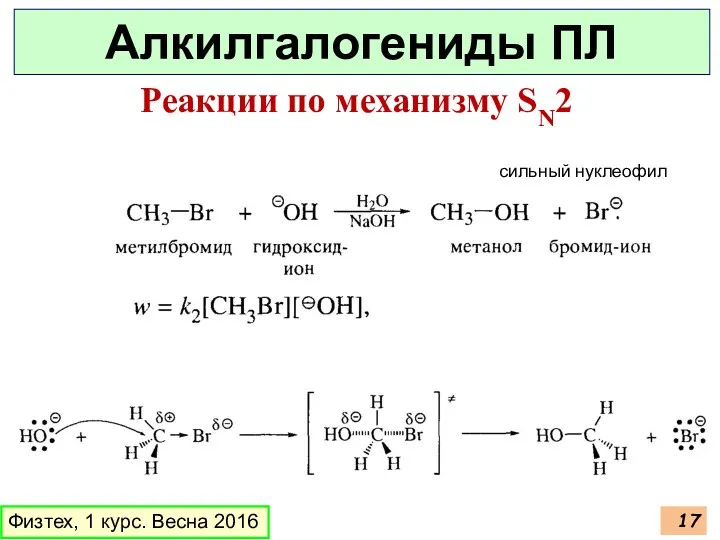
- 17. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Реакции по механизму SN2 сильный нуклеофил
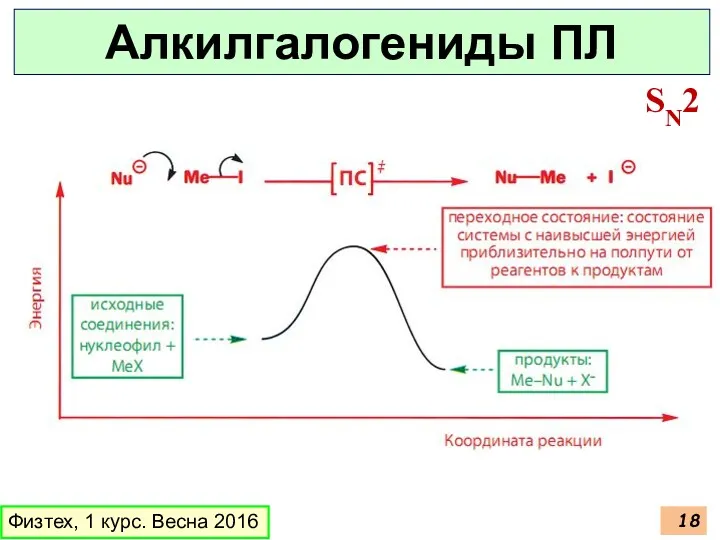
- 18. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2
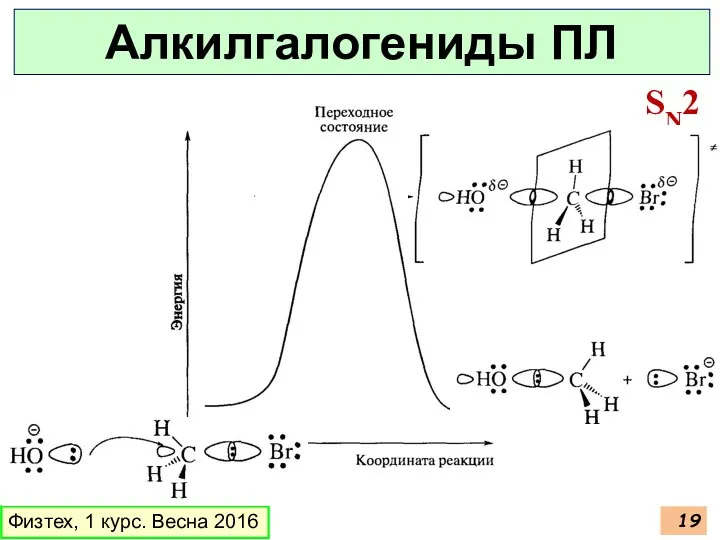
- 19. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2
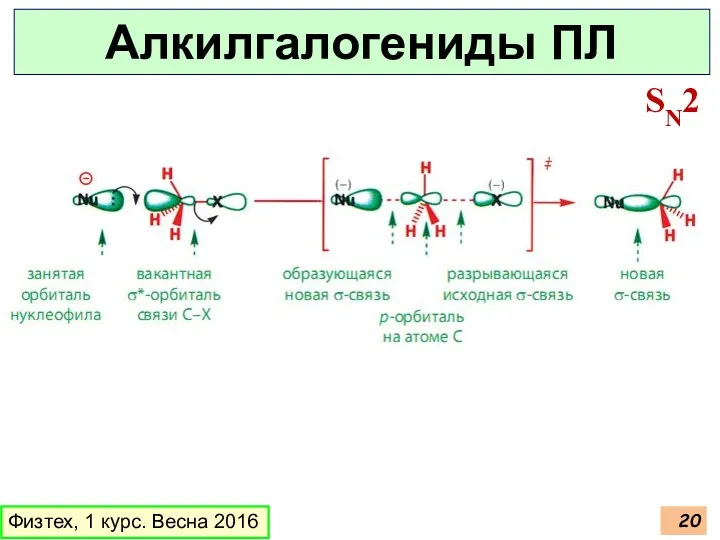
- 20. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2
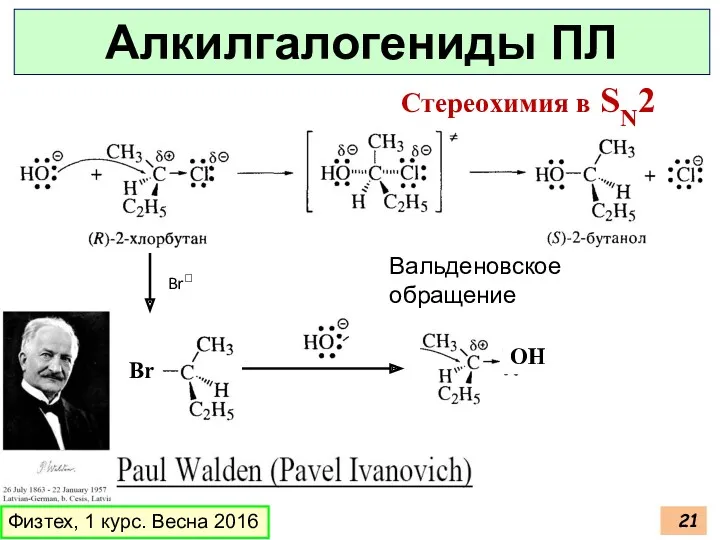
- 21. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Стереохимия в SN2 Br Br OH Вальденовское обращение
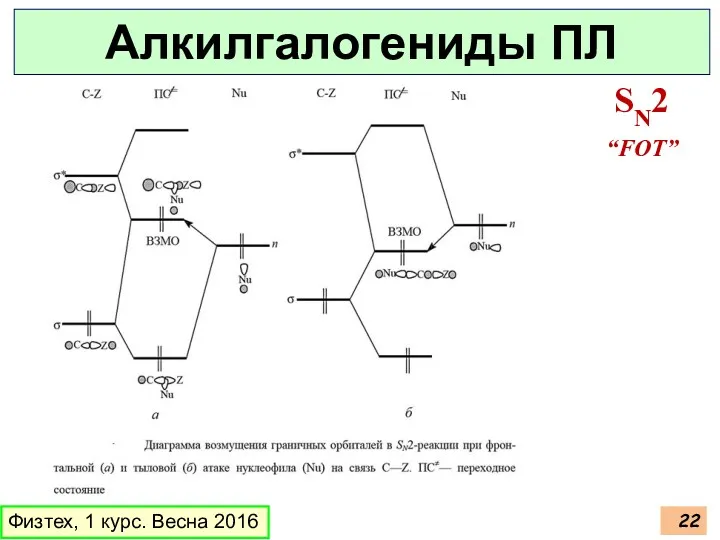
- 22. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2 “FOT”
- 23. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1 слабый нуклеофил, ионизирующий растворитель
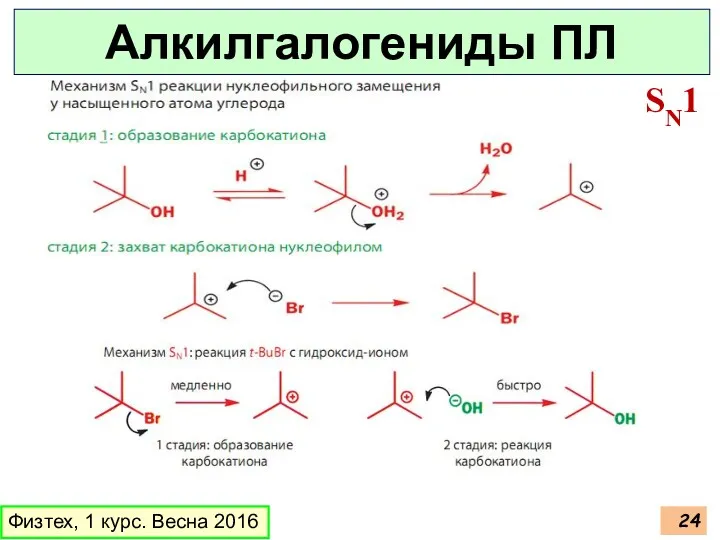
- 24. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1
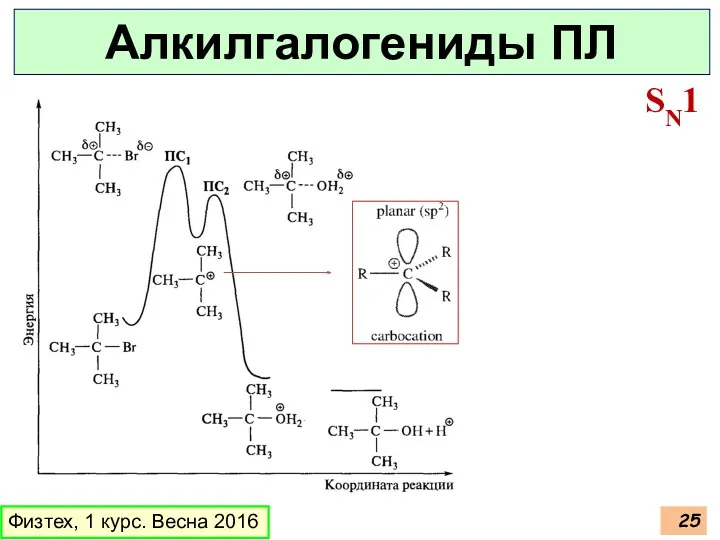
- 25. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1
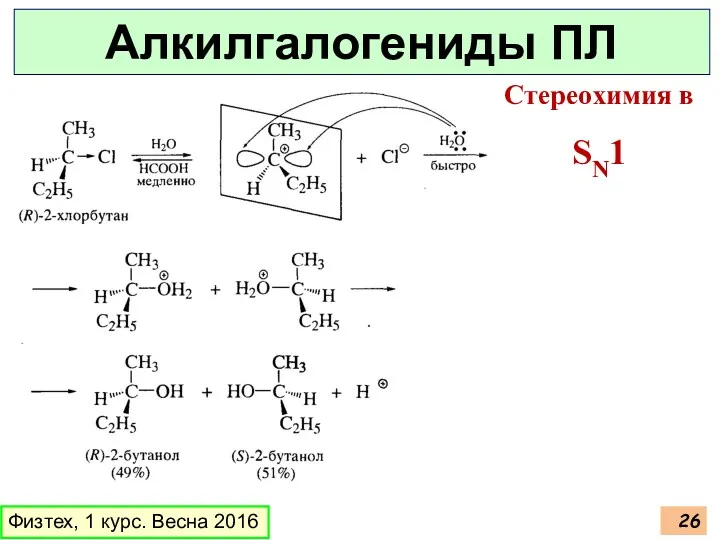
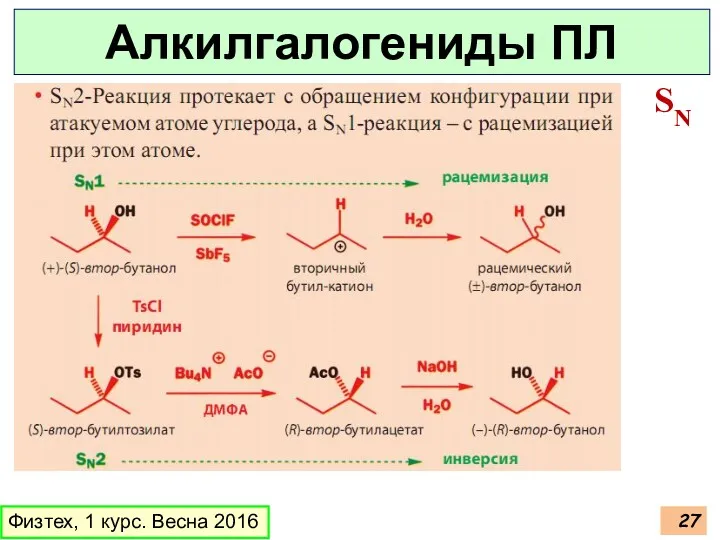
- 26. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Стереохимия в SN1
- 27. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN
- 28. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2 + + SN1 КИП — контактная ионная пара,
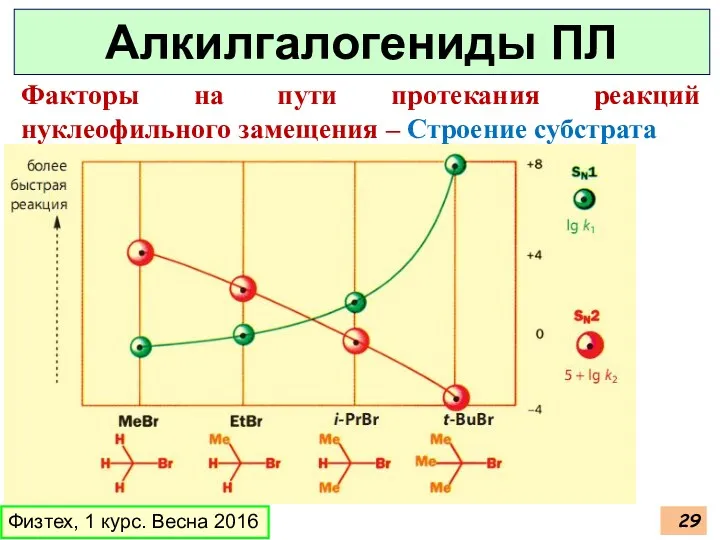
- 29. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – Строение
- 30. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2 SN1 Факторы на пути протекания реакций нуклеофильного замещения
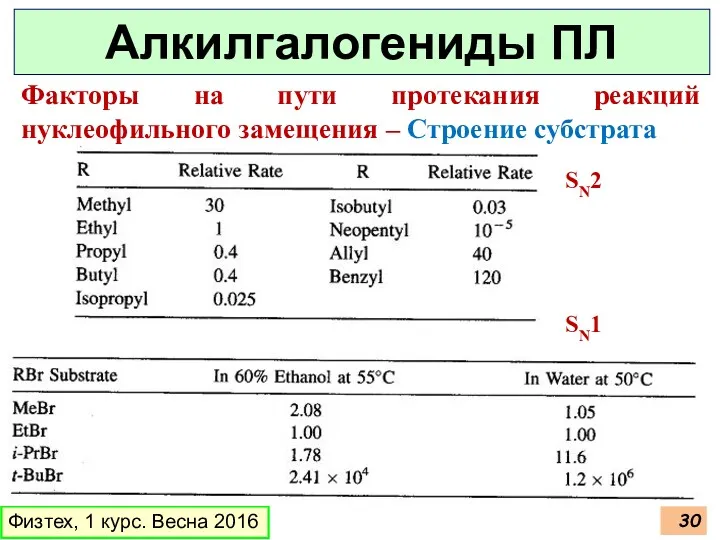
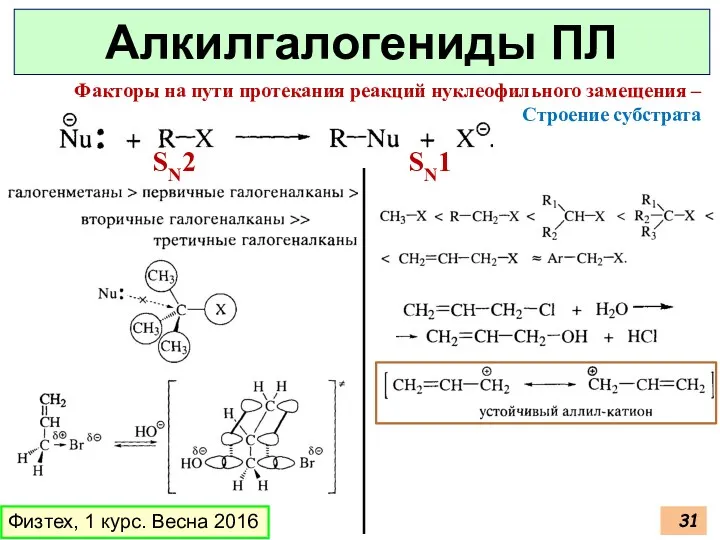
- 31. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – Строение
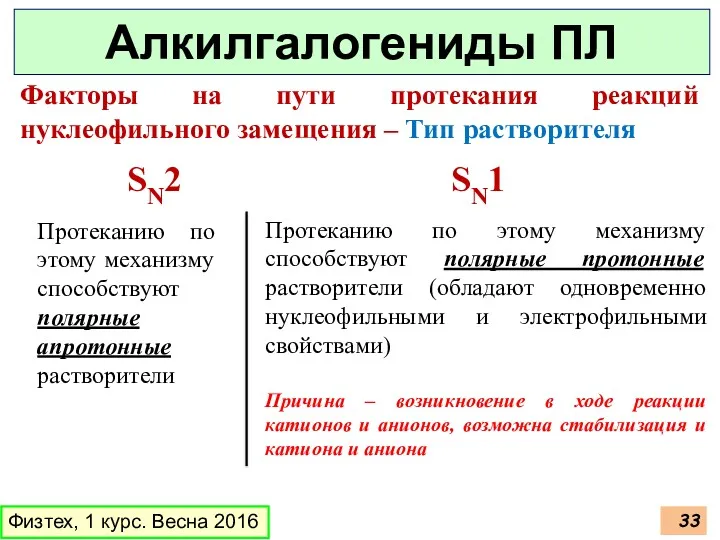
- 32. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – Тип
- 33. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – Тип
- 34. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2 Факторы на пути протекания реакций нуклеофильного замещения –
- 35. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Реакция идет тем быстрее, чем менее «энергетична» уходящая группа
- 36. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Замещение протекает тем легче, чем выше нуклеофильность реагента (способность
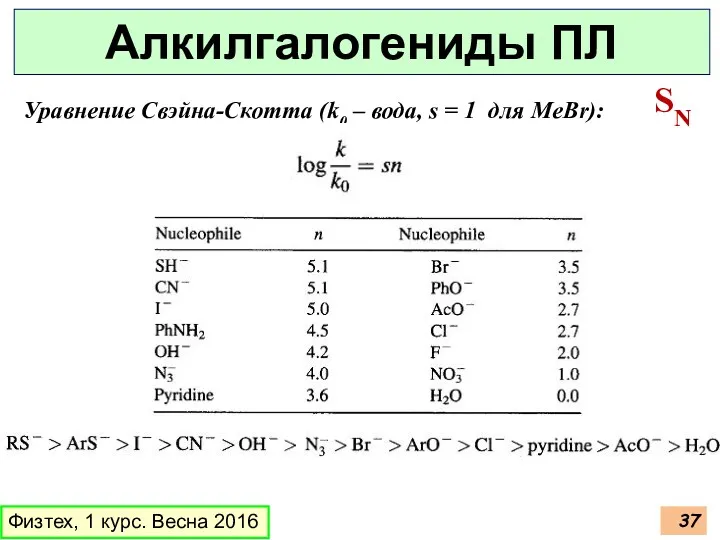
- 37. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN Уравнение Свэйна-Скотта (k0 – вода, s = 1
- 38. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Метилбромид и нуклеофил в воде Метилбромид и нуклеофил в
- 39. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Мягкость и жесткость нуклеофила. Принцип ЖМКО Пирсон (1963): жесткие
- 40. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Принцип ЖМКО
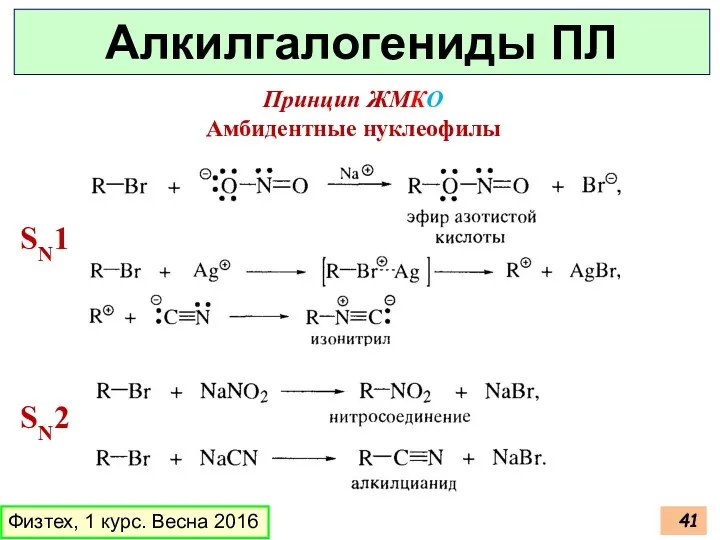
- 41. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1 SN2 Принцип ЖМКО Амбидентные нуклеофилы
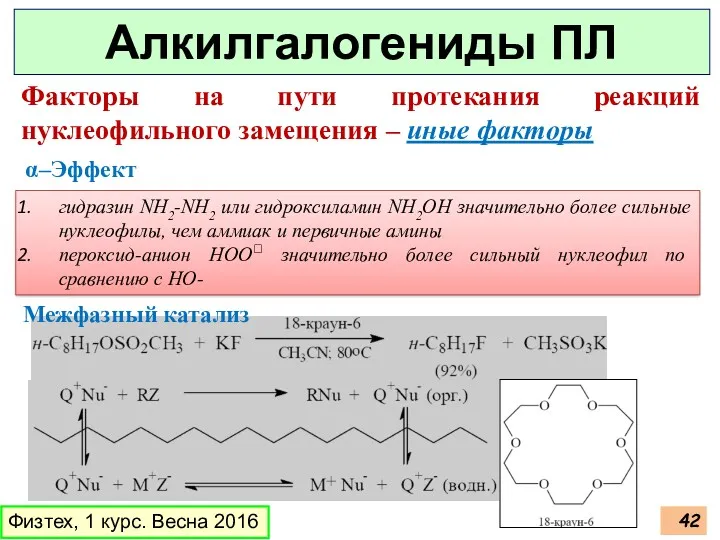
- 42. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – иные
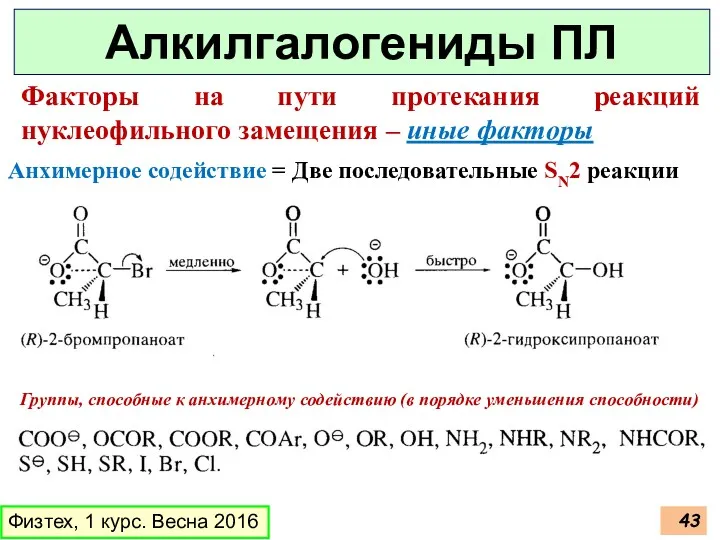
- 43. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – иные
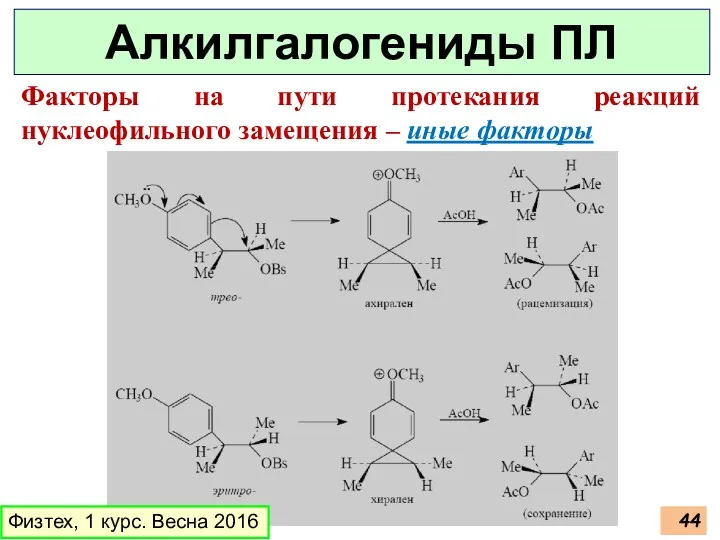
- 44. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Факторы на пути протекания реакций нуклеофильного замещения – иные
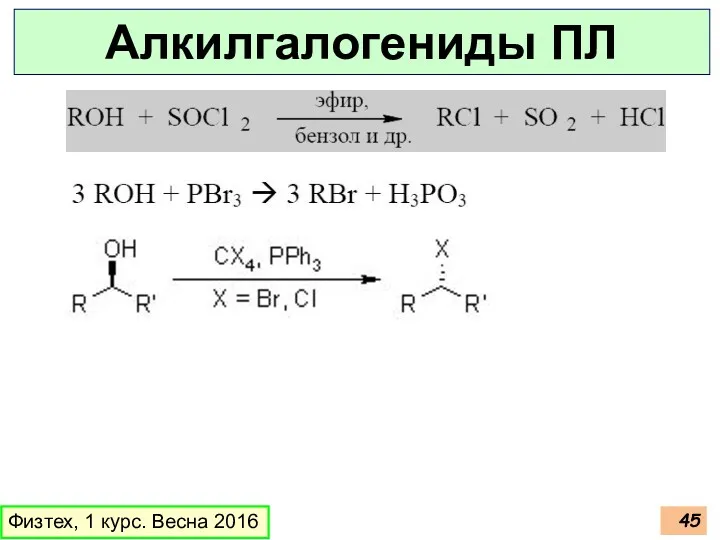
- 45. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
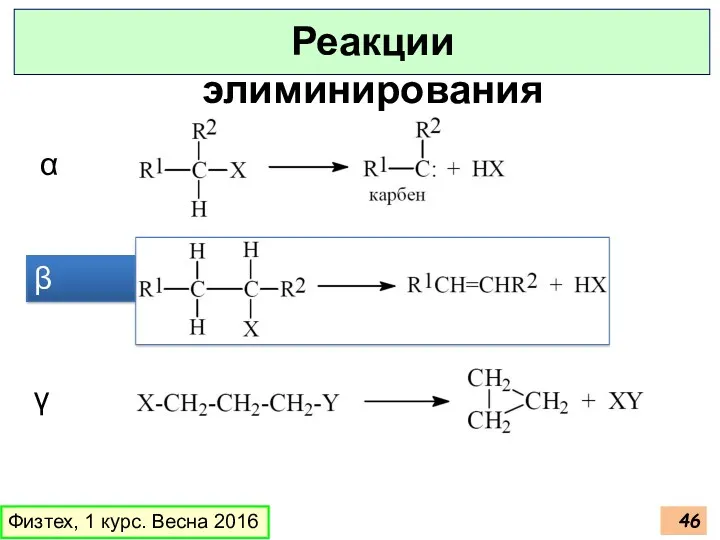
- 46. Физтех, 1 курс. Весна 2016 Реакции элиминирования α β γ
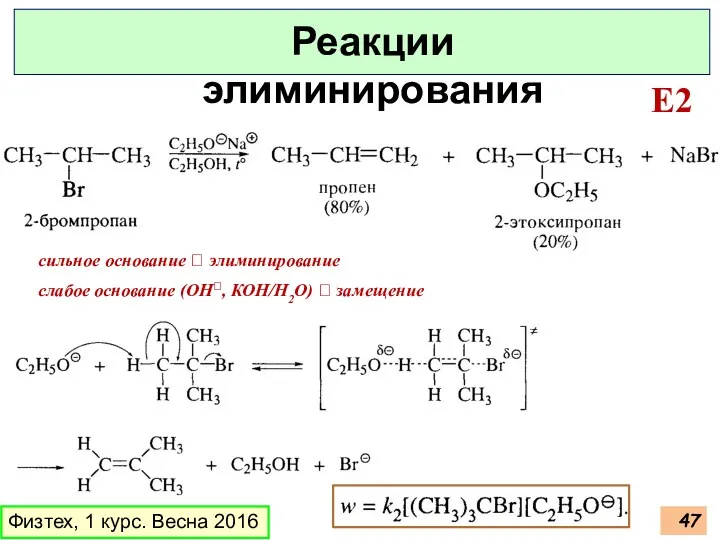
- 47. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2 сильное основание ? элиминирование слабое основание (ОН, КОН/Н2О)
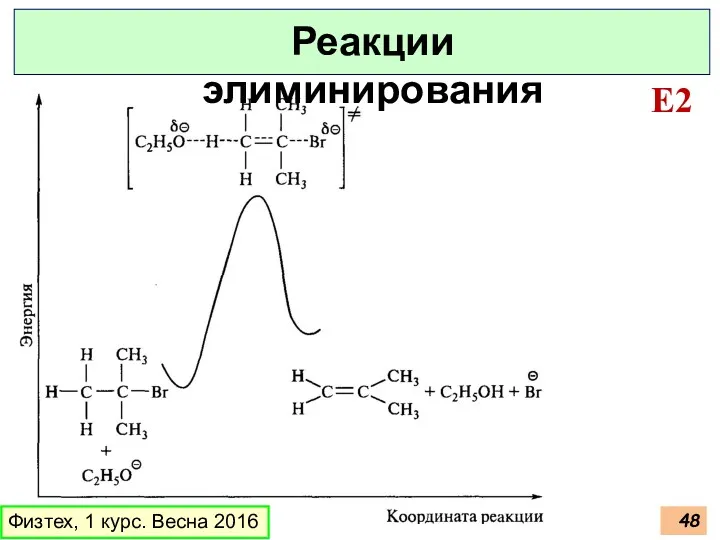
- 48. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2
- 49. Физтех, 1 курс. Весна 2016 Реакции элиминирования Региоселективность E2 Правило Зайцева (верно для случаев, когда уходящая
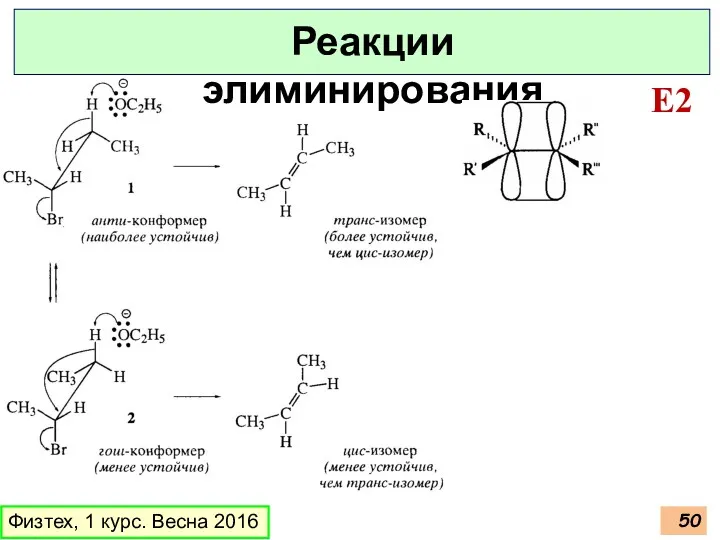
- 50. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2
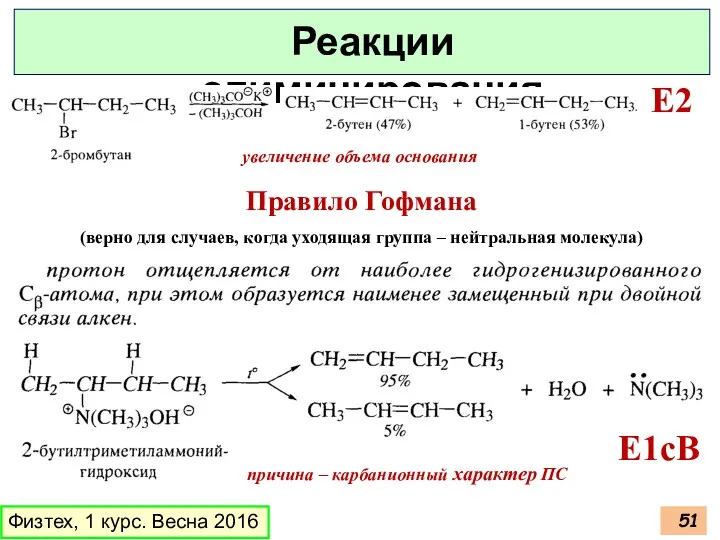
- 51. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2 увеличение объема основания Правило Гофмана (верно для случаев,
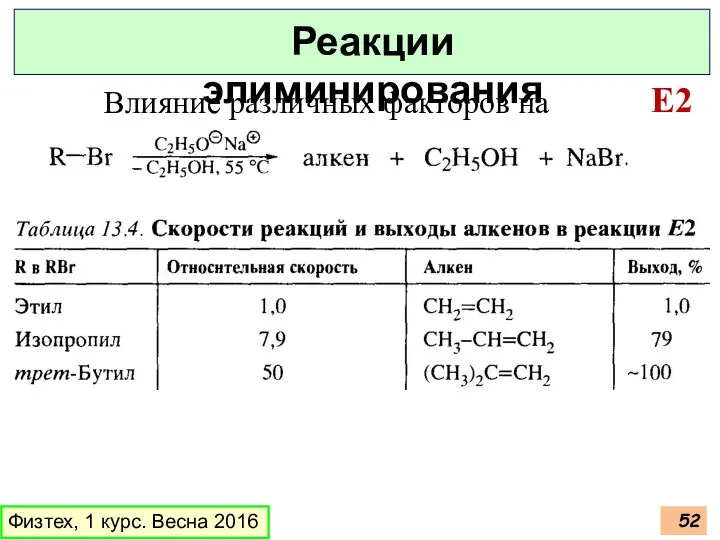
- 52. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2 Влияние различных факторов на
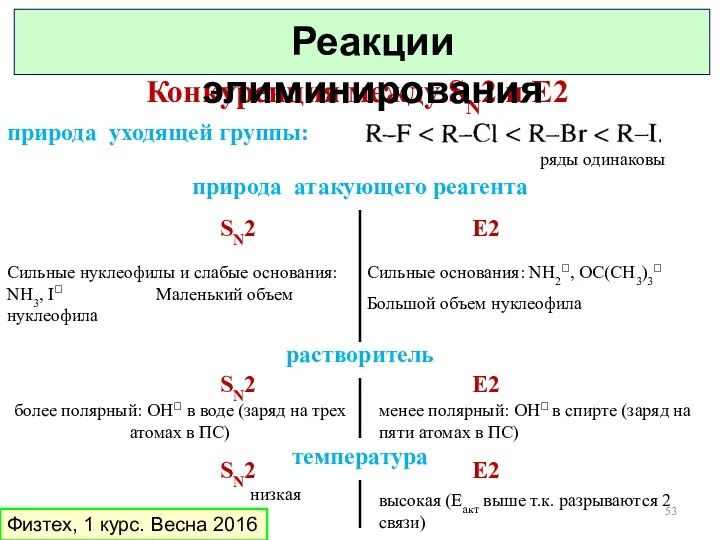
- 53. Конкуренция между SN2 и E2 природа уходящей группы: природа атакующего реагента SN2 E2 Сильные основания: NH2,
- 54. Физтех, 1 курс. Весна 2016 Реакции элиминирования E vs SN
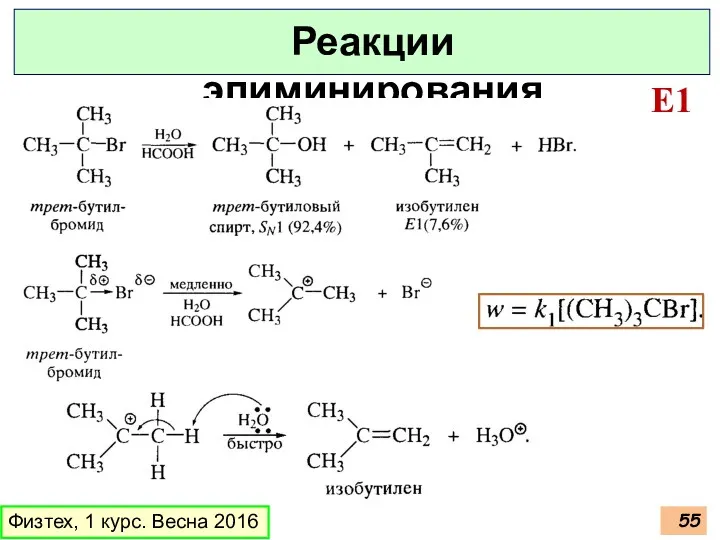
- 55. Физтех, 1 курс. Весна 2016 Реакции элиминирования E1
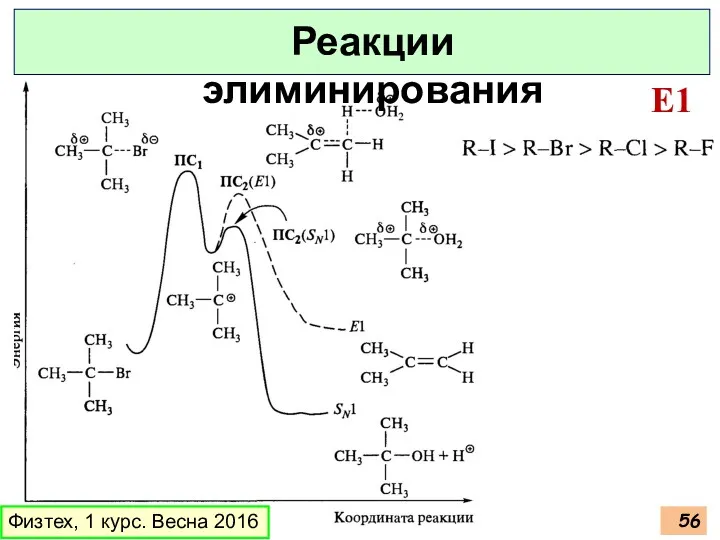
- 56. Физтех, 1 курс. Весна 2016 Реакции элиминирования E1
- 57. Физтех, 1 курс. Весна 2016 Реакции элиминирования E1 Против правила Зайцева – стерические препятствия отрыва бета-Н
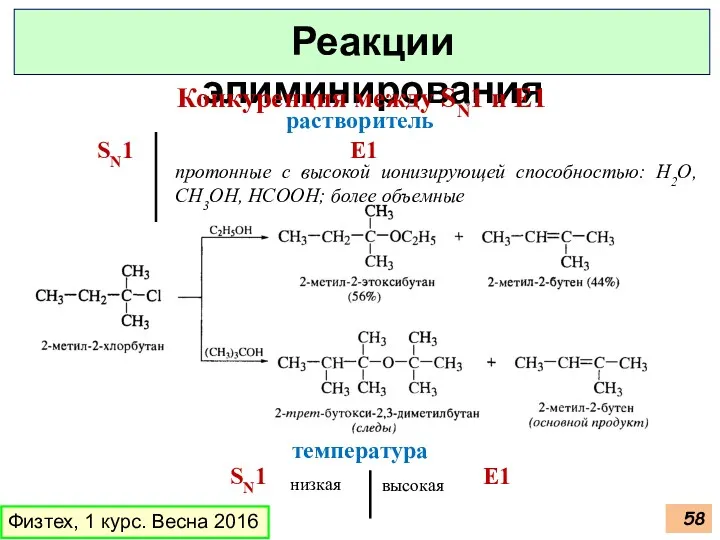
- 58. Физтех, 1 курс. Весна 2016 Реакции элиминирования Конкуренция между SN1 и E1 растворитель SN1 E1 протонные
- 60. Скачать презентацию












 Титрование в неводных средах. (Лекция 26)
Титрование в неводных средах. (Лекция 26) Химический элемент йод
Химический элемент йод Химическая промышленность
Химическая промышленность Соляная кислота и её соли
Соляная кислота и её соли Химическая промышленность
Химическая промышленность Пластмаси, синтетичні каучуки, гума, штучні й синтетичні
Пластмаси, синтетичні каучуки, гума, штучні й синтетичні Макро- и микроэлементы
Макро- и микроэлементы Алюминий и его соединения
Алюминий и его соединения В мире криссталлов
В мире криссталлов Проект: жило-было мыло
Проект: жило-было мыло Естери. Класифікація та номенклатура естерів
Естери. Класифікація та номенклатура естерів Химический элементы в нашей жизни
Химический элементы в нашей жизни Окислительно-восстановительные реакции
Окислительно-восстановительные реакции История развитии химии
История развитии химии Насыщенные углеводороды
Насыщенные углеводороды Материаловедение. Свойства материалов. (Тема 2)
Материаловедение. Свойства материалов. (Тема 2) Петрография некоторых распространенных метаморфических пород
Петрография некоторых распространенных метаморфических пород Растворы
Растворы Строение алканов. Физические и химические свойства алканов. Получение алканов
Строение алканов. Физические и химические свойства алканов. Получение алканов Соединения кальция. Жесткость воды и способы её устранения
Соединения кальция. Жесткость воды и способы её устранения Основные классы неорганических соединений
Основные классы неорганических соединений Алкиндер. Номенклатурасы, табиғатта кездесуі, физикалық және химиялық қасиеттері, алыну жолдары
Алкиндер. Номенклатурасы, табиғатта кездесуі, физикалық және химиялық қасиеттері, алыну жолдары Наноматериалы. Свойства наноматериалов. Особенности свойств
Наноматериалы. Свойства наноматериалов. Особенности свойств Итоговая контрольная работа по химии
Итоговая контрольная работа по химии Электроизоляционные жидкости на основе синтетических углеводородов и других соединений
Электроизоляционные жидкости на основе синтетических углеводородов и других соединений Теория электролитической диссоциации (ТЭД)
Теория электролитической диссоциации (ТЭД) Химия и производство
Химия и производство Классификация органических реакций
Классификация органических реакций