Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями презентация
Содержание
- 2. Цілі: встановити взаємозв’язок між будовою речовин та їх фізичними властивостями на підставі знань про типи хімічних
- 3. «Одного разу, під час бенкету Клеопатра заявила, що вип'є десять мільйонів сестерцій(93 млн.гр.) Вона вийняла з
- 4. Будова твердих речовин Аморфна Кристалічна Структурні частинки речовини розміщуються безладно Приклад: глина Структурні частинки речовини розміщуються
- 5. Кристалічна ґрадка - структурна впорядкованість кристалічних речовин Види кристалічних ґраток Атомна Йонна Молекулярна Металічна
- 6. Тип кристалічної решітки -йонниа. У вузлах кристалічних ґраток знаходяться йони Натрію і Хлору, які утримуються силами
- 7. Натрій хлорид (NaCl) – твердий, кристалічний, тугоплавкий, добре розчинний у воді. Хімічний зв’язок - йонний, у
- 8. Тип кристалічної решітки - атомна У вузлах кристалічних ґраток знаходяться атоми Карбону, які зв’язані між собою
- 9. Графіт (C )- тверда речовина, нерозчинна у воді. Хімічний зв'язок - ковалентний неполярний. Тип кристалічної решітки
- 10. Тип кристалічної решітки – молекулярна У вузлах кристалічних ґраток знаходяться молекули вуглекислого газу. Зв'язок між ними
- 11. Карбон (IV) оксид (CO2) - за н.у. газ, низькі температури плавлення, розчинний у воді. Хімічний зв’язок
- 12. Тип кристалічної решітки – металевий У вузлах кристалічних ґраток знаходяться атоми та йони Феруму, а між
- 13. Залізо – високі температури плавлення, нерозчинне у воді. Хімічний зв'язок - металічний Тип кристалічної решітки –
- 14. Інструкція з визначення типу кристалічної гратки 1. Проста речовина – визначити метал чи неметал: Ме –
- 15. 2. Складна речовина – визначити клас речовини: неМехОу – молекулярну кристалічну гратку; P2O5 МехОу – йонну
- 16. Завдання 1 За зразками кристалічних ґраток, з’ясувати, яку речовину ви отримали, довести це: Речовини: графіт, алмаз,
- 17. Завдання 2 Виправити помилки: Атомна кристалічна градка: Cl2, Fe , N2 H2O, C Молекулярна кристалічна градка:
- 18. Карбонат кальцію (CaCO3) має йонну кристалічну решітку, тому, можна з певність спрогнозувати повне розчинення цієї речовини
- 19. Домашнє завдання 1) Вивчити § підручника, опрацювати конспект. 2) Створити просторові моделі різних кристалічних ґраток; знайти
- 21. Скачать презентацию


















 Основания. 8 класс
Основания. 8 класс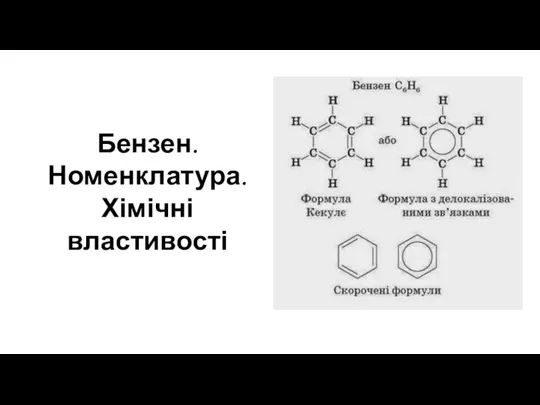 Бензен. Номенклатура. Хімічні властивості
Бензен. Номенклатура. Хімічні властивості Циклоалканы
Циклоалканы Неметаллы: общая характеристика
Неметаллы: общая характеристика Школьное мероприятие Д. И. Менделеев в высказываниях
Школьное мероприятие Д. И. Менделеев в высказываниях Изучение состава и свойств противогололедного материала Бионорд
Изучение состава и свойств противогололедного материала Бионорд Промежуточные фазы в металлических сплавах
Промежуточные фазы в металлических сплавах Сероводород. Сульфиды
Сероводород. Сульфиды Застосування неметалів
Застосування неметалів 20231110_zakon_avogadro
20231110_zakon_avogadro Производство азотной кислоты
Производство азотной кислоты Характеристика азота и фосфора. Свойства азота
Характеристика азота и фосфора. Свойства азота Подготовка пробы к анализу. Использование химических и физико-химических методов для идентификации вещества. (Лекция 11)
Подготовка пробы к анализу. Использование химических и физико-химических методов для идентификации вещества. (Лекция 11) Вуглецеві наноматеріали (наноматеріали із карбону). Алотропні модифікації карбону. Алмаз. Карбін. Графен
Вуглецеві наноматеріали (наноматеріали із карбону). Алотропні модифікації карбону. Алмаз. Карбін. Графен Щелочные металлы
Щелочные металлы Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ
Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Кислоты. Классификация кислот, их химические свойства
Кислоты. Классификация кислот, их химические свойства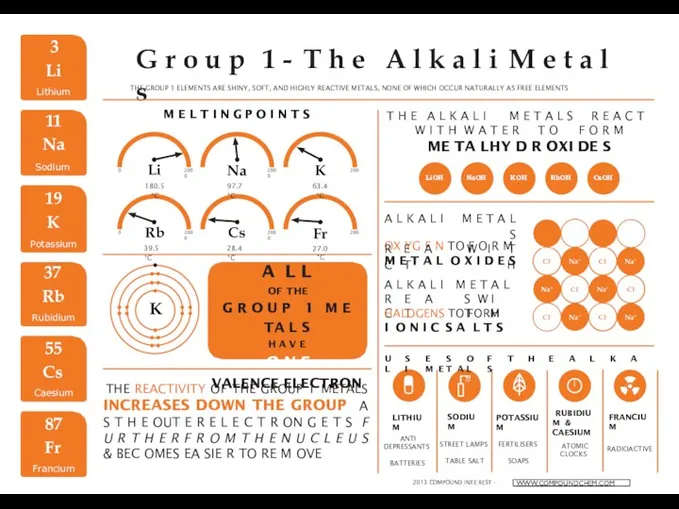 The alkali metals
The alkali metals Определение фосфатов, железа, хлоридов
Определение фосфатов, железа, хлоридов Автомобильные масла. Классификация и применение автомобильных масел
Автомобильные масла. Классификация и применение автомобильных масел Ферменты. Размеры ферментов и их строение
Ферменты. Размеры ферментов и их строение Лекции по курсу конструкционные и биоматериалы
Лекции по курсу конструкционные и биоматериалы Химическая связь
Химическая связь Кислоты и щелочи. Индикаторы. 6 класс
Кислоты и щелочи. Индикаторы. 6 класс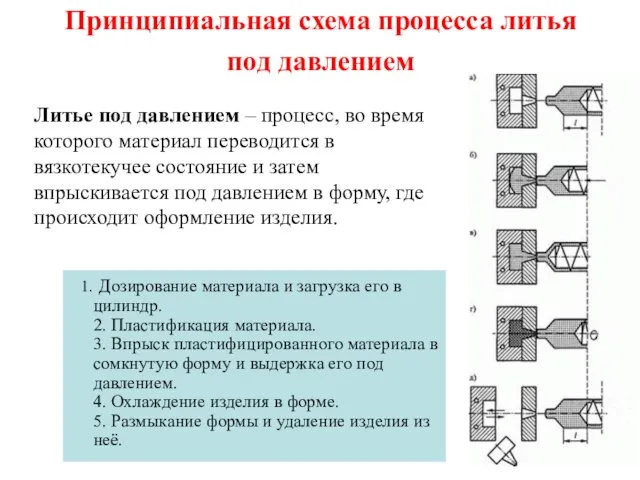 Принципиальная схема процесса литья под давлением
Принципиальная схема процесса литья под давлением Неметаллы. Занятие 20
Неметаллы. Занятие 20 Происхождение химических элементов
Происхождение химических элементов