Содержание
- 2. Цели урока: Систематизировать знания обучающихся о понятиях количество вещества, число Авогадро, молярная масса; раскрыть сущность закона
- 3. Вариант I Вариант II Отгадайте загадку: В чем горят дрова и газ, Фосфор, водород, алмаз? Дышит
- 4. Из курса физики . . . 1. Газообразные вещества состоят из молекул (О2, Н2, N2, Cl2,
- 5. Вспомним . . . 1 моль – это количество вещества, в котором содержится 6 ∙1023 частиц.
- 6. Закон Авогадро: В равных объёмах различных газов при одинаковых условиях содержится одинаковое число молекул. Амедео Авогадро
- 7. Закон Авогадро:
- 8. Следствие из закона: 1 моль любого газа занимает одинаковый объём равный 22,4 л. Этот объём называется
- 9. Решите задачу: При взаимодействии железа с кислородом образуется 23,2 г оксида железа (Fe3O4). Вычислите объём кислорода,
- 10. Рефлексия: Одним словом выразите тему сегодняшнего урока. Подберите к этому слову 2 прилагательных. Подберите к этому
- 12. Скачать презентацию









 Фосфор и его соединения
Фосфор и его соединения Химиялық байланыс және заттардың құрылымдық түрлі сатылары
Химиялық байланыс және заттардың құрылымдық түрлі сатылары Дистилляция и ректификация
Дистилляция и ректификация Металлы и их соединения
Металлы и их соединения Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение
Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение Кислородосодержащие производные углеводородов. Спирты. Фенолы. Простые эфиры
Кислородосодержащие производные углеводородов. Спирты. Фенолы. Простые эфиры Углеводы
Углеводы Металлическая связь
Металлическая связь Карбоновые кислоты. (Лекция 6.3)
Карбоновые кислоты. (Лекция 6.3) Стирка по научному
Стирка по научному Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов)
Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов) Спирты. Классификация, номенклатура, изомерия спиртов
Спирты. Классификация, номенклатура, изомерия спиртов Строение атома
Строение атома Углеводы, монозы, биозы. Лекция 15
Углеводы, монозы, биозы. Лекция 15 Атом – сложная частица
Атом – сложная частица Элементы пятой-А группы. Азот и фосфор
Элементы пятой-А группы. Азот и фосфор Идеальные и реальные кристаллы
Идеальные и реальные кристаллы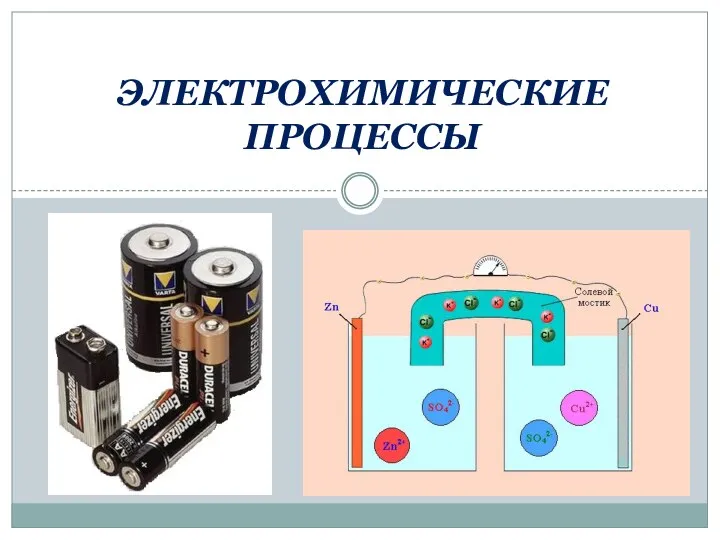 Электрохимические процессы
Электрохимические процессы Ядерное топливо
Ядерное топливо Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Палладий. История открытия химических веществ
Палладий. История открытия химических веществ Качественные реакции
Качественные реакции 20230219_prezentatsiya_k_uroku_neft
20230219_prezentatsiya_k_uroku_neft Аминокислоты, как структурные компоненты белков
Аминокислоты, как структурные компоненты белков Степень окисления. Составление химических формул бинарных соединений
Степень окисления. Составление химических формул бинарных соединений Основи. Фізичні властивості основ
Основи. Фізичні властивості основ Внеклассное мероприятие по химии. 9 класс
Внеклассное мероприятие по химии. 9 класс Водород. Характеристика положения водорода в ПСХЭ, строение атома и молекулы (8 класс)
Водород. Характеристика положения водорода в ПСХЭ, строение атома и молекулы (8 класс)