Содержание
- 2. Гетеролитический разрыв связей С-С и С-Н в обычных условиях не происходит. Это проявляется в устойчивости алканов
- 3. При достаочном количестве хлора реакция может продолжаться дальше и приводить к образованию смеси продуктов замещения 2-х,
- 4. Нитрование. На алканы действует разбавленная (12—14%-ной) азотная кислота при нагревании (~140°С) и давлении (реакция М. И.
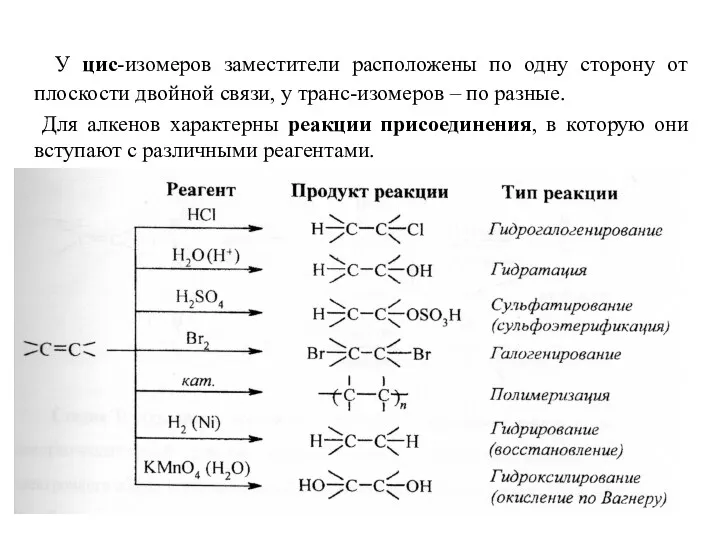
- 5. Алкены (этиленовые углеводороды или олефины) – это непредельные углеводороды, молекулы которых содержат одну двойную связь, общая
- 6. У цис-изомеров заместители расположены по одну сторону от плоскости двойной связи, у транс-изомеров – по разные.
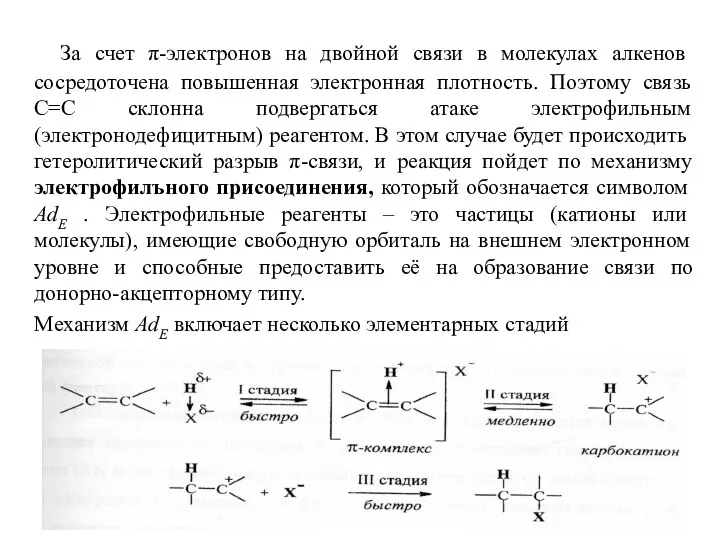
- 7. За счет π-электронов на двойной связи в молекулах алкенов сосредоточена повышенная электронная плотность. Поэтому связь С=С
- 8. Стадия I: образование промежуточной частицы, называемой π-комплексом. Это донорно-акцепторный комплекс, который возникает в результате взаимодействия π-электронного
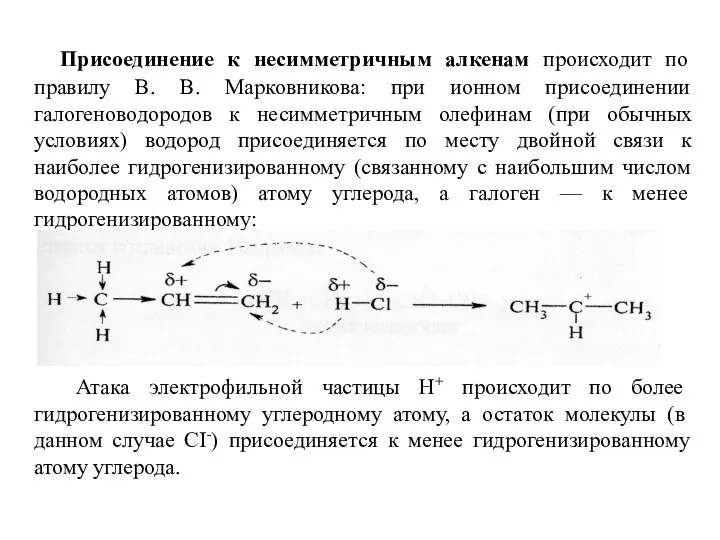
- 9. Присоединение к несимметричным алкенам происходит по правилу В. В. Марковникова: при ионном присоединении галогеноводородов к несимметричным
- 10. Реакции окисления. Алкены легко окисляются многими окислителями. При мягком окислении разрывается π-связь, а при жестком- и
- 11. Реакции полимеризации – образование высокомолекулярных соединений из низкомолекулярных за счет разрыва непрочных двойных связей в молекулах
- 12. Алкины или ацетиленовые углеводороды - ненасыщенные углеводороды, содержащие в молекуле одну тройную связь. Они имеют общую
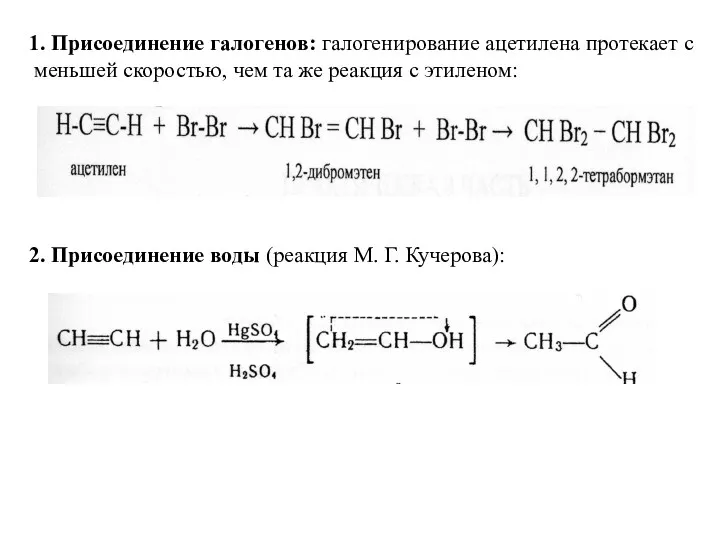
- 13. 1. Присоединение галогенов: галогенирование ацетилена протекает с меньшей скоростью, чем та же реакция с этиленом: 2.
- 14. Реакции замещения. Ацетилен и его гомологи с концевой тройной связью К-С≡С-Н вследствие полярности связи С (sр)-Н
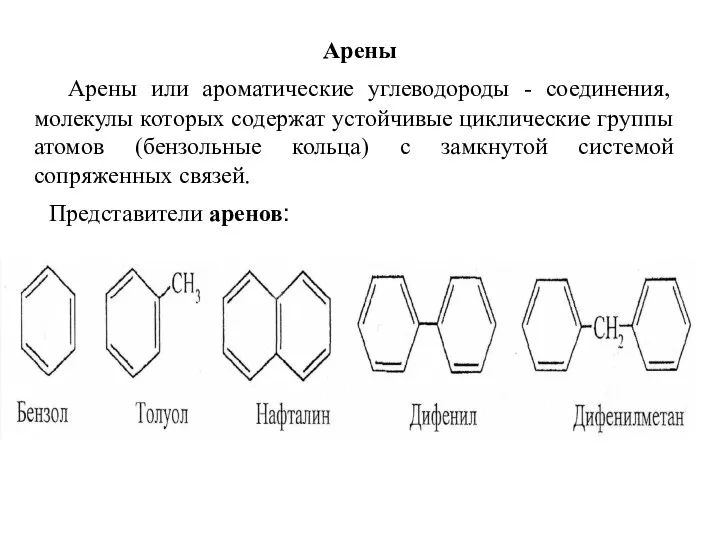
- 15. Арены Арены или ароматические углеводороды - соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные кольца)
- 16. По числу бензольных колец в молекуле арены подразделяются на группы. - Моноядерные арены - общая формула
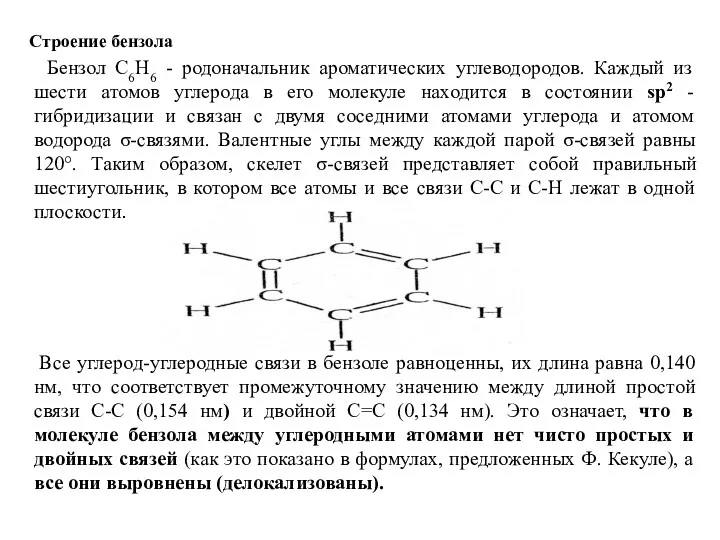
- 17. Строение бензола Бензол С6Н6 - родоначальник ароматических углеводородов. Каждый из шести атомов углерода в его молекуле
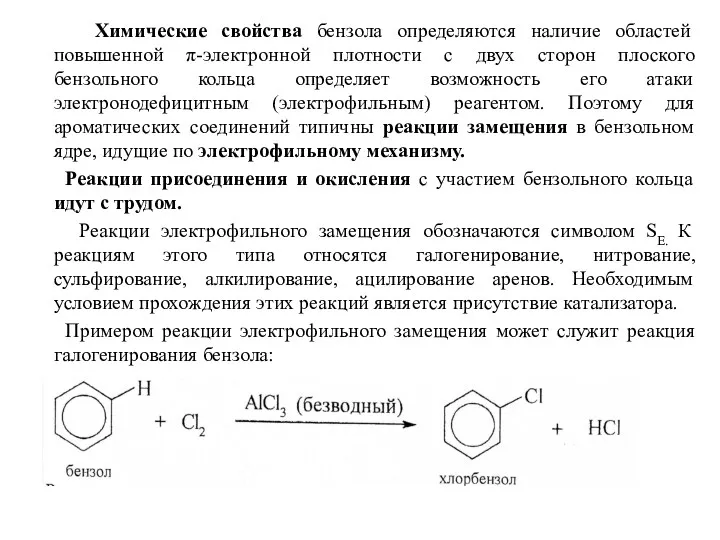
- 18. Химические свойства бензола определяются наличие областей повышенной π-электронной плотности с двух сторон плоского бензольного кольца определяет
- 19. Влияние заместителя в бензольном кольце на направление и скорость электрофильного замещения В незамещенном бензоле С6Н6 электронная
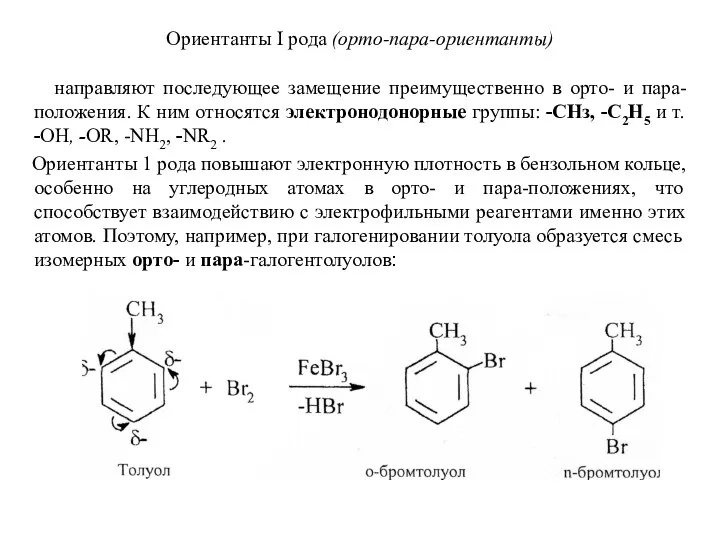
- 20. Ориентанты I рода (орто-пара-ориентанты) направляют последующее замещение преимущественно в орто- и пара-положения. К ним относятся электронодонорные
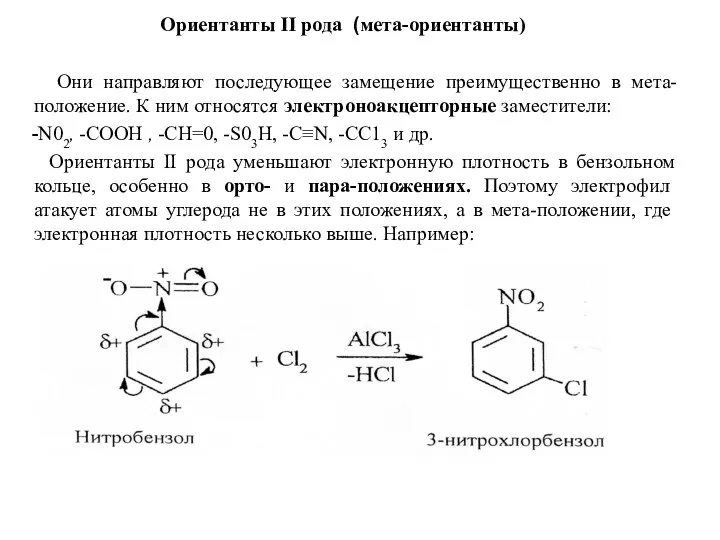
- 21. Ориентанты II рода (мета-ориентанты) Они направляют последующее замещение преимущественно в мета-положение. К ним относятся электроноакцепторные заместители:
- 22. ГИДРОКСИСОЕДИНЕНИЯ К органическим гидроксисоединениям относятся вещества, которые содержат в молекулах одну или более гидроксильных групп -ОН,
- 23. двухатомный спирт, трехатомный спирт: Спирты с двумя ОН-группами при одном и том же атоме углерода, такие
- 24. В реакциях гидроксисоединений по функциональной группе возможен разрыв одной из двух связей: С-ОН с отщеплением ОН-группы,
- 25. Реакции по связи О-Н К наиболее характерным реакциям гидроксисоединений, идущим с разрывом связи О-Н, относятся: замещение
- 26. Кислотные свойства гидроксисоединений Спирты. Одноатомные спирты реагируют с активными металлами (Nа, К, Мg, А1 и др.),
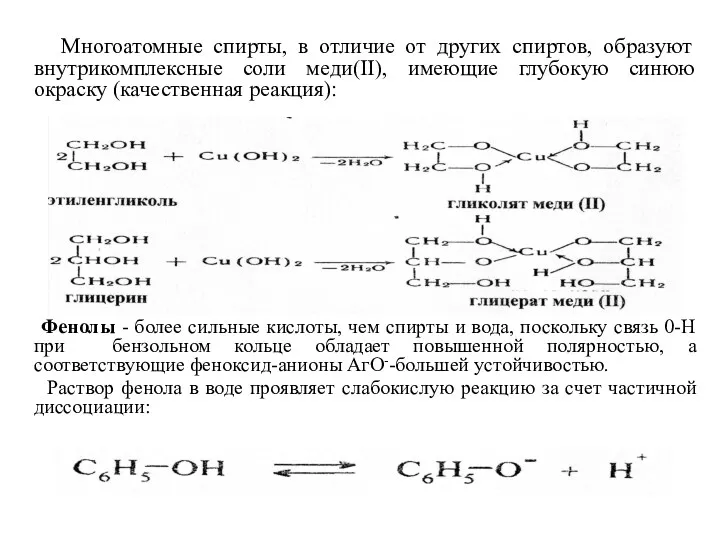
- 27. Многоатомные спирты, в отличие от других спиртов, образуют внутрикомплексные соли меди(II), имеющие глубокую синюю окраску (качественная
- 28. Фенолы реагируют как с активными металлами, так и с их гидроксидами, образуя соли - феноляты (феноксиды):
- 29. ОКСОСОЕДИНЕНИЯ (АЛЬДЕГИДЫ И КЕТОНЫ) Органические соединения, молекулы которых содержат карбонильную группу (оксо-группу) называют карбонильными или оксосоединениями
- 30. Кетоны - органические вещества, молекулы которых содержат карбонильную группу, соединенную с двумя углеводородными радикалами. Свойства альдегидов
- 31. Химические свойства альдегидов и кетонов Для карбонильных соединений характерны реакции различных типов: реакции, по карбонильной группе;
- 32. Наличие в молекуле альдегида или кетона электрофильного центра - атома углерода карбонильной группы - предопределяет возможность
- 33. Реакции восстановления оксидов и гидроксидов металлов альдегидной группой. Альдегиды легко восстанавливают оксид серебра и гидроксид меди
- 34. КАРБОНОВЫЕ КИСЛОТЫ Карбоновые кислоты - органические соединения, молекулы которых содержат одну или несколько карбоксильных групп -СООН,
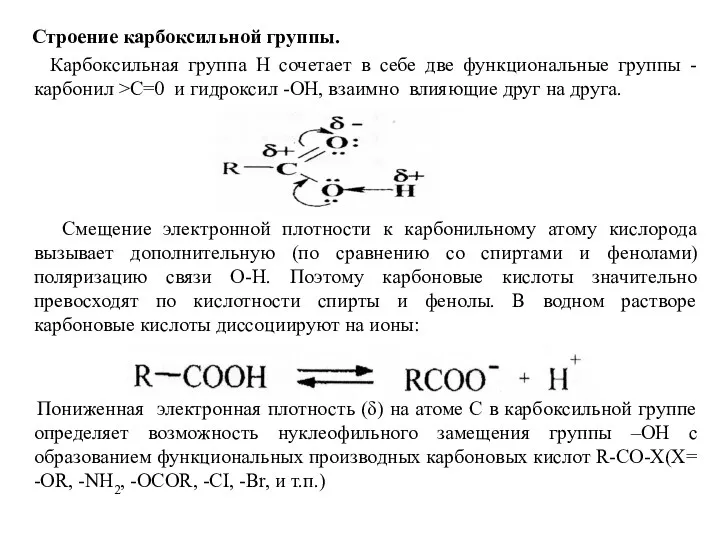
- 35. Строение карбоксильной группы. Карбоксильная группа Н сочетает в себе две функциональные группы - карбонил >С=0 и
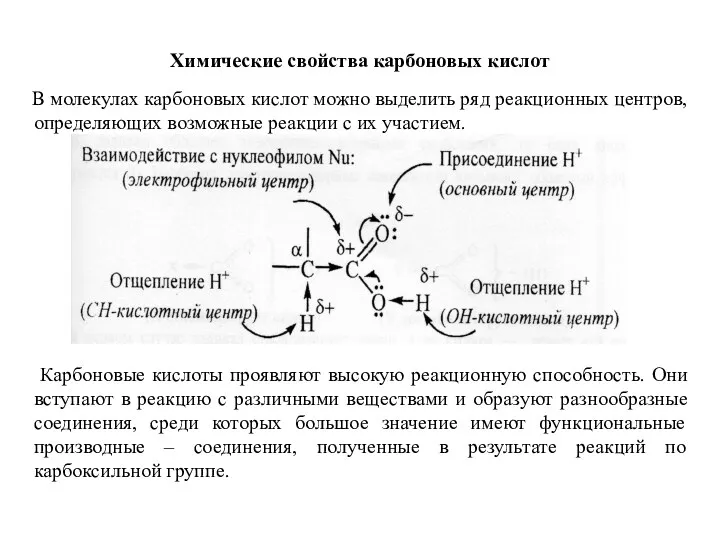
- 36. Химические свойства карбоновых кислот В молекулах карбоновых кислот можно выделить ряд реакционных центров, определяющих возможные реакции
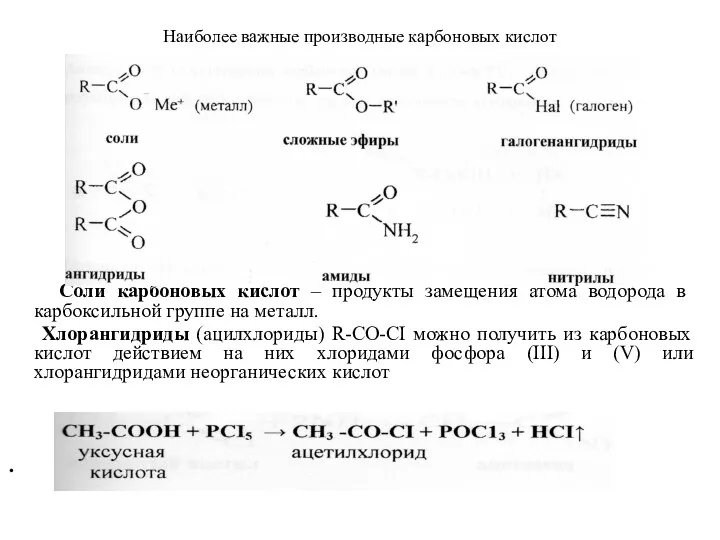
- 37. Наиболее важные производные карбоновых кислот Соли карбоновых кислот – продукты замещения атома водорода в карбоксильной группе
- 38. Сложные эфиры, R-COOR' - производные карбоновых кислот, в которых гидраксильная группа –ОН карбоксила замещена на группу
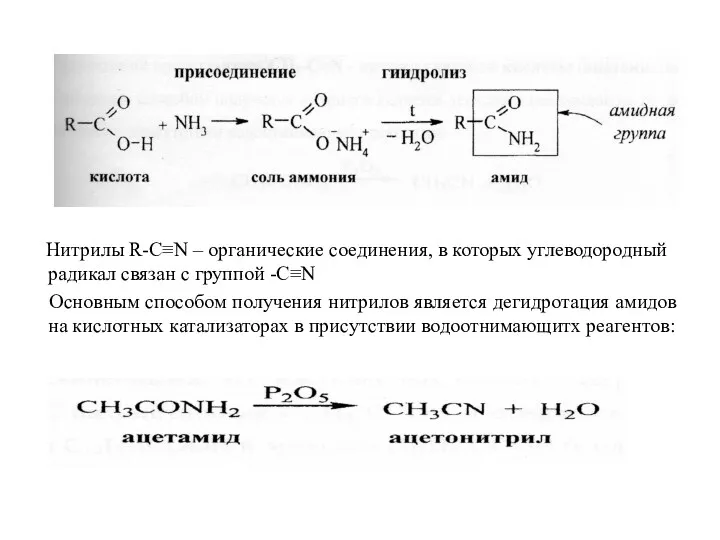
- 39. Нитрилы R-C≡N – органические соединения, в которых углеводородный радикал связан с группой -С≡N Основным способом получения
- 40. Аминокислоты Аминокислоты - органические соединения, содержащие в молекуле два типа функциональных групп: карбоксильную -СООН, и аминогруппу
- 41. Физические и химические свойства а-Аминокислоты - кристаллические вещества, растворимые в воде. Многие из них обладают сладким
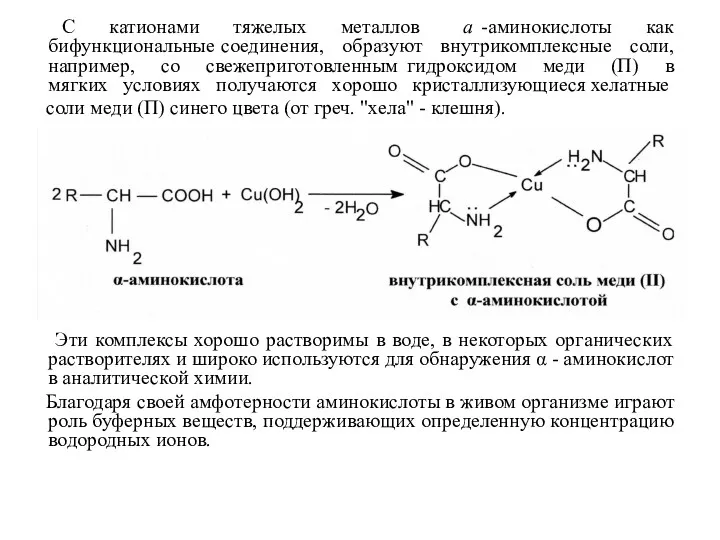
- 42. С катионами тяжелых металлов а -аминокислоты как бифункциональные соединения, образуют внутрикомплексные соли, например, со свежеприготовленным гидроксидом
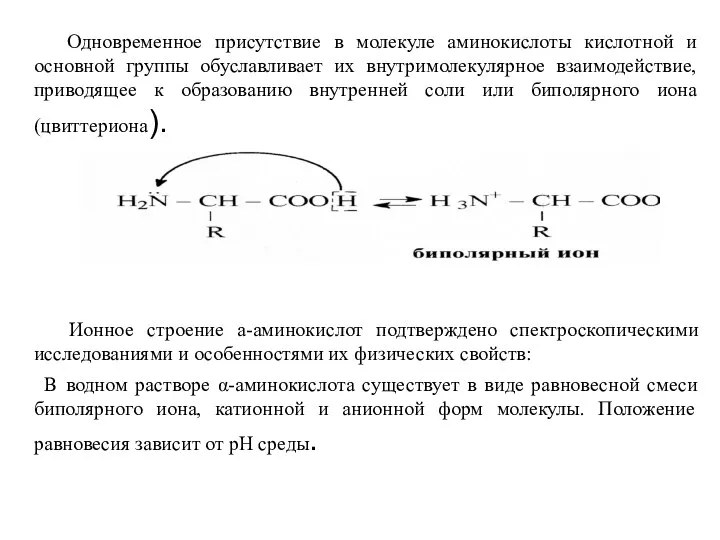
- 43. Одновременное присутствие в молекуле аминокислоты кислотной и основной группы обуславливает их внутримолекулярное взаимодействие, приводящее к образованию
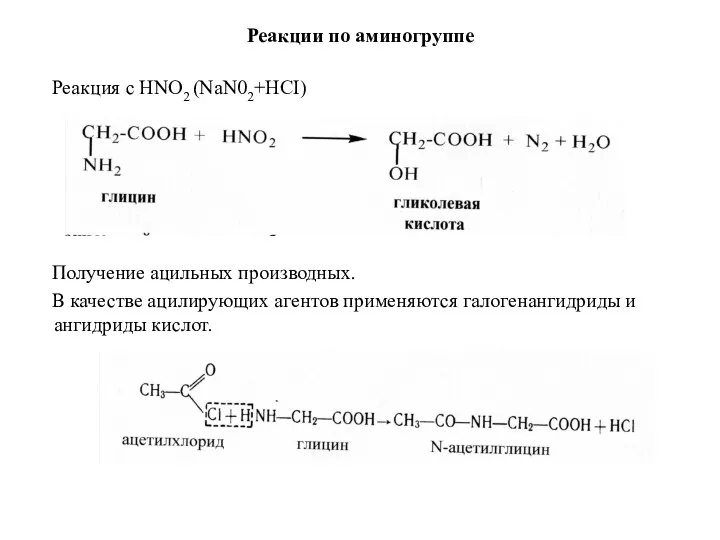
- 45. Реакции по аминогруппе Реакция с HNO2 (NaN02+HCI) Получение ацильных производных. В качестве ацилирующих агентов применяются галогенангидриды
- 47. Скачать презентацию



























 Галогены. История открытия галогенов
Галогены. История открытия галогенов Коррозия металлов. Причины коррозии металлов
Коррозия металлов. Причины коррозии металлов Всероссийская олимпиада школьников по химии (региональный этап). Разбор заданий, 9 класс
Всероссийская олимпиада школьников по химии (региональный этап). Разбор заданий, 9 класс Класифікація та властивості оксидів
Класифікація та властивості оксидів Коллоидная химия
Коллоидная химия Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Теория электролитической диссоциации (ТЭД)
Теория электролитической диссоциации (ТЭД) Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Влияние фтора на организм человека
Влияние фтора на организм человека Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Кислород и оксиген
Кислород и оксиген Алкины
Алкины Шампуни: классификация по составу и назначению
Шампуни: классификация по составу и назначению Виды химической связи
Виды химической связи Химическая термодинамика. Экзаменационные вопросы
Химическая термодинамика. Экзаменационные вопросы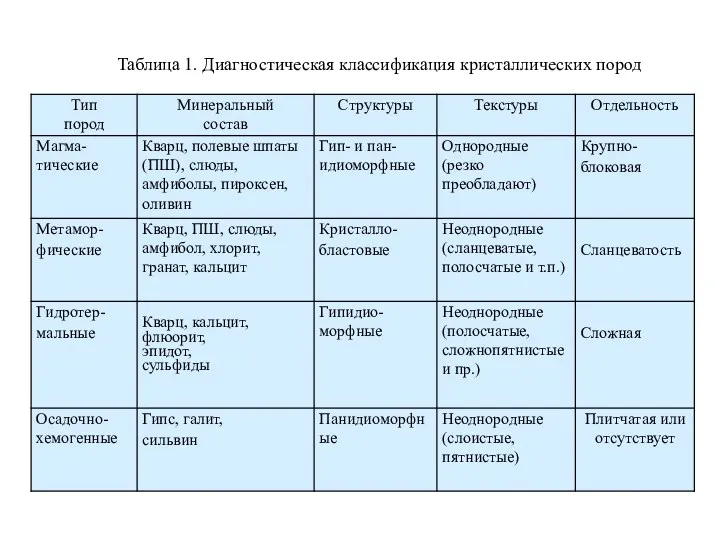 Диагностика метаморфических и гидротермальных горных пород
Диагностика метаморфических и гидротермальных горных пород Закон сохранения массы вещества. Химические уравнения
Закон сохранения массы вещества. Химические уравнения Массовая доля растворенного вещества в растворе
Массовая доля растворенного вещества в растворе Формирование ключевых компетенций на уроках химии
Формирование ключевых компетенций на уроках химии Atmospheric chemistry
Atmospheric chemistry Масова частка розчиненої речовини
Масова частка розчиненої речовини Разбор заданий #ОВРновый, #реакционно и #соточка
Разбор заданий #ОВРновый, #реакционно и #соточка 20230419_azot
20230419_azot Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Новые интеллектуальные материалы на основе полимеров
Новые интеллектуальные материалы на основе полимеров Удивительное вещество - вода
Удивительное вещество - вода Химический элементы в нашей жизни
Химический элементы в нашей жизни Кристаллическое состояние вещества
Кристаллическое состояние вещества