Содержание
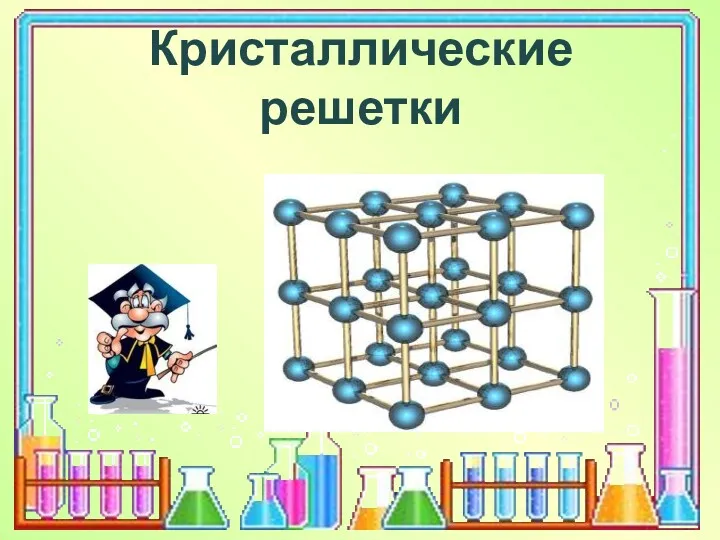
- 2. Кристаллические решетки
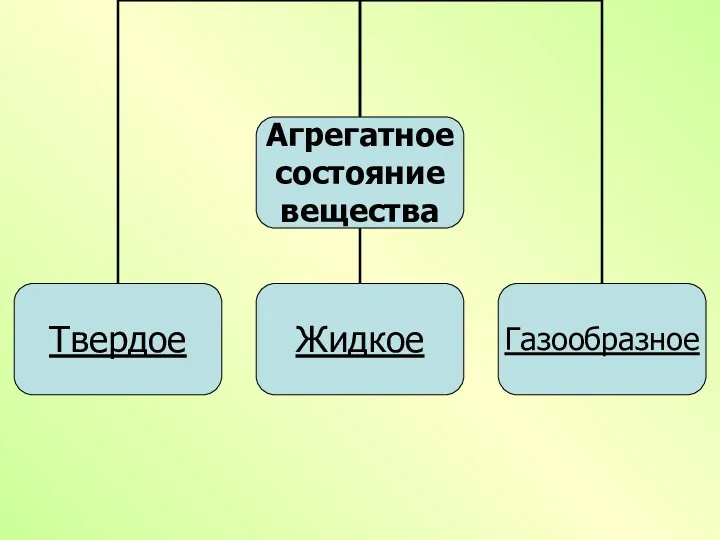
- 3. Цель урока - установить взаимосвязь между строением и свойствами веществ Задачи: Выяснить в каком виде может
- 4. Вещество – это то, ... из чего состоит физическое тело.
- 6. Кристаллическая решётка вещества – это упорядоченное расположение частиц (атомов, молекул, ионов) в строго определённых точках пространства.
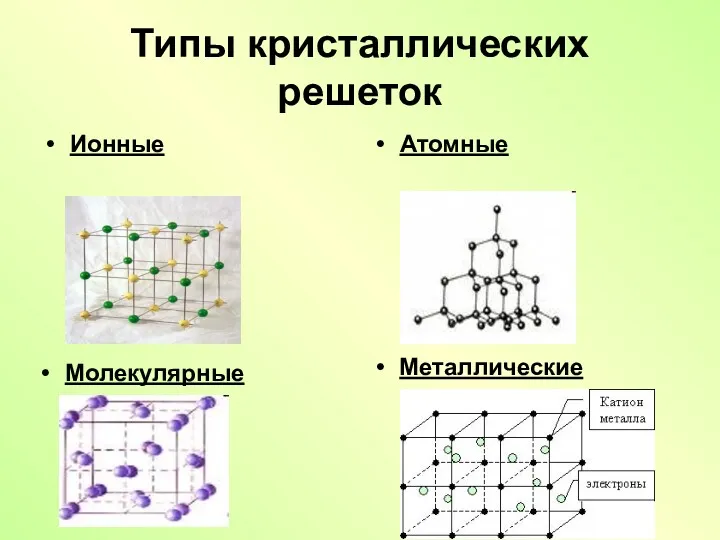
- 7. Типы кристаллических решеток Ионные Атомные Молекулярные Металлические
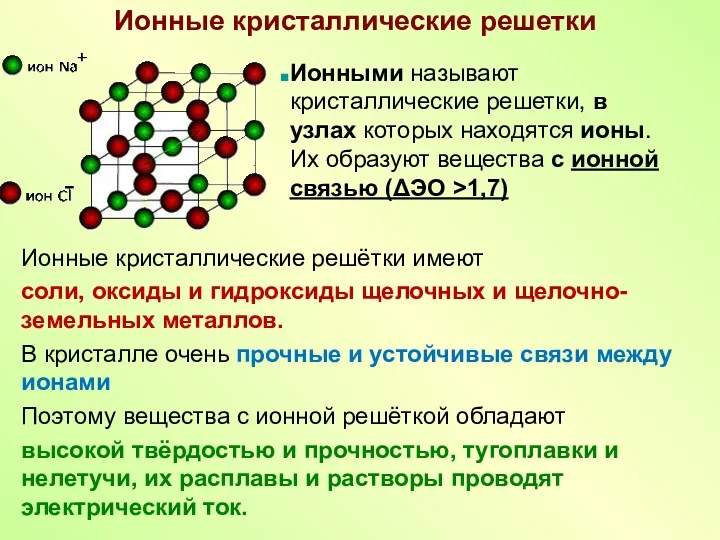
- 8. Ионные кристаллические решетки Ионные кристаллические решётки имеют соли, оксиды и гидроксиды щелочных и щелочно-земельных металлов. В
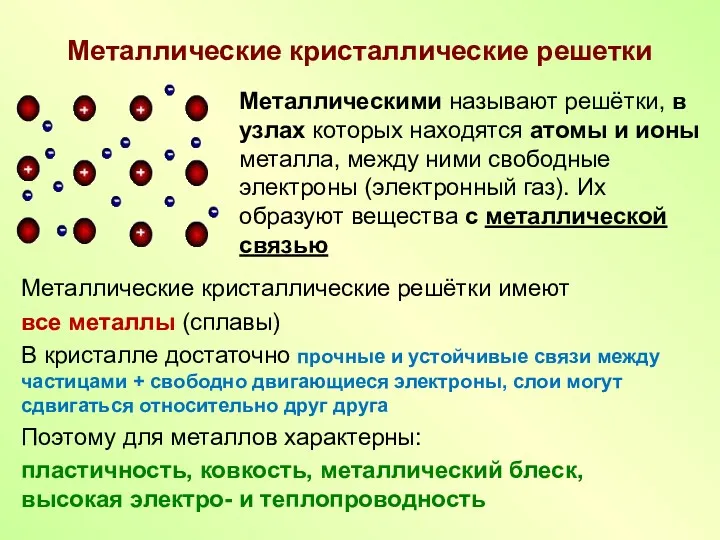
- 9. Металлические кристаллические решетки Металлические кристаллические решётки имеют все металлы (сплавы) В кристалле достаточно прочные и устойчивые
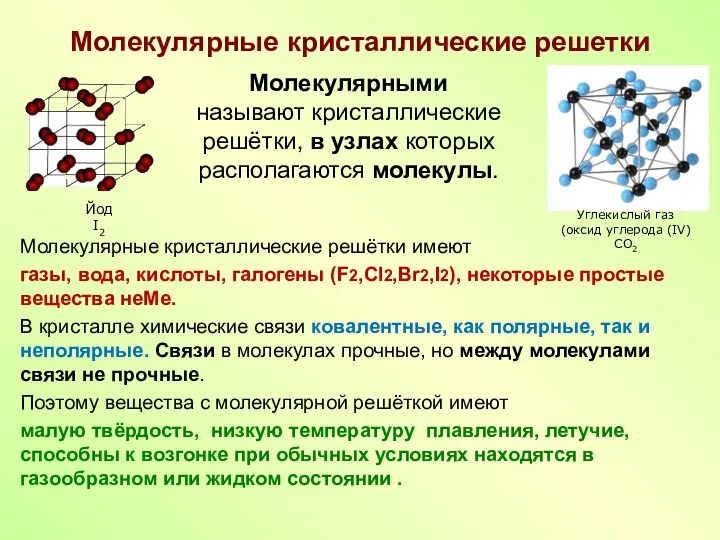
- 10. Молекулярные кристаллические решетки Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Йод I2 Углекислый газ
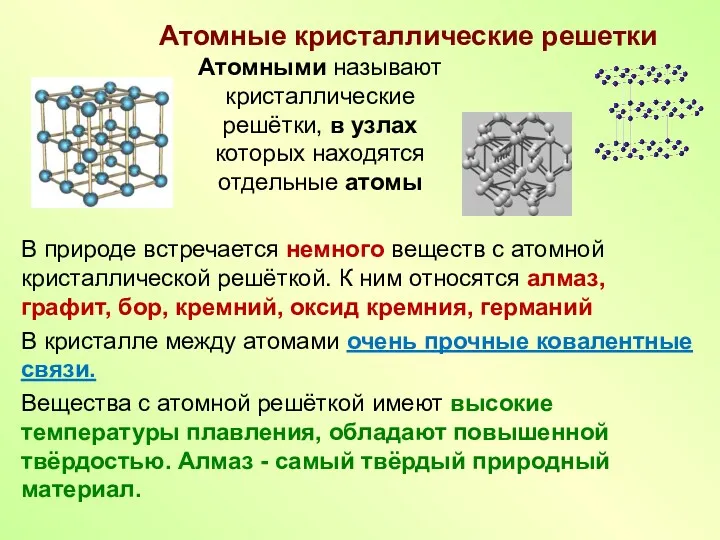
- 11. Атомные кристаллические решетки В природе встречается немного веществ с атомной кристаллической решёткой. К ним относятся алмаз,
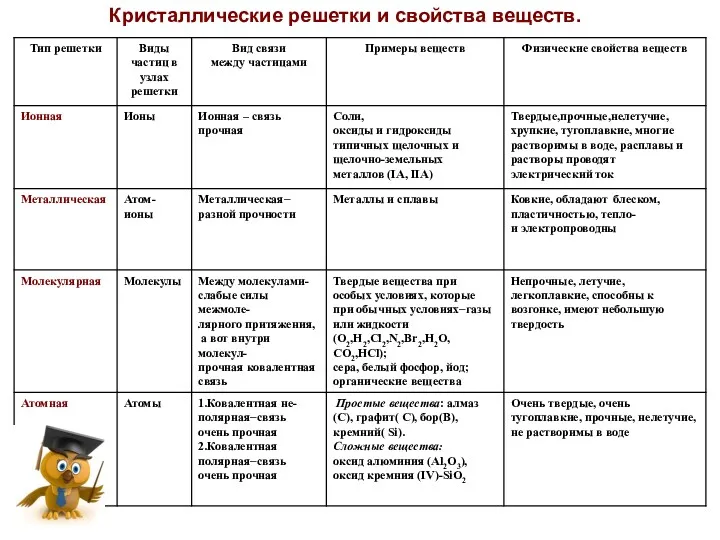
- 12. Кристаллические решетки и свойства веществ.
- 13. Отчего зависят свойства вещества? Строение атома Электроотрицательность Вид химической связи Тип кристаллической решетки Свойства веществ
- 14. Вывод: Свойства веществ в твердом состоянии зависят от типа кристаллической решетки (прежде всего от того, какие
- 15. Определите тип кристаллической решетки Вольфрам (W)– самый тугоплавкий металл Хлорид железа (FeCl3)– соль, раствор которой проводит
- 16. тип кристаллической решетки Вольфрам (W)– металлическая Хлорид железа (FeCl3)– ионная Йод (I2) – молекулярная Натрий (Na)
- 18. Скачать презентацию







 Подгруппа серы и ее соединения
Подгруппа серы и ее соединения Поверхностные явления. Типы поверхностных явлений
Поверхностные явления. Типы поверхностных явлений Химия: основные понятия. Периодическая система химических элементов Д. И. Менделеева
Химия: основные понятия. Периодическая система химических элементов Д. И. Менделеева Общая характеристика неметаллов
Общая характеристика неметаллов Устранение жёсткости воды на промышленных предприятиях
Устранение жёсткости воды на промышленных предприятиях Общие сведения об электрорадиоматериалах
Общие сведения об электрорадиоматериалах Вода – основа жизни на Земле
Вода – основа жизни на Земле Формування поняття про окисно-відновні реакції в процес і вивчення шкільного курсу хімії
Формування поняття про окисно-відновні реакції в процес і вивчення шкільного курсу хімії Азот
Азот Анри Ле Шателье. 1850-1963. Принцип Ле Шателье в химии
Анри Ле Шателье. 1850-1963. Принцип Ле Шателье в химии Соли. Названия солей
Соли. Названия солей Пиролиз углеводородов
Пиролиз углеводородов Минерал чароит. Месторождения
Минерал чароит. Месторождения Магний (Mg)
Магний (Mg) Жоғары молекулалық қосылыстар химиясы
Жоғары молекулалық қосылыстар химиясы Углеводы (сахариды)
Углеводы (сахариды) α-Аминокислоты. Белки
α-Аминокислоты. Белки Окислительно-восстановительные реакции. Подготовка к К/Р. 9 класс
Окислительно-восстановительные реакции. Подготовка к К/Р. 9 класс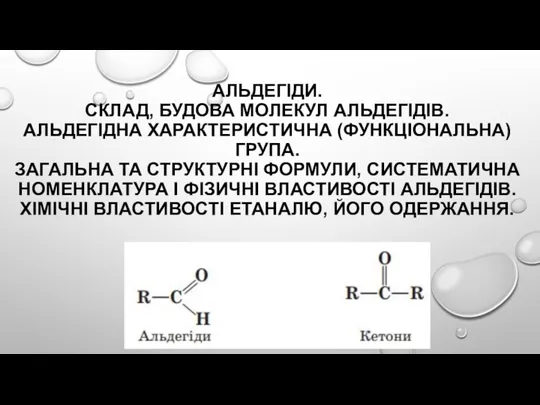 Альдегіди. Склад, будова молекул альдегідів. Альдегідна характеристична (функціональна) група
Альдегіди. Склад, будова молекул альдегідів. Альдегідна характеристична (функціональна) група Le trasformazioni fisiche della materia. Tema 3
Le trasformazioni fisiche della materia. Tema 3 Углеводороды. Применение природных источников углеводородов и продуктов их переработки
Углеводороды. Применение природных источников углеводородов и продуктов их переработки Химическая кинетика. Раздел 2
Химическая кинетика. Раздел 2 Химические свойства солей
Химические свойства солей Органикалық заттардың ерекшелігі
Органикалық заттардың ерекшелігі Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Соединения водорода
Соединения водорода Кристаллохимия негіздері
Кристаллохимия негіздері Кинетика химических реакций. Химическое равновесие. (Лекция 5)
Кинетика химических реакций. Химическое равновесие. (Лекция 5)