Содержание
- 2. R-СН2-СН2-СН-СООН
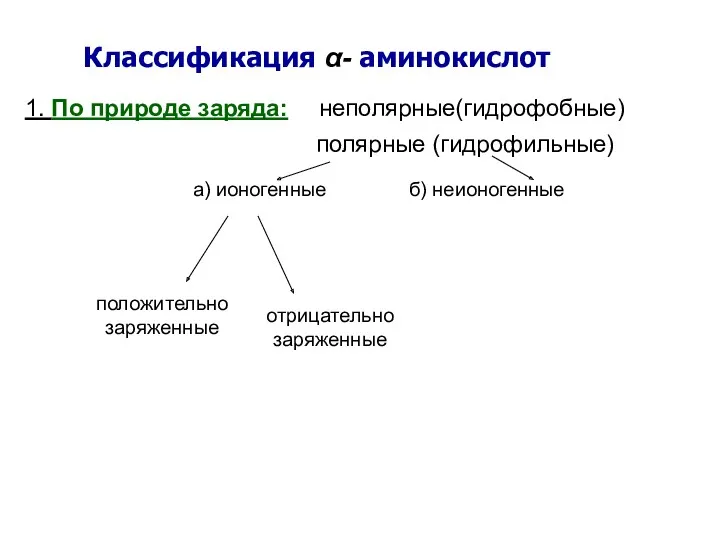
- 4. 1. По природе заряда: неполярные(гидрофобные) полярные (гидрофильные) а) ионогенные б) неионогенные Классификация α- аминокислот положительно заряженные
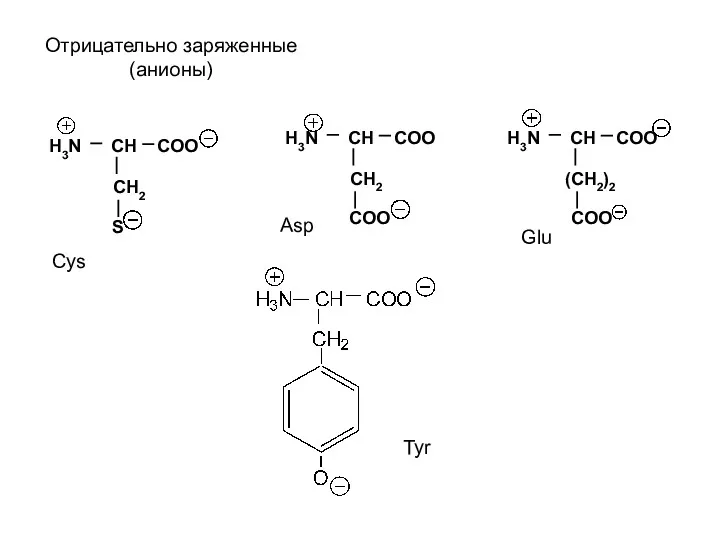
- 5. H3N CH COO CH2 S H3N CH COO CH2 COO H3N CH COO (CH2)2 COO Отрицательно
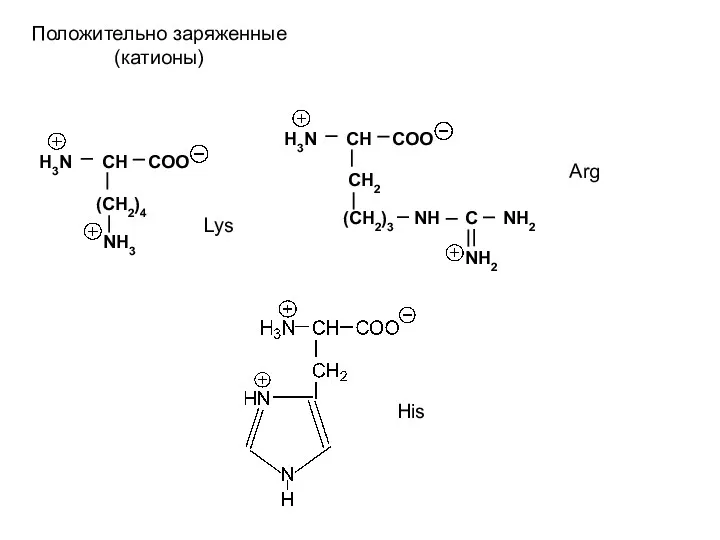
- 6. H3N CH COO (CH2)4 NH3 H3N CH COO CH2 (CH2)3 NH C NH2 NH2 Положительно заряженные
- 7. 2. Природа радикала: ароматические (Phe, Tyr) гетероциклические (Trp, His, Pro) алифатические (Ala, Lys, Asn) 3. Медико-биологическое
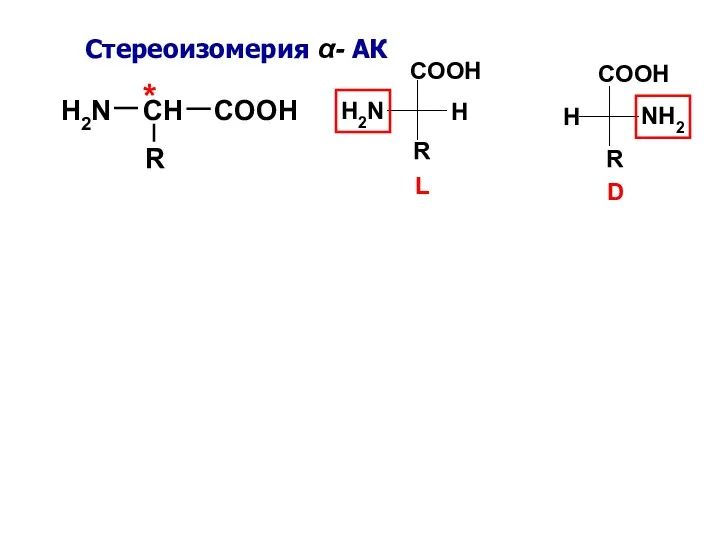
- 8. H2N CH COOH R * COOH COOH R R H2N NH2 H H L D Стереоизомерия
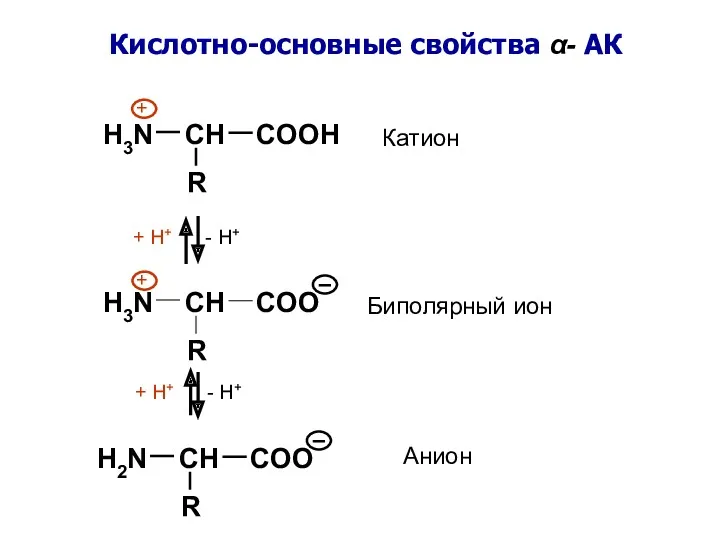
- 9. H3N CH COO R H3N CH COOH R H2N CH COO R Биполярный ион Катион Анион
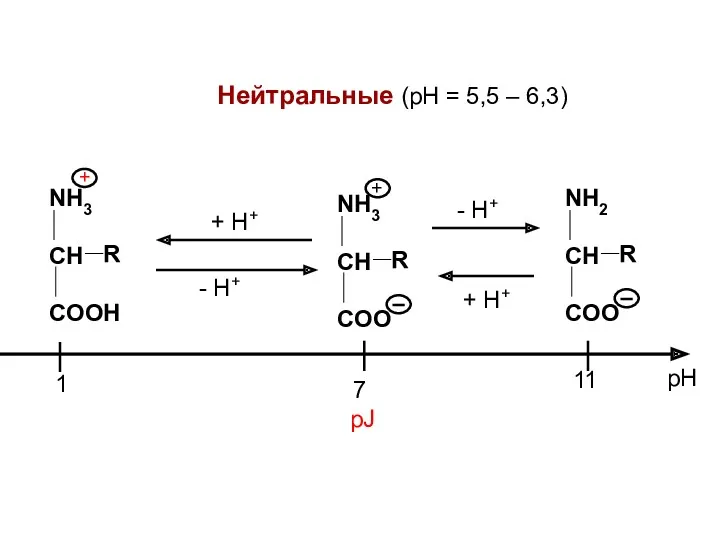
- 10. Нейтральные (рН = 5,5 – 6,3) NH2 CH COO R NH3 CH COO R NH3 CH
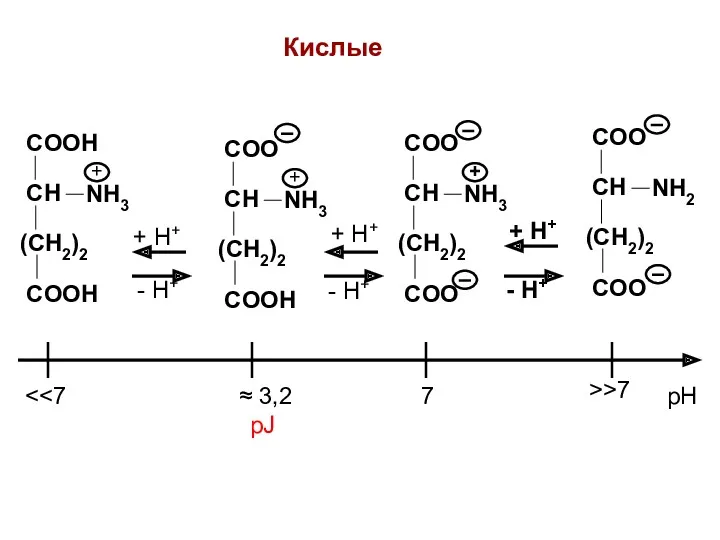
- 11. COOH CH (CH2)2 COOH NH3 + COO CH (CH2)2 COOH NH3 + COO CH (CH2)2 COO
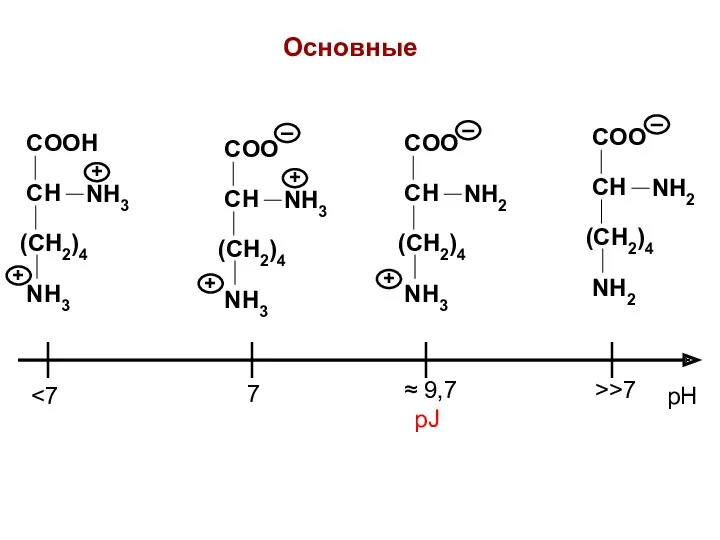
- 12. NH3 + COO CH (CH2)4 NH3 NH3 + COO CH (CH2)4 NH3 NH2 COO CH (CH2)4
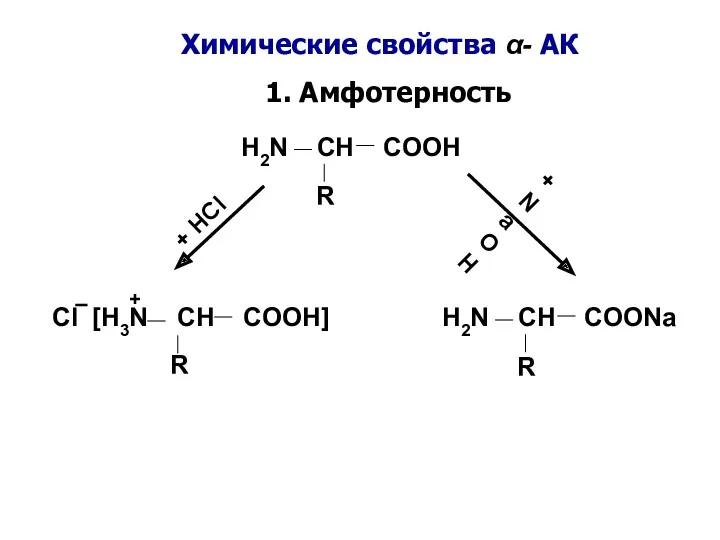
- 13. 1. Амфотерность H2N CH COOH R + HCl + NaOH Cl [H3N CH COOH] R H2N
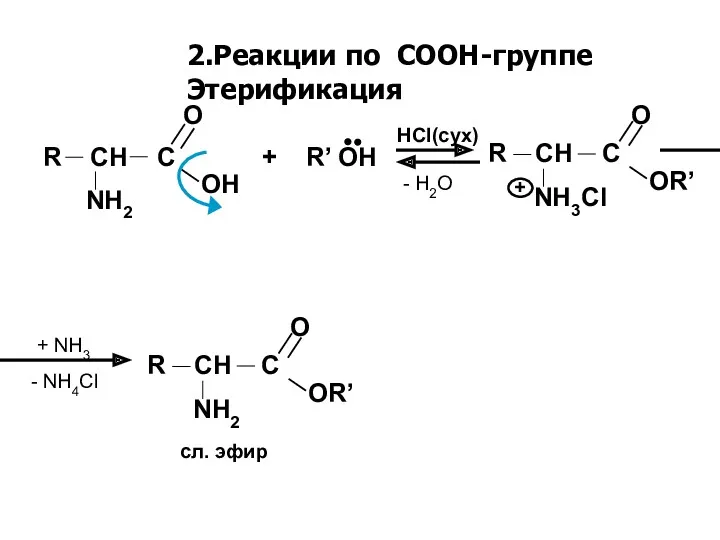
- 14. 2.Реакции по СООН-группе Этерификация R CH C + R’ OH NH2 OH O NH3Cl OR’ R
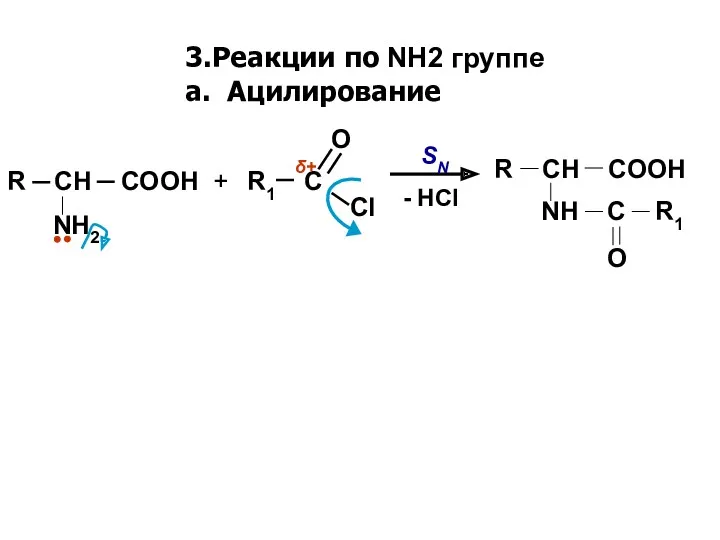
- 15. 3.Реакции по NH2 группе а. Ацилирование Cl R1 C O NH2 R CH COOH + SN
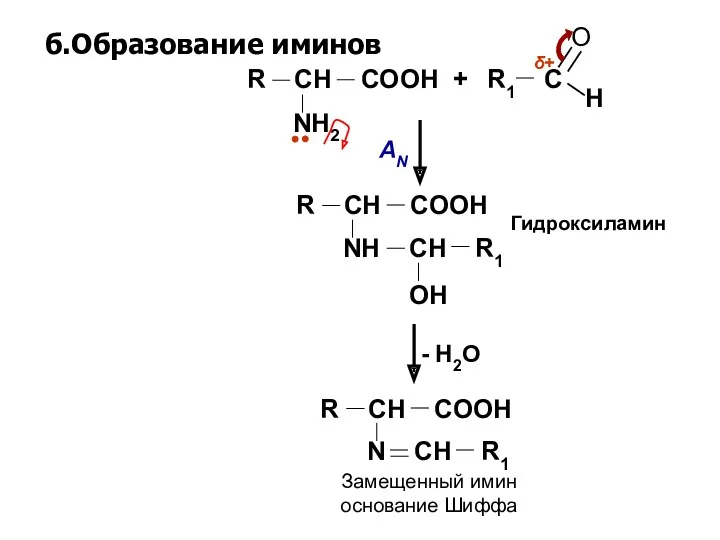
- 16. б.Образование иминов H R1 C NH2 R CH COOH + O AN - H2O N CH
- 17. Биологически важные реакции АК
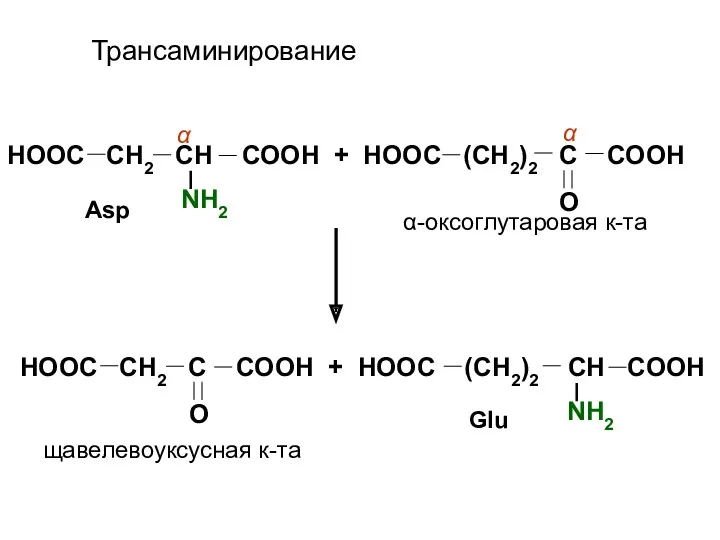
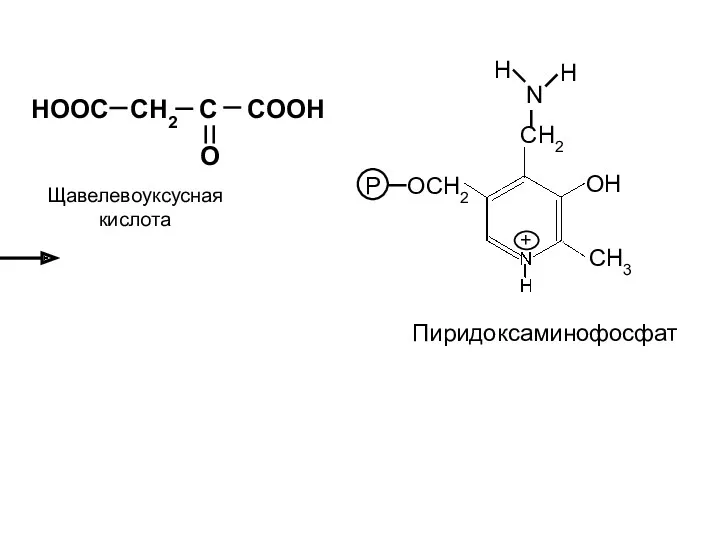
- 18. Трансаминирование HOOC CH2 CH COOH + HOOC (CH2)2 C COOH NH2 O HOOC CH2 C COOH
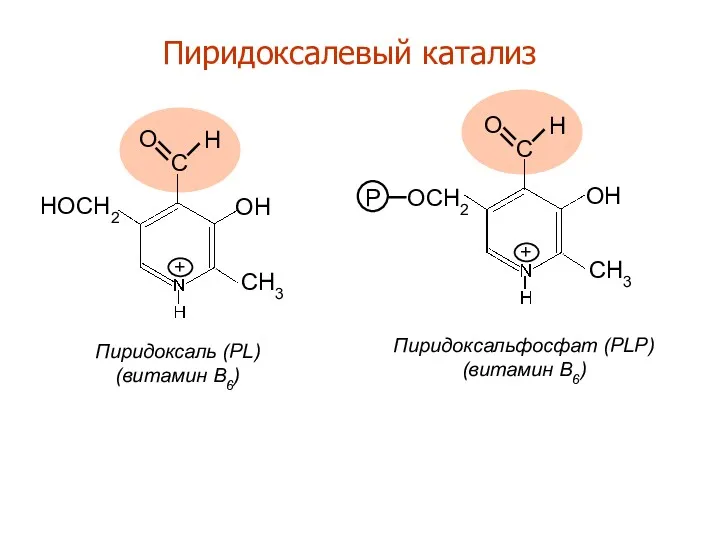
- 19. OH OH CH3 CH3 HOCH2 P OCH2 C H O C H O + + Пиридоксалевый
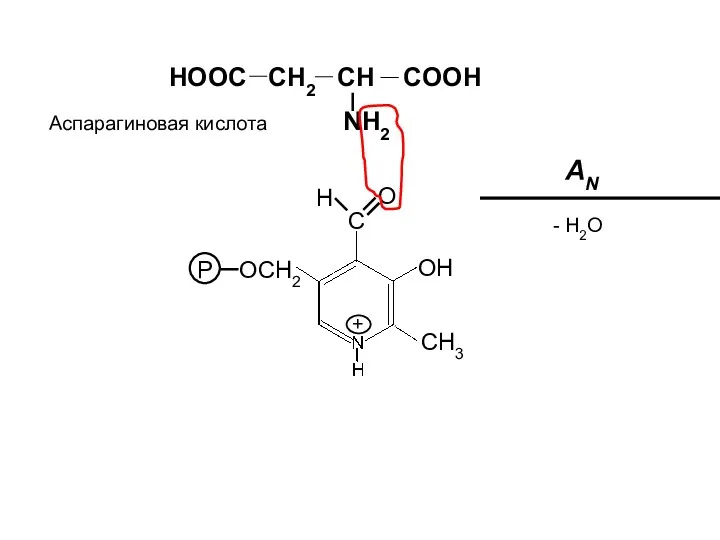
- 20. HOOC CH2 CH COOH NH2 OH CH3 P OCH2 C H O + AN - H2O
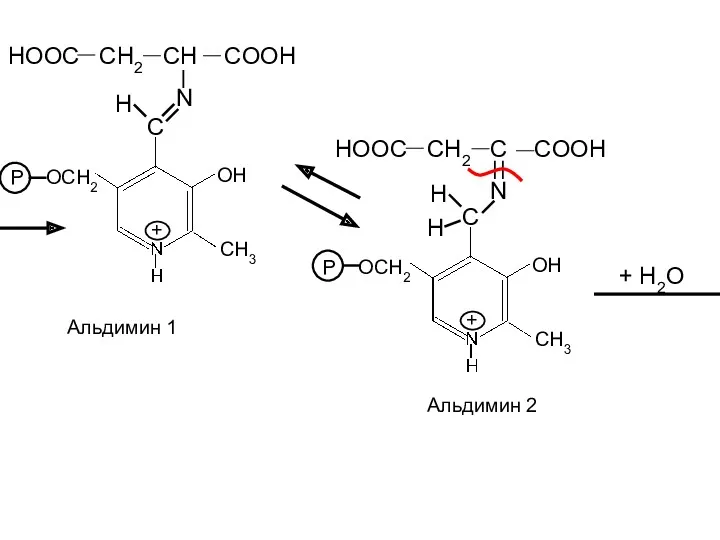
- 21. HOOC CH2 CH COOH N OH CH3 P OCH2 C H + HOOC CH2 C COOH
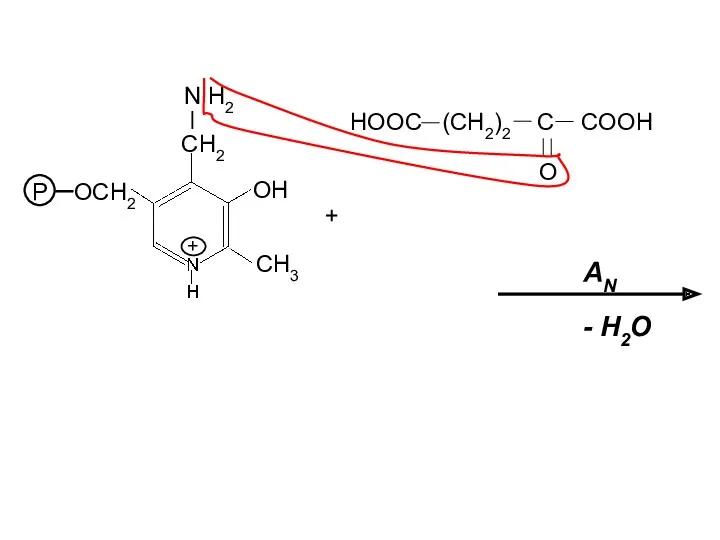
- 22. HOOC CH2 C COOH O OH CH3 P OCH2 CH2 H H + Щавелевоуксусная кислота Пиридоксаминофосфат
- 23. OH CH3 P OCH2 CH2 + N H2 HOOC (CH2)2 C COOH O AN - H2O
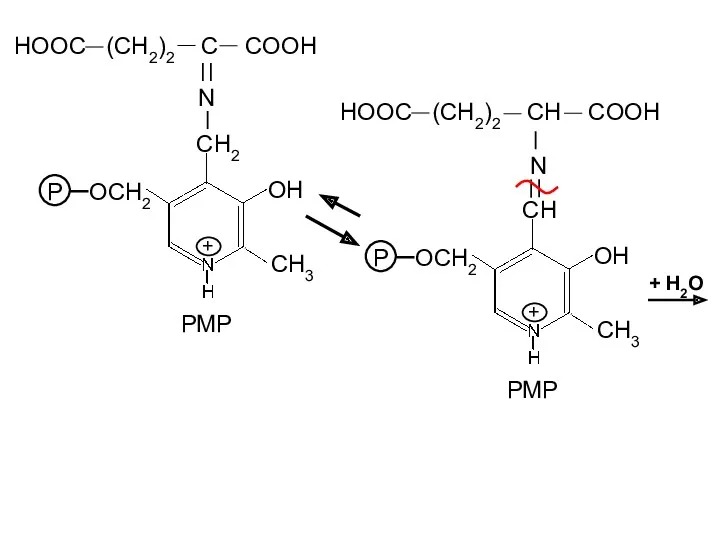
- 24. OH CH3 P OCH2 CH2 + РМР N HOOC (CH2)2 C COOH OH CH3 P OCH2
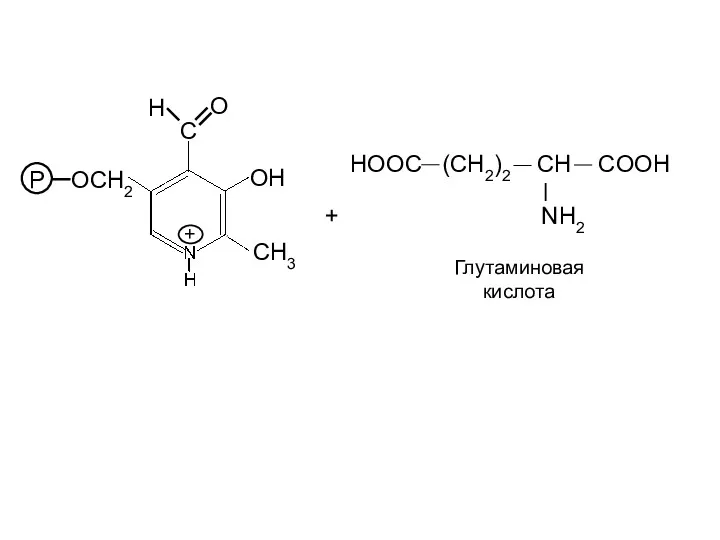
- 25. OH CH3 P OCH2 C H O + NH2 HOOC (CH2)2 CH COOH Глутаминовая кислота +
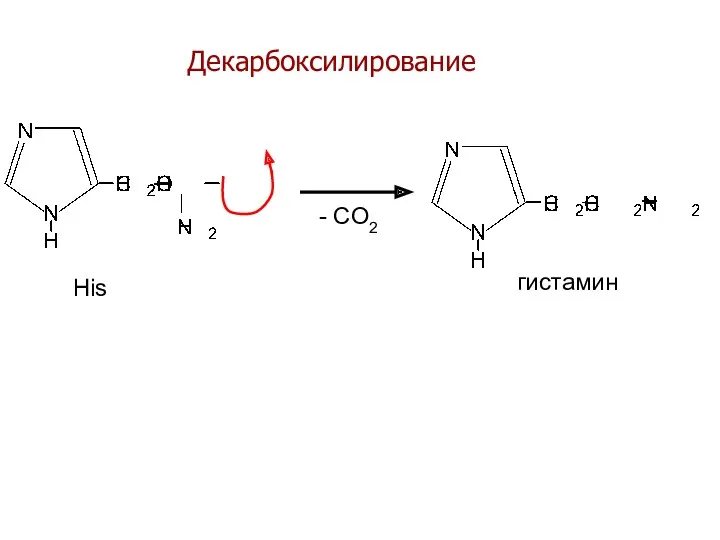
- 26. Декарбоксилирование - CO2 His гистамин
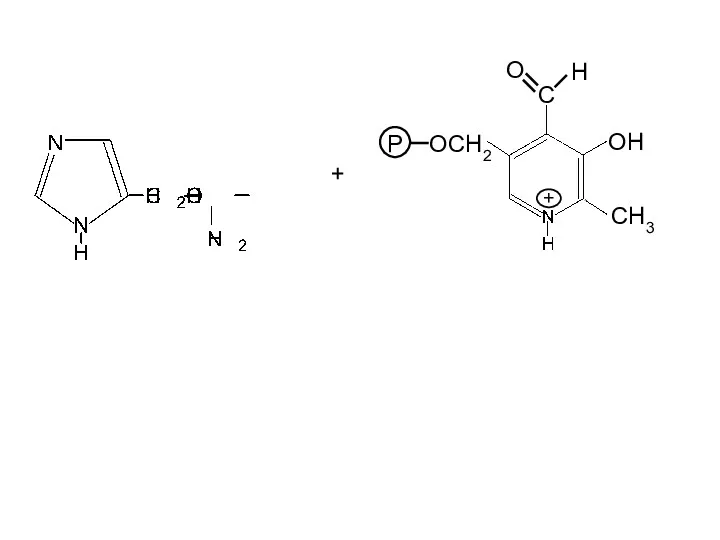
- 27. OH CH3 P OCH2 C H O + +
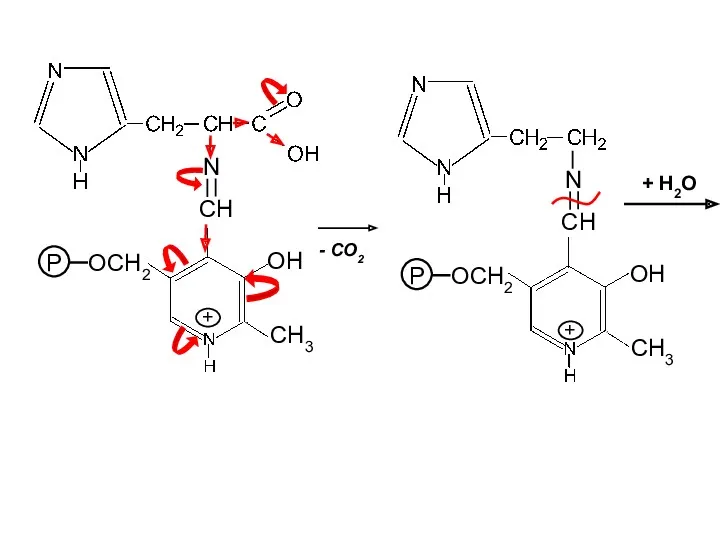
- 28. OH CH3 P OCH2 + CH N - CO2 OH P OCH2 + CH N CH3
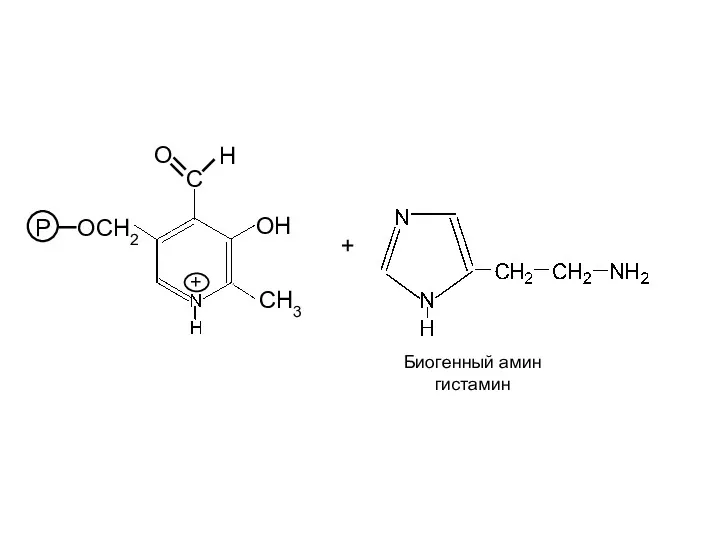
- 29. OH CH3 P OCH2 C H O + + Биогенный амин гистамин
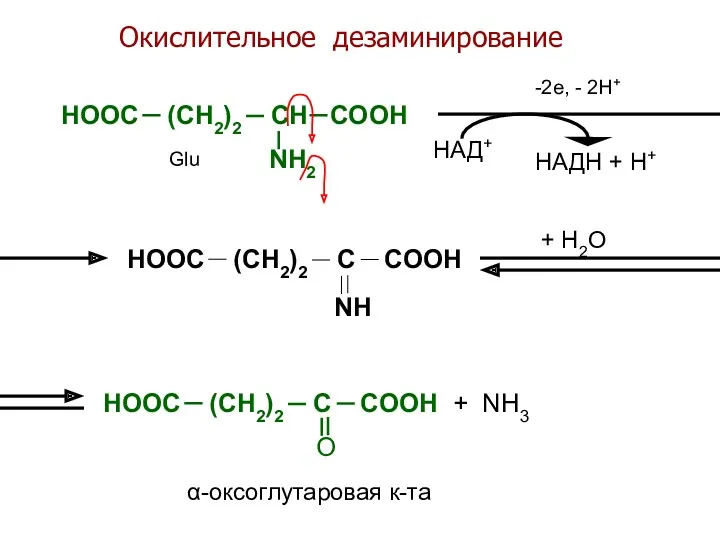
- 30. Окислительное дезаминирование HOOC (CH2)2 CH COOH NH2 HOOC (CH2)2 C COOH NH HOOC (CH2)2 C COOH
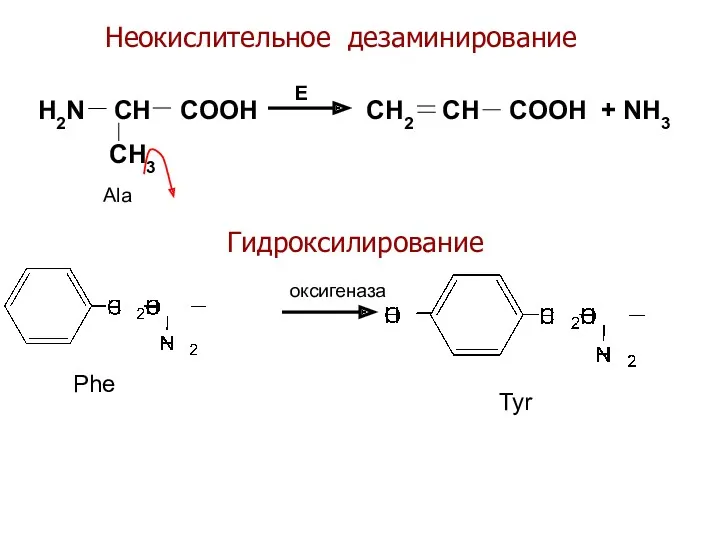
- 31. CH3 H2N CH COOH CH2 CH COOH + NH3 E Ala Phe Tyr оксигеназа Неокислительное дезаминирование
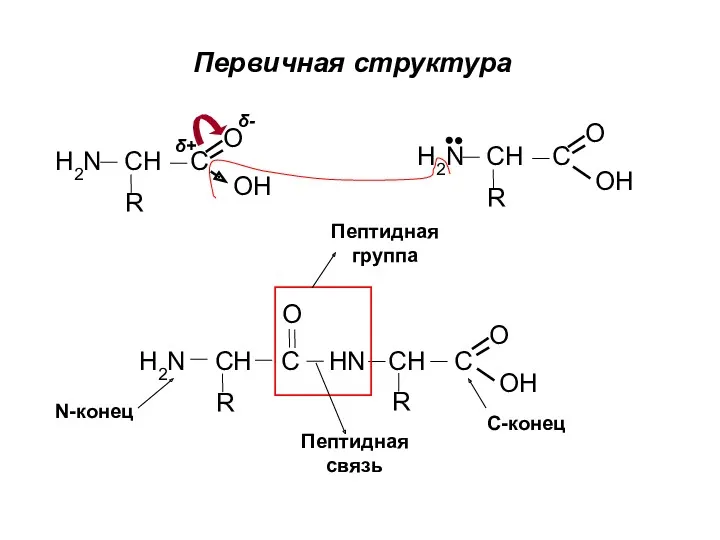
- 32. Первичная структура H2N CH C OH O R H2N CH C OH O R δ+ δ-
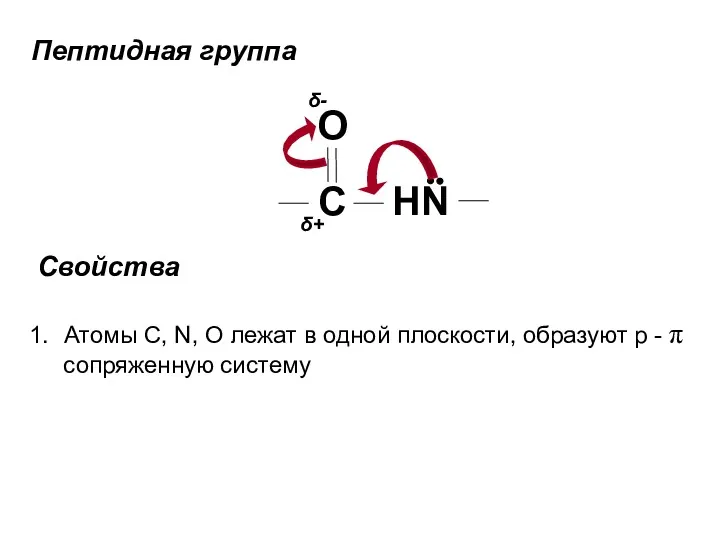
- 33. Пептидная группа C HN O δ- δ+ Свойства Атомы C, N, O лежат в одной плоскости,
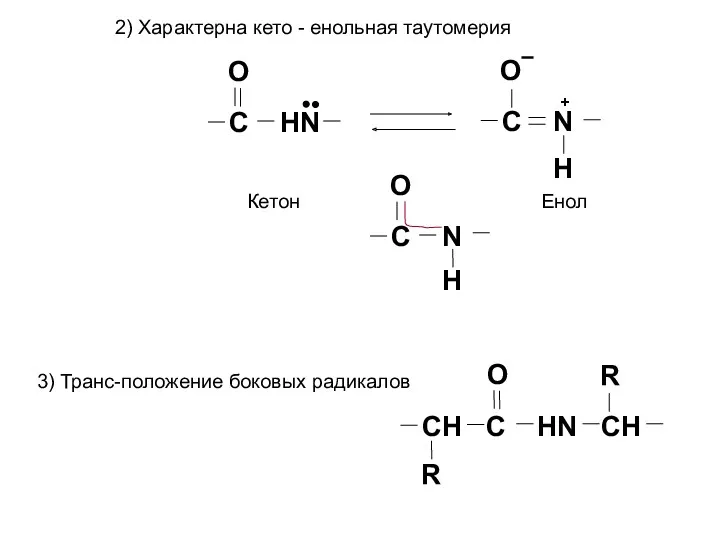
- 34. C HN O C N O Н + C N O Н CH C HN CH
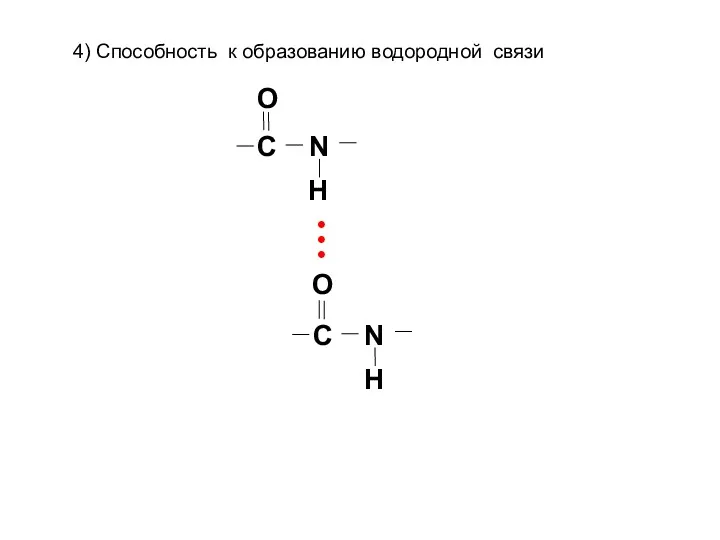
- 35. C N O Н C N O Н • • • 4) Способность к образованию водородной
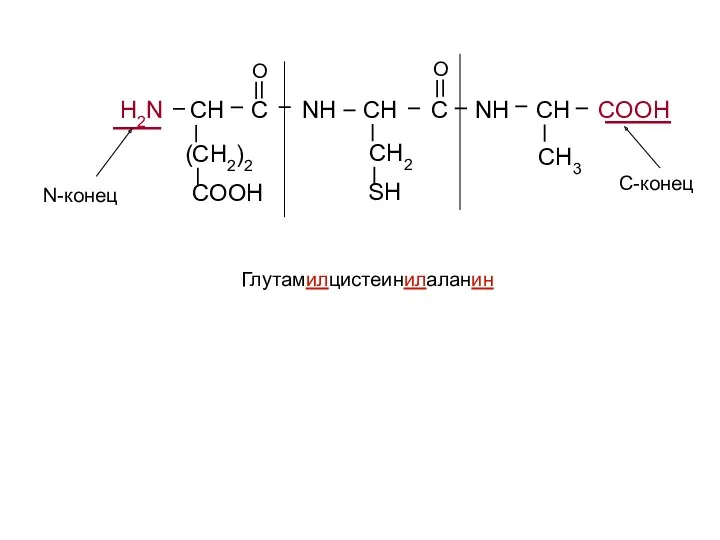
- 36. H2N CH C NH CH C NH CH COOH (CH2)2 COOH CH2 SH CH3 O O
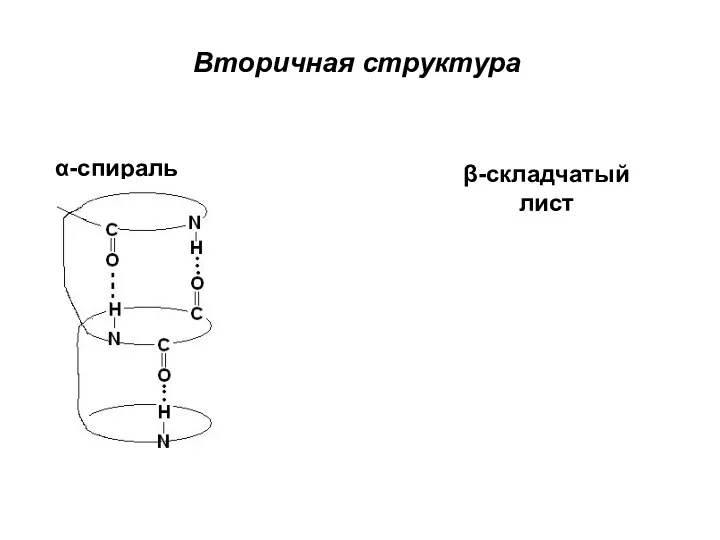
- 37. Вторичная структура α-спираль β-складчатый лист
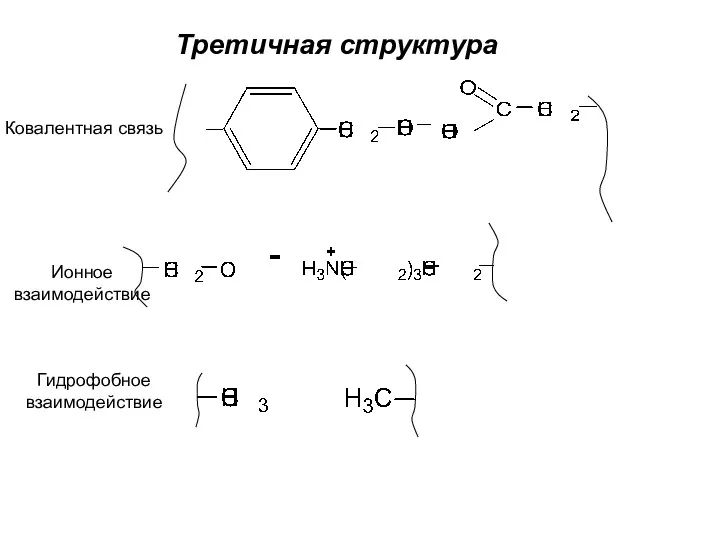
- 38. Третичная структура Ковалентная связь Ионное взаимодействие Гидрофобное взаимодействие
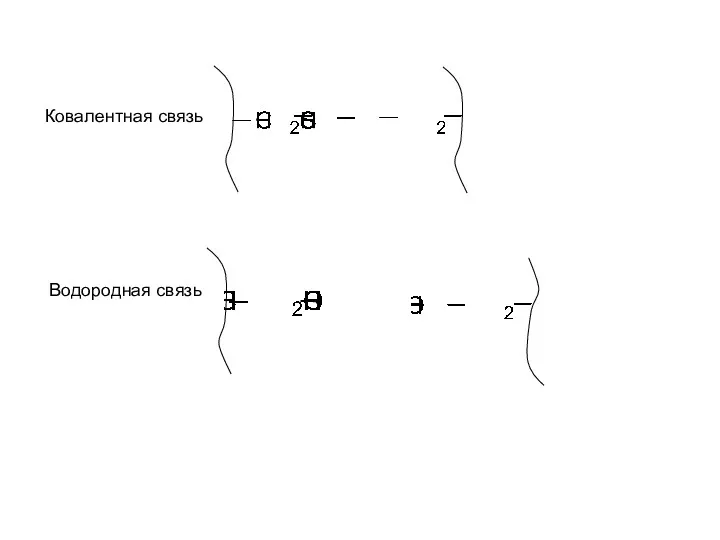
- 39. Ковалентная связь Водородная связь
- 40. Качественные реакции на α-АК, пептиды и белки Универсальные 1 на α-аминокислоты с нингидрином 2. на пептидную
- 41. 1. Ксантопротеиновая + HNO3 + NaOH Специфические
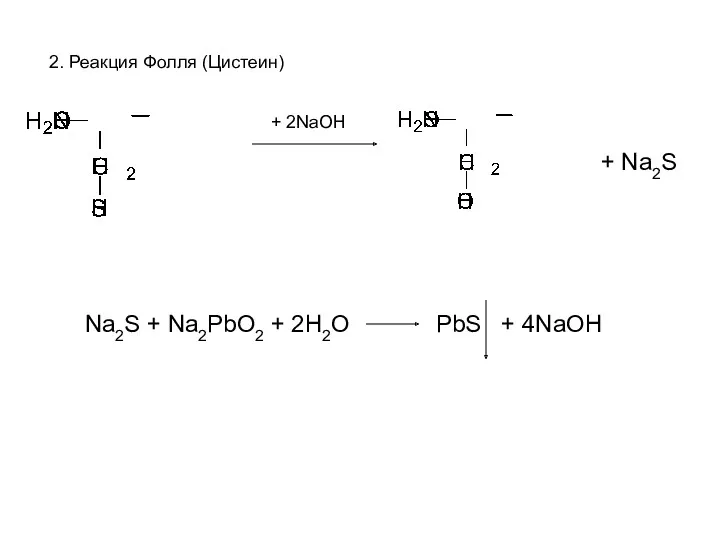
- 42. 2. Реакция Фолля (Цистеин) + 2NaOH + Na2S Na2S + Na2PbO2 + 2H2O PbS + 4NaOH
- 44. Скачать презентацию






 Окислительно- восстановительные реакции
Окислительно- восстановительные реакции Валентність хімічних елементів
Валентність хімічних елементів Алкены. Ненасыщенные углеводороды, непредельные углеводороды, этиленовые углеводороды. Олефины (10 класс)
Алкены. Ненасыщенные углеводороды, непредельные углеводороды, этиленовые углеводороды. Олефины (10 класс) Адсорбция
Адсорбция Аммиак. Строение атома азота
Аммиак. Строение атома азота Строение и свойства циклоалканов
Строение и свойства циклоалканов Основная. Первоначальные представления об органических веществах
Основная. Первоначальные представления об органических веществах Поверхностно-активные вещества (ПАВ)
Поверхностно-активные вещества (ПАВ) Елементи VІ групи головної підгрупи
Елементи VІ групи головної підгрупи История открытия кислорода
История открытия кислорода Алкены (этиленовые углеводороды)
Алкены (этиленовые углеводороды) Химический состав нефти
Химический состав нефти Электронное строение элементов-органогенов. Типы химической связи
Электронное строение элементов-органогенов. Типы химической связи Валентность химических элементов
Валентность химических элементов Некоторые структурные особенности макромолекул
Некоторые структурные особенности макромолекул Цинк
Цинк Тотығу-тотықсыздану титрлеу әдісі
Тотығу-тотықсыздану титрлеу әдісі Арены
Арены Наноматериалы. Свойства наноматериалов. Особенности свойств
Наноматериалы. Свойства наноматериалов. Особенности свойств 20230419_eds
20230419_eds Виділення з суміші речовин. Прості речовини
Виділення з суміші речовин. Прості речовини Кислотно-основные свойства органических соединений. (Лекция 3)
Кислотно-основные свойства органических соединений. (Лекция 3) Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона
Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона Спекание порошковых систем
Спекание порошковых систем Решение задач. Органическая химия
Решение задач. Органическая химия Рекомендации по использованию пластмасс в быту. Опасные типы пластмасс
Рекомендации по использованию пластмасс в быту. Опасные типы пластмасс Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Электроотрицательность химических элементов
Электроотрицательность химических элементов