Содержание
- 2. Ароматические соединения, или арены, — большая группа соединений карбоциклического ряда, молекулы которых содержат устойчивую циклическую группировку
- 3. Фридрих Август Кекуле 7.09. 1829 г.–13.07. 1896 г. Первую наиболее удачную структурную формулу строения бензола предложил
- 5. Атомы углерода в бензоле замкнуты в цикл, в котором соблюдается валентность углерода (IV) и двойные связи
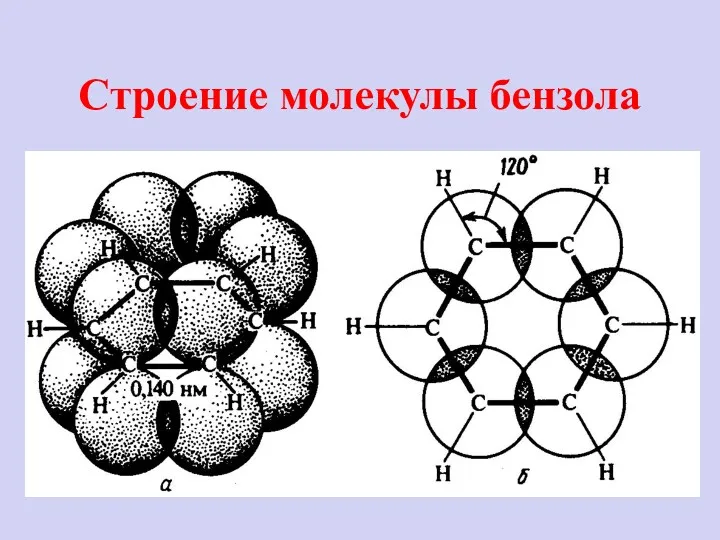
- 6. Строение молекулы бензола
- 7. Строение молекулы бензола Совокупность свойств бензола называется ароматичностью.
- 8. С6Н6 Номенклатура и изомерия Бензол
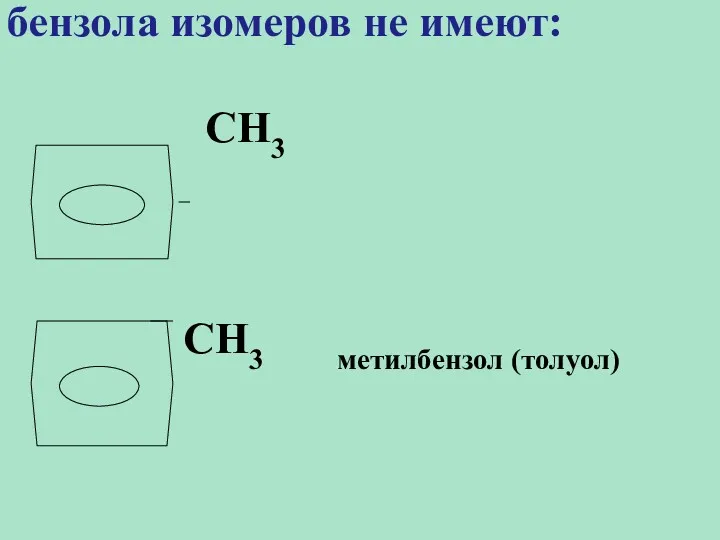
- 9. 1. Монозамещенные производные бензола изомеров не имеют: СН3 СН3 метилбензол (толуол)
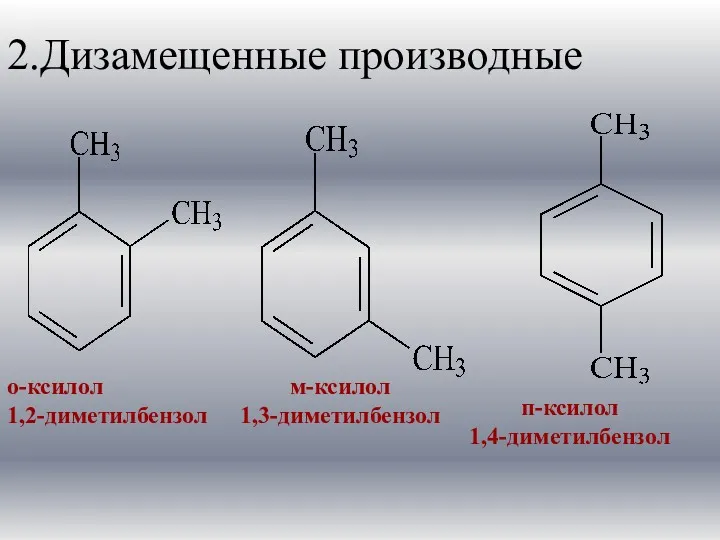
- 10. 2.Дизамещенные производные о-ксилол 1,2-диметилбензол м-ксилол 1,3-диметилбензол п-ксилол 1,4-диметилбензол
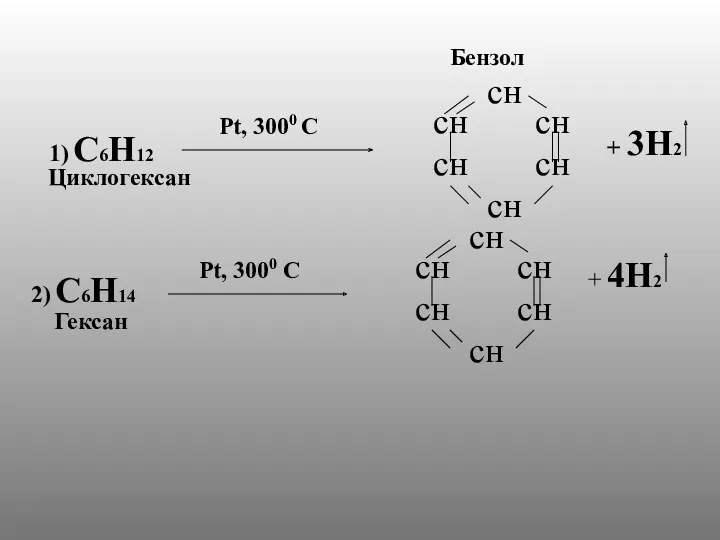
- 11. Получение 1) . Бензол образуется из циклогексана 2) . Бензол образуется из гексана 3) .Бензол образуется
- 12. Бензол Циклогексан Гексан
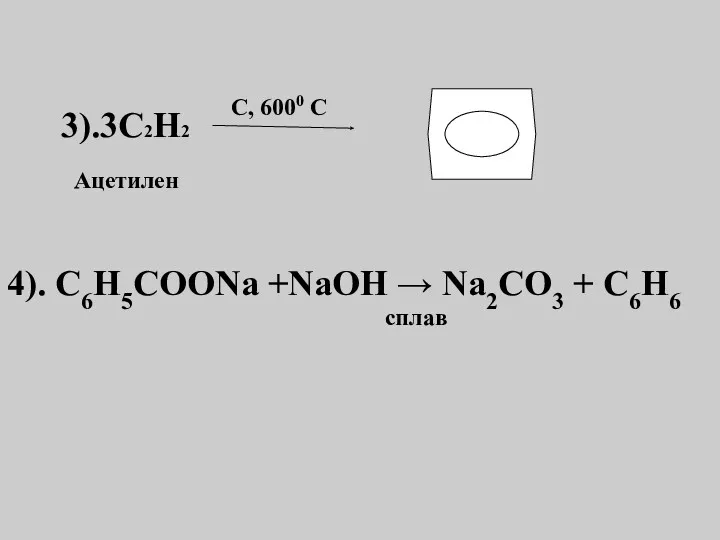
- 13. 3).3С2Н2 C, 6000 C Ацетилен 4). С6Н5СООNа +NаОН → Nа2СО3 + С6Н6 сплав
- 14. Физические свойства Агрегатное состояние Температура плавления Температура кипения ЖИДКОСТЬ 5,50С (ПОВЫШАЕТСЯ С УВЕЛИЧЕНИЕМ относительных молекулярных МАСС)
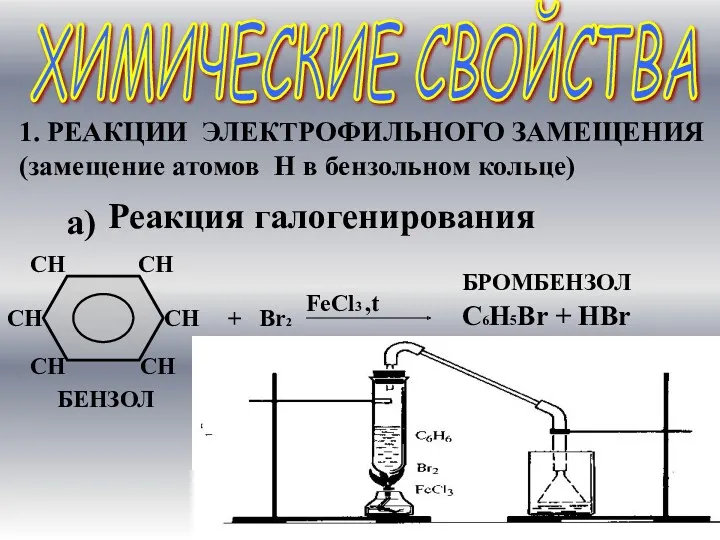
- 15. ХИМИЧЕСКИЕ СВОЙСТВА 1. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ (замещение атомов Н в бензольном кольце) а) Реакция галогенирования +
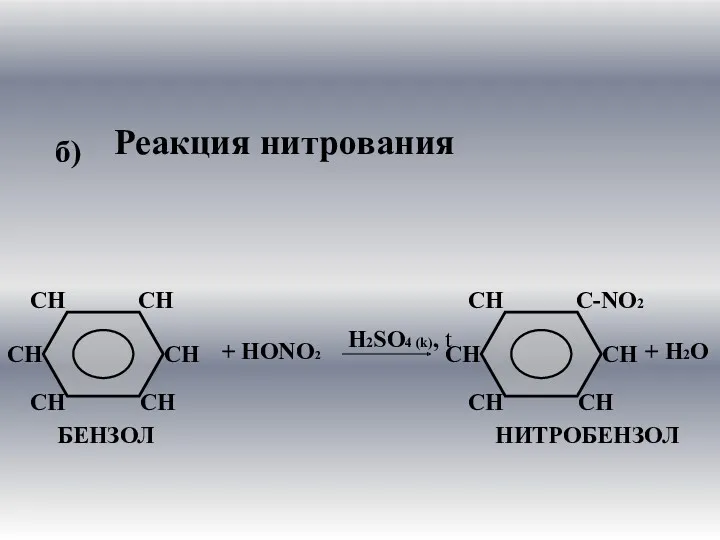
- 16. б) Реакция нитрования + НОNО2 + Н2О H2SO4 (k), t
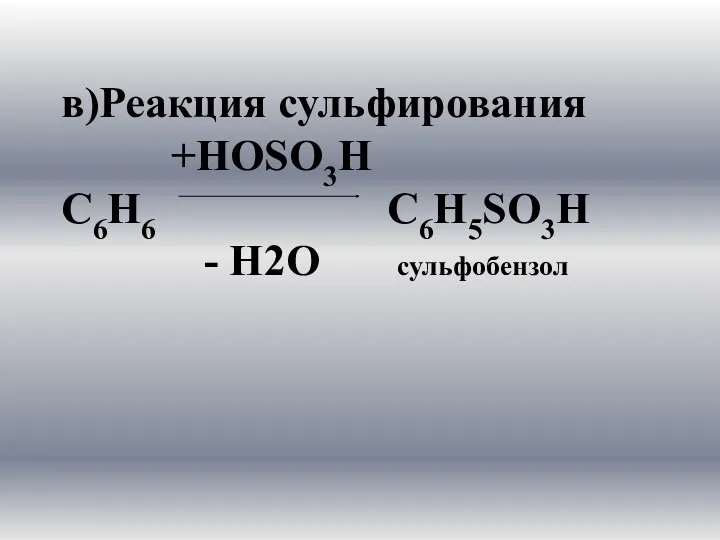
- 17. в)Реакция сульфирования +НОSО3Н С6Н6 С6Н5SО3Н - Н2О сульфобензол
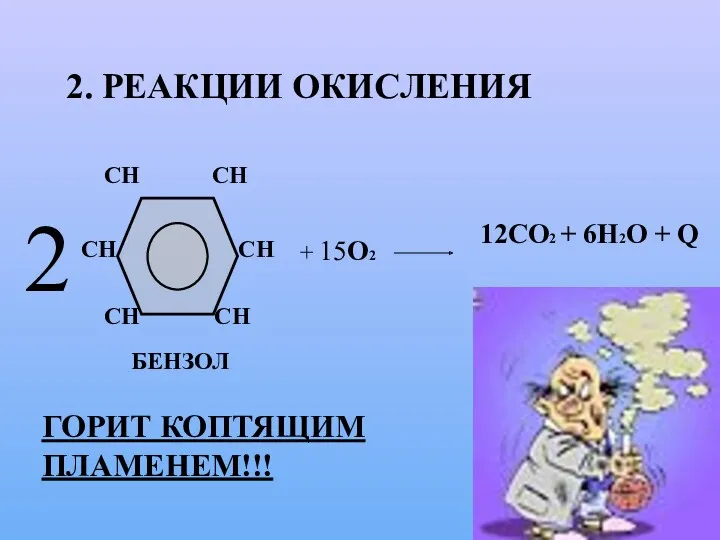
- 18. 2. РЕАКЦИИ ОКИСЛЕНИЯ 2 + 15О2 12СО2 + 6Н2О + Q ГОРИТ КОПТЯЩИМ ПЛАМЕНЕМ!!!
- 19. [О] [О]= КМnО4 + Н2SО4 СН3 СООН Толуол Бензойная кислота Реакция окисления гомологов бензола
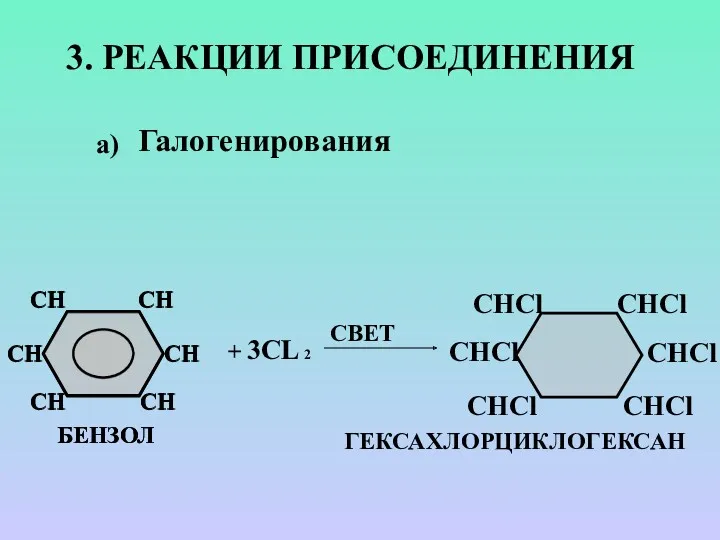
- 20. 3. РЕАКЦИИ ПРИСОЕДИНЕНИЯ + 3CL 2 СВЕТ ГЕКСАХЛОРЦИКЛОГЕКСАН а) Галогенирования
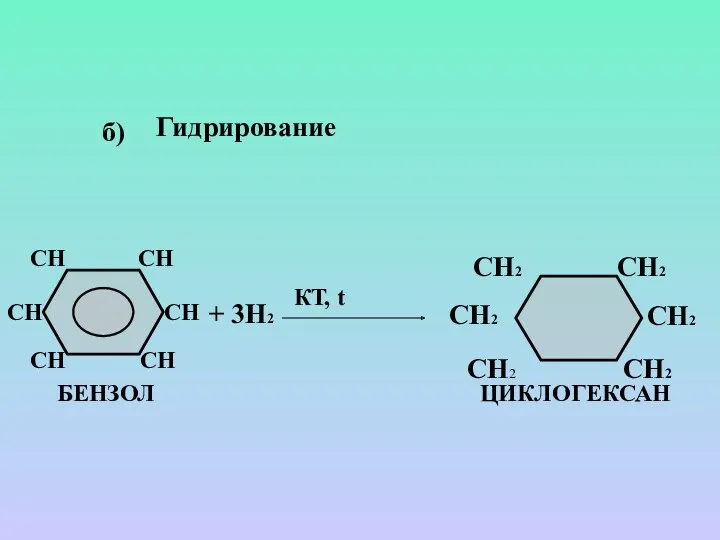
- 21. б) Гидрирование + 3Н2 КТ, t ЦИКЛОГЕКСАН
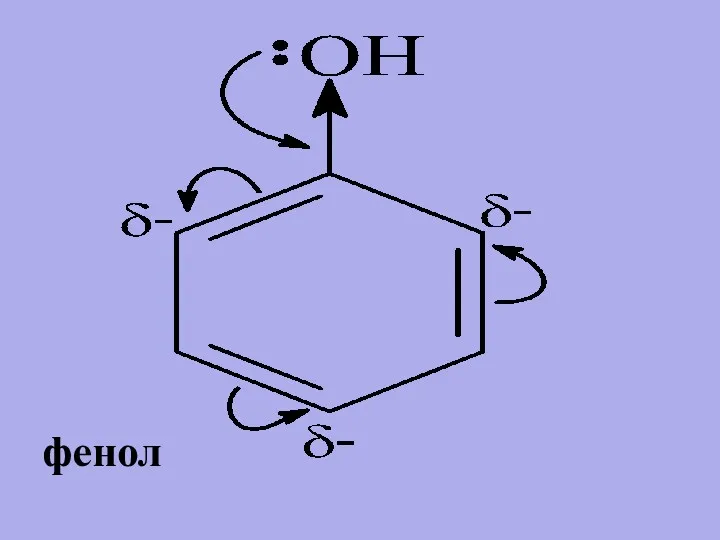
- 22. Эффекты заместителей при электрофильном замещении Реакции электрофильного замещения для гомологов бензола 1. Заместители (ориентанты) первого рода:
- 23. фенол
- 24. 2. Заместители (ориентанты) второго рода: —CN, —СООН, —SO3H, —СНО, —COR, —COOR, —NO2. Эти заместители смещают электронную
- 25. нитробензол
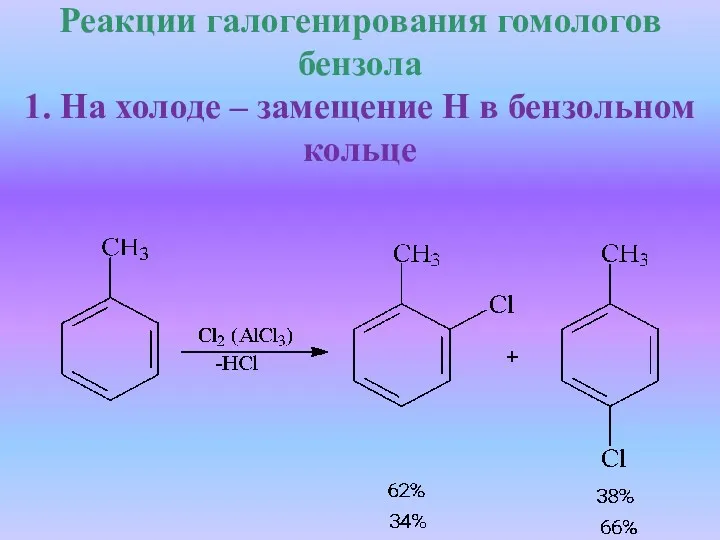
- 26. Реакции галогенирования гомологов бензола 1. На холоде – замещение Н в бензольном кольце
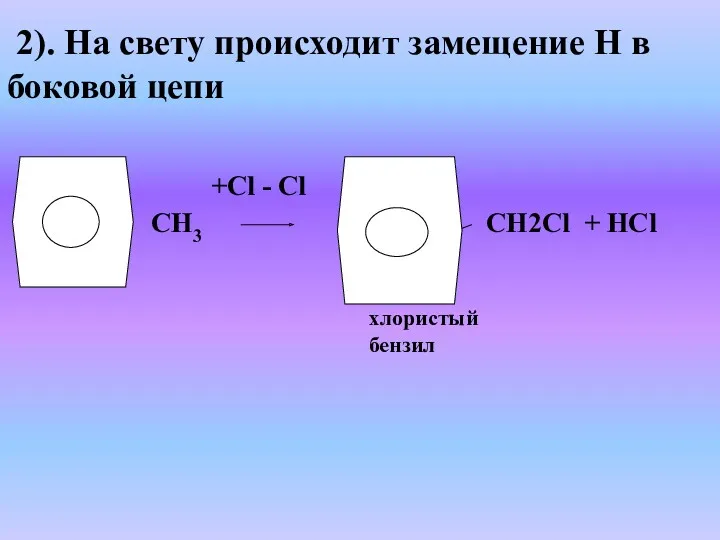
- 27. 2). На свету происходит замещение Н в боковой цепи хлористый бензил СН3 +Сl - Сl СН2Сl
- 28. Многоядерные арены Нафталин - бесцветное кр.вещество, tплавл. = 800 С
- 29. Антрацен – белое кр. вещество tплавл. = 2170С имеет ряд производных являющихся слабительными средствами
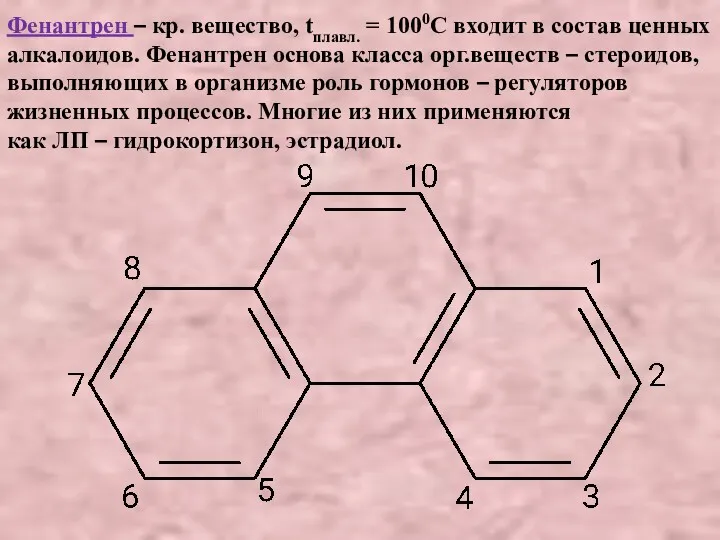
- 30. Фенантрен – кр. вещество, tплавл. = 1000С входит в состав ценных алкалоидов. Фенантрен основа класса орг.веществ
- 32. Скачать презентацию








![[О] [О]= КМnО4 + Н2SО4 СН3 СООН Толуол Бензойная кислота Реакция окисления гомологов бензола](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/191025/slide-18.jpg)





 Алкадиены, нафтены
Алкадиены, нафтены Аминокислоты
Аминокислоты Биологически важные пяти- и шестичленные гетероциклы с одним и двумя гетероатомами
Биологически важные пяти- и шестичленные гетероциклы с одним и двумя гетероатомами Серная кислота
Серная кислота Фізичні та хімічні властивості кислот (урок хімії у 8 класі)
Фізичні та хімічні властивості кислот (урок хімії у 8 класі) Типы химических реакций , признаки и условия их протекания
Типы химических реакций , признаки и условия их протекания Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Азот
Азот Хімічні властивості кислот
Хімічні властивості кислот Поширення солей у природі
Поширення солей у природі Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия ПЛАСТИК НОВЫЙ
ПЛАСТИК НОВЫЙ Stirring in liquid media
Stirring in liquid media Литий
Литий Липиды (Жиры)
Липиды (Жиры) В чём соль соли
В чём соль соли Классификация химических реакций по различным основаниям. 9 класс
Классификация химических реакций по различным основаниям. 9 класс Технологии получения полимерных нанокомпозитов
Технологии получения полимерных нанокомпозитов Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Правила роботи на уроці
Правила роботи на уроці Задачи на процентную концентрацию
Задачи на процентную концентрацию Углероды. Строение и свойства атомов
Углероды. Строение и свойства атомов Спирт µндіру технологиясы
Спирт µндіру технологиясы Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Основная. Первоначальные представления об органических веществах
Основная. Первоначальные представления об органических веществах Химические свойства серной кислоты
Химические свойства серной кислоты Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Полистирол өндірісі
Полистирол өндірісі