Содержание
- 2. 1. Химический потенциал
- 3. 1. Химический потенциал
- 4. 1. Химический потенциал
- 5. 1. Химический потенциал
- 6. 1. Химический потенциал
- 7. 1. Химический потенциал Для идеального газа G = G0 + nRT ln (p/p0) Уравнение выражает изменение
- 8. 1. Химический потенциал Изменение химического потенциала характеризует способность 1 моля вещества производить работу (способность переходить из
- 9. 1. Химический потенциал Активность характеризует активную концентрацию газа μ = μ 0 + RT ln а,
- 10. 2. Фазовые равновесия. Основные понятия Основные формы, в которых существует вещество, называют агрегатными или фазовыми состояниями.
- 11. 2. Фазовые равновесия. Основные понятия Для любого вещества существует одна форма газообразного состояния и одна форма
- 12. 2. Фазовые равновесия. Основные понятия Фаза – гомогенная часть системы, которая на всём протяжении обладает одинаковыми
- 13. 2. Фазовые равновесия. Основные понятия Наименьшее число компонентов системы, через которое выражается состав любой фазы, называется
- 14. 2. Фазовые равновесия. Основные понятия Число независимых компонентов может совпадать и не совпадать с числом индивидуальных
- 15. 2. Фазовые равновесия. Основные понятия Пример. Химическая реакция В смеси трёх газов HI, I2 и H2
- 16. 2. Фазовые равновесия. Основные понятия Фазовый переход – переход какого-либо из компонентов системы из одной фазы
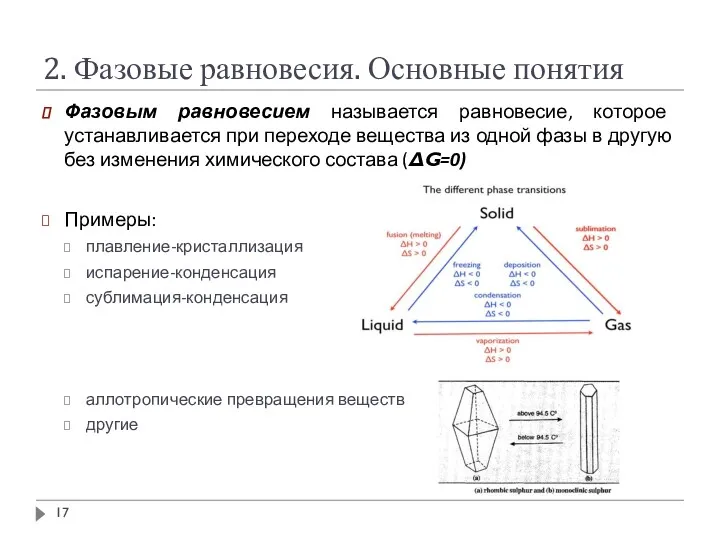
- 17. 2. Фазовые равновесия. Основные понятия Фазовым равновесием называется равновесие, которое устанавливается при переходе вещества из одной
- 18. 2. Фазовые равновесия. Основные понятия
- 19. 2. Фазовые равновесия. Основные понятия
- 20. 2. Фазовые равновесия. Основные понятия
- 21. 3. Правило фаз Гиббса Числом степеней свободы (или вариантностью) системы называют число параметров, которые можно независимо
- 22. 3. Правило фаз Гиббса Основной закон фазового равновесия Является применением второго закона термодинамики к изучению превращений
- 23. 3. Правило фаз Гиббса С = К - Ф + N Число внешних условий N, оказывающих
- 24. 3. Правило фаз Гиббса. Классификация систем по числу степеней свободы Безвариантные (нонвариантные) системы, число степеней свободы
- 25. 3. Правило фаз Гиббса. Классификация систем по числу степеней свободы
- 26. 4. Фазовые равновесия в однокомпонентных системах Примеры однокомпонентных систем: вода образует три фазы: водяной пар, жидкая
- 27. 4. Фазовые равновесия в однокомпонентных системах. Уравнение Клаузиуса-Клапейрона Даёт зависимость давления p фазового перехода от температуры
- 28. 4. Фазовые равновесия в однокомпонентных системах. Уравнение Клаузиуса-Клапейрона Фазовый переход твёрдое тело – жидкость Фазовый переход
- 29. 4. Фазовые равновесия в однокомпонентных системах. Энтропия испарения. Правило Трутона
- 30. 4. Фазовые равновесия в однокомпонентных системах. Энтропия испарения. Правило Трутона
- 31. 5. Диаграммы состояния однокомпонентных систем (фазовые диаграммы) Состояние однокомпонентной системы определяется двумя независимыми параметрами, например, давлением
- 32. 5. Диаграммы состояния однокомпонентных систем (фазовые диаграммы) Пространственные диаграммы сложны и неудобны в применении Используют плоские
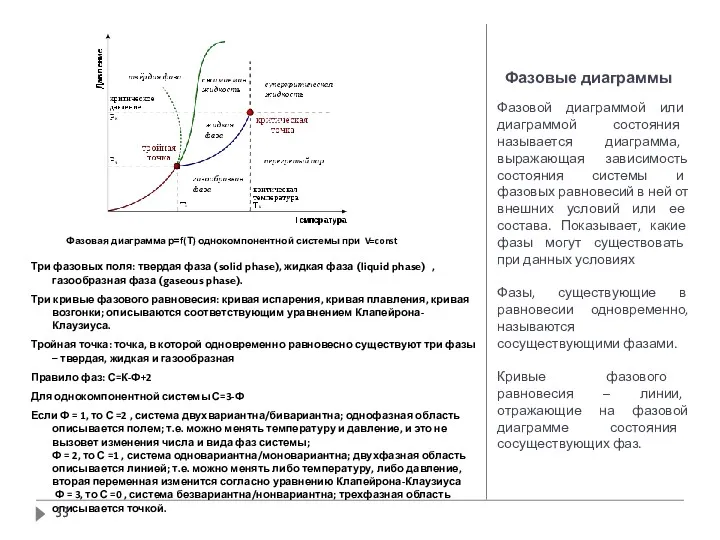
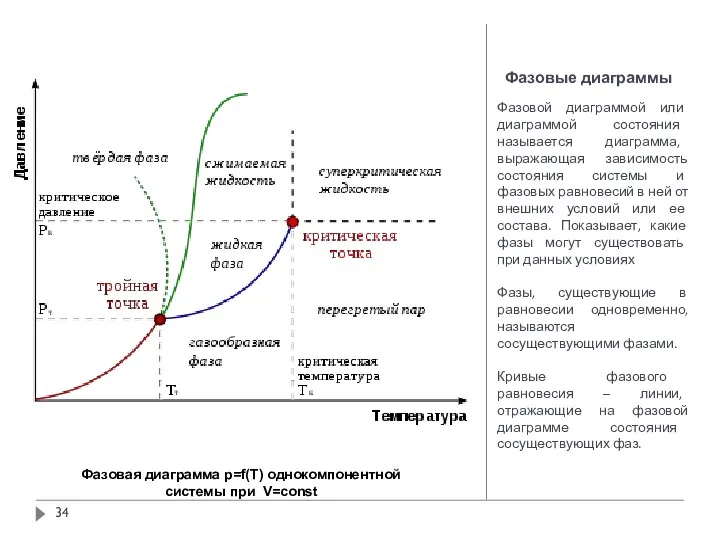
- 33. Фазовые диаграммы Фазовой диаграммой или диаграммой состояния называется диаграмма, выражающая зависимость состояния системы и фазовых равновесий
- 34. Фазовые диаграммы Фазовой диаграммой или диаграммой состояния называется диаграмма, выражающая зависимость состояния системы и фазовых равновесий
- 35. Для вещества с несколькими кристаллическими модификациями диаграмма состояния имеет более сложный характер На рисунке изображена диаграмма
- 36. Диаграмма состояния для каждого конкретного вещества строится на основе экспериментальных данных. Зная диаграмму состояния, можно предсказать,
- 37. 5.1 Фазовая диаграмма воды Диаграмма состояния воды при средних давлениях (до 1 МПа)
- 38. 5.1 Фазовая диаграмма воды
- 39. 5.1 Фазовая диаграмма воды
- 40. 5.1 Фазовая диаграмма воды
- 41. 5.1 Фазовая диаграмма воды
- 42. Диаграмма состояния воды при высоких давлениях
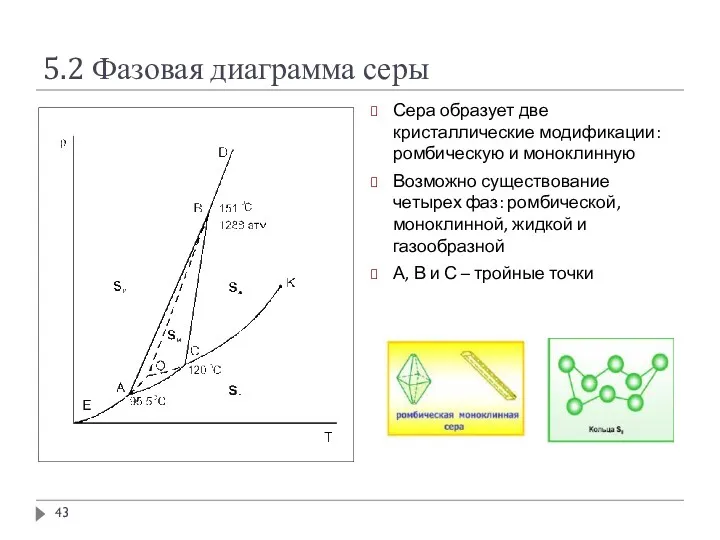
- 43. 5.2 Фазовая диаграмма серы Сера образует две кристаллические модификации: ромбическую и моноклинную Возможно существование четырех фаз:
- 44. 5.2 Фазовая диаграмма серы
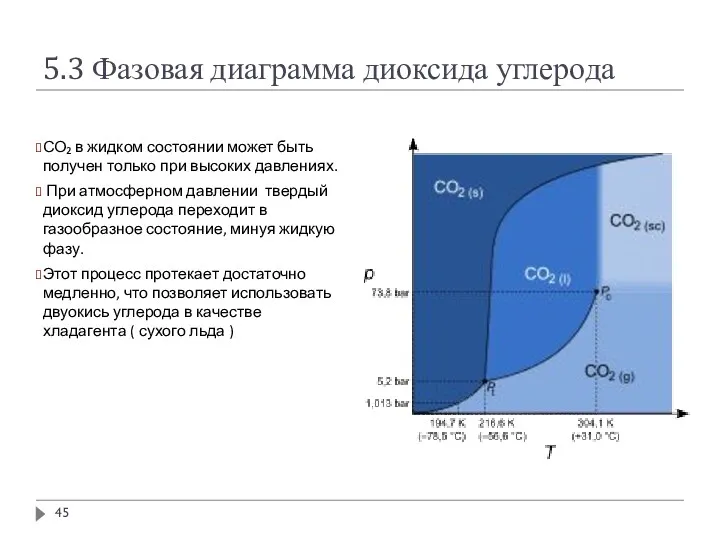
- 45. 5.3 Фазовая диаграмма диоксида углерода СО₂ в жидком состоянии может быть получен только при высоких давлениях.
- 47. Скачать презентацию







































 Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії Группа ультраосновных пород
Группа ультраосновных пород Аммиак
Аммиак Физические и химические свойства алмаза. Алмазная промышленность в России
Физические и химические свойства алмаза. Алмазная промышленность в России Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Карбонильные соединения. Альдегиды
Карбонильные соединения. Альдегиды Уральские самоцветы
Уральские самоцветы Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Гибридизация. Формы электронных облаков
Гибридизация. Формы электронных облаков Классификация химических реакций
Классификация химических реакций Общая характеристика халькогенов. Кислород
Общая характеристика халькогенов. Кислород Electrochemistry. Oxidation-reduction equilibrium in water solutions
Electrochemistry. Oxidation-reduction equilibrium in water solutions Задачи на вывод формулы органических веществ
Задачи на вывод формулы органических веществ Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях кл.химия 24.01
кл.химия 24.01 Химические свойства получение и применение солей
Химические свойства получение и применение солей Массовая и объемная доли компонентов смеси (раствора)
Массовая и объемная доли компонентов смеси (раствора) Введение в количественный анализ
Введение в количественный анализ Хімічна кінетика
Хімічна кінетика Различные теории кислот и оснований
Различные теории кислот и оснований Кристалдардың ішкі құрылымы
Кристалдардың ішкі құрылымы Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.) Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение
Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение Галогены. История открытия галогенов
Галогены. История открытия галогенов Introduction in bioorganic chemistry. Isomerism and structure of organic compounds
Introduction in bioorganic chemistry. Isomerism and structure of organic compounds Щелочные породы среднего состава
Щелочные породы среднего состава Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность
Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность Назначение установки Пенекс
Назначение установки Пенекс