Содержание
- 2. Содержание Положение в таблице Менделеева Нахождение в природе Физические свойства Химические свойства Применение
- 3. Положение в таблице Минделеева Литий (лат. Lithium), Li, химический элемент 1 группы периодической системы Менделеева, атомный
- 4. Нахождение в природе Распространение в природе. Л. - типичный элемент земной коры (содержание 3,2×10-3% по массе),
- 5. Физические свойства Простое вещество литий - мягкий щелочной металл серебристо-белого цвета. Из всех щелочных металлов он
- 6. Химические свойства Литий проявляет типичные свойства щелочных металлов, взаимодействуя с водой, кислородом, другими неметаллами. Хранить его
- 7. Применение Металлический литий - высокопрочные и сверхлегкие сплавы с магнием и алюминием для авиационной и космической
- 9. Скачать презентацию
Слайд 2Содержание
Положение в таблице Менделеева
Нахождение в природе
Физические свойства
Химические свойства
Применение
Содержание
Положение в таблице Менделеева
Нахождение в природе
Физические свойства
Химические свойства
Применение
Слайд 3Положение в таблице Минделеева
Литий (лат. Lithium), Li, химический элемент 1 группы периодической системы Менделеева,
Положение в таблице Минделеева
Литий (лат. Lithium), Li, химический элемент 1 группы периодической системы Менделеева,
атомный номер 3, атомная масса 6,941, относится к щелочным металлам. Природный Л. состоит из двух стабильных изотопов - 6Li (7,42%) и 7Li (92,58%).
Л. был открыт в 1817 шведским химиком А. Аведсоном в минерале петалите; название от греч. líthos - камень. Металлический Л. впервые получен в 1818 английским химиком Г. Дэви.
Л. был открыт в 1817 шведским химиком А. Аведсоном в минерале петалите; название от греч. líthos - камень. Металлический Л. впервые получен в 1818 английским химиком Г. Дэви.
Слайд 4Нахождение в природе
Распространение в природе. Л. - типичный элемент земной коры (содержание
Нахождение в природе
Распространение в природе. Л. - типичный элемент земной коры (содержание
3,2×10-3% по массе), он накапливается в наиболее поздних продуктах дифференциации магмы - пегматитах. В мантии мало Л. - в ультраосновных породах всего 5×10-3% (в основных 1,5×10-3%, средних - 2×10-3%, кислых 4×10-3%). Близость ионных радиусов Li+, Fe2+ и Mg2+ позволяет Л. входить в решётки магнезиально-железистых силикатов - пироксенов и амфиболов. В гранитоидах он содержится в виде изоморфной примеси в слюдах. Только в пегматитах и в биосфере известно 28 самостоятельных минералов Л. (силикаты, фосфаты и др.). Все они редкие (см. Литиевые руды). В биосфере Л. мигрирует сравнительно слабо, роль его в живом веществе меньше, чем остальных щелочных металлов. Из вод он легко извлекается глинами, его относительно мало в Мировом океане (1,5×10-5%). Промышленные месторождения Л. связаны как с магматическими породами (пегматиты, пневматолиты), так и с биосферой (солёные озёра).
Слайд 5Физические свойства
Простое вещество литий - мягкий щелочной металл серебристо-белого цвета. Из всех
Физические свойства
Простое вещество литий - мягкий щелочной металл серебристо-белого цвета. Из всех
щелочных металлов он самый твердый, высокоплавкий (Ткип=180,5 и Тпл=1340° С). Это самый легкий металл (плотность 0,533 г/см3), он плавает не только в воде, но и в керосине. Литий и его соли окрашивают пламя в карминно-крастный цвет.
Слайд 6Химические свойства
Литий проявляет типичные свойства щелочных металлов, взаимодействуя с водой, кислородом, другими неметаллами.
Химические свойства
Литий проявляет типичные свойства щелочных металлов, взаимодействуя с водой, кислородом, другими неметаллами.
Хранить его приходится под слоем под слоем минерального масла, придавливая сверху, чтобы не всплывал.
В соответствии с положением в ПСХЭ, литий наименее активный щелочной металл. Так в реакции с кислородом он образует в основном оксид лития, а не гедроксиды как другие металлы. Подобно натрию литий растворяется в жидком аммиаке, образуя синий раствор с металлической проводимостью. Растворенный литий постепенно реагирует с аммиаком: 2Li + 2NH3 = 2LiNH2 + H2.
Литий отличается повышенной активностью при взаимодействии с азотом, образуя с ним уже при обычной температуре нитрид Li3N.
По некоторым свойствам литий и его соединения напоминают соединения магния (диагональное сходство в таблице Менделеева).
Слайд 7Применение
Металлический литий - высокопрочные и сверхлегкие сплавы с магнием и алюминием для
Применение
Металлический литий - высокопрочные и сверхлегкие сплавы с магнием и алюминием для
авиационной и космической техники. Легирующая добавка в металлургии (связывает азот, кремний, углерод). Теплоноситель (расплав) в ядерных реакторах.
Из лития изготовляют аноды химических источников тока и гальванических элементов с твёрдым электролитом.
Соединения: специальные стекла, глазури, эмали, керамика. Монокристаллы фторида лития используются для изготовления высокоэффективных (КПД 80 %) лазеров LiOH как добавка в электролит щелочных аккумуляторов. Карбонат лития – добавка в расплав при производстве алюминия: снижает температуру плавления электролита, увеличивает силу тока, уменьшает нежелательное выделение фтора.
Металлоорганические соединения лития (например бутиллитий LiС4Н9) - широко применяются в промышленном и лабораторном органическом синтезе и как катализаторы полимеризации.
Дейтерид лития-6: как источник дейтерия и трития в термоядерном оружии (водородная бомба). См. Ядерные реакции дейтерида лития. (анимированные модели).
Содержание лития в организме человека составляет около 70 мг. В течение суток в организм взрослого человека поступает около 100 мкг лития. Литий способствует высвобождению магния из клеточных «депо» и тормозит передачу нервного импульса, ингибируя проводимость нервной системы. Соли лития применяются психотропные лекарственные средства, оказывая успокаивающий эффект при лечении шизофрении и депрессии. Однако передозировка может привести к тяжелым осложнениям и летальному исходу.
Из лития изготовляют аноды химических источников тока и гальванических элементов с твёрдым электролитом.
Соединения: специальные стекла, глазури, эмали, керамика. Монокристаллы фторида лития используются для изготовления высокоэффективных (КПД 80 %) лазеров LiOH как добавка в электролит щелочных аккумуляторов. Карбонат лития – добавка в расплав при производстве алюминия: снижает температуру плавления электролита, увеличивает силу тока, уменьшает нежелательное выделение фтора.
Металлоорганические соединения лития (например бутиллитий LiС4Н9) - широко применяются в промышленном и лабораторном органическом синтезе и как катализаторы полимеризации.
Дейтерид лития-6: как источник дейтерия и трития в термоядерном оружии (водородная бомба). См. Ядерные реакции дейтерида лития. (анимированные модели).
Содержание лития в организме человека составляет около 70 мг. В течение суток в организм взрослого человека поступает около 100 мкг лития. Литий способствует высвобождению магния из клеточных «депо» и тормозит передачу нервного импульса, ингибируя проводимость нервной системы. Соли лития применяются психотропные лекарственные средства, оказывая успокаивающий эффект при лечении шизофрении и депрессии. Однако передозировка может привести к тяжелым осложнениям и летальному исходу.
- Предыдущая
Поздравление с новым годомСледующая -
Феодальная раздробленность на Руси Высокомолекулярные соединения полимеры
Высокомолекулярные соединения полимеры Дисперсные системы. Дисперсное состояние вещества. Лекция 10
Дисперсные системы. Дисперсное состояние вещества. Лекция 10 Чистые вещества и смеси
Чистые вещества и смеси Распространенные названия некоторых неорганических веществ
Распространенные названия некоторых неорганических веществ Гидролиз солей
Гидролиз солей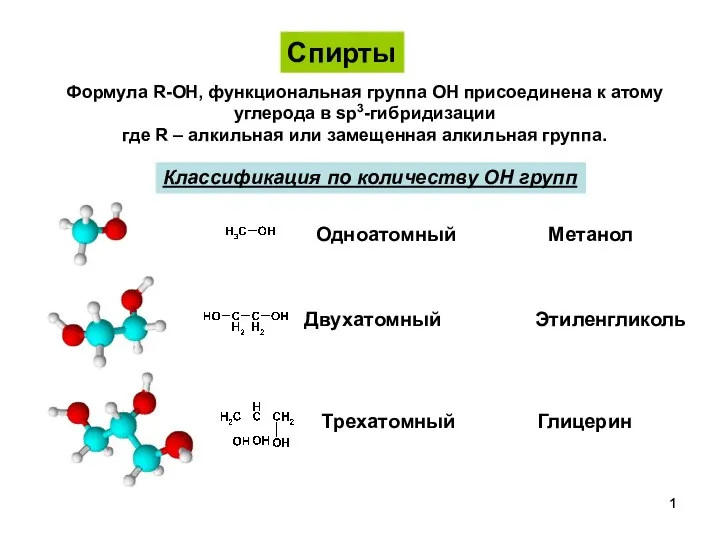 СпиртыПростыеЭфиры-1
СпиртыПростыеЭфиры-1 Углекислый газ, угольная кислота и её соли
Углекислый газ, угольная кислота и её соли Алкани
Алкани Застосування солей і оксидів
Застосування солей і оксидів Физико-химические свойства белков. Количественные (колориметрические) методы определения концентрации белка
Физико-химические свойства белков. Количественные (колориметрические) методы определения концентрации белка Тайна мыльного пузыря
Тайна мыльного пузыря Альдегиды и кетоны
Альдегиды и кетоны Композиционные материалы для изоляции электрических машин
Композиционные материалы для изоляции электрических машин Проект установки каталитического риформинга мощностью 1200 тыс. тонн
Проект установки каталитического риформинга мощностью 1200 тыс. тонн Физические свойства металлов
Физические свойства металлов Калийные удобрения
Калийные удобрения Особенности химического состава клетки
Особенности химического состава клетки Горные породы Крыма
Горные породы Крыма Зависимость биохимических изменений в мясе от условий хранения
Зависимость биохимических изменений в мясе от условий хранения Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Медь. Химические свойства. Получение меди. Применение
Медь. Химические свойства. Получение меди. Применение Узагальнення й систематизація знань з теми Початкові хімічні поняття (1 частина)
Узагальнення й систематизація знань з теми Початкові хімічні поняття (1 частина) Кристаллография, кристаллохимия, минералогия
Кристаллография, кристаллохимия, минералогия Соли. Определение солей
Соли. Определение солей Химические свойства металлов
Химические свойства металлов Азотная кислота. К уроку химии для 9 класса
Азотная кислота. К уроку химии для 9 класса Курс лекций: Методы диагностики и анализа микро- и наносистем
Курс лекций: Методы диагностики и анализа микро- и наносистем Тепловий ефект хімічних реакцій. Екзотермічні ї ендотермічні реакції термохімічні рівняння
Тепловий ефект хімічних реакцій. Екзотермічні ї ендотермічні реакції термохімічні рівняння